高二上学期化学期中考试测试题 (26)
- 格式:doc
- 大小:961.81 KB
- 文档页数:18

2017年度第一学期高二化学期中试卷
(考试时间:90分钟 满分:100分)
可能用到的相对原子量:H-1 O-16 Na-23 Mg-24 Al-27 Cl-35.5 Fe-56
一、 选择题(共 分,每小题2分,每小题只有一个正确选项。)
1、不能发生铝热反应的是 ( )
A.V2O5 B.Cr2O3 C.MnO2 D.MgO
2、不属于中学化学的基本理论知识的是 ( )
A.勒夏特利原理 B.元素周期律 C.电解质 D.硫铁矿的成分
3、下列各物质中,不能由组成它的两种元素的单质直接化合得到的是 ( )
A. FeS B. FeCl2 C. FeCl3 D.Fe3O4
4、金属晶体的形成是因为晶体中主要存在 ( )
A.金属离子之间的相互作用 B.金属原子之间的作用
C.金属离子与自由电子间的相互作用 D.金属原子与自由电子间的相互作用
5、我国最新报道的高温超导体中, 铊是组成成分之一。已知铊与铝是同族元素, 关于铊的判断有错误的是 ( )
A.氢氧化铊是两性氢氧化物 B.铊能置换出盐酸中的氢
C.铊是质软的银白色的金属 D.铊能生成+3价的化合物
6、有关物质结构的叙述正确的是 ( )
A.有较强共价键存在的物质熔沸点一定很高
B.由电子定向移动而导电的物质是金属晶体
C.只含有共价键的物质不一定是共价化合物
D.在离子化合物中不可能存在非极性共价键
7、下列各分子中,所有原子都满足最外层为8电子结构的是 ( )
A.H2O B.BF3 C.CCl4 D.PCl5

- 1 - 2017-2018学年度第一学期期中考试
高二化学
可能用到的相对原子质量H-1 O-16 Na-23 Cl-35.5 Fe-56 Cu-64 Zn-65
一、单项选择题(本大题包含25个小题,每个小题均只有一个正确答案。每小题2分,共50分)
1、化学反应都伴随着能量变化,下列反应中属于吸热反应的是
A.生石灰吸收水 B.SO2的催化氧化 C.工业合成氨 D.氯化铵的水解
2、10mL浓度为1mol/L的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应速率但又不影响氢气生成的是
A.KNO3 B.CH3COONa C.CuSO4 D.Na2CO3
3、向含有MgCO3固体的溶液中滴加少许浓盐酸(忽略体积变化),下列数值变小的是
A.c(Mg2+) B.c(CO32-) C.c(H+) D.Ksp(MgCO3)
4、N2(g)+3H2(g)2NH3(g) △H<0。当反应达到平衡时,下列措施能提高N2转化率的是
①降温②恒压通入惰性气体③增加N2的浓度④加压
A.①② B.①④ C.②③ D.③④
5、短周期元素W、X、Y、Z的原子序数依次增大,其简单离子都能破坏水的电离平衡的是
A.W2-、X+ B.X+、Y3+ C.X+、Z2- D.Y3+、Z2-
6、下列溶液一定呈酸性的是
A.滴加酚酞显无色溶液 B.含有较多H+的溶液
C.c(OH-)<c(H+)的溶液 D.pH<7的溶液
7、常温下,在等体积①pH=0的硫酸、②0.01mol/L NaOH溶液、③pH=10的纯碱溶液、④pH=5的NH4Cl溶液中,水电离程度的大小顺序是
A.①>②>③>④ B.②>①>④>③ C.④>③>②>① D.③>④>②>① - 2 - 8、能证明乙酸是弱酸的实验事实是

- 1 - 太原市2020-2021学年高二上学期期中考试
化学试题
可能用到的相对原子质量:H 1 C 12 O 16
一、选择题(本题共20小题,每小题2分,共40分)
1.2020年7月,由“长征五号”运载火箭搭载的我国首个火星探测器“天问一号”成功发射。该火箭使用的无毒燃料是液氢和航天煤油,下列说法不正确的是
A.火箭燃料燃烧时,化学能转化为热能 B.液氢和航天煤油燃烧时,均作还原剂
C.航天煤油可通过石油干馏得到 D.与航天煤油相比,液氢燃烧后的产物对环境影响较小
2.下列电离方程式正确的是
A.NaHCO3溶于水:NaHCO3Na++HCO3-
B.NaHSO4溶于水:NaHSO4=Na++H++SO42-
C.HF溶于少量水:HF=H++F-
D.H2CO3溶液:H2CO3=2H++CO32-
3.下列措施与控制化学反应速率无关的是
A.汽车加大油门 B.使用加酶洗衣粉
C.搅拌使食盐在水中溶解 D.在月饼包装中放置脱氧剂
4.下列事实一定能说明亚硝酸(HNO2)是弱电解质的是
①常温下HNO2溶液中存在的微粒有:H+、NO2-、HNO2,OH-、H2O
②用HNO2溶液做导电性实验,灯泡很暗
③10 mL 1 mol·L-1 HNO2溶液恰好与10 mL 1 mol·L-1 NaOH溶液完全反应
④0.1 mol·L-1 HNO2溶液的c(H+)<0.1 mol·L-1
A.①③ B.②③ C.①④ D.②④
5.下列事实不能用勒夏特列原理解释的是
A.H2(g)+I(g)2HI(g)反应达平衡后,压缩体积气体颜色变深 - 2 - B.Fe(SCN)3溶液中加入固体KSCN后颜色变深
C.N2(g)+3H2(g)2NH3(g) △H<0,工业上采用高压条件更有利于合成氨
D.浸泡在冰水中的NO2球的红棕色明显变浅

第 1 页 共 13 页 太原市高二上学期化学期中考试试卷A卷
姓名:________ 班级:________ 成绩:________
一、 单选题 (共20题;共40分)
1. (2分) (2019高二上·宾阳月考) 在 CO(g)+H2O(g) CO2(g)+H2(g)反应中,正反应为放热反应。改变下列条件,不能使化学反应速率增大的是
A . 增大压强
B . 使用催化剂
C . 降低温度
D . 增大 H2O(g)的浓度
2. (2分) 下列说法中正确的是( )
A . 所有自发进行的化学反应都是放热反应
B . 熵值增大的反应都能自发进行
C . 由能量判据和熵判据组合而成的复合判据,适合于所有的反应
D . 同一物质的固、液、气三种状态的熵值相同
3. (2分) (2018高二上·定远月考) 某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)
Z(g)+W(s) ΔH>0,下列叙述正确的是( )
A . 加入少量W,逆反应速率增大
B . 当容器中气体压强不变时,反应达到平衡
C . 升高温度,平衡逆向移动
D . 平衡后加入X,上述反应的ΔH增大
4. (2分) (2016高一下·广东期末) 下列有关热化学方程式及其叙述正确的是( )
A . 已知S(g)+O2(g)═SO2(g)△H1;S(s)+O2(g)═SO2(g)△H2 , 则△H1<△H2
B . HCl和NaOH反应的中和热△H=﹣57.3kJ•mol﹣1 , 则H2SO4和Ba(OH)2反应的中和热△H=2×(﹣57.3) 第 2 页 共 13 页 kJ•mol﹣1
C .
已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定

第1页/共3页 高二上学期化学期中考试总结
期中考试已经落下帷幕,回顾这两个月的教学,我们高二化学组全体教师认真备课,激情上课,细心批改作业,贴心个别辅导,化学教学取得了较好的成绩。现将考试情况及今后措施做一小结:
一、考试情况 考试题中选择题侧重基础知识、基本技能,符合教学实际,测试了学生的基础知识;必考试题中非选择题侧重基本技能和化学学科能力;能力要求适中。 考试情况来看,对于这次的试卷,总体感觉对于知识点的把握比较好,题目出的也很到位,易难度的比例大致为5:3:2,但是题目对于我们的学生来说,还是有些过于灵活。我们的学生能力普遍不强,不会全面的分析问题,再加上基础知识掌握不牢,很难在脑中建立一个逻辑性比较强的知识网络,特别是一些综合性的题目,由于教与练的脱节,导致很多学生中等难度的题目分数拿不全,而难题就很难拿到分。加上平行班之间教学进度有些不一致,学生习题的练 习和 老师的讲解得不到保障,这样学生就孤陋寡闻,见识太少,遇见中难度题好似猫吃刺猬,无所适从。这次考试全校90分以上16人(平行班2人),80分以上78人,70分以上365人,60分以上468人。全校平均分52.92分。实验班平均分75.28分
二、教与学中存在的问题:1、教学中的问题主要表现在:①基础知识网络的教学反馈没有形成,导致学生对知识的理第2页/共3页 解没有系统性,而是片面的、狭隘的、零散和独立地。②题目训练与应试训练明显不足,导致学生考试时准确率和速度下降,特别是资料没有赶上教学进度的要求,加上本阶段的知识点又是整个高二阶段的难点和重点,学生来不及消化,谈不上课后对知识的反刍了。③个别班课后查漏补缺和个别辅导相结合工作没有跟上,以致出现了低分学生④有些班学生迟交作业、抄袭作业、订正、重做的后续工作没有跟上,客观上时间不允许,主观上也没有挤时间、没有努力、责任心还不够。⑤我们的老师和家长的沟通相结合教育做得欠缺,遇有情况没有及时和家长取得联系,今后加强这方面的工作,力争及时互馈信息,学生取得进步表扬也要和家长联系,不能一味只要联系家长就是坏消息。

1 高二上学期期中考试 化学试题
本试题满分100分,时间90分钟。分为第I卷(选择题)和第II卷(非选择题)两部分
第I卷(选择题,共48分)
可能用到的相对原子质量:
H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 Fe 56 Cu 64 Zn 65
一、选择题(本题包括16小题,每题3分,共48分。每小题只有一个....选项符合题意)
1.下列描述中,正确的是( )
A.反应CaO+H2O== Ca(OH)2能放出大量的热,故可通过原电池实现该反应,并把化学能转化为电能
B.在原电池或电解池装置中,都可实现反应:Cu+2H+ = Cu2++H2
C.若原电池的两极是活泼性不同的两种金属,则活泼的金属不一定做负极
D.在钢铁制品上镶嵌锌块构成原电池以防治钢铁生锈,这种防护方法叫外加电源阴极保护法
2. 室温下向10mL pH=11的稀氨水溶液中加入水稀释后,下列说法正确的是( )
A.溶液中导电粒子的数目增加,导电性增强
B.氨水的电离程度增大,[OH-]减小
C.再加入10mL pH=3 HCl溶液,混合液pH=7
D.溶液中由水电离出的[OH-]=1×10-3 mol·L-1
3.下列有关说法错误的是( )
A.物质在不电离的条件下,也能导电
B.若化学平衡向逆反应方向移动,则正反应速率不一定减小
C.硫酸钡、醋酸铵、碳酸氢钠都是强电解质
D.导电性强的溶液里自由移动离子数目一定比导电性弱的溶液里自由移动离子数目多
4.830K时,在恒容密闭容器中进行的可逆反应:C(s)+H2O(g) H2(g)+CO(g),下列哪种情况下,可说明该反应已经达到化学平衡状态( )
A.v正(C):v逆(H2)=1:1的状态
B.用H2O、CO、H2的物质的量浓度变化表示的反应速率的比为1∶1∶1的状态

1 高二上学期期中考试化学试题
本试卷分第I卷和第Ⅱ卷两部分,共100分,考试时间90分钟
可能用到的相对原子质量:H:1 C:12 O:16
第Ⅰ卷(选择题,共48分)
一、选择题(本题包括16小题,每小题3分,共48分。每小题只有一个....选项符合题意。)
1. 沸腾时只需克服范德华力的物质是( )
A.水 B.CCl4 C.氨水 D.水银
2. 下列叙述中,正确的是( )
A.原子晶体中只含有共价键 B.分子晶体中只存在分子间作用力,不存在化学键
C.离子晶体中只含有离子键,不含共价键 D.任何晶体中,若含有阳离子也一定含有阴离子
3. 下列各组物质中,化学键类型相同,晶体类型也相同的是( )
A.金刚石和干冰 B.NaBr和HBr C.CH4和H2O
D.Cl2和KCl
4. 下列有关表述中正确的是( )
A.35Br的电子排布式可简写为25[Ar]4s4p
B.16O与18O互为同位素,H216O、H218O互为同素异形体
C.CH4、4NH粒子的空间构型均为正四面体形
D.NH4Cl的电子式为
5. 化学反应中通常伴随着能量变化,下列说法中错误的是( )
A.煤燃烧时将部分化学能转化为热能 B.动物体内葡萄糖被氧化成CO2是热能转变成化学能
C.炸药爆炸时将部分化学能转化为动能 D.镁条燃烧时将部分化学能转化为光能
6. 反应3224NH(g) 5O(g)4NO(g) 6HO(g)====+ + 在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此段时间内,该反应的速率可表示为( )
A.3(NH)0.010 mol/(Ls) B.2(O)0.0010 mol/(Ls)

2020—2021学年上期中考
22届 高二 化学试题
说明:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)满分100分,考试时间90分钟。
2.将第Ⅰ卷的答案代表字母填(涂)在第Ⅱ卷的答题表(答题卡)中。
3.可能用到的相对原子质量:H-1 O-16 Na-23 Si-28 Cl-35.5 Ca-40
第Ⅰ卷(选择题,共48分)
一、单项选择题:本题共16小题,每小题3分,共48分。
1.下列说法正确的是( )
A.水是一次能源,水煤气是二次能源,天然气是可再生能源
B.Ba(OH)2·8H2O+2NH4Cl===BaCl2+2NH3+10H2O ΔH=+80 kJ·mol-1能自发进行,原因是体系有自发向混乱度增大的方向转变的倾向
C.需要加热才能发生的反应一定是吸热反应
D.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向
2.科学家用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程的示意图如下:
下列说法正确的是( )
A.CO和O生成CO2是吸热反应
B.在该过程中,CO断键形成C和O
C.CO和O生成了具有极性共价键的CO2
D.状态Ⅰ→状态Ⅲ表示CO与O2反应生成CO2的过程
3.下列热化学方程式或离子方程式中,正确的是( )
A.由热化学方程式CH3OH(g)+12O2(g)===CO2(g)+2H2(g);ΔH=-192.9 kJ·mol-1,可推知CH3OH(g)的燃烧热为192.9 kJ·mol-1
B.已知H2(g)的燃烧热为285.8 kJ·mol-1,则2H2O(l)===2H2(g)+O2(g);ΔH=+571.6 kJ·mol-1
C.HCl(aq)和NaOH(aq)反应的中和热ΔH=-57.3 kJ·mol-1,则稀H2SO4(aq)和Ba(OH)2 (aq)反应生成2molH2O(l)的反应热ΔH=2×(-57.3 kJ·mol-1)

第 1 页 共 15 页 山东省高二上学期化学期中考试试卷
姓名:________ 班级:________ 成绩:________
一、
单选题 (共30题;共60分)
1.
(2分) (2018高二上·广州期中)
下列各组关于强电解质、弱电解质、非电解质的归类符合题意的( )
A B C D
强电解质 Fe NaCl CaCO3 HNO3
弱电解质 CH3COOH BaSO4 H2CO3 Fe(OH)3
非电解质 蔗糖 CCl4 酒精 H2O
A . A
B . B
C . C
D . D
2. (2分) (2016高二上·承德期中) pH相同的醋酸溶液和盐酸,分别用蒸馏水稀释到原溶液的m倍和n倍,稀释后两溶液的pH仍相同,则m和n的关系量是( )
A . m=n
B . m>n
C . m<n
D . 无法判断
3. (2分) (2019高三上·济宁期末) 25℃时,用NaOH溶液滴定H2C2O4溶液,溶液中 和
[或 和 ]的关系如图所示。下列说法错误的是( )
第 2 页 共 15 页
A . 曲线M表示 和 的关系
B . Ka1(H2C2O4)的数量级为10-2
C . 向NaHC2O4溶液中加少量NaOH至c(HC2O4-)和c(C2O42-)相等,此时溶液pH约为5
D .
在NaHC2O4溶液中c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
4. (2分) (2018高二上·哈尔滨月考) 室温下,某溶液中由水电离产生的c(H+)等于10-13mol·L-1,该溶液的溶质不可能是( )
A . NaHSO4
B . NaCl
C . HCl
D . Ba(OH)2
第 1 页 共 9 页 郑州市2020-2021年高二上学期化学期中考试试卷(I)卷
姓名:________ 班级:________ 成绩:________
一、
单选题 (共14题;共28分)
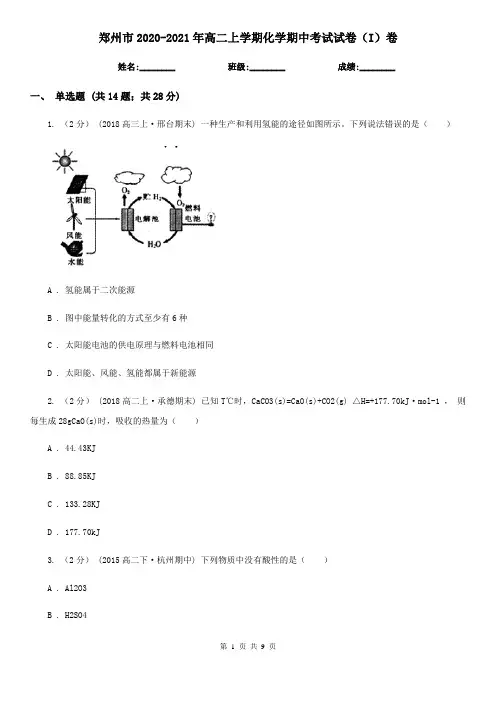
1. (2分) (2018高三上·邢台期末) 一种生产和利用氢能的途径如图所示。下列说法错误的是( )
A . 氢能属于二次能源
B . 图中能量转化的方式至少有6种
C . 太阳能电池的供电原理与燃料电池相同
D . 太阳能、风能、氢能都属于新能源
2. (2分) (2018高二上·承德期末) 已知T℃时,CaCO3(s)=CaO(s)+CO2(g) △H=+177.70kJ·mol-1 , 则每生成28gCaO(s)时,吸收的热量为( )
A . 44.43KJ
B . 88.85KJ
C . 133.28KJ
D . 177.70kJ
3. (2分) (2015高二下·杭州期中) 下列物质中没有酸性的是( )
A . Al2O3
B . H2SO4 第 2 页 共 9 页 C . KClO3
D . NaHSO4
4.
(2分) (2019高二下·长春月考)
下列物质中所含微粒的个数比是1∶1的是( )
A . CH3COONa溶液中CH3COO-和Na+
B . NH4+中的质子和电子
C . Na2O2固体中阴、阳离子
D . 原子中的质子和中子
5. (2分) (2018高二上·慈溪期中) 一定温度下,0.1mol N2(g)与 0.3mol H2(g)在密闭容器中发生反应:N2(g)+3H2(g) 2NH3(g) ,ΔH=-akJ·molˉ1。下列说法正确的是( )
A . 达到化学平衡状态时,反应放出 0.1a kJ热量

1 2015-2016学年度第一学期
高二化学期中试卷(必修)
命题人:张林
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Na-23 Ca—40 Fe—56 Cu—64
Ba-137 Ag-108 Cl-35.5
第I卷(选择题,共69分)
一、单项选择题(在每题4个选项中,只有1个选项是符合要求的。每题3分,共69分。)
1.于谦的《石灰吟》,借石灰石(碳酸钙)表现了作者“粉身碎骨浑不怕,要留清白在人间”的人格精神。碳酸钙属于
A.单质 B.氧化物 C.酸 D.盐
2.工业焊接钢管时常用137
55Cs进行“无损探伤”,这里的“137”是指该原子的
A.质子数 B.中子数 C.电子数 D.质量数
3.下列过程中,不涉及化学变化的是
A.明矾净水 B.海水晒盐 C.铁锅生锈 D.海水制镁
4.下列物质属于硅酸盐产品的是
A.尼龙绳 B.保鲜膜 C.青花瓷 D.金刚石
5.以下物质间的转化不能通过一步反应实现的是
A.HClO → O2 B.SiO2 → H2SiO3 C.CO2→ CaCO3 D.Cu → CuSO4
6. 下列化学用语表示正确的是
A.氮气的结构式:NN B.Cl—的结构示意图:
C.水的电子式: D.磷酸钠的电离方程式:Na3PO4=Na33++PO43—
7.下列气体不能用碱石灰(氢氧化钠固体和生石灰的混合物)干燥的是
A.H2 B.Cl2 C.NH3 D.CO
8.下列化学式与指定物质的主要成分对应正确的是
A.CH4——天然气 B.CO——水煤气
第 1 页 共 15 页 高二上学期化学期中考试试卷(选修)
姓名:________ 班级:________ 成绩:________
一、
单项选择题 (共10题;共20分)
1.
(2分) 能源与人类的生活和社会发展密切相关,下列关于能源开发和利用的说法中不正确的是( )
A . 因地制宜开发利用风能、水能、地热能、潮汐能
B . 大力推广并充分利用太阳能
C . 合理、安全开发利用氢能、核能
D . 能源都是通过化学反应获得的
2. (2分) (2018高二下·高明期末) 下图一是维生素C的键线式结构。有关说法中错误的是( )
A . 图二不是维生素C的结构简式
B . 维生素C在碱性溶液中不能稳定存在
C . 维生素C易发生起氧化及加成反应
D . 维生素C易溶于水
3. (2分) (2018高二下·吉安期末) 下列各化合物的命名中正确的是( )
A . CH2=CH-CH=CH2 1,3-二丁烯
B . 3-丁醇
第 2 页 共 15 页 C .
2-甲基苯酚
D . 2—乙基丙烷
4. (2分) (2016高三上·长春期中) 关于阿伏伽德罗常数NA , 下列叙述正确的是( )
A . 标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA
B . 1.0L0.1 mol•L﹣1 AlCl3溶液中所含的Al3+离子数为0.1NA
C . 标准状况下,11.2LSO3中含有分子数目为0.5NA
D . 常温常压下,3.2gO2和O3混合气体中含有的氧原子数目为0.2NA
5. (2分) (2017高二上·景德镇期末) 某化合物的结构(键线式)及球棍模型如图1:该有机分子的核磁共振氢谱图如图2(单位是ppm):下列关于该有机物的叙述正确的是( )
- 1 - 高二化学试题
(卷面满分:100分 考试时间:90分钟)
第Ⅰ卷(共48分)
选择题(本题包括16小题,每小题3分,共42分。每小题只.有一个...选项符合题意)。
1.下列属于对环境不产生污染的二次能源的是
A.煤炭 B.核能 C.风能 D.氢能
2.一定能反映化学平衡向正反应方向移动的是
A.生成物的物质的量分数增大。
B. v正 > v逆
C.反应物浓度降低
D.反应物的体积分数减少
3.下列反应符合(右)图示的是
A.酸碱中和反应
B.Ba(OH)2·8H2O与NH4Cl晶体的反应
C.黑火药爆炸
D.用焦炭制水煤气
4.下列变化过程,属于放热反应的是
① 水蒸气变成液态水 ② 生石灰与水反应
③ 浓H2SO4稀释 ④ 醋酸电离。
⑤ Na投入水中 ⑥ 反应物的键能总和小于生成物的键能总和
A、②③④⑤ B、②⑤⑥
C、②③④ D、①②⑤⑥
5.反应mA(s)+nB(g) pC(g) △H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如右图所示,下列叙述中一定正确的是
①m+n>p ②y点表示的正反应速率小于逆反应速率
③n>p ④x点比y点时的反应速率慢
⑤若降低温度,该反应的平衡常数增大
A.①②⑤ B.②④⑤
C.只有①③ D.①③⑤
6.在恒温恒容的容器中进行下列反应:N2O4(g) 2NO2(g),若NO2的浓度由0.1mol/L增大到0.2mol/L时,需要5 s,那么NO2的浓度继续由0.2mol/L增大到0.4mol/L时,所需反应的时间为
A.小于10s B.等于10s C.大于10s D.等于5s
1 洛阳市2019-2020学年第一学期期中考试
高二化学试卷
本试卷分第I卷(选择题)和第Ⅱ卷(非选择题)两部分,共100分。考试时间90 分钟。
第I卷(选择题,共50分)
注意事项:
1.答题前,考生务必将自己的姓名、考号、考试科目涂写在答题卷上。
考试结束,将答题卷交回。
2.本试卷可能用到的相对原子质量:H:1 0:16 Na:23 S:32
一、选择题(本题共10小题,每小题只有一个选项......符合题意,每小题2分,共20分)
1.下列过程或现象与盐类水解无关的是
A.向Na2CO3溶液中滴加酚酞试液变红色
B.加热FeCl3溶液颜色会变深
C.实验室保存硫酸亚铁溶液时加入少量铁粉
D. KAl(S04)2·12 H2O)可用于净水
2.下列溶液一定显碱性的是
A.PH = 8的某电解质溶液 B. c(OH-)>lX10-7 mol·L-1
C.含有OH-的溶液 D.溶液中 c(OH-)>C(H+)
3.对于可逆反应 2AB3 (g)=2A(g)+ 3B2 (g), △H>0,下列图像不正确的是
4.在一定温度下的某容积不变的密闭容器中,建立下列化学平衡: C(s)+H20(g)=C()(g) +
H2(g),不能确定上述可逆反应在一定条件下已达到化学平衡状态的是
A.体系的压强不再发生变化
B.(H2O)(CO)逆正
C.生成n mol CO的同时生成n mol H2
2 D. 1 mol H—H键断裂的同时断裂2 mol H—O键
5.浓度均为0. 1 mol • L-1的下列溶液,其pH由小到大的排列顺序是 ①NaHC03溶液②NaHS04溶液③NaCl溶液④A1C13溶液⑤NaClO溶液
A.①<②<③<④<⑤ B.④<②<⑤<③<①
C.②<④<③<①<⑤ D.②<④<③<⑤<①
6.氯化银在水中存在沉淀溶解平衡,25 ℃时,氯化银的Ksp= l.8Xl0-10。现将足量氯化银分别放入:①5 mL蒸馏水中②20 mL 0. 2 mol • L-1 MgCl2溶液中③ 10 mL 0.5 mol • L-1NaCl溶液中,充分搅拌后,在相同温度下,c( Ag+)由大到小的顺序是
高二上学期化学期中考试试卷
一、单选题
1. 下列我国科技创新的产品设备在工作时有化学能转变成电能的是 A . 长征5号火箭使用的液氧煤油发动机B .
北斗导航卫星的太阳能电池板C . 位于江苏的海上风力发电厂D . 世界首部可折叠柔屏手机
2. 在食品中使用下列试剂的目的与化学反应速率无关的是( )
A . 着色剂B . 催熟剂C . 抗氧化剂D . 防腐剂
3. 一定条件下反应: 则
中R的化合价是( ) A . B . C . D .
4. 下列判断不正确的是 ( )
①反应NH3+HCl ═ NH4Cl在室温下可自发进行,则该反应的ΔH>0
②CaCO3 ═ CaO+CO2室温下不能自发进行,说明该反应的ΔH<0
③一定温度下,反应MgCl2 ═ Mg+Cl2的ΔH>0、ΔS>0
④常温下,反应C+CO2 ═ 2CO不能自发进行,则该反应的ΔH>0
A . ①③B . ②③C . ②④D . ①②
5. 把一定量的X气体和Y气体混合于容积为2L的容器中,使其发生如下反应: ,5min达到平衡状态,消耗Y为 ,这段时间用W表示的平均速率为 ,则n的值( )
A . 1B . 2C . 3D . 4
6. 少量铁粉与 的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变 的产量,可以使用如下方法中的( )
①加 ②加 固体 ③滴入几滴浓盐酸
④改用 的硝酸 ⑤加 溶液 ⑥滴加几滴硫酸铜溶液
⑦升高温度(不考虑盐酸挥发) ⑧改用 的盐酸
高二上学期期中考试(化学)
(考试总分:100 分)
一、 单选题 (本题共计20小题,总分60分)
1.(3分)下列过程中,需要加快化学反应速率的是( )
A.钢铁的腐蚀 B.食物腐烂
C.工业炼钢 D.塑料老化
2.(3分)下列关于化学反应速率的叙述,正确的是( )
A.化学反应速率可用某时刻生成物的浓度表示
B.在同一反应中,用反应物或生成物物质的量浓度在单位时间内的变化表示的化学反应速率的大小相等
C.化学反应速率通常用单位时间内反应物浓度的减小或生成物浓度的增大来表示
D.在任何反应中,反应现象在较短时间内出现,则反应速率大;反应现象在很长时间内才出现,则反应速率小
3.(3分)某一反应物的浓度为3mol/L,经5秒钟后,浓度变为2mol/L,则这5秒里该反应物的平均反应速率是( )
A.0.2mol/s B.0.2mol·L/s
C.0.2mol/(L·s) D.12mol/(L·min)
4.(3分)下列说法错误的是( )
A.当碰撞的分子具有足够的能量和适当的取向时,才能发生化学反应
B.发生有效碰撞的分子一定是活化分子
C.活化分子间的碰撞一定是有效碰撞
D.活化分子间每次碰撞不一定发生化学反应
5.(3分)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是( )
A.CH3OH(l)+3/2O2(g)→CO2(g)+2H2O(l)△H=+725.8 kJ/mol B.2CH3OH(l)+3O2(g)→2CO2(g)+4H2O(l)△H=-1452 kJ/mol
C.2CH3OH(l)+3O2(g)→2CO2(g)+4H2O(l)△H=-725.8 kJ/mol
D.2CH3OH(l)+3O2(g)→2CO2(g)+4H2O(l)△H=+1452 kJ/mol
6.(3分)决定化学反应快慢的主要因素是( )