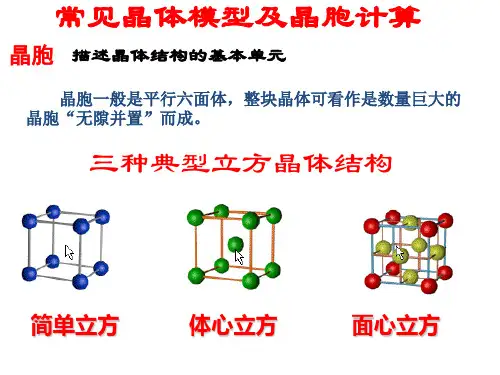
金属及各类晶体配位数计算图总结
- 格式:ppt
- 大小:6.10 MB
- 文档页数:138

离子(价态)常有配位数常有配合体常有颜色Ag(+1)2NH3,CN-Cu(+2)4,(+1)2(X-)NH3,H2O,en,Ni(+2,+4)4,6CO,NH3Al(+3)6F-,OH-,Co(+2,+3)4,6CO,NH3,H2O,Cl,Fe(+3,+2)6--CN,SCN,NH3,COPt(+2)4,(+4)6Cl,NH3Ca(+2),Mg(+2)6EDTACr(+3)6NH3,NO2,H2OZn(+2)4NH3Zr(+4)7F-,+2Au(+3)2,4X-[Cu(NH3)4]2+绛蓝[Fe(SCN)6]3-血红[Pt(NH3)4}2+顺式绿色反式黄色Fe3+与苯酚的配合物紫色Fe3+与CO的配合物血红二茂铁橙黄色铝与铝试剂的配合物玫瑰色红色Fe(SCN)]2+(血红色);Cu2O(砖红色);Fe2O3(红棕色);红磷(红棕色);液溴(深红棕色);Fe(OH)3(红褐色);I2的CCl4溶液(紫红色);MnO4-(紫红色);Cu(紫红色);在空气中久置的苯酚(粉红色).橙色:溴水;K2Cr2O7溶液.黄色:AgI(黄色);AgBr(浅黄色);K2CrO4(黄色);Na2O2(淡黄色);S(黄色);FeS2(黄色);久置浓HNO3(溶有NO2);工业浓盐酸(含Fe3+);Fe3+水溶液(黄色);久置的KI溶液(被氧化I2)绿色:Cu2(OH)CO3;Fe2+的水溶液;FeSO4.7H2O;Cl2(黄绿色);F2(淡黄绿色);Cr2O3蓝色:Cu(OH)2;CuSO4.5H2O;Cu2+的水溶液;I2与淀粉的混淆物.紫色:KMnO4(紫黑色);I2(紫黑色);石蕊(pH=8--10);Fe3+与苯酚的混淆物.黑色:FeO,Fe3O4,FeS,CuS,Cu2S,Ag2S,PbS,CuO,MnO2,C粉.白色:Fe(OH)2,AgOH,无水CuSO4,Na2O,Na2CO3,NaHCO3,AgCl,BaSO4,CaCO3,CaSO3,Mg(OH)2,Al(OH)3,三溴苯酚,MgO,MgCO3,绝大多半金属等.一、单质绝大多半单质:银白色。

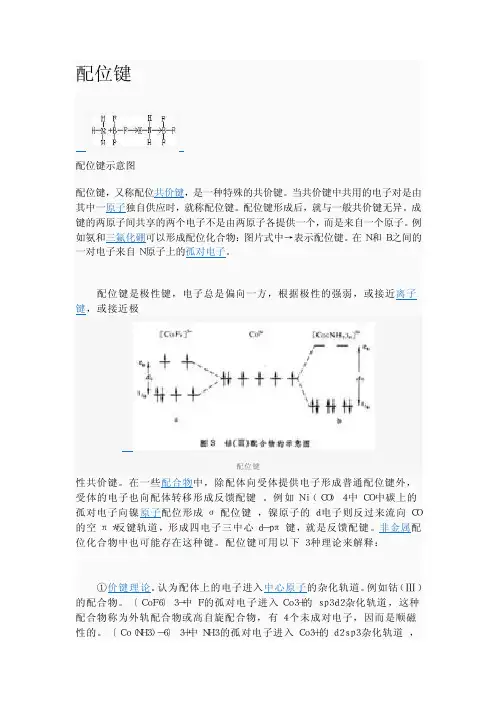
配位键 配位键示意图 配位键,又称配位共价键,是一种特殊的共价键。
当共价键中共用的电子对是由其中一原子独自供应时,就称配位键。
配位键形成后,就与一般共价键无异。
成键的两原子间共享的两个电子不是由两原子各提供一个,而是来自一个原子。
例如氨和三氟化硼可以形成配位化合物:图片式中→表示配位键。
在N和B之间的一对电子来自N原子上的孤对电子。
配位键是极性键,电子总是偏向一方,根据极性的强弱,或接近离子键,或接近极 配位键性共价键。
在一些配合物中,除配体向受体提供电子形成普通配位键外,受体的电子也向配体转移形成反馈配键 。
例如Ni(CO)4中CO中碳上的孤对电子向镍原子配位形成σ配位键 ,镍原子的d电子则反过来流向CO的空π*反键轨道,形成四电子三中心d-pπ键,就是反馈配键。
非金属配位化合物中也可能存在这种键。
配位键可用以下3种理论来解释: ①价键理论。
认为配体上的电子进入中心原子的杂化轨道。
例如钴(Ⅲ)的配合物。
〔CoF6〕3-中F的孤对电子进入Co3+的sp3d2杂化轨道,这种配合物称为外轨配合物或高自旋配合物,有4个未成对电子,因而是顺磁性的。
〔Co(NH3)-6〕3+中NH3的孤对电子进入Co3+的d2sp3杂化轨道 ,这种配合物称为内轨配合物或低自旋配合物,由于所有电子都已成对,因而没有顺磁性而为抗磁性。
②晶体场理论。
晶体场理论将配体看作点电荷或偶极子,同时考虑配体产生的静电场对中心原子的原子轨道能级的影响[1]。
例如,把中心原子引入位于正八面体6个顶角上的6个配体中,原来五重简并的d轨道就分裂成一组二重简并的eg(-y2、dz2)轨道和一组三重简并的t2g(dxy、dxz、dyz)轨道 。
eg和t2g轨道的能量差 ,称为分离能Δ0,Δ0≡10Dq,Dq称为场强参量。
在上述钴(Ⅲ)配合物中,6个F-产生的场不强,Δ0较小,d电子按照洪特规则排布,有四个未成对电子,因而〔CoF6〕3-为弱场配合物或高自旋配合物 。
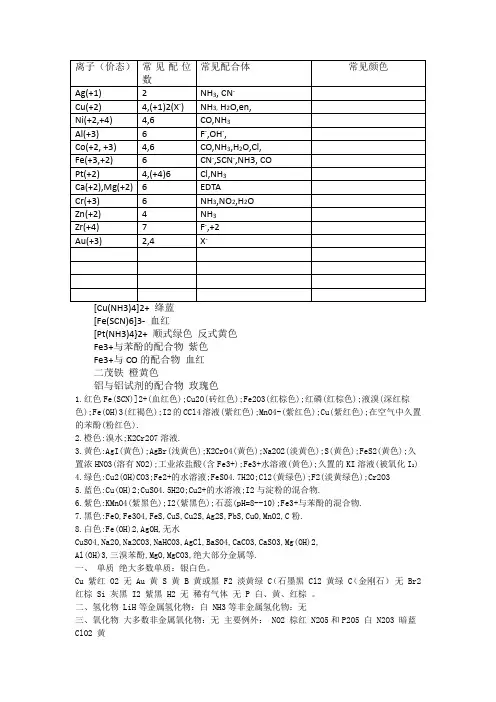
[Fe(SCN)6]3- 血红[Pt(NH3)4}2+ 顺式绿色反式黄色Fe3+与苯酚的配合物紫色Fe3+与CO的配合物血红二茂铁橙黄色铝与铝试剂的配合物玫瑰色1.红色Fe(SCN)]2+(血红色);Cu2O(砖红色);Fe2O3(红棕色);红磷(红棕色);液溴(深红棕色);Fe(OH)3(红褐色);I2的CCl4溶液(紫红色);MnO4-(紫红色);Cu(紫红色);在空气中久置的苯酚(粉红色).2.橙色:溴水;K2Cr2O7溶液.3.黄色:AgI(黄色);AgBr(浅黄色);K2CrO4(黄色);Na2O2(淡黄色);S(黄色);FeS2(黄色);久置浓HNO3(溶有NO2);工业浓盐酸(含Fe3+);Fe3+水溶液(黄色);久置的KI溶液(被氧化I2)4.绿色:Cu2(OH)CO3;Fe2+的水溶液;FeSO4.7H2O;Cl2(黄绿色);F2(淡黄绿色);Cr2O35.蓝色:Cu(OH)2;CuSO4.5H2O;Cu2+的水溶液;I2与淀粉的混合物.6.紫色:KMnO4(紫黑色);I2(紫黑色);石蕊(pH=8--10);Fe3+与苯酚的混合物.7.黑色:FeO,Fe3O4,FeS,CuS,Cu2S,Ag2S,PbS,CuO,MnO2,C粉.8.白色:Fe(OH)2,AgOH,无水CuSO4,Na2O,Na2CO3,NaHCO3,AgCl,BaSO4,CaCO3,CaSO3,Mg(OH)2,Al(OH)3,三溴苯酚,MgO,MgCO3,绝大部分金属等.一、单质绝大多数单质:银白色。
Cu 紫红 O2 无 Au 黄 S 黄 B 黄或黑 F2 淡黄绿 C(石墨黑 Cl2 黄绿 C(金刚石)无 Br2 红棕 Si 灰黑 I2 紫黑 H2 无稀有气体无 P 白、黄、红棕。
二、氢化物 LiH等金属氢化物:白 NH3等非金属氢化物:无三、氧化物大多数非金属氧化物:无主要例外: NO2 棕红 N2O5和P2O5 白 N2O3 暗蓝ClO2 黄大多数主族金属的氧化物:白主要例外: Na2O2浅黄 PbO 黄 K2O 黄 Pb3O4 红 K2O2 橙Rb2O 亮黄 Rb2O2 棕 Cs2O 橙红 Cs2O2 黄大多数过渡元素氧化物有颜色 MnO 绿 CuO 黑MnO2黑 Ag2O 棕黑 FeO 黑 ZnO 白 Fe3O4 黑 Hg2O 黑 Fe2O3 红棕 HgO 红或黄 Cu2O 红V2O5 橙四、氧化物的水化物大多数:白色或无色其中酸:无色为主碱:白色为主主要例外: CsOH 亮黄 Fe(OH)3红褐 HNO2 溶液亮蓝 Cu(OH)2 蓝 Hg(OH)2 桔红五、盐大多数白色或无色主要例外: K2S 棕黄 CuFeS2 黄 KHS 黄 ZnS 白 Al2S3 黄 Ag2S 黑 MnS 浅红 CdS 黄 FeS 黑棕 SnS 棕 FeS2 黄 Sb2S3 黑或橙红 CoS 黑 HgS 红 NiS 黑PbS 黑 CuS、Cu2S 黑 Bi2S3 黑FeCl3·6H2O 棕黄 Na3P 红FeSO4·9H2O 蓝绿 NaBiO3 黄Fe2(SO4)3·9H2O 棕黄 MnCl2 粉红 Fe3C 灰 MnSO4 淡红 FeCO3 灰 Ag2CO3 黄 Fe(SCN)3 暗红 Ag3PO4 黄 CuCl2 棕黄 AgF 黄CuCl2·7H2O 蓝绿 AgCl 白 CuSO4 白 AgBr 浅黄CuSO4·5H2O 蓝 AgI 黄 Cu2(OH)2CO3 暗绿盐溶液中离子特色: NO2- 浅黄 Cu2+或[Cu (H2O)4]2+ 蓝 MnO4- 紫红 [CuCl4]2-黄 MnO42-绿 [Cu(NH3)4]2+深蓝 Cr2O72-橙红 Fe2+ 浅绿 CrO42- 黄 Fe3+ 棕黄非金属互化物 PCl3 无 XeF2、XeF4、XeF6 无 PCl5 浅黄氯水黄绿 CCl4 无溴水黄—橙 CS2 无碘水黄褐 SiC 无或黑溴的有机溶液橙红—红棕SiF4 无 I2的有机溶液紫红六.其它甲基橙橙 CXHY(烃)、CXHYOZ 无(有些固体白色)石蕊试液紫大多数卤代烃无(有些固体白色)石蕊试纸蓝或红果糖无石蕊遇酸变红葡萄糖白石蕊遇碱变蓝蔗糖无酚酞无麦芽糖白酚酞遇碱红淀粉白蛋白质遇浓HNO3变黄纤维素白I2遇淀粉变蓝 TNT 淡黄 Fe3+遇酚酞溶液紫焰色反应 Li 紫红 Ca 砖红 Na 黄 Sr 洋红 K 浅紫(通过蓝色钴玻璃) Ba 黄绿 Rb 紫 Cu 绿稀有气体放电颜色 He 粉红 Ne 鲜红 Ar 紫V,Ti及其化合物:黄色的CrO42-,紫色的MnO4-.二氧化钛(金红石),TiCl3紫色粉末状固体,V2O5砖红色或橙黄色粉末,淡黄色的钒二氧基VO2+,VO2+蓝色,黄色的二过氧钒酸根阴离子[VO2(O2)2]3-,红棕色的过氧钒阳离子[V(O2)]3+,Cr,Mo,W:Cr2O3绿色固体,Cr(OH)3灰蓝色胶状沉淀,Cr3+紫色,CrO2−绿色,CrO42−黄色硫酸铬因含结晶水数量不同而有不同颜色:Cr2(SO4)3·18H2O紫色,Cr2(SO4)3·6H2O绿色, Cr2(SO4)3棕红。