化妆品中10种着色剂的检测方法
- 格式:doc
- 大小:203.00 KB
- 文档页数:6

化妆品中抗坏血酸磷酸酯镁等11种原料的检验方法咱今天就来说说化妆品中抗坏血酸磷酸酯镁等 11 种原料的检验方法。
嘿,你可别小瞧了这些个检验方法,那可真是相当重要呢!想象一下,你每天往脸上涂的那些化妆品,要是里面的这些原料有问题,那会咋样?是不是有点吓人?所以啊,检验方法就得靠谱!首先呢,对于抗坏血酸磷酸酯镁的检验,得用专门的试剂和仪器。
就好像医生看病得有合适的工具一样,咱这检验也不能含糊。
得精确地测量出它的含量,看看是不是符合标准。
这就好比你挑水果,得挑个又甜又好的,不能随便拿一个就完事儿了。
还有其他那 10 种原料,每种都有自己独特的检验方式呢!有的需要在特定的温度下进行,有的需要特定的酸碱度。
这就跟人一样,每个人都有自己的脾气和特点。
比如说其中一种原料,它就特别“娇气”,检验的时候得小心翼翼的,稍微有点差错,结果可能就不准确啦。
这可真是考验检验人员的技术和耐心啊!再想想,如果没有这些严格的检验方法,那些不良商家不就可以随便往化妆品里加些乱七八糟的东西了吗?那我们的脸还不得遭殃啊!所以说啊,这些检验方法就是我们的保护神!它们能确保我们用的化妆品是安全可靠的。
就像一把锁,把那些不好的东西都挡在外面。
咱平时买化妆品的时候,也得留个心眼儿。
看看包装上有没有相关的检验标志,这也是对自己负责呀!别光看广告打得响不响,那些可不一定靠谱呢!总之,化妆品中抗坏血酸磷酸酯镁等 11 种原料的检验方法那是相当重要啊!可不能马虎!咱得好好重视起来,这样才能让我们的脸蛋儿美美的,还不用担心有啥问题。
这多好呀!大家说是不是这个理儿?。
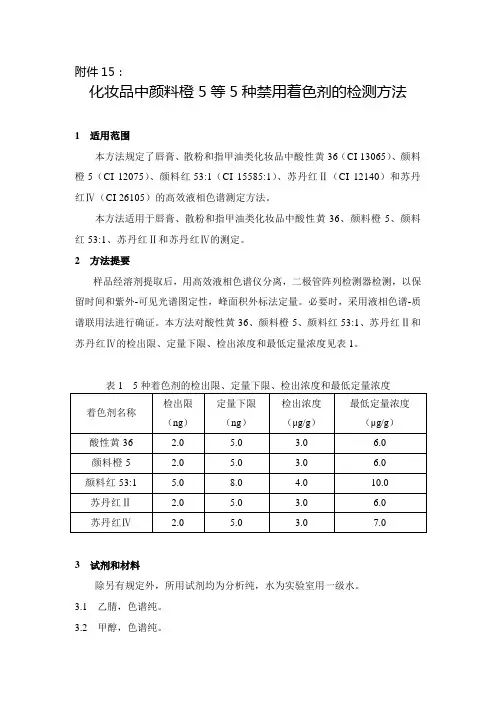
附件15:化妆品中颜料橙5等5种禁用着色剂的检测方法1 适用范围本方法规定了唇膏、散粉和指甲油类化妆品中酸性黄36(CI 13065)、颜料橙5(CI 12075)、颜料红53:1(CI 15585:1)、苏丹红Ⅱ(CI 12140)和苏丹红Ⅳ(CI 26105)的高效液相色谱测定方法。
本方法适用于唇膏、散粉和指甲油类化妆品中酸性黄36、颜料橙5、颜料红53:1、苏丹红Ⅱ和苏丹红Ⅳ的测定。
2 方法提要样品经溶剂提取后,用高效液相色谱仪分离,二极管阵列检测器检测,以保留时间和紫外-可见光谱图定性,峰面积外标法定量。
必要时,采用液相色谱-质谱联用法进行确证。
本方法对酸性黄36、颜料橙5、颜料红53:1、苏丹红Ⅱ和苏丹红Ⅳ的检出限、定量下限、检出浓度和最低定量浓度见表1。
表1 5种着色剂的检出限、定量下限、检出浓度和最低定量浓度3 试剂和材料除另有规定外,所用试剂均为分析纯,水为实验室用一级水。
3.1 乙腈,色谱纯。
3.2 甲醇,色谱纯。
3.3 四氢呋喃,色谱纯。
3.4 二甲基亚砜。
3.5 乙醇,色谱纯。
3.6 四丁基氢氧化铵,浓度为55%。
3.7 柠檬酸。
3.8 氨水,浓度为25~28%。
3.9 酸性黄36,纯度≥99%。
3.10 苏丹红Ⅳ,纯度≥94%。
3.11 苏丹红Ⅱ,纯度≥90%。
3.12 颜料橙5,纯度≥97%。
3.13 颜料红53:1,纯度≥95%。
3.14 酸性黄36标准储备溶液(ρ=500 μg/mL):称取酸性黄36(3.9)对照品50 mg(精确至0.1 mg),置于100 mL容量瓶中,用甲醇(3.2)溶解并稀释至刻度,摇匀,即得500 μg/ mL的标准储备溶液。
3.15 苏丹红Ⅳ标准储备溶液(ρ=500 μg/mL):称取苏丹红Ⅳ(3.10)对照品50 mg(按实际含量折算,精确至0.1 mg),置于100 mL容量瓶中,用四氢呋喃(3.3)和乙腈(3.1)混合液(体积比1:9)溶解并稀释至刻度,摇匀,即得500 μg/ mL的标准储备溶液。

高效液相色谱法检测化妆品中着色剂罗丹明B、金光红C和颜料红57田富饶;杨委;杨兰花;孙文闪【摘要】采用N,N-二甲基甲酰胺提取样品中的待测物,建立了化妆品中禁、限用着色剂罗丹明B、颜料红57和金光红C的高效液相色谱检测方法.以XDB-C18柱为分析柱,5 mmol/L四丁基氢氧化铵-氢氧化钾水溶液(磷酸调至pH 7.00)和甲醇为流动相,梯度洗脱,550 nm(罗丹明B)和480 nm(颜料红57和金光红C)为检测波长,柱温30°C,流速1.0 mL/min,保留时间定性,外标法定量.结果表明在0.25~20 mg/L(罗丹明B和金光红C)、0.5~40mg/L(颜料红57)浓度范围内线性关系良好,检出限分别为5,20,20 mg/kg(S/N=10),实际样品中的加标回收率分别为94.8%~100.5%,95.1%~103.1%,82.5%~90.5%,相对标准偏差为0.9%~4.6%.该方法前处理简单、易操作,检测结果准确可靠,能够满足化妆品中这3种着色剂的检测要求和监管需要.%The cosmetic samples were extracted by DMF, a quantitative detection method for determination of Rhodamine B, Lake Red C and Pigment Red 57, which were forbidden or limited to be used in cosmetics was established by high performance liquid chromatography with diode array detector. The target compounds were separated on a XDB-C18 column in gradient elution mode using 5 mmol/L tetrabutylammonium hydroxide and K.OH aqueous solution (pH 7.00, adjusted by phosphoric acid) and methanol as mobile phase. The detective wavelength was 550 nm for Rhodamine B and 480 nm for Pigment Red 57 and Lake Red C, and the column temperature was 30℃ while the flow rate of the mobile phase was 1.0 mL/min. Under the optimal chromatographicconditions, the three colorants were analyzed qualitatively based on its retention time while the quantitative analysis was carried out by external standard method. The calibration plot of peak area versus concentration showed good linearity between 0.25 and 20.0 mg/L for Rhodamine B and Lake Red C ,0.5-40.0 mg / L for Pigment Red 57, the correlation coefficients were more than 0.999 9, the detection limits and recoveries of Rhodamine B, Lake Red C and Pigment Red 57 were 5,20,20 mg/kg ( S/N=l0 ) and 94.8%-100.5%, 95.1%-103.1%, 82.5%-90.5%, respectively. The relative standard deviation was 0.9%-4.6%. The results indicated that the developed method is sample, rapid, accurate and suitable for the detection of three colorants in cosmetics samples and requirements of supervision.【期刊名称】《化学分析计量》【年(卷),期】2012(021)006【总页数】4页(P36-39)【关键词】化妆品;着色剂;罗丹明B;颜料红57;金光红C【作者】田富饶;杨委;杨兰花;孙文闪【作者单位】义乌出入境检验检验局,浙江义乌 322000;义乌出入境检验检验局,浙江义乌 322000;义乌出入境检验检验局,浙江义乌 322000;义乌出入境检验检验局,浙江义乌 322000【正文语种】中文【中图分类】O657.7+2随着我国国民经济的蓬勃发展和人民生活水平的不断提高,化妆品逐步从奢侈品转变为日常生活的必需品。

化妆品中色素安全性检验流程及标准规定化妆品中的色素是为了增加产品的色彩和吸引力而添加的,但不同的色素成分可能存在安全隐患。
因此,对于化妆品中使用的色素,需要进行安全性检验。
下面将介绍一下色素安全性检验流程及标准规定。
色素安全性检验流程分为以下几个步骤:第一步:确定色素的实际用途。
在进行安全性检验之前,需要明确色素在化妆品中的具体用途,例如颜料、调整颜色等。
这有助于确定检验的重点和标准。
第二步:选择适当的检测方法。
对于色素的安全性检验,通常采用实验室研究和临床评估两种方法。
实验室研究可以通过体外试验和动物试验来评估色素对皮肤的敏感性和刺激性。
而临床评估则是通过人类试验评估色素在人体上的反应和影响。
第三步:进行实验室研究。
实验室研究可以通过使用细胞培养、皮肤透过性试验等方法来评估色素的毒性和生物相容性。
细胞培养可以通过观察色素对细胞的影响来判断其潜在的有害作用。
皮肤透过性试验则可以模拟色素在皮肤中的渗透情况,评估其对皮肤的刺激性和敏感性。
第四步:进行动物试验。
动物试验可以通过给小鼠、兔子等实验动物涂抹色素并观察其反应来评估色素的刺激性和毒性。
这种试验主要关注色素在动物身上的消化、吸收和代谢情况。
第五步:进行临床评估。
临床评估是将色素应用到人体上,并通过观察个体的反应和改变来评估色素的安全性。
这一步骤通常需要招募一批志愿者,将色素应用于他们的皮肤上,并观察其对色素的反应。
色素安全性检验的标准规定主要包括以下几个方面:1. 刺激性和敏感性。
色素在化妆品中使用时,应确保不对皮肤和眼睛造成刺激和过敏。
对于化妆品中使用的色素,其刺激性和敏感性成分应符合相关标准规定。
2. 毒性。
色素应保证在使用量和浓度限制范围内不对人体造成毒性作用。
毒性测试主要包括急性毒性、亚慢性毒性和慢性毒性等实验。
3. 致畸性和致突变性。
色素在化妆品中的使用应确保不对胚胎、胎儿和遗传物质造成损害。
4. 长期稳定性。
色素在储存和使用过程中应保持其色彩和化学稳定性,不会产生有害物质或导致产品质量下降。
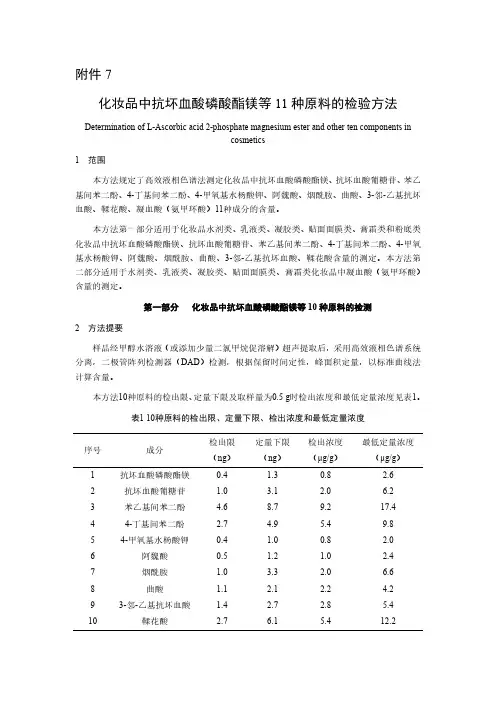
附件7化妆品中抗坏血酸磷酸酯镁等11种原料的检验方法Determination of L-Ascorbic acid2-phosphate magnesium ester and other ten components incosmetics1范围本方法规定了高效液相色谱法测定化妆品中抗坏血酸磷酸酯镁、抗坏血酸葡糖苷、苯乙基间苯二酚、4-丁基间苯二酚、4-甲氧基水杨酸钾、阿魏酸、烟酰胺、曲酸、3-邻-乙基抗坏血酸、鞣花酸、凝血酸(氨甲环酸)11种成分的含量。
本方法第一部分适用于化妆品水剂类、乳液类、凝胶类、贴面面膜类、膏霜类和粉底类化妆品中抗坏血酸磷酸酯镁、抗坏血酸葡糖苷、苯乙基间苯二酚、4-丁基间苯二酚、4-甲氧基水杨酸钾、阿魏酸、烟酰胺、曲酸、3-邻-乙基抗坏血酸、鞣花酸含量的测定。
本方法第二部分适用于水剂类、乳液类、凝胶类、贴面面膜类、膏霜类化妆品中凝血酸(氨甲环酸)含量的测定。
第一部分化妆品中抗坏血酸磷酸酯镁等10种原料的检测2方法提要样品经甲醇水溶液(或添加少量二氯甲烷促溶解)超声提取后,采用高效液相色谱系统分离,二极管阵列检测器(DAD)检测,根据保留时间定性,峰面积定量,以标准曲线法计算含量。
本方法10种原料的检出限、定量下限及取样量为0.5g时检出浓度和最低定量浓度见表1。
表110种原料的检出限、定量下限、检出浓度和最低定量浓度序号成分检出限(ng)定量下限(ng)检出浓度(μg/g)最低定量浓度(μg/g)1抗坏血酸磷酸酯镁0.4 1.30.8 2.6 2抗坏血酸葡糖苷 1.0 3.1 2.0 6.2 3苯乙基间苯二酚 4.68.79.217.4 44-丁基间苯二酚 2.7 4.9 5.49.8 54-甲氧基水杨酸钾0.4 1.00.8 2.0 6阿魏酸0.5 1.2 1.0 2.4 7烟酰胺 1.0 3.3 2.0 6.6 8曲酸 1.1 2.1 2.2 4.2 93-邻-乙基抗坏血酸 1.4 2.7 2.8 5.4 10鞣花酸 2.7 6.1 5.412.23试剂和材料除另有规定外,本方法所用试剂均为分析纯,水为GB/T6682规定的一级水。

附件3化妆品中10种着色剂的检测方法1 适用范围本方法规定了化妆品中CI16185、CI16255、CI16035、CI14700、CI45380、CI15510、CI59040、橙黄Ⅰ、CI15985、CI10316着色剂含量的高效液相色谱测定方法和橙黄Ⅰ的阳性结果确证方法。
本方法适用于胭脂、口红、粉底、指甲油、睫毛膏、眼影等修饰类化妆品中CI16185、CI16255、CI16035、CI14700、CI45380、CI15510、CI59040、橙黄Ⅰ、CI15985、CI10316含量的测定。
2 方法提要试样经甲醇超声提取后, 过0.45 μm滤膜, 采用高效液相色谱系统分离, 二极管阵列检测器进行检测, 外标法定量。
本方法的检出限、定量下限和取样品5.0 g时的检出浓度、定量浓度见表1。
表1 各种着色剂的检出限和检出浓度着色剂索引号着色剂索引通用中文名CAS号检出限( μg)定量下限( μg)检出浓度( μg/g)定量浓度( μg/g)CI 16185 食品红9 915-67-3 0.3 1.0 0.06 0.20 CI 16255 食品红7 1390-65-4 0.3 1.0 0.06 0.20 CI 16035 食品红17 25956-17-6 0.3 1.0 0.06 0.20CI 14700 食品红1 4548-53-2 0.3 1.0 0.06 0.20CI 45380 酸性红87 548-26-5 0.3 1.0 0.06 0.20CI 15510 酸性橙7 633-96-5 0.3 1.0 0.06 0.20CI 59040 溶剂绿7 6358-69-6 5.0 16.5 1.0 3.3——橙黄Ⅰ523-44-4 5.0 16.5 1.0 3.3CI 15985 食品黄3 2783-94-0 15.0 50.0 3.0 10.0CI 10316 酸性黄1 846-70-8 15.0 50.0 3.0 10.03试剂和材料除另有规定外, 所用试剂均为色谱纯, 水为一级水。
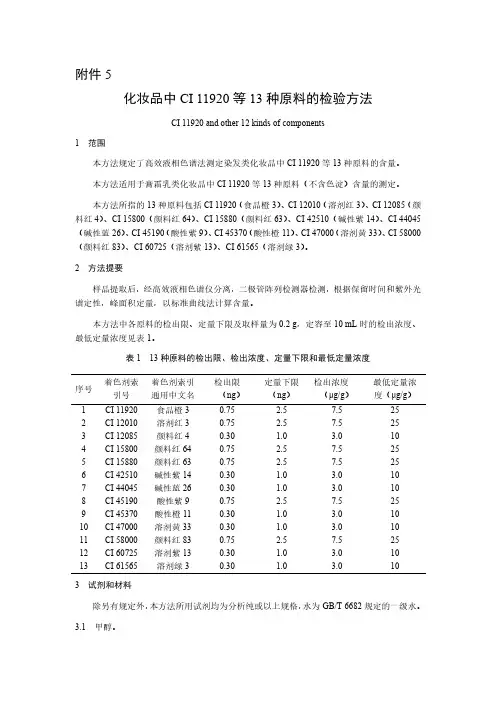
附件5化妆品中CI11920等13种原料的检验方法CI11920and other12kinds of components1范围本方法规定了高效液相色谱法测定染发类化妆品中CI11920等13种原料的含量。
本方法适用于膏霜乳类化妆品中CI11920等13种原料(不含色淀)含量的测定。
本方法所指的13种原料包括CI11920(食品橙3)、CI12010(溶剂红3)、CI12085(颜料红4)、CI15800(颜料红64)、CI15880(颜料红63)、CI42510(碱性紫14)、CI44045(碱性蓝26)、CI45190(酸性紫9)、CI45370(酸性橙11)、CI47000(溶剂黄33)、CI58000(颜料红83)、CI60725(溶剂紫13)、CI61565(溶剂绿3)。
2方法提要样品提取后,经高效液相色谱仪分离,二极管阵列检测器检测,根据保留时间和紫外光谱定性,峰面积定量,以标准曲线法计算含量。
本方法中各原料的检出限、定量下限及取样量为0.2g,定容至10mL时的检出浓度、最低定量浓度见表1。
表113种原料的检出限、检出浓度、定量下限和最低定量浓度序号着色剂索引号着色剂索引通用中文名检出限(ng)定量下限(ng)检出浓度(μg/g)最低定量浓度(μg/g)1CI11920食品橙30.75 2.57.5252CI12010溶剂红30.75 2.57.5253CI12085颜料红40.30 1.0 3.0104CI15800颜料红640.75 2.57.5255CI15880颜料红630.75 2.57.5256CI42510碱性紫140.30 1.0 3.0107CI44045碱性蓝260.30 1.0 3.0108CI45190酸性紫90.75 2.57.5259CI45370酸性橙110.30 1.0 3.01010CI47000溶剂黄330.30 1.0 3.01011CI58000颜料红830.75 2.57.52512CI60725溶剂紫130.30 1.0 3.01013CI61565溶剂绿30.30 1.0 3.0103试剂和材料除另有规定外,本方法所用试剂均为分析纯或以上规格,水为GB/T6682规定的一级水。
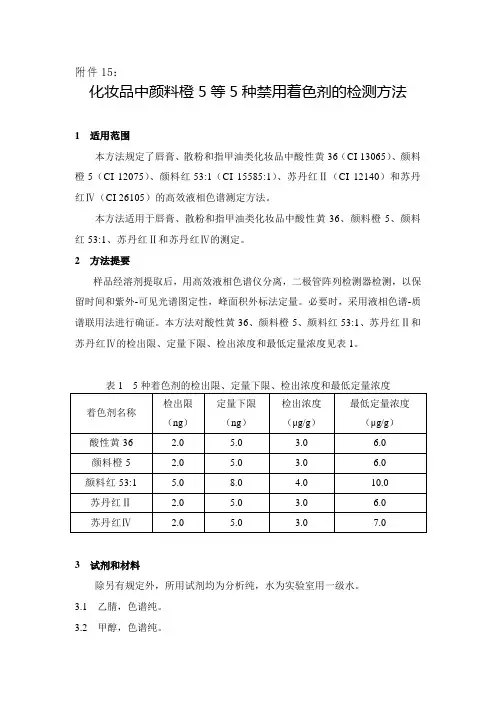
附件15:化妆品中颜料橙5等5种禁用着色剂的检测方法1 适用范围本方法规定了唇膏、散粉和指甲油类化妆品中酸性黄36(CI 13065)、颜料橙5(CI 12075)、颜料红53:1(CI 15585:1)、苏丹红Ⅱ(CI 12140)和苏丹红Ⅳ(CI 26105)的高效液相色谱测定方法。
本方法适用于唇膏、散粉和指甲油类化妆品中酸性黄36、颜料橙5、颜料红53:1、苏丹红Ⅱ和苏丹红Ⅳ的测定。
2 方法提要样品经溶剂提取后,用高效液相色谱仪分离,二极管阵列检测器检测,以保留时间和紫外-可见光谱图定性,峰面积外标法定量。
必要时,采用液相色谱-质谱联用法进行确证。
本方法对酸性黄36、颜料橙5、颜料红53:1、苏丹红Ⅱ和苏丹红Ⅳ的检出限、定量下限、检出浓度和最低定量浓度见表1。
表1 5种着色剂的检出限、定量下限、检出浓度和最低定量浓度3 试剂和材料除另有规定外,所用试剂均为分析纯,水为实验室用一级水。
3.1 乙腈,色谱纯。
3.2 甲醇,色谱纯。
3.3 四氢呋喃,色谱纯。
3.4 二甲基亚砜。
3.5 乙醇,色谱纯。
3.6 四丁基氢氧化铵,浓度为55%。
3.7 柠檬酸。
3.8 氨水,浓度为25~28%。
3.9 酸性黄36,纯度≥99%。
3.10 苏丹红Ⅳ,纯度≥94%。
3.11 苏丹红Ⅱ,纯度≥90%。
3.12 颜料橙5,纯度≥97%。
3.13 颜料红53:1,纯度≥95%。
3.14 酸性黄36标准储备溶液(ρ=500 μg/mL):称取酸性黄36(3.9)对照品50 mg(精确至0.1 mg),置于100 mL容量瓶中,用甲醇(3.2)溶解并稀释至刻度,摇匀,即得500 μg/ mL的标准储备溶液。
3.15 苏丹红Ⅳ标准储备溶液(ρ=500 μg/mL):称取苏丹红Ⅳ(3.10)对照品50 mg(按实际含量折算,精确至0.1 mg),置于100 mL容量瓶中,用四氢呋喃(3.3)和乙腈(3.1)混合液(体积比1:9)溶解并稀释至刻度,摇匀,即得500 μg/ mL的标准储备溶液。

纯化化妆品中的着色剂成分化妆品是人们日常生活中不可或缺的一部分。
它们有助于人们改善外貌,塑造自信和美丽。
然而,我们在选择化妆品时,往往会被各种花样繁多的着色剂成分所迷惑。
着色剂是化妆品中常见的添加剂,用于增加产品的吸引力和消费者的购买欲望。
本文将探讨纯化化妆品中的着色剂成分以及对人体健康的潜在风险。
着色剂是用来给化妆品赋予颜色的化学物质。
它们可以在化妆品中起到突出特定颜色、改善外观和提高产品吸引力的作用。
常见的着色剂成分包括红色、黄色、蓝色和绿色染料,如甲基红、氧化铁、铬氧化绿等。
这些着色剂成分被广泛用于化妆品中的眼影、腮红、唇膏等产品中。
然而,纯化化妆品中的着色剂成分可能存在潜在的健康风险。
一些着色剂成分可能含有重金属汞、铅和镉等有害物质。
这些有害物质一旦被人体吸收,可能会对身体产生负面影响。
据研究表明,长期接触高含量重金属的化妆品可能导致皮肤刺激、过敏反应和激素失调等问题。
尤其是对于孕妇和婴儿来说,这些有害物质的潜在风险更为严重。
为了确保消费者的健康与安全,各国都制定了严格的化妆品安全标准和监管措施。
例如,欧盟颁布了《化妆品法规》,规定了化妆品中所使用的着色剂成分的限量要求和安全标准。
在美国,食品药品监督管理局(FDA)也对化妆品中的着色剂成分进行了监管,并制定了一系列的安全限量。
此外,消费者在选择化妆品时,也可以通过一些方法来避免潜在的健康风险。
首先,要注意产品的标签,选择那些明确标明成分和含量的产品。
其次,可以选择纯化化妆品,即不含有机溶剂或化学添加剂的产品。
另外,多了解有关该品牌的背景和口碑,选择有信誉和口碑的品牌也是一种有效的方法。
总之,纯化化妆品中的着色剂成分是化妆品中常见的添加剂。
虽然它们可以给产品带来视觉上的吸引力,但消费者在选择化妆品时应当注意其潜在的健康风险。
对于化妆品企业来说,应该加强对着色剂成分的研发和安全性评估,确保产品的安全和有效。
对于消费者来说,选择合格和安全的化妆品是保护自己健康的重要措施。

化妆品中苯酚、氢醌的测定方法苯酚(C6H5OH)分子量94.11,是简单的一元酚。
无色、易挥发、具有恶臭味、沸点182℃,能溶于水,并能以任何比例与醇相溶。
氢醌〔C6H4(OH)2〕分子量110.10,二元酚,为白色晶体。
沸点286.2℃,能溶干水,并能以任何比例与醇相溶。
氢醌、苯酚二者均具有一定毒性,人体接触过多易引起白血病和心脏病。
氢醌、苯酚在祛斑类化妆品中为禁用物质。
但可在染发用的氧化着色剂及香波产品中限量使用。
我国化妆品卫生标准规定其限用量分别为:染发剂中氢醌2%;洗发香波中酚1%。
氢醌、苯酚可用气相色谱和比色法分别进行测定。
本法采用高效液相色谱,一次进样同时测定二个化合物。
本方法简单,分离效果好,灵敏度也较高(1)。
1应用范围本法适用于测定祛斑类、洗发类及染发用氧化着色剂中的氢醌、苯酚。
苯酚最低检测量为0.03μg,氢醌最低检测量为0.06μg。
2原理以甲醇提取化妆品中氢醌、苯酚,用高效液相色谱进行分析,以保留时间定性,以标准品峰高或峰面积进行定量。
3试剂3.1甲醇优级纯3.2氢醌标准溶液:准确称取0.1000g氢醌置于烧杯中,用少量甲醇(3.1)溶解后移至100ml容量瓶中,用甲醇稀释至刻度。
此标准溶液浓度为1.00mg/ml,可稳定一个月。
3.3苯酚标准溶液:准确称取0.1000g苯酚置于烧杯中,用少量甲醇(3.1),溶解后移至100ml溶量瓶中,用甲醇稀释至刻度。
此标准溶液浓度为1.00mg/ml,可稳定一个月。
3.4氢醌、苯酚混合标准溶液:分别取20.0ml氢醌标准溶液(3.2)、50.0ml 苯酚标准溶液(3.3)置于100ml容量瓶中,加甲醇至刻度,此溶液1.0ml分别含氢醌、苯酚0.20mg、0.20mg。
4仪器4.1高效液相色谱仪。
4.2振荡器。
4.3超声波清洗机。
5分析步骤5.1样品预处理称取检测样品1~2g于三角瓶中,在水浴上馏除有机溶剂。
用甲醇稀释至20ml振荡10min(2),超声15min,取上清液过0.45μm滤膜后备用。

简述人工着色剂的常用测定方法
人工着色剂广泛应用于食品、化妆品、纺织品等领域,因此对其进行准确测定十分必要。
常用的人工着色剂测定方法包括光度法、高效液相色谱法、气相色谱法等。
光度法是一种常用的人工着色剂测定方法,它利用分光光度计测定样品中着色剂的吸光度来计算其浓度。
该方法简单快速,适用于许多人工着色剂的测定。
高效液相色谱法(HPLC)是另一种常用的人工着色剂测定方法,它采用高压泵将样品通过一根特定的柱子,通过柱子的色谱分离作用来分离出人工着色剂。
该方法准确可靠,适用于许多人工着色剂的测定。
气相色谱法(GC)是一种基于气相色谱技术的人工着色剂测定方法,其原理是利用样品的挥发性物质在特定条件下分离和分析。
该方法对样品的纯度要求较高,但准确度和灵敏度较高,适用于许多人工着色剂的测定。
综上所述,人工着色剂的测定方法较多,选择合适的测定方法需要根据不同的样品性质和要求进行选择。
- 1 -。
化妆品中ci 10020等11种原料的检验方法一、CI 10020的检验方法1.检验步骤(1)外观检验:观察样品的颜色、气味和质地,检查有无异物或沉淀物。
(2)PH值检验:使用PH试纸或PH仪器测量样品的PH值,通常CI 10020的PH值为5.5-6.5。
(3)纯度检验:通过对样品进行色谱分析、质谱分析等方法来检测CI 10020的纯度。
2.常见问题及处理方法(1)颜色异常:如果发现CI 10020的颜色异常,可以通过色谱分析来检测其中可能的杂质,并采取相应的处理方法。
(2)PH值偏离:如果测得的PH值偏离了正常范围,可能是因为样品中含有酸碱度较大的物质,可以通过中和或稀释来调整PH值。
(3)其他异常:如果出现其他异常情况,需要通过多种分析方法来确定问题所在,并采取相应的处理方法。
3.相关检验设备色谱仪、质谱仪、PH试纸、PH仪器等。
二、CI 10021的检验方法1.检验步骤(1)外观检验:观察样品的颜色、气味和质地,检查有无异物或沉淀物。
(2)纯度检验:通过色谱分析、质谱分析等方法来检测CI 10021的纯度。
(3)稳定性检验:样品在不同温度、光照条件下的稳定性测试,以确定其在不同环境下的表现。
2.常见问题及处理方法(1)纯度不足:如果发现CI 10021的纯度不足,可以通过色谱分析来检测其中可能的杂质,并采取相应的处理方法。
(2)不稳定:如果样品在不同环境条件下表现不稳定,需要重新调整配方或添加稳定剂来改善产品性能。
3.相关检验设备色谱仪、质谱仪、恒温箱、光照箱等。
三、CI 10022的检验方法1.检验步骤(1)外观检验:观察样品的颜色、气味和质地,检查有无异物或沉淀物。
(2)纯度检验:通过色谱分析、质谱分析等方法来检测CI 10022的纯度。
(3)安全性检验:对CI 10022进行皮肤刺激、眼部刺激等测试,以确定其对人体的安全性。
2.常见问题及处理方法(1)纯度不足:可以通过色谱分析来检测其中可能的杂质,并采取相应的处理方法。
常用着色剂标准着色剂检测范围:食品着色剂、火腿着色剂、天然着色剂、有机着色剂、混凝土着色剂、复配着色剂、塑料着色剂、合成着色剂、饲料着色剂、石材着色剂、水性着色剂、无机着色剂等。
1、SN/T 4575-2016 出口化妆品中多种禁限用着色剂的测定高效液相色谱法和液相色谱-串联质谱法2、GB/T 37545-2019 化妆品中38种准用着色剂的测定高效液相色谱法3、GB/T 34806-2017 化妆品中13种禁用着色剂的测定高效液相色谱法4、GB 5009.35-2016 食品安全国家标准食品中合成着色剂的测定5、JIS L1940-1-2019 纺织品. 某些来自偶氮着色剂的芳香胺的测定方法. 第1部分: 不论是否提取纤维的情形下均可使用的某些偶氮着色剂的用法检测6、GB/T 30927-2014 化妆品中罗丹明B等4种禁用着色剂的测定高效液相色谱法7、GB/T 9695.6-2008 肉制品.胭脂红着色剂测定8、SN/T 4457-2016 出口饮料、冰淇淋等食品中11种合成着色剂的检测液相色谱法9、GB/T 5009.35-2003 食品中合成着色剂的测定10、GB/T 21916-2008 水果罐头中合成着色剂的测定.高效液相色谱法11、JIS L1940-3-2019 纺织品. 某些来自偶氮着色剂的芳香胺的测定方法. 第3部分: 可释放4-氨基偶氮苯的某些偶氮着色剂的用法检测12、GB/T 31858-2015 眼部护肤化妆品中禁用水溶性着色剂酸性黄1和酸性橙7的测定高效液相色谱法13、ISO 14362-1-2017 纺织品. 源于偶氮着色剂的某些芳香胺的测定方法. 第1部分: 通过或未经萃取纤维获得某些偶氮着色剂的使用检测14、BS EN ISO 14362-3-2017 纺织品.源于偶氮着色剂的某些芳香胺的测定方法. 某些可能释放4-氨基偶氮苯的偶氮着色剂使用检测15、GB 7300.901-2019 饲料添加剂第9部分:着色剂β-胡萝卜素粉16、GB/T 13787-1992 纺织纤维鉴别试验方法着色剂法。
化妆品中10种着色剂的检测方法1适用范围本方法规定了化妆品中CI16185、CI16255、CI16035、CI14700、CI45380、CI15510、CI59040、橙黄I、CI15985、CI10316着色剂含量的高效液相色谱测定方法和橙黄I的阳性结果确证方法。
本方法适用于胭脂、口红、粉底、指甲油、睫毛膏、眼影等修饰类化妆品中CI16185、CI16255、CI16035、CI14700、CI45380、CI15510、CI59040、橙黄I、CI15985、CI10316含量的测定。
2方法提要试样经甲醇超声提取后,过0.45gm滤膜,采用高效液相色谱系统分离,二极管阵列检测器进行检测,外标法定量。
本方法的检出限、定量下限和取样品5.0g时的检出浓度、定量浓度见表1。
表1各种着色剂的检出限和检出浓度检出限定量下限检出浓度定量浓度着色剂着色剂索引CAS号索引号通用中文名(gg)(gg)(gg/g)(gg/g)CI16185食品红9915-67-30.3 1.00.060.20CI16255食品红71390-65-40.3 1.00.060.20CI16035食品红1725956-17-60.3 1.00.060.20CI14700食品红14548-53-20.3 1.00.060.20CI45380酸性红87548-26-50.3 1.00.060.20CI15510酸性橙7633-96-50.3 1.00.060.20CI59040溶剂绿76358-69-6 5.016.5 1.0 3.3——橙黄I 523-44-4 5.016.5 1.0 3.3CI15985食品黄32783-94-015.050.0 3.010.0CI10316酸性黄1846-70-815.050.0 3.010.03试剂和材料除另有规定外,所用试剂均为色谱纯,水为一级水。
3.1甲醇。
3.2四氢呋喃。
3.3乙酸铵:分析纯。
着色剂(色素)测验着色剂亦称色素。
化妆品添加着色剂主要是使产品着色,通过消费者的视觉提高产品的吸引力;还可以用来调整原料对产品色调的影响;或者用以区分产品品种等。
着色剂按来源和性质分以下几类:着色剂分为染料和颜料,染料包括天然染料和合成染料,颜料包括无机颜料和有机颜料。
染料一般可溶于水或有机溶剂,具有一定染色能力。
按用途分为酸性染料、碱性染料、氧化染料和油溶性染料等;颜料一般是不溶于水或有机溶剂。
化妆品中使用染料多数是合成染料,其中大部分是以煤干馏的副产品如苯、蒽等为原料,所以称其为焦油色素。
合成染料从结构上可分为下列几种:(1)硝基染料:以硝基为发色团。
随着硝基的增加,颜色加深,一般为黄色。
(2)偶氮染料:以偶氮基为发色团,以偶氮苯为色原体的染料。
占合成染料二分之一左右。
其中构造简单的苯化合物呈黄色、橙色或褐色。
随其含有助色团的不同,又分为以下五类:①含有羟基或羰基,但不含磺酸基的颜料。
②不含羧基、磺酸基的染料。
③含羟基或(和)羧基、磺酸基的不溶性颜料。
④含羟基或(和)磺酸基的染料。
⑤吡唑啉酮型。
(3)亚硝基染料:具有亚硝基的发色团染料,几乎全为绿色。
(4)三苯甲烷染料:甲烷结构的四个氢有三个被苯取代,一般为绿色。
(5)氧杂蒽染料:根据所含功能团分为:①醌型,②酚型,③氨型。
(6)喹啉染料:以喹啉为母体,呈黄色。
(7)蒽醌染料:以蒽醌核为原体,又分为:①含磺酸基,②不含磺酸基。
(8)靛蓝染料。
(9)芘类染料。
(10)酞蓝染料。
化妆品中使用的颜料一般是无机颜料。
无机颜料分有色颜料、白色颜料和体质颜料。
化妆品中常用的有:铁氰化合物、氧化物、硅酸盐、磷酸盐,炭黑和珠光颜料等。
大多数的合成着色剂对动物是有危害的。
有的着色剂会引起人的光敏反应,尤其是某些焦油色素甚至可以诱发癌症。
为了安全起见,世界上有些国家对化妆品用着色剂作了法律性规定。
我国化妆品卫生标准对化妆品用着色剂品种、使用范围和限制条件都作了明确的规定。
附件3
化妆品中10种着色剂的检测方法
1 适用范围
本方法规定了化妆品中CI16185、CI16255、CI16035、CI14700、CI45380、CI15510、CI59040、橙黄Ⅰ、CI15985、CI10316着色剂含量的高效液相色谱测定方法和橙黄Ⅰ的阳性结果确证方法。
本方法适用于胭脂、口红、粉底、指甲油、睫毛膏、眼影等修饰类化妆品中CI16185、CI16255、CI16035、CI14700、CI45380、CI15510、CI59040、橙黄Ⅰ、CI15985、CI10316含量的测定。
2 方法提要
试样经甲醇超声提取后,过0.45 μm滤膜,采用高效液相色谱系统分离,二极管阵列检测器进行检测,外标法定量。
本方法的检出限、定量下限和取样品5.0 g时的检出浓度、定量浓度见表1。
表1 各种着色剂的检出限和检出浓度
着色剂索引号着色剂索引
通用中文名
CAS号
检出限
(μg)
定量下限
(μg)
检出浓度
(μg/g)
定量浓度
(μg/g)
CI 16185 食品红9 915-67-3 0.3 1.0 0.06 0.20 CI 16255 食品红7 1390-65-4 0.3 1.0 0.06 0.20 CI 16035 食品红17 25956-17-6 0.3 1.0 0.06 0.20 CI 14700 食品红1 4548-53-2 0.3 1.0 0.06 0.20 CI 45380 酸性红87 548-26-5 0.3 1.0 0.06 0.20 CI 15510 酸性橙7 633-96-5 0.3 1.0 0.06 0.20 CI 59040 溶剂绿7 6358-69-6 5.0 16.5 1.0 3.3 ——橙黄Ⅰ523-44-4 5.0 16.5 1.0 3.3 CI 15985 食品黄3 2783-94-0 15.0 50.0 3.0 10.0 CI 10316 酸性黄1 846-70-8 15.0 50.0 3.0 10.0 3试剂和材料
除另有规定外,所用试剂均为色谱纯,水为一级水。
3.1 甲醇。
3.2 四氢呋喃。
3.3 乙酸铵:分析纯。
3.4 乙酸铵溶液(0.02 mol/L):称取1.54 g乙酸铵,加水至1000 mL,溶解,经0.45 μm滤膜过滤。
3.5 着色剂:CI16185、CI16255、CI 16035、CI14700、CI 45380、CI15510、CI59040、橙黄Ⅰ、CI15985、CI10316,含量纯度均大于等于90 %。
3.6 着色剂混合标准储备液(1.0 mg/mL):分别称取着色剂标准物质(3.5)0.1 g(精确至0.1 mg)于100 mL容量瓶中,甲醇(3.1)稀释定容。
3.7 着色剂混合标准系列溶液:分别移取一定量的着色剂标准储备液(3.6),用甲醇配制成浓度为5.0、10.0、20.0、30.0、40.0、50.0、100.0 μg/mL的系列标准溶液。
4仪器与设备
4.1 高效液相色谱仪:配二极管阵列检测器。
4.2 液相色谱-三重四极杆串联质谱仪:配电喷雾离子源。
4.3 分析天平:感量分别为0.1 mg和1.0 mg。
4.4 超声波清洗器。
4.5 涡旋混匀器。
4.6 有机微孔滤膜:0.45 μm。
5分析步骤
5.1 样品预处理
准确称取试样5.0 g(精确至1 mg)于25 mL比色管中,加入1.0ml四氢呋喃(3.2),加入20.0 mL甲醇(3.1),在涡旋混匀器上高速振荡5 min,在超声提取30 min后,放置至室温,用甲醇(3.1)定容,摇匀,过0.45 μm滤膜,待测。
5.2色谱参考条件
色谱柱:十八烷基硅烷键合硅胶色谱柱,250 mm×4.6 mm(内径),5 μm;或相当者;
流动相:A相(甲醇)+B相(0.02 mol/L乙酸铵(用乙酸调节pH=4.0)),梯度洗脱程序见表2;
流速:1.0 mL/min;
柱温:30 ℃;
进样量:10 μL;
检测器:二极管阵列检测器;
检测波长:CI59040为245 nm;CI16185、CI16255、CI16035、CI14700、CI45380为520 nm;CI15985、CI10316、橙黄Ⅰ、CI15510为480 nm。
表2 梯度洗脱程序
时间,min 流动相A(%)流动相B(%)
0 5 95
7.5 30 70
15 30 70
25 80 20
30 80 20
30.1 5 95
36 5 95
5.3 测定
本方法采用外标校准曲线法定量测定。
以标准系列溶液浓度为横坐标,峰面积为纵坐标,作标准曲线线性回归方程,以试样的峰面积与标准曲线比较定量。
6 计算
试样中各种着色剂的含量(μg/g),按式(1)计算:
w
C V
m
⨯=
式中:w ——试样中着色剂的含量,μg/g;
C ——试样溶液中着色剂的含量,μg/mL;
V ——提取溶液体积,mL;
m ——样品质量,g。
7 回收率和精密度
多家实验室验证的平均回收率为84.7%~104.6%,相对标准偏差小于6%(n=6)。
8质谱确证
如检出橙黄Ⅰ阳性样品,需经液相色谱-三重四级杆质谱法进行阳性确证。
8.1 前处理过程见5.1
8.2色谱参考条件
色谱柱:十八烷基硅烷键合硅胶色谱柱,100 mm×2.1 mm(内径),1.7 μm,或相当者;
流动相:A相:乙腈+B相20 mmol/L乙酸铵水溶液(用氨水调节pH=8.0);
梯度洗脱程序见表3;
表3 梯度洗脱程序
时间,min 流动相A(%)流动相B(%)
0 5 95
3 5 95
6 30 70
6.01 5 95
8 5 95
流速:0.3 mL/min;
柱温:30 ℃;
进样量:2 μL。
8.3质谱参考条件
离子源:电喷雾离子源(ESI);
扫描方式:负离子扫描;
监测方式:多反应监测模式(MRM);
干燥气:N2;
碰撞气:Ar;
雾化器温度:250℃;
雾化器气流:3.0 L/min;
干燥气气流:15 L/min;
离子化电压:3.5 kv;
脱溶剂气温度:250℃;
加热块温度:400℃;
碰撞气电压:230 KPa。
表4 母离子、特征碎片离子、裂解电压及碰撞能
待测物/母离子(m/z)碎片离子(m/z)碰撞能(V) 碎片离子丰度比
橙黄Ⅰ/327 171 21
27.8% 156 32
8.4定性
用液相色谱-三重四级杆串联质谱仪进行样品定性测定,进行样品测定时,如果样品中橙黄Ⅰ的色谱峰保留时间与浓度相近标准工作溶液相一致(变化范围在±2.5%之内),并且在扣除背景后样品的质谱图中,所选择的检测离子均出现,而且样品中所选择的的离子对相对丰度与标准样品的离子对相对丰度相一致(离子相对丰度比见表4),相对丰度偏差符合表5要求,则可以判断样品中存在橙黄Ⅰ。
表5 相对离子丰度的最大允许偏差
相对离子丰度>50% 20%~50% 10%~20% ≤10%
允许相对偏差±20% ±25% ±30% ±50%
8.5 检出限
本方法对橙黄Ⅰ的检出浓度为1.0 μg/g。
9 色谱图
图1 混合标准溶液在245nm下的高效液相色谱图
1(CI 59040):2.845 min
图2 混合标准溶液在520nm下的高效液相色谱图
1(CI 16185):9.222 min;2(CI 16255):12.364 min;3(CI 16035): 21.280 min;4(CI 14700):
24.863 min;5(CI 45380):26.674 min
图3 混合标准溶液在480nm下的高效液相色谱图
1(CI 10316):13.610 min;2(CI 15985): 16.066 min;3(橙黄Ⅰ):25.217 min;4(CI
15510):27.411 min
橙黄Ⅰ:4.887 min。