第十四章 硼族元素(IIIA族)B Al Ga In Tl 硼铝镓铟铊
- 格式:ppt
- 大小:1007.00 KB
- 文档页数:56
高中化学奥林匹克竞赛辅导硼族元素一、硼族元素简介硼族元素包括硼(B)、铝(Al)、镓(Ga)、铟(In)、铊(Tl),在周期表中处于第Ⅲ A族。
硼族元素的价电子构型为n s2n p1,除硼外其余元素均为金属元素,金属性随原子序数的增加而增强。
B的半径较小,失去三个电子非常困难,因此硼不能形成简单阳离子B3+,只能通过共用电子对形成共价化合物。
Al、Ga、In、Tl在水溶液中可以形成M3+。
因为惰性电子对效应,Tl3+具有强氧化性。
在硼族元素形成的共价分子中,中心原子最外层只有6个电子,未达到8电子的外层结构,属于缺电子化合物,它们具有一个空p轨道,可以接受孤对电子形成配位键,是强的路易斯酸。
硼族元素的性质二、硼及其化合物1.硼的单质硼的非金属单质以原子晶体形式存在。
单质硼有无定形硼和晶体硼两种,无定形硼为棕色粉末,晶体硼为黑灰色原子晶体。
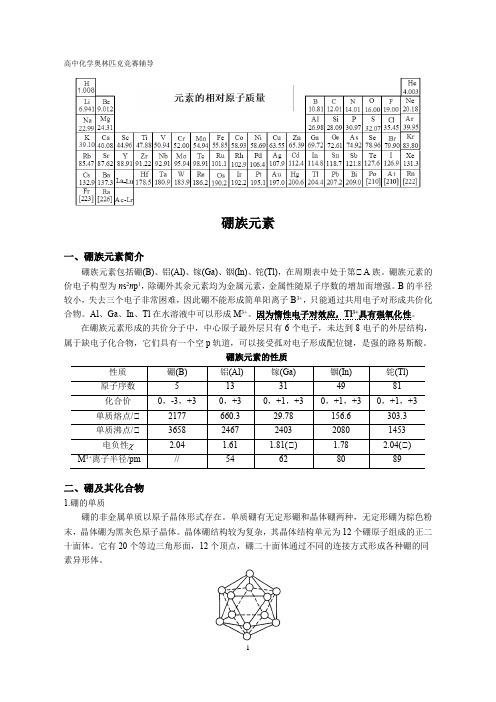
晶体硼结构较为复杂,其晶体结构单元为12个硼原子组成的正二十面体。
它有20个等边三角形面,12个顶点,硼二十面体通过不同的连接方式形成各种硼的同素异形体。
晶体硼的化学活性较低,无定形硼较活泼。
常温下,硼能与F 2反应,高温下能与N 2、O 2、S 等非金属单质反应。
无定形硼可被热的浓硝酸、浓硫酸氧化成硼酸,也能与强碱作用放出氢气。
2B+N 22BN(与金刚石C 2互为等电子体,是原子晶体) B+3HNO 3(浓)B(OH)3+3NO 2↑2B+2NaOH+2H 2O2NaBO 2+3H 2↑(与Al 的性质相似)2.硼的氧化物及含氧酸硼最重要的氧化物是B 2O 3,熔融B 2O 3能溶解许多金属氧化物,形成具有特征颜色的偏硼酸盐,这个反应用于定性分析,称为硼珠实验:CuO+B 2O 3Cu(BO 2)2(蓝色) NiO+B 2O 3Ni(BO 2)2(绿色) B 2O 3的水化物为硼酸H 3BO 3或B(OH)3。
H 3BO 3是白色的片状晶体,具有片层结构,层和层 之间存在范德华力,容易发生滑动,其中氢键对其结构的形成具有支配的作用。





7主族元素口诀
7个主族(ⅠA、ⅡA、ⅢA、ⅣA、ⅤA、ⅥA、ⅦA)包含元素
第一主族,氢锂钠钾铷铯钫
IA:Li Na K Rb Cs Fr
第二主族,铍镁钙锶钡镭
ⅡA:Be Mg Ca Sr Ba Ra
第三主族,硼铝镓铟铊
ⅢA:B Al Ga In Tl
第四主族,碳硅锗锡铅
ⅣA:C Si Ge Sn Pb
第五主族,氮磷砷锑铋
ⅤA:N P As Sb Bi
第六主族,氧硫硒碲钋
ⅥA:O S Se Te Po
第七主族,氟氯溴碘砹
ⅦA:F Cl Br I At
化学元素记忆方法(谐音)
氢锂钠钾铷铯钫请李娜加入私访
铍镁钙锶钡镭媲美盖茨被累
硼铝镓铟铊碰女嫁音他
碳硅锗锡铅探归者西迁
氮磷砷锑铋蛋临身体闭
氧硫硒碲钋养牛西蹄扑
氟氯溴碘砹父女绣点爱
氦氖氩氪氙氡害耐亚克先动。
讲座十三硼族元素王振山2017年12月9日,2018年1月27日,2中一、硼族元素概述硼族元素又称土族元素,其中Al2O3为黏土的主要成分,既难溶又难熔。
电子亲和能E A1规律性不强,电离能I1基本逐渐减小锯齿变化,氢化物稳定性减弱,+3氧化态为缺电子化合物。
2、硼族元素基本性质◆价电子构型:n s2n p1,◆最大特征是缺电子元素:价电子数3<价层轨道数4,可形成缺电子化合物。
▽缺电子化合物:成键电子对数<价层轨道数。
缺电子原子的特征表现:①、有空轨道,可形成多中心缺电子键(如B2H6中有3c-2e 键);②、缺电子化合物是典型的Lewis酸(如BF3)。
易形成配位化合物(如H[BF4]),易形成双聚物(如Al2Cl6)。
注意:H[BF4]不是缺电子化合物。
3、硼族元素的电势图二、硼及其化合物硼在自然界中的存在:自然界没有游离硼,硼是自然界中分布较广的元素,存地壳中的质量分数为1.0×10-3%。
最丰富的硼矿是电气石,它是一种复杂的铝硅酸盐,约含10%的硼。
硼在自然界主要以含氧化合物的形式存在,其主要的矿物有:硼砂Na2B4O7·10H2O、斜方硼砂Na2B4O7·4H2O(四水硼砂)、方硼矿Mg5B14O26·MgCl2(2Mg3B8O15·MgCl2)、硼镁矿Mg2B2O5·H2O、硬硼钙石Ca2B6O11·5H2O、纤维硼镁石Mg(BO2)OH、硼钠钙石NaCa(B5O9)·8H2O、少量的天然硼酸H3BO3等。
硼在自然界中丰度之所以低,是因为105B+10n→42He+73Li,所以硼材料可作为核反应堆的减速剂和生物防护。
单质硼是高效的中子吸收剂,含硼控制棒是核电站的最重要部件之一,用于控制核反应的速率。
1、硼原子成键的三大特性:⑴、共价性(主要特征)B原子半径小,电离能(I1、I2、I3)大,B以形成共价键为特征。