钠的氧化物
- 格式:pptx
- 大小:228.67 KB
- 文档页数:9

4.将1
5.6g Na2O2投入到84.4g水中,所得溶液溶质的质量分数为( )
A. 15.6%
B. 16%
C. 16.5%
D.19.1%
5.现行高一新教材中有一个演示实验,用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂上
滴水,可观察到脱脂棉剧烈燃烧起来。
(1)由实验现象所得出的有关Na2O2和H2O反应的结论是:
a:有氧气生成;b:。
(2)写出Na2O2和H2O反应的化学方程式并标明电子转移数目:。
(3)某学校研究性学习小组拟用下图装置进行实验,以证明上述结论。
①用以验证结论a的实验操作方法及现象是:。
②用以验证结论b的实验操作方法及现象是:。
(4)该研究性学习小组的同学认为Na2O2和H2O反应可生成H2O2,现请你设计一个简单的实验以证明Na2O2和足量的H2O充分反应后的溶液中有H2O2存在。
(只要求列出实验所用的试剂及观察到的现象)
试剂:
现象:。


高中化学《钠的氧化物》练习题(附答案解析)学校:___________姓名:___________班级:____________一、单选题1.下列事实及其解释不正确的是 ( )A .钠保存在煤油中,是因为煤油不与钠发生反应,钠比煤油密度大,煤油可以使钠隔绝空气和水蒸气B .滴有酚酞的NaHCO 3溶液呈浅红色,微热后红色加深,是因为NaHCO 3分解生成了Na 2CO 3C .用洁净的玻璃管向包有Na 2O 2的脱脂棉吹气,脱脂棉燃烧,说明CO 2、H 2O 与Na 2O 2的反应是放热反应D .钠长期暴露在空气中的产物是Na 2CO 3,原因是钠与氧气生成的Na 2O 与水和二氧化碳反应 2.(标况下)将3.36LCO 2气体缓慢通过足量的Na 2O 2固体后,所得气体的质量为 ( ) A .3.8g B .2.4g C .5.4g D .6.6g3.化学与生产、生活密切相关,下列叙述中正确的是 ( )A .绿化造林助力实现碳中和目标B .PM2.5在空气中一定能产生丁达尔效应C .用二氧化碳灭火器扑灭金属钠的燃烧D .氯气和活性炭均可作为漂白剂,若同时使用,漂白效果会明显加强4.下列物质的应用错误的是 ( )A .金属钠可用于冶炼金属钛B .活性炭用于杀菌除异味C .2ClO 用作漂白剂和消毒剂D .22Na O 用作供氧剂5.下列关于钠及其化合价的说法正确的是 ( )A .NaOH 的摩尔质量为40gB .由Na 生成Na 2O 2的反应是氧化还原反应C .将Na 2O 固体加到酚酞溶液中,溶液先变红后褪色D .Na 2CO 3的电离方程式:Na 2CO 3=Na ++CO 236.下列说法错误的是 ( )A .34Fe O 常用作油漆、涂料、油墨和橡胶的红色颜料B .大气中游离态的氮转化为氮的化合物的过程叫氮的固定C .放电影时,放映机到银幕间光柱的形成是因为丁达尔效应D .过氧化钠可在呼吸面具或潜水艇中作为氧气的来源7.下列转化关系能一步实现的是 ( )A .Na 2O 点燃−−−→Na 2OB .Fe 2Cl 点燃−−−→FeCl 2 C .Na 2O 22CO −−−→Na 2CO 3D .CuO 2H O −−−→Cu(OH)2 8.下列关于各物质用途的解释不正确...的是 ( )A .AB .BC .CD .D 9.下列说法正确的是 ( )A .将铁粉加入FeCl 3、CuCl 2混合溶液中,充分反应后剩余的固体中必有铁B .CO 2和SO 2混合气体分别通入BaCl 2溶液、Ba(NO 3)2溶液中,最终都有沉淀生成C .钠、镁着火时,不可用泡沫灭火器灭火D .用加热分解的方法可将NH 4Cl 固体和Ca(OH)2固体的混合物分离10.下列关于钠的说法不正确的是 ( )A .金属钠与氧气反应,条件不同,产物不同B .钠在空气中燃烧,发出黄色的火焰C .少量的钠可保存在煤油中,钠着火时可以用沙土盖灭D .将金属钠投入水中,生成氢氧化钠,同时放出氧气11.下列画有横线的物质,在反应中不能被完全消耗的是 ( )①将含有少量H 2O (g )的H2通过盛有足量Na 2O 2的容器中并不断用电火花点燃①将1 molCu 置于含2mol H 2SO 4的浓硫酸中加热①1molMnO2与含4mol HCl 的浓盐酸加热反应①密闭体系中,在强光持续照射下,向过量的Ca(ClO)2溶液中通入少量CO 2A.①①B.①①C.①①D.①①12.将一块银白色的金属钠放在空气中会发生一系列的变化:表面迅速变暗→“出汗”→变成白色固体(粉末),下列有关叙述不正确的是()A.表面迅速变暗是因为钠与空气中的氧气反应生成了氧化钠B.该过程中所有化学反应均为化合反应C.最后变成碳酸钠粉末D.“出汗”是因为生成的氢氧化钠吸收空气中的水蒸气在表面形成了溶液二、填空题13.写出相应反应的化学方程式.....:(1)过氧化钠与CO2反应的方程式:________________________________________________。
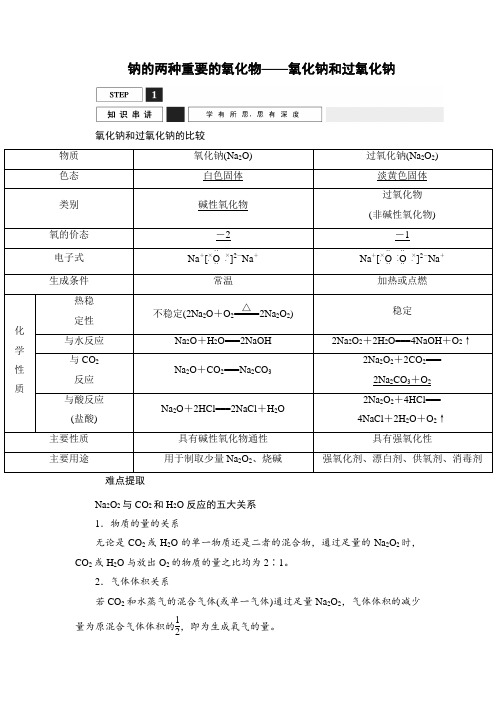
钠的两种重要的氧化物——氧化钠和过氧化钠氧化钠和过氧化钠的比较难点提取Na2O2与CO2和H2O反应的五大关系1.物质的量的关系无论是CO2或H2O的单一物质还是二者的混合物,通过足量的Na2O2时,CO2或H2O与放出O2的物质的量之比均为2∶1。
2.气体体积关系若CO2和水蒸气的混合气体(或单一气体)通过足量Na2O2,气体体积的减少量为原混合气体体积的12,即为生成氧气的量。
3.固体质量关系相当于固体Na2O2只吸收了CO2中的“CO”,H2O中的“H2”;可以看做发生相应的反应:Na2O2+CO===Na2CO3,Na2O2+H2===2NaOH(实际上两反应都不能发生)。
4.电子转移关系当Na2O2与CO2、H2O反应时,每产生1 mol O2转移2 mol e-。
5.先后顺序关系一定量的Na2O2与一定量的CO2和H2O(g)的混合物的反应,可看做Na2O2先与CO2反应,待CO2反应完全后,Na2O2再与H2O(g)发生反应。
【互动思考】1.判断正误,正确的划“√”,错误的划“×”(1)过氧化钠能与水反应,所以过氧化钠可以做气体的干燥剂()(2)过氧化钠与二氧化碳反应时,过氧化钠既是氧化剂又是还原剂()(3)78 g Na2O2中含阴离子的个数是2 N A()(4)Na2O2与H2O反应制备O2的离子方程式:Na2O2+H2O===2Na++2OH-+O2↑()(5)Na2O、Na2O2组成元素相同,与CO2反应产物也相同()(6)Na2O2的电子式为()(7)1 mol钠与氧气反应生成Na2O或Na2O2时,失去的电子数目均为N A()(8)1 mol Na2O2与足量CO2反应时,转移2N A个电子()答案(1)×(2)√(3)×(4)×(5)×(6)×(7)√(8)×2.如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应。
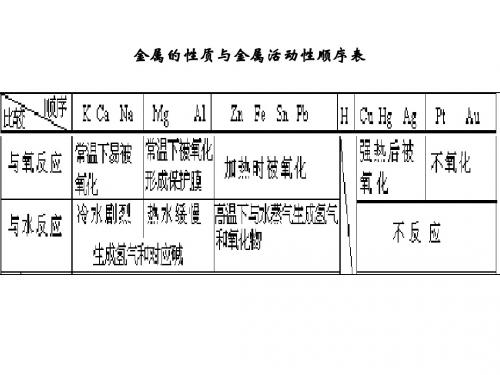

钠的氧化物说课稿各位评委老师大家好!我要说课的内容是人教版化学必修1,第三章,第二节的第一课时钠的氧化物,下面我将从教材,教法,学法,教学程序设计四个方面对本节课作如下说明:一.说教材1.1教材的地位与作用:本节课是钠金属化学性质知识的延伸与发展。
在自然界中金属元素大部分都以化合物的形式存在。
只有既了解金属单质的化学性质,又了解它们化合物的性质才是比较全面的了解金属。
金属化合物的性质是建立在金属单质性质的基础之上,金属在化学反应中失去部分电子转变为金属阳离子生成金属化合物,所以它们之间存在着因果关系。
因此本节课的学习能让学生更全面地认识钠金属,为以后在生产和生活中的应用打下基础。
1.2教学目标依据新课程理念,本着对教材结构和内容的深刻理解,提出本节教学的目标:1.知识目标:使学生掌握钠氧化物(氧化钠,过氧化钠)的化学性质。
2.技能目标:培养学生观察实验现象、分析实验结论的能力。
3.情感目标:通过钠金属及氧化物,提高学生学习化学的兴趣。
1.3、重点、难点重难点: 过氧化钠的化学性质。
二、教法以上的重点和难点的突破是本节成功与否的关键,通过什么样的教法和学法显得异常重要。
我的教法是:本节课的实验和科学探究都比较多我采用边讲边实验的形式来完成。
为了激发学生的学习兴趣,充分发挥学生的主体作用,对一些必须让学生亲身体会的实验,如吹气生火,滴水生火实验,而且这两个实验有违人们的常识,吹气生火就是用呼吸产生的二氧化碳产生火,滴水生火是利用水产生火,让学生通过自己动手做实验,观察实验现象,分析得出有关的结论,体验实验的乐趣。
三.学法利用师生互动的方式,以学生为主,老师为辅的形式,发挥学生的主体作用,通过学生实验,引导学生发现问题,分析,解决问题。
四、教学过程(一)引入课堂。
利用魔术的神秘感引入课题。
人们知道生活中二氧化碳用来灭火,可是在引课时用在二氧化碳中棉花的燃烧这种有违常识的“魔术”引课,而能发生这样的现象就是因为有“魔术粉—过氧化钠”,从而直接引入了主题。