活性炭吸附碘量法测定金
- 格式:pdf
- 大小:1.72 MB
- 文档页数:3

活性炭吸附-碘量法测定金2016-05-20 13:03来源:内江洛伯尔材料科技有限公司作者:研发部碘量法测定金试料经灼烧、王水溶解。
活性炭吸附金。
Au(Ⅲ)与碘化钾反应生成碘化亚金,并游离出碘,以淀粉为指示剂,用硫代硫酸钠标准滴定溶液滴定以测定金量。
本法适用于冶金物料、载金炭、浸出液等中0.x % (g/L)~xx % (g/L)的金含量的测定。
(1) 主要试剂王水;盐酸溶液(2+98);氟化氢铵溶液(20 g/L);氯化钠溶液(25 g/L);淀粉溶液(10 g/l);EDTA溶液(250 g/L);醋酸溶液(7+93)。
活性炭(粒度200目):将活性炭置于氟化氢铵溶液中,浸泡2~3日,抽滤。
以盐酸溶液(2+98)及水洗涤至无 F-为止。
活性炭在氢氧化钠溶液(200 g/L)中煮沸3 h,抽滤,以水洗涤。
于盐酸溶液(1+3)中煮沸2 h后使用。
金标准储备溶液称取0.50 g纯金(≥99.99%)于400 mL烧杯中,加20 mL王水,加热溶解。
加5 mL氯化钠溶液,水浴蒸至湿盐状。
加3 mL盐酸,水浴蒸至湿盐状,重复3~4次。
加20 mL盐酸,转入500 mL容量瓶中,加145 mL盐酸,用水稀释至刻度,混匀。
此溶液1 mL含1 mg金。
金标准溶液(100 µg/mL)。
硫代硫酸钠标准滴定溶液:称取25.2 g硫代硫酸钠(Na2S2O4·5H2O),溶于新煮沸并冷却的蒸馏水中,加入0.1~0.2 g碳酸钠,转入1000 mL容量瓶中,用水稀释至刻度,混匀。
此溶液1 mL相当于10 mg金。
放置7天后使用。
取上述溶液30 mL、100 mL,各加入1~2 g碳酸钠,分别用新煮沸并冷却的蒸馏水稀释至10000 mL,混匀。
此溶液1 mL相当于30 µg、100 µg金。
标定后使用。
标定分别移取10.00 mL金标准溶液,加0.1~0.3 g碘化钾,搅匀,立即用相应浓度的硫代硫酸钠标准滴定溶液滴定至微黄色。

活性炭吸附碘量法测定常量金金矿试样组成复杂,除以单体自然金存在外,常与硫化物、锑化物等伴生。
试样的完全溶解成为准确测定金的前提条件。
本文采用加热溶解法,采用活性炭吸附,硫代硫酸钠标准溶液滴定测定金的含量。
1. 试验部分1.1 分析试剂金标准溶液:取纯金0.05 克于250 毫升烧杯中加王水溶解后加入 1 克氯化钠蒸干,用盐酸处理后吹水煮沸稀释到500 毫升容量瓶中,每毫升溶液含金100 微克。
硫代硫酸钠标准溶液:称取纯结晶硫代硫酸钠 2.52 克溶解于少量蒸馏水中加0.1 克无水碳酸钠稀释至1000 毫升容量瓶中,放置一周后备用。
EDTA( 2% 水溶液淀粉(0.5%)氟化氢铵冰乙酸所有试剂均为分析纯1.2 试验方法活性炭吸附柱:将内径为35mm高90mmf的玻璃吸附柱插入抽滤孔中,柱中放一片外径为34mm的多孔塑料板,倒入纸浆层厚约3〜4mn,再加入活性炭抽滤,抽滤后总厚约5〜7mm用水冲洗柱壁。
装上布氏漏斗,在漏斗上垫两张滤纸并加入少许水润湿,再倒入少许纸浆,抽干,备用。
样品分析:称取矿石试样10 克于瓷坩埚中,置于高温炉中,从室温缓慢升至700C后焙烧1小时(主要适用含硫高的样品,含硫低的样品可直接加王水加热分解完全)。
取出冷却;将试样移入400 毫升烧杯中,加入水50 毫升王水50 毫升,低温加热分解蒸至体积约为60 毫升取下,用水冲洗表面皿和杯壁,加入少许纸浆,将溶液倒入以备好的活性炭吸附柱上的布氏漏斗中,抽滤,用热的2%HC洗涤烧杯和残渣,取下布氏漏斗,用热的2% 氟化氢铵热溶液洗涤吸附柱7〜8次,再用热水1000毫升洗涤,停止抽滤,将活性炭和纸浆移入瓷坩埚中,将塑料板取下,将瓷坩埚放入预热300C高温炉中,稍开炉门在700C灼烧大约1小时,烧成白色粉末状,取出冷却。
加入25%氯化钠溶液3〜4滴,王水2毫升在水浴盘上加温溶解蒸干,加3〜4滴浓HCI在蒸干至无酸味,需反复处理3〜 4 遍。

碘量法测金实践过程中的注意事项当前在选矿冶金行业,活性炭吸附-碘量法测金的方法应用最为普遍,笔者从事多年的金矿石分析工作,取得了一些有益的认识。
在这里简单谈谈这一分析方法在实践操作过程中几个重要环节的注意事项,仅供参考。
标签:碘量法;金矿石分析;注意事项1 常用的活性炭吸附-碘量法的操作步骤(1)试样的溶解:在感量0.1g的天平上称取试样10g—30g(精矿称取10g,原矿样称取20g,尾矿、溢流分别称取试样30g),于400ml烧杯中,用水润湿,加反王水50ml加热后,再加正王水50ml,加热溶解。
一般的硅酸盐矿,硫化矿、金精粉含碳等有机物的样品,先加HCl 20ml,放在电热板上,加热至不反应为止,然后再加入浓HNO3处理。
应分数次加入,每次加入量不能太大,以样品反应不溢出为准,加热分解至试样中无黄烟(NO2)后,再补加少许浓HNO3继续加热至体积50ml左右,然后加入2%KMnO4溶液30ml,NaCl(33%)饱和溶液30ml,用洗瓶清洗杯壁至体积在110ml左右,盖上表面皿,然后加热使试样分解溶解,保持30—60分钟微沸状,使溶液的体积在30—50ml时取下,用温热的水洗涤表面皿及杯壁,并用热水稀释到100—150ml摇匀,使可溶性盐类溶解,放置待溶液冷却后至40—60℃过滤吸附。
(2)过滤及吸附:将带有活动滤板的吸附柱紧装于抽滤箱上,倒入适量的滤纸浆抽干后约为2—3mm厚,压紧再倒入含有活性炭的纸浆,抽干后高度约为5—7mm(若金含量较高,则应增至10—14mm),使炭浆层与柱壁紧贴,用洗瓶洗净柱壁上的活性炭,将布氏漏斗装于吸附柱上,铺上大小合适的定性滤纸(中速),倒入少许的细纸浆于滤纸边缘处,使吸附柱内有水柱存在。
然后将试样溶液连同残渣一起倒入漏斗中进行抽滤及动态吸附,待漏斗内溶液全部滤干后,用温热的9%HCl洗涤烧杯2-3次,洗残渣5-8次,拿掉布氏漏斗,用温热的5%NH4HF2洗吸附柱5-8次,再用温热的5%HCl洗吸附柱5-8次,最后,用温热的水洗3-4次,抽干后停止抽气。

讲稿九——活性炭吸附柱┉碘量法测定金说明一、原理金在自然界中以单质形式存在,其原因在于其化学性特别不活泼,金在矿石中分布也极不均匀,因为它以颗粒或片状形式存在,这就给取样带来了难度,要求取样量大,磨样细度要求极高,以后再详述。
任何一种强酸均不能单独将金溶解。
唯有王水才能。
王水为硝酸、盐酸的混合物,三体积的浓盐酸与一体积的浓硝酸,对金的溶解效果最佳,通常称为正王水。
如果将三体积的浓硝酸与一体积的浓盐酸相混合,则成为反王水,或称逆王水。
在含硫很高的含金矿样中,要首先加反王水,后加正王水,溶解效果才好。
盐酸无氧化性,不能氧化单质金,硝酸虽是强氧化剂,但其标准电极电位没有金高,遇到王水时情况发生了变化:Au +3HCl + HNO3 H+ + A uCl3 + 2H2O +NO三价金离子与Cl-形成络合物:A uCl3 + HCl = H++ A uCl4-根据奈斯脱方程式:E= E0 + 0.059 lg[A u3+] = E0 + 0.059 lg[A u3+]n 1 n在A uCl4-被还原成A uCl 或 A uI时,n=2,由于绝大多数三价金离子被络合,故其氧化还原电位大为降低,从而硝酸得以氧化A u。
碘I2本是一种中等强度的氧化剂,A uCl4-的标准电极电位与I2相差无几,本来不足以充分氧化KI为I2(即负一价的碘成为零价的碘),但由于AuI的离子积(或者说溶度积)很小,2I—-2e I2 电对的电极电位则大大降低。
从而化学反应能定量地进行:H A uCl4+ 3KI = A uI + I2 +3KCl + HClI2对能在一定条件下(弱酸性)与硫代硫酸钠(市售产品通常为五水合硫代硫酸钠Na2S2O3·5H2O形式)定量地进行,化学方程式如下: I2 + 2Na2S2O3 = 2NaI + Na2S4O6由以上诸化学方程式可以看出:一个分子的H A uCl4能与2个分子的KI 起氧化还原反应(生成一个碘分子),而一个碘分子又能与2个硫化硫酸钠分子起氧化还原反应,如果后者以五水合盐的形式存在,则其反应按以下量比进行,A u :2Na2S2O3 ·5H2O = 197.0 :2× (23×2+32×2+16×3+5×18)=197.0:2×248=1:2.52 这个比例极为重要,是配标准溶液及化验结果的理论依据。



活性炭吸附原子吸收法测定金1.方法提要称取一定量(视样品的均匀性而定)的样品。
用HNO3-KClO3硝化除炭、硫以及有机物。
最后用王水溶解;动物胶凝聚沉淀硅酸后,在稀王水介质中,用布氏漏斗过滤分离残渣。
AuCl4-被装有活性炭-纸浆吸附柱动态吸附,与绝大部分基体组分分离。
活性炭经灰化后,用王水溶解,用原子吸收法测定矿石中的金。
本法适用于一般试样中ω(Au)/10-6=0.01~100的测定。
2.试剂2.1.氯酸钾,分析纯。
2.2.盐酸(p1.19g/mL),分析纯。
2.3.硝酸(p1.42g/mL),分析纯。
2.4.氟化氢铵,分析纯。
2.5.动物胶溶液:称取5g动物胶于1000mL水中,加热溶解氢钾;2.6.活性炭-纸浆:将粒径为0.074mm的活性炭在20g/LNH4HF2溶液中浸泡3天,过滤,用HCl(2+98)及热水各洗涤7~8次。
将处理后的活性炭与纸浆以干时的质量比按比1+2混匀。
2.7.活性炭-纸浆吸附柱的制备:将吸附柱紧密装在抽滤筒的圆孔中,在吸附柱内加入纸浆,开动真空泵,抽干压紧,纸浆约为4~5mm厚,在加少许稀纸浆,抽干,加入活性炭-纸浆混合物(绝对防止活性炭渗漏),上面覆盖一层纸浆。
装上布氏漏斗,铺上滤纸即可过滤。
2.8.金标准贮存溶液:称取0.5000g 99.99%的金粉于250mL烧杯中,加50mL王水,用水浴溶解,转入500mL容量瓶中,用水稀释至刻度,摇匀。
此溶液含金为1000ug/mL。
2.9.金标准溶液:移取50.00mL金标准贮存溶液于500mL容量瓶中, 加50mL王水,用水稀释至刻度,摇匀。
此溶液含金为100ug/mL。
2.10.原子吸收分光光度计,附空心阴极灯。
在仪器最佳工作条件下,凡能达到下列指标者均可使用。
灵敏度:在与测量样品溶液的基体相一致的溶液中,金的特征浓度应不大于0.10ug/mL。
精密度:用最高浓度的标准溶液测量10次吸光度,其标准偏差应不超过平均吸光度的1.0%;用最低浓度的标准溶液(不是零标准溶液)测量10次吸光度,其标准偏差应不超过最高浓度标准溶液平均吸光度的0.5%。

金测定——碘量法(活性炭吸附)一、方法原理:此法基于用王水溶解试样中的金,以活性炭富集,然后用碘量法完成测定。
1、对试样要求:金在试样中一般呈单质状态,分布极不均匀,故欲得准确分析结果,试样必须有足够的细度和均匀性,以增加其代表性。
本法要求一般的矿的试样必须通过180网目。
2、测定原理:试样中的金溶于王水后生成三氯化金,它再与NaCl作用生成易离解的氯金酸盐:Au+3HCl+HNO3== AuCl3+2H2O+NO↑AuCl3+NaCl==Na AuCl4或AuCl3 +HCl== HAuCl4Na AuCl4== Na++ AuCl4—氯金酸根络离子经活性炭吸附后达到了富集金并使金与多数金属离子分离的目的。
活性炭经过灰化灼烧AuCl3又被还原为单质金。
2 AuCl3+3C+3 H2O==2 Au+6 HCl+3CO↑三氯化合物又能够氧化碘化钾而析出等当量的碘。
AuCl3+3KI==AuI+I2+3KCl最后用Na2S2O3标液滴定析出的碘,间接计算出Au的含量。
3、干扰与分离:活性炭富集Au后,虽使Au与大多数金属元素和残渣已经分离,但少量的硅酸及部分的Cu、Pb、Fe也被吸附并对测定有影响。
硅酸、Fe、Pb可用NH4HF2洗脱。
残余的Fe和Cu、Pb可分别与I-及EDTA络合而消除其影响。
Fe3++6F-==FeF63-Cu2++H2Y2-==Cu Y2-+2H +Pb2++H2Y2-==Pb Y2-+2H +4、适用范围:经过方法考查和生产实践检验,本法对本地矿的地质样试样和选矿各种产品适用。
测定范围为可测定含金在0.3g/t以上的试样。
二、试剂的配制与标定:1、HCl(分析纯)比重1.192、HNO3(分析纯)比重1.423、正王水(1∶1) HCl∶HNO3∶H2O=3∶1∶44、反王水(1∶1) HCl∶HNO3∶H2O=1∶3∶4王水(1∶1) HCl∶HNO3 =3∶15、NaCl 分析纯固体及饱和溶液6、KI 分析纯固体7、稀醋酸(7%) 93ml H2O加7 ml冰醋酸8、氟化氢氨分析纯固体及5%的水溶液9、1%淀粉指示剂 1 g可溶性淀粉溶于100 ml H2O中,煮沸至透明,冷却后即可。

载金碳碘量法化验步骤1.称样,灰化载金碳样称0.5g左右,置于高温炉中600-800℃灰化。
2.溶样试样取出冷却至室温,移入400ml烧杯中,润湿,加10ml浓硝酸,预处理(在电热板上微热),待无红棕色气体产生后,加入120ml1:1王水,在电加热板上,微沸50min,待体积剩余50-60ml时取下冷却。
3.活性炭吸附柱活性炭吸附柱分三层,依次为白纸浆作底层,中间层活性炭纸浆层和白纸浆顶层。
白纸浆厚度3mm,活性炭纸浆层厚度8-9mm。
4.活性炭吸附漏斗中铺一张定性滤纸将冷却好的试样依次倒入布氏漏斗中,进行抽滤,烧杯洗涤3次。
用温热的5%HCl溶液洗布氏漏斗内的残渣7-8次,取下漏斗,再依次分别用温热的(50℃):6%氟化氢铵(NH4HF2)溶液、5%HCl溶液洗涤吸附柱7-8次,最后用温水清洗活性炭吸附层7-8次后抽干。
5.活性炭层高温灰化将活性炭层取下放入50ml瓷坩埚中,在电热板上低温灰化, 40min后,观察无明火,随后放入650℃高温炉中高温灰化,20min 后观察无火星,灰化完全,取出冷却至室温。
6.水浴蒸酸向瓷坩埚中加入2-3滴25%NaCl溶液,润湿,再加1ml王水,水浴,待坩埚底部蒸干至湿盐状,加2ml浓盐酸继续水浴蒸干,加浓盐酸重复两次,待蒸至无酸味,取下冷却。
7.碘量法测金向坩埚中加入3-5ml 7%醋酸溶液和1ml NH4HF2,2ml 1%EDTA溶液和0.1gKI,迅速滴定至淡黄色,加淀粉指示剂,滴定至无色,记下消耗硫代硫酸钠标准溶液体积V。
8.计算含量(g/t)=T*V/mT—硫代硫酸钠对金的滴定度,单位:ug/mlV—消耗硫代硫酸钠体积,单位:mlm—称样量,单位:g9.试剂配制①活性炭纸浆:首先处理活性炭。
将粒径为0.074的活性炭在20g/l的NH4HF2溶液中浸泡3天,过滤,用HCl(2+98)及热水各洗涤7-8次,将处理后的活性炭与纸浆按干时的质量比1:2混匀。
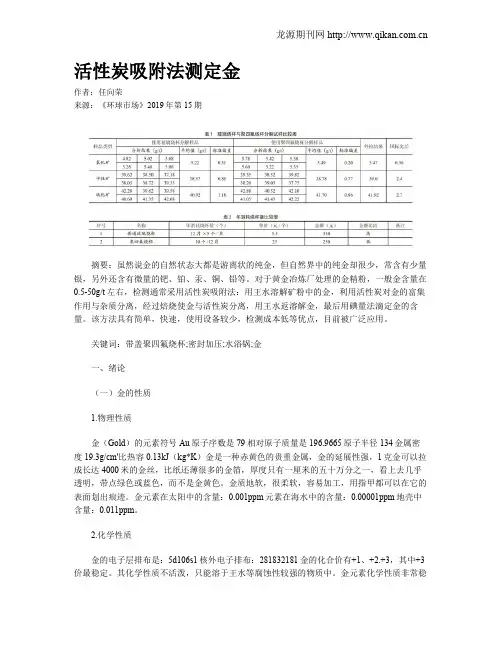
活性炭吸附法测定金作者:任向荣来源:《环球市场》2019年第15期摘要:虽然说金的自然状态大都是游离状的纯金,但自然界中的纯金却很少,常含有少量银,另外还含有微量的钯、铂、汞、铜、铅等。
对于黄金冶炼厂处理的金精粉,一般金含量在0.5-50g/t左右,检测通常采用活性炭吸附法:用王水溶解矿粉中的金,利用活性炭对金的富集作用与杂质分离,经过焙烧使金与活性炭分离,用王水返溶解金,最后用碘量法滴定金的含量。
该方法具有简单,快速,使用设备较少,检测成本低等优点,目前被广泛应用。
关键词:带盖聚四氟烧杯;密封加压;水浴锅;金一、绪论(一)金的性质1.物理性质金(Gold)的元素符号Au原子序数是79相对原子质量是196.9665原子半径134金属密度19.3g/cm'比热容0.13kJ(kg*K)金是一种赤黄色的贵重金属,金的延展性强,1克金可以拉成长达4000米的金丝,比纸还薄很多的金箔,厚度只有一厘米的五十万分之一,看上去几乎透明,带点绿色或蓝色,而不是金黄色。
金质地软,很柔软,容易加工,用指甲都可以在它的表面划出痕迹。
金元素在太阳中的含量:0.001ppm元素在海水中的含量:0.00001ppm地壳中含量:0.011ppm。
2.化学性质金的电子层排布是:5d106s1核外电子排布:281832181金的化合价有+1、+2.+3,其中+3价最稳定。
其化学性质不活泼,只能溶于王水等腐蚀性较强的物质中。
金元素化学性质非常稳定的原因是,金原子的最外层的三个电子之间的相互作用非常紧密,原子体积被压缩,电子不容易被氧化剂夺取。
因此能够再在地层中形成比较稳定的单质,这就是我们说的黄金。
金的化合物:氯化金:AuCl、氧化金:Au2O3等。
氧化金:三价金的氧化物,分子式Au2O,水合物分子式为Au2O;*3H2O;分子量495.98;含金量77.0%;外观棕色粉末;储存方法:常温干燥密封储存。
化学特性:加热时放出氧气,生成单质金。

矿石中金的测定(碘量法)
在微酸性溶液中,氯化金与碘化钾作用产生单质碘,以淀粉为指示剂,用硫代硫酸钠溶液进行滴定。
该法的终点变化敏锐,但干扰因素较多,锑、矾和硒等也与碘化钾作用产生碘,使结果偏高。
另外,少量的铁、铜、铅等对金的测定也有干扰。
活性炭吸附-碘量法具体步骤如下:矿样经王水分解后,用活性炭吸附金使之与大量的干扰元素分离。
灼烧除去炭质残留,用王水溶解金,再用碘化钾还原,以淀粉为指示剂,用硫代硫酸钠溶液滴定,间接测定金的质量分数。
也可经活性炭吸附后灼烧除炭,再用王水溶解,在稀的乙酸介质中,用氟化氢铵、EDTA掩蔽铁、铜、铅等干扰因素,用碘化钾还原金,以淀粉为指示剂,用硫代硫酸钠溶液滴定,测定金的质量分数。
有关碘量法测金的报道也很多,吴敏等研究了用MIBK萃取-碘化钾容量法测定载金炭和地质样品中的金,提出了碘量法测定时消除分析误差的措施。
经典的化学分析方法准确度高,适用于常量分析。
对于微量和痕量组分,精密度不如仪器分析。
由于样品中其它离子的干扰,终点误差不易观察,因此必须经验丰富的的工作人员测定才可,而且容量分析法试剂消耗多。
活性炭吸附碘量法测定金试剂配制:抽滤吸附装置:将带活动过滤板的吸附柱装于抽滤筒上,先加白纸将,抽干,2-3mm厚,用滤板压平,再加混有活性炭的纸浆,抽干压平,在6mm以上,再加少量白纸浆抽干压平,做到层次分明,把布氏漏斗装于吸附柱上,加一张滤纸及少量纸浆,抽干。
活性炭:粒度0.074mm,将分析纯或化学纯活性炭放入20g/L氟化氢铵或氟氰酸溶液中浸泡3天后抽滤,以盐酸2%及水洗净氟根。
纸浆:用定性滤纸在水中浸泡,捣碎备用。
稀王水:V(盐酸)+V(硝酸)+V(水)=3+1+4聚环氧乙烷:称1g聚环氧乙烷用少量水调成糨糊状,再加200ml水及4—5滴盐酸,缓缓加热溶解。
冰乙酸体积比7%的水溶液(7+93)氯化钠200g/l的水溶液EDTA 乙二胺四乙酸二钠25g/l水溶液称取25gEDTA,加水400ml,加热搅拌溶解,冷却后用水稀释至1000ml金标准溶液(1mg/ml):硫代硫酸钠标准滴定溶液:称取2.52g 硫代硫酸钠溶于新煮沸后冷却的蒸馏水中,加0.1g 碳酸钠,用水定容1000 ml(溶液PH为7.2—7.5),此溶液1ml约相当于1mg金。
取30ml,100ml,200ml上述溶液,各加0.1g碳酸钠,用煮沸后冷却的蒸馏水稀释至1000ml,即分别得到1ml硫代硫酸钠标准滴定溶液,分别相当于30ug,100ug,200ug的金的溶液。
经标定后使用。
标定:分取5ml金标准溶液三份于50ml瓷坩埚中,加0.1gKI,搅拌,立即用相应含量的硫代硫酸钠标准滴定溶液滴定至微黄色后,加3—5滴10g/L淀粉指示剂,继续滴定,近终点时应充分搅拌,逐渐滴入至溶液由蓝色变为无色,即为终点。
按下式计算硫代硫酸钠标准滴定溶液对金的滴定系数:FAu=Mo/V o式中:FAu—滴定系数,与1.00ml硫代硫酸钠标准滴定溶液相当的金的质量,ug/ml.Mo—吸取金标准溶液含量ug.V o—标定时消耗硫代硫酸钠标准滴定溶液体积,ml分析步骤:在感量0.1g的天平称取10g-20g试样于于高温炉中焙烧。
2011年6月June2011岩 矿 测 试ROCKANDMINERALANALYSISVol.30,No.3370~374收稿日期:2010-05-13;修订日期:2010-11-02作者简介:汪永顺,工程师,从事岩矿测试工作。
E mail:593375906@qq.com。
文章编号:02545357(2011)03037005活性炭吸附-碘量法测定金矿石中金的不确定度评定汪永顺,范广勤,曹开科,王文芳(青海省有色地质矿产勘查局测试中心,青海西宁 810007)摘要:根据测量不确定度的评定方法,对活性炭吸附-碘量法测定金矿石中的金进行不确定度评定。
实验样品从低温升至650℃灼烧2h除硫,用50%(体积分数)的王水溶解1h,经活性炭动态吸附抽滤,将载金炭灰化复溶,用硫代硫酸钠标准溶液滴定,该方法简便、快速、实用性强。
测量结果的不确定度由滴定样品消耗的硫代硫酸钠标准工作溶液体积、硫代硫酸钠对金的滴定度、称量质量、重复测定等不确定度分量组成。
对各个不确定度分量进行分析并量化,合成得到测量结果的标准不确定度,换算成扩展不确定度。
通过评定不确定度主要是由硫代硫酸钠对金的滴定度引入。
关键词:活性炭吸附;碘量法;金;金矿石;不确定度评定UncertaintyEvaluationforIodometricDeterminationofGoldinGoldOreswithActivatedCarbonAdsorptionWANGYong shun,FANGuang qin,CAOKai ke,WANGWen fang(TestingCenter,BureauofNonferrousMetalsGeologicalandMineralExplorationofQinghaiProvince,Xining 810007,China)Abstract:Accordingtotheevaluationmethodtomeasureuncertainty,weevaluatedtheuncertaintyofthegolddeterminationinorebyusingactivatedcarbonadsorption iodimertric.Theexperimentalsampleswerecalcinedfromroomtemperatureto650℃for2htoremovesulphur,thendissolvedbythe50%(volumefraction)aquaregiafor1h.Thegoldwasabsorbedfromthesolutionbyactivatedcarbondynamicadsorptionsuctionfilter.Thecarriedgoldcarboncinerationwasdissolvedagainbeforethegoldwastitratedbysodiumhyposulfitestandardsolution.Thismethodissimple,rapidandstrongpracticability.Theuncertaintiesofmeasurementconsistoftheconsumedvolumesandtiterofsodiumhyposulfitestandardsolutiontogold,sampleweight,duplicationsandsoon.Thestandarduncertaintywasobtainedbyquantifingandsynthesizingeachbranchofuncertaintiesmeasurementresults,thenconvertedintotheexpansionuncertainty.Theresultindicatesthatthemainuncertaintyisfromthetiterofsodiumhyposulfitestandardsolution.Keywords:activatedcarbonadsorption;iodometricmethod;gold;goldore;uncertaintyevaluation任何测量都存在缺陷,所有的测量结果都或多或少地偏离被测量的真值,因此在给出测量结果的同时,还必须指出所报测量结果的可靠程度。
金矿化验方法,金矿的化验,金矿石化验,金的化验化验分析 所需时间所需设备 所需药剂 高灵敏度化学光谱法快速测定痕量金 一、方法提要 试样经650℃灼烧后,王水溶样,在约10%(V/V )的王水介质中,加入聚氧化乙烯溶液,沉淀分离可溶性... 8小时 一米平面光栅摄谱仪、光栅刻线、三透镜照明系统、WPF-20型交直流电弧发生器、天津紫外Ⅰ型或Ⅱ型相板、A 、B显影液、测微光度计、S标尺王水、聚氧倾乙烯溶液、蒸馏水、缓冲剂、石墨粉 活性炭吸附化学光谱法测定痕量金 一、方法提要 试样灼烧后以王水溶解,以活性炭吸附柱动态吸附富集Au 。
ZnO 作缓冲剂,Pd 作内标。
用热的NH4HF2... 8小时 WPG-100型1米平面光栅摄谱仪、光栅刻线、三透镜照明系统、WPF-20型交直流电弧发生器、天津紫外Ⅰ型相板、A 、B 显影液、东德MD-100型或上海产9W 型、王水、LNH4HF2溶液、HCl(1+19)、内标溶液C 、石墨粉 泡塑吸附法测定金泡塑吸附硫代米氏酮目视比色法测定金 一、方法提要 试样经HCl 、HNO3溶解,聚氨酯泡沫塑料吸附Au ,在混合掩蔽...8小时 锥形瓶、比色管、出坩埚 HCl 、HNO3、EDTA 二钠盐、冰乙酸、HCI (1+99)、TMK 乙醇溶液、异戊醇 活性炭纸浆吸附碘量法测定金 活性炭吸附碘量法测定金 一、方法提要 试样用王水分解,在稀王水介质中用活性炭富集Au ,活性炭灰化灼烧后用王水复溶...8小时 高温炉、烧杯 王水、HCI 、NH4HF2溶液、NaCl 溶液、代硫酸钠(Na2S2O3·5H2O)、Na2CO3、HNO3-KClO3 密封溶样石墨炉法测定痕量银和金一、方法提要 试样经焙烧,用王水、HF 密封分解,于同一份试样中,取分液在H3BO3和洗涤灵存在下,于波长328.1...8小时 日立Z-8000型偏振塞曼原子吸收光谱仪、金空心阴极灯、石墨炉 王水(1+1)、5mL HF 、(V/V )洗涤灵、H3BO3溶液泡沫塑料分离富集石墨炉法测定痕量金(Ⅰ) 一、方法提要 试样经灼烧、王水分解,于15%(V/V )王水8小时 PE-Z3030型原子吸收光谱仪、普通石墨管、金空心阴极灯、石墨炉 王水(1+1)、硫脲-HCl(1+99)、Au 的标准溶液介质中,用泡沫塑料富集Au ,硫脲解脱。
活性炭吸附碘量法测定金
一、方法提要
试样用王水分解,在稀王水介质中用活性炭富集Au,活性炭灰化灼烧后用王水复溶,加HCI蒸干,在乙酸介质中以NH4HF2、EDTA掩蔽少量的Fe、Cu等干扰元素,加入KI将Au3+还原为Au+,同时析出游离I2,以淀粉为指示剂,用硫代硫酸钠标准溶液滴定。
本法适用于一般矿石中ω(Au)/10-6>0.5的测定。
二、试剂配制
活性炭-纸浆:首先处理活性炭。
将粒径为0.074mm的活性炭在20g/L NH4HF2溶液中浸泡3d,过滤,用HCl (2+98)及热水各洗涤7~8次。
将处理后的活性炭与纸浆以干时的质量比按1+2混匀。
金标准溶液:称取0. 0500g纯金(99.99%以上)于100mL瓷坩埚中,加l0mL王水,盖表面皿,在60~70℃水浴上加热溶解后立即加入8~10滴250g/L NaCl溶液,再在沸水浴上加热蒸干,取下,加1mL HCI,继续在沸水浴上蒸干。
取下加少量水,微热使盐类全溶,取下冷至室温,移入盛有5mL HCI的500mL容量瓶中,用水稀释至刻度,混匀。
此溶液含100μg/mLAu。
硫代硫酸钠标准溶液:称取25. 2g硫代硫酸钠(Na2S2O3·5H2O)溶于新煮沸后冷却的蒸馏水中,加0. 1g Na2CO3,用水稀释至1L(溶液pH7.2~7.5),此溶液1mL相当于l0mg Au.分别取30mL和100mL上述溶液于l0L下口瓶内,各加入1g无水Na2CO3和l0mL氯仿,用冷却的新蒸馏水稀释至10L,摇匀,放置一周后,进行标定:取30μg或100μg Au于50mL 瓷坩埚中,加3~5滴250g/L NaCl溶液,加2~3mL王水,水浴蒸干,加3~4滴HCI,蒸干,重复两次。
然后用两种硫代硫酸钠标准溶液按碘量法滴定。
求出其1mL溶液相当Au的质量(1mL分别相当30μg和l00μg),μg/mL。
三、分析手续
称取10-30g(精确至0. 01g)试样于瓷方舟中,在高温炉中于600℃灼烧40min,取出放冷,将试样转入400mL烧杯中,用少量水润湿,加100mL王水(1+1),加热微沸30~60min,中间摇动数次,取下趁热加l0mL l0g/L动物胶溶液,搅拌,用温水稀释至100~120mL,将溶液注入连接在装有活性炭-纸浆吸附柱的布氏漏斗中,用热HCl (2+98)洗涤烧杯2次、残渣7~8次。
取下布氏漏斗,用热的20g/L NH4HF2溶液洗涤活性炭3~4次,再用热HCI(2+98)洗3~4次,量后用温水洗3~4次,抽干.取出活性炭-纸浆吸附饼,放入50mL瓷坩埚中,放在电炉盘上低温烘干,并升温炭化,再移入650~700℃高温炉内灼烧至无炭粒存在,取出冷却。
在瓷坩埚内加入5滴250g/L NaCl溶液,沿坩埚壁加入2-3mL王水,放在沸水浴上蒸干,滴加3~5滴HCI,继续蒸干,重复两次,最后蒸至无酸味。
取下坩埚,加3~5mL乙酸(7+93),搅动使可溶性盐类全部溶解,冷至室温。
加入0.1g NH4HF2,搅匀。
滴加数滴25g/L EDTA溶液后,立即加入0.5g KI,用硫代硫酸钠标准溶液滴定至淡黄色,加入3~5滴l0g/L淀粉溶液,继续滴定至蓝色消失即为终点。
四、分析结果的计算
按下式计算试样中Au的含量。
ω(Au)/10-6=(f T×V T)/(ms)
式中 f T——1mLNa2S2O3标准溶液相当于Au的质量,μg/mL;
V T——滴定时消耗Na2S2O3标准溶液的体积,mL;
ms——称取试样的质量,g。
五、注意事项
(1)试样的粒径应小于0.074mm,以保证试样的均匀性.(2)视试样性质不同,可用下列方法溶解:1)含硫高的硫化矿。
先用逆王水(1+1)溶解,每次加入l0mL,待激烈反应结束后,再加100-200mL王水(1+1);2)含硫低的矿样。
一次加入100~120mL王水(1+1);
3)氧化铁矿样。
加50~60mL HCl,煮沸,再加50~60mL王水(1+1);4)含炭质和有机物的矿样.经600~700℃灼烧除炭,然后按氧化矿样进行处理,或用HNO3-KClO3氧化除炭。
(3)活性炭用量应根据金的含量而定,一般Au量在5mg以下,活性炭用量为0. 5~0. 8g; Au量在5~30mg ,其用量为1g左右;Au量30~60mg,活性炭用量则为1~1. 5g. (4)吸附柱安装:将吸附柱紧密装在抽滤筒的圆孔中,在吸附柱内加入纸浆,开动真空泵,抽干压紧,纸浆约为
4~5mm厚,再加少许稀纸浆抽干,加入活性炭-纸浆混合物(绝对防止活性炭渗漏),上面复盖一层纸浆。
装上布氏漏斗,铺上滤纸即可过滤。
(5)活性炭-纸浆炭化的时候,切勿着火,以免Au损失。
(6)EDTA对三氯化金有还原作用,加入EDTA应立即加入KI,迅速滴定。
活性炭富集火焰法测定金
一、方法
试样经650℃灼烧,王水分解、动物胶凝聚硅酸后,用活性炭动态吸附Au,再经灰化、提取,制成HCl(1+11)溶液。
将试液吸入空气-乙炔火焰中,用AAS法测定Au的吸光度,本法适用于岩右石、矿物中ω(Au)/10-6=0.05~100的测定。
二、设备及试剂配制
活性炭吸附柱:将内径为35mm、高90mm的玻璃吸附柱插入抽滤孔中,柱内放一片外径为34mm的多孔塑料板,倾入纸浆抽滤,滤干后纸浆层厚约3~4mm,再加入活性炭与纸浆的混合物(1+2),抽滤,抽干后厚度为5~7mm(视Au含量高低而使活性炭为0.5~1g),以水吹洗柱壁,再加一层薄纸浆。
装上布氏漏斗,在漏斗上垫两张滤纸并加入少许纸浆,备用。
活性炭及其处理:活性炭的粒度应为0.075mm,若使用的活性炭纯度不够可分别采用如下两种方法处理:(1)将活性炭置于塑料烧杯中,加入热的40g/LNH4HF2,溶液浸没活性炭并放置48h以上,然后过滤,用HCl(1+24)洗涤8~10次,再用热水洗涤8次,放置晾干备用,(2)将活性炭置于烧杯中、加入HCl(1+5)浸没活性炭,加热煮沸1h,再浸泡数小时后过滤,用水洗涤,反复处理数次,直至滤渡不呈现Fe3+的黄色为止。
金标准贮存溶液:称取1.0000g高纯Au于烧杯中,加入20mL王水,低温加热溶解,移入1000mL容量瓶中,加入80mL王水,用水稀释至刻度,混匀。
此溶液含1000μg/mLAu.
金标准溶液:移取25.0mLAu标准贮存溶液于500mL容量瓶中。
加入40mL王水,用水稀释至刻度混匀。
此溶液含50.0μg/mLAu.
三、仪器及工作条件
WFX-1B型原子吸收光谱仪。
金空心阴极灯;灯电流3mA;波长242.8mm;光谱通带
0.4nm;燃烧器高度6mm;空气流量7.0L/min;乙炔流量1.8L/min.
四、分析步骤
称取10.00~30.00g试样于瓷坩埚中,从低温升至650℃灼烧2h(中途搅拌一次)。
取出冷却,转入烧杯中,用水润湿,加入80mL王水,低温加热分解并蒸至体积约为25mL,取下,用水冲洗表皿和杯壁,加入10mL10g/L动物胶溶液,搅拌数分钟,加入100mL水,搅匀。
将试样溶液倒入已制备好的活性炭吸附柱上的布氏漏斗中,抽滤,用热HCl(1+19)洗涤烧杯及残渣4~5次,取下布氏漏斗,用50g/LNH4F热溶液洗涤吸附柱7~8次,再用热HCl(1+19)洗涤7~8次,热水7~8次。
停止抽滤,将活性炭和纸浆移入瓷坩埚中,用小张滤纸擦将残留的活性炭,合并于坩埚中,将坩埚置于电炉上,待坩埚中内容物干燥炭化后,移入700℃马弗炉中灼烧至完全灰化并保温10min,取出坩埚冷却。
于坩埚中加入5mL王水,低温加热溶解并蒸至2~3mL时取下,移入25mL容量瓶中用水稀释至刻度,混匀。
调整AAS仪至似定的工作条件,将试液吸入空气-乙炔火焰中,测定Au的吸光度。
工作曲线的绘制:分别移取含0、25、50、75、100、150、200、250μgAu标准溶液于一组25mL容量瓶中,加入2mL王水,用水稀释至刻度,混匀。
与试样溶液同批测定。
以Au的质量浓度为横坐标,相应的吸光度为纵座标,绘制工作曲线。
五、分析结果的计算
按下式计算试样中Au的含量。
式中ωB——被测元素(组分)的质量分数,其中B指被测元素(组分)
ρB2——工作曲线上查得试液中被测元素的质量浓度,μg/mL;
ρB1——工作曲线上查得空白试液中被测元素的质量浓度,μg/mL;
Vs——试样溶液的总体积,mL;
ms——称取试样的质量,g.
六、注意事项
(1)试样要充分灼烧,以除尽有机物、炭、硫等,否则会使分析结果偏低,(2)用活性炭富集后的灰化温度不宜太高,以防Au的损失,但灰化必须完全,否则结果偏低。
(3)根据Au的含量高低可以扩大或缩小测定试液的体积。
(4)分析含Sb、As高的试样时,先用HCl-SnCl2分解,经过滤分离和残渣于700℃灼烧,将Sb、As等共存干扰元素除去。
再用王水分解、泡沫塑料吸附、硫脲解脱。
将解脱液吸入空气-乙炔火焰中,用AAS法测定Au的吸光度。
本法适用于含Sb、As量高的岩石矿物中w(As)/10-6=0.1~30和测定。