醋酸乙烯酯溶液聚合生产工艺.ppt
- 格式:pdf
- 大小:1.46 MB
- 文档页数:13


高分子化学实验报告08高分子材料与工程(1)班刘奕杉0814121024刘莹0814121025醋酸乙烯酯的溶液聚合实验目的(1)通过聚醋酸乙烯酯的制备,掌握溶液聚合的一般方法和基本实验技巧。
(2)通过实验了解醋酸乙烯酯的特点。
实验原理溶液聚合是将单体和引发剂溶于适当的溶剂中进行的聚合反应,生戊的聚合物能济于溶剂的叫均相溶液聚合,聚合物不溶于溶剂而析出者,称异相溶液聚合或沉淀聚合。
在聚合过程中存在向溶剂链转移的反应,使产物分子量降低。
因此,在选择溶剂时必须注意溶剂的活性大小。
各种溶剂的链转移常数变动很大,水为零,苯较小,卤代烃较大。
一般根据聚合物分子量的要求选择合适的溶剂。
另外还要注意溶剂对聚合物的溶解性能,选用良溶剂时,反应为均相聚合,可以消除凝胶效应,遵循正常的自由基动力学规律。
选用沉淀剂时,则成为沉淀聚合,凝胶效应显著。
产生凝胶效应时,反应自动加速,分子量增大,劣溶剂的影响介于其间,影响程度随溶剂的优劣程度和浓度而定。
本实验以偶氮二异丁腈为引发剂,甲醇为溶剂的醋酸乙烯酯的溶液聚合,属于自由基聚合反应实验步骤在装有搅拌器、回流冷凝管和温度汁的反应瓶中加入醋酸乙烯酯20g(可折算成体积后用移液管虽取),再将另一小烧杯重预先准备好的偶氮二异丁腈溶液(0.05g 溶于5mI 甲醇中)倒入反应瓶,升温,控制反应瓶内温度61—63℃,注意观察体系内粘度的变化,3h 后。
停止反应,将瓶内的物料倒入表面皿中,放入50℃真空烘箱中干燥.得无色透明树脂,称重。
在升温前,应将引发剂充分振荡,均匀分散在单体中。
实验过程补充说明:反应后期,聚合物极粘稠,搅拌阻力较大,加入了少量甲醇。
前期的引发剂量不够,反应比较平和,循环水的量比起前几次的小在反应的中期补加一定的引发剂。
实验装置图实验注意事项1 转速要保持一定,以保证反应稳定进行,聚合产物较为均一。
2 为避免反应过程中出现冻胶甚至产物结块,引发剂的滴加速度要慢,如反应过程中发现可能出现的冻胶时,应加快搅拌速度,并适当补加一些甲醇。

实验02 醋酸乙烯酯的溶液聚合与聚乙烯醇的制备一.实验目的二.实验原理三.主要仪器和试剂四.实验步骤五.注意事项六.问题与讨论一.实验目的1.通过本实验掌握醋酸乙烯酯溶液聚合方法;2.了解聚醋酸乙烯酯制备聚乙烯醇方法;3.通过高分子转化反应了解溶液聚合、高分子侧基反应原理及醇解度测定方法。
二.实验原理本实验采用自由基溶液聚合反应。
选用乙醇作溶剂,是由于PVAc能溶于乙醇,而且聚合反应中活性链对乙醇的链转移常数较小。
而且在醇解制取PVA时,加入催化剂后在乙醇中经侧基转化反应即可直接进行醇解。
二.实验原理PVAc的醇解可以在酸性或碱性催化下进行,目前工业上都采用碱性醇解法。
另一方面,乙醇中的水对醇解会产生阻碍作用,因为水的存在使反应体系内产生CH3COONa,消耗了NaOH,而NaOH 在此是起催化作用,因此要严格控制乙醇中的水的含量。
三.主要仪器和试剂1.实验仪器250ml三口瓶x1、回流冷凝管x1、搅拌器x1、100ml滴液漏斗x12.实验试剂醋酸乙烯酯、氢氧化钠(NaOH)、乙醇、偶氮二异丁腈(AIBN)三.主要仪器和试剂图2-1 聚醋酸乙烯酯醇解装置四.实验步骤1.聚醋酸乙烯酯(PVAc)的制备:如图1-1搭好装置,在250ml三口烧瓶中加入20g乙醇、40g醋酸乙烯酯和0.05g AIBN,开始搅拌。
当AIBN完全溶解后,升温至60±2℃反应3小时,加入40g乙醇备醇解用。
2.将大部分聚合物溶液倒入回收瓶中,反应瓶内留下约15g。
用15ml乙醇将瓶口处的溶液冲净。
四.实验步骤醇解:如图2-1搭好装置,在反应瓶中加入85ml乙醇。
开动搅拌,待溶解均匀后,在25℃下慢慢滴加5%的NaOH/乙醇溶液2.8ml (约2秒/滴)。
仔细观察,约1~1.5小时发生相转变。
这时再滴加1.2ml的NaOH/乙醇溶液,继续反应1小时,用布氏漏斗抽滤,所得聚醋酸乙烯酯(PVA)为白色沉淀,分别用15ml乙醇洗涤3次。




高分子化学实验醋酸乙烯酯的溶液聚合一、目的要求1、通过本实验掌握溶液聚合的实验方法和溶液聚合的特点。
2、掌握醋酸乙烯酯聚合原理及溶剂对醋酸乙烯酯溶液聚合的影响。
二、实验基本原理1、单体的性质醋酸乙烯酯的分子量为86.09。
纯的醋酸乙烯酯的聚合能力很强,在常温下能缓慢聚合,在光和引发剂的作用下聚合的速度显著提高。
聚合过程为放热反应,故聚合开始后即能自行加快聚合速度。
醋酸乙烯醋在无机酸或碱的作用下易发生水解,生成乙醛和乙酸。
受热的稳定温度可达到400℃。
醋酸乙烯酯(VAC)的物化常数凝固点(℃) -84沸点(℃) 73密度 0.9342n 1.3958折光率20D膨胀系数(5-250)(l/℃) 0.00155粘度(20℃)厘泊 0.432燃烧热(kJ/mol) 2072.07生成热(kJ/mol) 118.46蒸馏潜热(kJ/mol) 32.65闪点(℃) -5—8水中溶解度(20℃)% 2.5水在VAC中溶解度(20℃)% 0.12、聚合反应机理醋酸乙烯酯的聚合方式按自由基型链式反应进行。
常用的引发剂是过氧化物体系和偶氮双腈体系、反应过程中除链引发、链增长、链终止三个分数外还有链转移反应,反应机理如下:(1) 链引发(2)链增长(3)链转移在醋酸乙烯酯聚合反应中,由于RCH 2CHOCOCH 3的活性大,增长的活性链容易向溶剂,向单体以及向已生成的聚合物大分子转移。
① 向溶剂转移ktr n n M HA M H A +−−→+如果A·不活泼,不与单体发反,或反应速度很小HA 就称为阻聚剂或缓聚剂。
如A ·很活泼,易与单体发生反应,重新引起聚合反应,HA 就称为链转移剂。
有溶剂情况下平均聚合度式中:DP0—无溶剂存在条件下时聚合物平均聚合度。
[S] —溶剂浓度[M]—单体浓度Cs —链转移常数② 向单体转移,可形成支链聚合物232332323222222~~R nM RCH CHOOCCH CH CHOOCCH RCH CHOOCCH CH CHOOCCH RCH CHOOCCH CH CHOOCCH CH CHOOCCH RCH CHOOCCH +=⇒→=+→+==−−→或③ 向大分子转移,也可形成支链聚合物(4)终止链链终止一般按偶合终止和歧化终止两种方式进行。

醋酸⼄烯酯的溶液聚合⾼分⼦化学实验醋酸⼄烯酯的溶液聚合⼀、⽬的要求1、通过本实验掌握溶液聚合的实验⽅法和溶液聚合的特点。
2、掌握醋酸⼄烯酯聚合原理及溶剂对醋酸⼄烯酯溶液聚合的影响。
⼆、实验基本原理1、单体的性质醋酸⼄烯酯的分⼦量为86.09。
纯的醋酸⼄烯酯的聚合能⼒很强,在常温下能缓慢聚合,在光和引发剂的作⽤下聚合的速度显著提⾼。
聚合过程为放热反应,故聚合开始后即能⾃⾏加快聚合速度。
醋酸⼄烯醋在⽆机酸或碱的作⽤下易发⽣⽔解,⽣成⼄醛和⼄酸。
受热的稳定温度可达到400℃。
醋酸⼄烯酯(VAC)的物化常数凝固点(℃) -84沸点(℃) 73密度 0.9342n 1.3958折光率20D膨胀系数(5-250)(l/℃) 0.00155粘度(20℃)厘泊 0.432燃烧热(kJ/mol) 2072.07⽣成热(kJ/mol) 118.46蒸馏潜热(kJ/mol) 32.65闪点(℃) -5—8⽔中溶解度(20℃)% 2.5⽔在VAC中溶解度(20℃)% 0.12、聚合反应机理醋酸⼄烯酯的聚合⽅式按⾃由基型链式反应进⾏。
常⽤的引发剂是过氧化物体系和偶氮双腈体系、反应过程中除链引发、链增长、链终⽌三个分数外还有链转移反应,反应机理如下:(1)链引发(2)链增长(3)链转移在醋酸⼄烯酯聚合反应中,由于RCH 2CHOCOCH 3的活性⼤,增长的活性链容易向溶剂,向单体以及向已⽣成的聚合物⼤分⼦转移。
①向溶剂转移ktr n n M HA M H A +??→+如果A·不活泼,不与单体发反,或反应速度很⼩HA 就称为阻聚剂或缓聚剂。
如A ·很活泼,易与单体发⽣反应,重新引起聚合反应,HA 就称为链转移剂。
有溶剂情况下平均聚合度式中:DP0—⽆溶剂存在条件下时聚合物平均聚合度。
[S] —溶剂浓度[M]—单体浓度Cs —链转移常数②向单体转移,可形成⽀链聚合物232332323222222~~R nM RCH CHOOCCH CH CHOOCCH RCH CHOOCCH CH CHOOCCH RCH CHOOCCH CH CHOOCCH CH CHOOCCH RCH CHOOCCH +=?→=+→+==??→或③向⼤分⼦转移,也可形成⽀链聚合物(4)终⽌链链终⽌⼀般按偶合终⽌和歧化终⽌两种⽅式进⾏。

醋酸乙烯酯溶液聚合及官能团反应聚乙烯醇缩丁醛的制备一、目的要求1.掌握溶液聚合的基本原理和实验技术2.了解聚合物中官能团反应的知识。
二、原理从醋酸乙烯酯制备聚乙烯醇和聚乙烯醇缩丁醛,共三部分。
1.醋酸乙烯酯(V AC )溶液聚合。
在本实验采用均相溶液聚合方法,在溶液聚合中选择适当的溶剂是聚合过程的关键之一,在选择溶剂时除了考虑溶剂对单体和引发剂有良好的溶解性外,还必须考虑其链转移常数。
因为直接影响聚合物的分子量和分子量分布。
能溶解V AC 的溶剂很多,如甲醇、苯、甲苯、丙酮、二氯乙烷、醋酸乙酯、无水乙醇等。
本实验的最终产物是为了合成聚乙烯醇(PV A ),所以采用甲醇为溶剂是有利的,因为甲醇的链转移常数比较小,制成的醋酸乙烯酯—甲醇溶液不需要进行分离,可直接进行醇解。
聚合反应式:nCH 2CHO C CH 3OAIBNCH 2CH O C CH 3On2.聚醋酸乙烯酯的醇解反应—大分子官能团反应聚醋酸乙烯酯(PV AC )的醇解属大分子功能团反应。
PV AC 可以在酸(如硫酸、盐酸和高氯酸等)的作用下,进行水解生成聚乙烯醇,一般称为酸法水解,也可以在碱的作用下进行水解生成PV A ,一般称为碱法水解,这一过程通常叫做醇解或皂化,而碱法醇解又分为湿法(高碱)和干法(低碱)两种。
所谓湿法醇解就是原料PV AC 甲醇溶液中含有 1 ~ 2 % 的水,催化剂碱也配成水溶液。
湿法醇解的特点是反应速度快,但副反应多,生成的醋酸钠多。
所谓干法醇解就是PV AC 甲醇溶液中不含水,碱也溶于甲醇中,碱的 mol 比也低(只有湿法醇解的十分之一)。
干法醇解的优点是克服了湿法醇解的缺点,但它的醇解速度慢。
本实验采用干法醇解反应主要是酯交换反应。
酯交换反应式:CH2CH O C CH 3OnnCH 3OHNaOHCH 2CH OHnnCH 3C OCH 3O如果是湿法醇解或体系中存在水,则同时发生皂化反应。
皂化反应式:CH2CH O C CH 3OnCH 2CH OHnNaOHCH 3OHCH 3COONa副反应:CH 3COOCH 3 + NaOH → CH 3OH + CH 3COONa 3.聚乙烯醇缩丁醛:CH2CH OHCH 2CHOHCH 3CH 2CH 2CHOHCOOHH2OCH 2CH CH 2CHOOO H 2CH 2CH 3三、药品和仪器 1.药品:1.醋酸乙烯酯的溶液聚合在250 mL 烧杯中加入70 g (75.3 mL )V AC 30 g (38 mL )甲醇和0.210 gAIBN ,用玻璃棒搅拌,待AIBN 完全溶解后将此溶液倒入装有搅拌器、冷凝管和温度计的三颈瓶中。

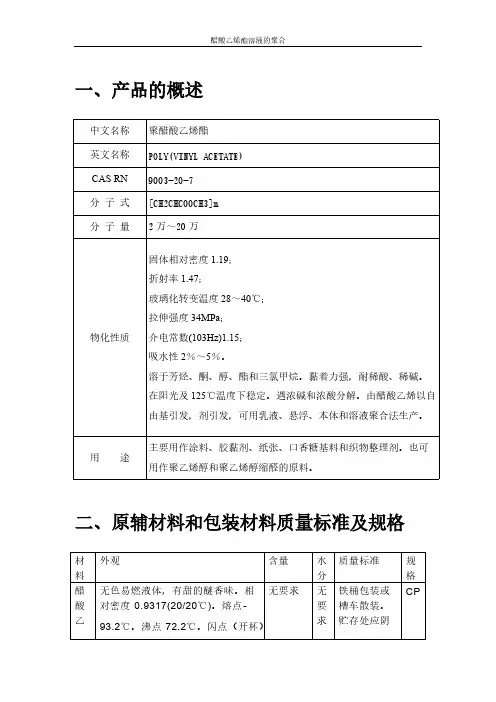
一、产品的概述二、原辅材料和包装材料质量标准及规格三、文献综述3.1实验目的掌握溶液聚合的特点,增强对溶液聚合的感性认识。
同时通过实验了解聚醋酸乙烯酯的聚合特点。
3.1溶液聚合的基本概念定义:将单体和引发剂溶于适当溶剂中,在溶液状态下进行的聚合反应组成:单体+(油溶性)引发剂+溶剂优点:聚合热易扩散,聚合反应温度易控制;可以溶液方式直接成品缺点:单体被溶剂稀释,聚合速率慢,产物分子量较低;消耗溶剂,溶剂的回收处理,设备利用率低,导致成本增加;溶剂的使用导致环境污染问题02醋酸乙烯酯溶液的聚合3.3实验原理溶液聚合一般具有反应均匀、聚合热易散发、反应速度及温度易控制、分子量分布均匀等优点。
在聚合过程中存在向溶剂链转移的反应,使产物分子量降低。
因此,在选择溶剂时必须注意溶剂的活性大小。
各种溶剂的链转移常数变动很大,水为零,苯较小,卤代烃较大。
一般根据聚合物分子量的要求选择合适的溶剂。
另外还要注意溶剂对聚合物的溶解性能,选用良溶剂时,反应为均相聚合,可以消除凝胶效应,遵循正常的自由基动力学规律。
选用沉淀剂时,则成为沉淀聚合,凝胶效应显著。
产生凝胶效应时,反应自动加速,分子量增大,劣溶剂的影响介于其间,影响程度随溶剂的优劣程度和浓度而定。
本实验以甲醇为溶剂进行醋酸乙烯酯的溶液聚合。
根据反应条件的不同,如温度、引发剂量、溶剂等的不同可得到分子量从2000到几万的聚醋酸乙烯酯。
聚合时,溶剂回流带走反应热,温度平稳。
但由于溶剂引入,大分子自由基和溶剂易发生链转移反应使分子量降低。
聚醋酸乙烯酯适于制造维尼纶纤维,分子量的控制是关键。
由于醋酸乙烯酯自由基活性较高,容易发生链转移,反应大部分在醋酸基的甲基处反应,形成链或交链产物。
除此之外,还向单体、溶剂等发生链转移反应。
所以在选择溶剂时,必须考虑对单体、聚合物、分子量的影响,而选取适当的溶剂。
温度对聚合反应也是一个重要的因素。
随温度的升高,反应速度加快,分子量降低,同时引起链转移反应速度增加,所以必须选择适当的反应温度。
高分子化学实验报告10高二醋酸乙烯酯的溶液聚合实验三危平福1014122030丁胜10141220072013/5/8一、实验目的:1、学习水溶液的聚合方法制备醋酸乙烯酯溶液2、了解水溶液聚合机理及聚合中各个组分的作用。
二、实验原理:i[聚醋酸乙烯酯]〔也称作聚乙酸乙烯酯,简称PVA、PVAc是一种有弹性的合成聚合物。
聚醋酸乙烯酯是通过醋酸乙烯酯〔VAM的聚合而制备的。
聚合物的部分或全部水解用于制备聚乙烯醇。
聚乙烯醇产品的水解率一般在87%至99%之间。
聚醋酸乙烯酯是弗里溶液聚合是将单体和引发剂溶于适当的溶剂中进行的聚合反应,生成的聚合物能溶于溶剂的叫均相溶液聚合,聚合物不溶于溶剂而析出者,称异相溶液聚合或沉淀聚合。
茨·克拉特1912年在德国发现的;它是最常用的木材用胶,被称作白胶水〔白胶浆,聚醋酸乙烯酯被广泛地应用于印刷装订和书籍艺术溶液聚合是将单体和引发剂溶于适当的溶剂中进行的聚合反应生成的聚合物能溶于溶剂的叫均相溶液聚合聚合物不溶于溶剂而析出者称异相溶液聚合或沉淀聚合。
优点:一、与本体聚合相比,溶液聚合有溶剂为传热介质聚合强度容易控制;二、体系中聚合物浓度较低能消除自动加速现象聚合物分子量比较均—;三、不易进行链自由基向大分子转移而生成支化或交联的产物;四、反应后的物料也可直接使用。
缺点:一、单体浓度小聚合速率低设备利用率;二、低单体浓度低和向溶剂链转移结果致使聚合物分子量不高;三、聚合物中夹带微量溶剂溶解回收麻烦而且多为易染、易爆的有毒物。
这些缺点使得溶液聚合在工业上应用不如悬浮聚合和乳液聚合多。
本实验以偶氮二异丁腈为引发剂甲醇为溶剂的醋酸乙烯酯的溶液聚合属于自由基聚合反应。
自由基聚合微观动力学:链引发速率:链增长速率:链终止速率:总速率方程表明聚合速率与发剂浓度的平方根、单体浓度的一次方根成正比。
本次实验中引发剂用量由0.05g提高到0.2g,溶剂用量由5ml提高到20ml,假设各反应物混合后体积不变,则引发剂浓度由0.05/〔5+20/0.93=0.001887g/ml提高到0.2/〔20+20/0.93=0.004819g/ml所以[I]提高2.55倍,单体浓度20/25.5=0.7843g/ml降低到20/41.5=0.4819g/ml [M]降低1.63倍,所以总速总速率并未提高,反而下降了。
实验五醋酸乙烯酯的溶液聚合及聚醋酸乙烯酯的醇解聚乙烯醇是制备维纶的原材料。
由于乙烯醇很不稳定,极易异构化成乙醛。
所以聚乙烯醇通常都是通过醋酸乙烯溶液聚合以及聚醋酸乙烯酯的醇解这两个步骤来制得的。
本实验是以偶氮二异丁腈为引发剂;甲醇为溶剂的醋酸乙烯酯的溶液聚合。
这是个自由基聚合反应。
一、实验目的1、通过实验掌握醋酸乙烯酯溶液聚合的方法以及聚醋酸乙烯酯醇解的方法。
2、进一步掌握溶液聚合原理及高分子侧基反应原理。
3、掌握醇解度测定方法。
二、实验原理本实验采用溶液聚合的自由基聚合原理。
选用甲醇作溶剂是由于聚醋酸乙烯酯(PV Ac)能溶于甲醇,而且聚合反应中活性链对甲醇的链转移常数较小。
且在醇解制取聚乙烯醇(PV A)时,加入催化剂后在甲醇中即可直接进行醇解。
醋酸乙烯(V Ac)在聚合过程中,容易发生向聚合物链的链转移反应。
聚合物浓度越大,支化越容易发生。
聚合物活性自由基链除了向聚醋酸乙烯酯(PV Ac)主链上的α、β氢处链转移,形成水解不掉的支链,还会向乙酰基上活泼氢原子转移,在乙酰基上形成支链。
这部分支链容易水解脱掉,导致聚合度降低。
在聚合反应的同时,可能存在副反应:(2)在单体浓度为85%时聚合得聚醋酸乙烯酯(PVAc),醇解后聚合度下降38.15%。
单体浓度为67%时醇解后只降低了6.89%。
因此,要降低溶液中单体浓度。
但单体浓度过低,会影响产物的最终聚合度。
表1 60℃甲醇中不同单体浓度溶液聚合得到PVAc和PVA的聚合度单体浓度/% 聚合时间/h 转化率/% PVAc聚合度PVA聚合度聚合度降低/%85 16 96.2 1903 1177 38.1567 17 96.6 668 622 6.89聚醋酸乙烯酯(PVAc)的醇解可以在酸性或碱性的催化下进行,用酸性醇解时,由于痕量级的酸很难从PVA中除去,而残留的酸可加速PVA的脱水作用,使产物变黄或不溶于水,所以一般均采用碱性醇解法。
另外,甲醇中的水对醇解会产生阻碍作用。
实验五醋酸乙烯酯的溶液聚合及聚醋酸乙烯酯的醇解聚乙烯醇是制备维纶的原材料。
由于乙烯醇很不稳定,极易异构化成乙醛。
所以聚乙烯醇通常都是通过醋酸乙烯溶液聚合以及聚醋酸乙烯酯的醇解这两个步骤来制得的。
本实验是以偶氮二异丁腈为引发剂;甲醇为溶剂的醋酸乙烯酯的溶液聚合。
这是个自由基聚合反应。
二、实验原理本实验采用溶液聚合的自由基聚合原理。
选用甲醇作溶剂是由于聚醋酸乙烯酯(PV Ac)能溶于甲醇,而且聚合反应中活性链对甲醇的链转移常数较小。
且在醇解制取聚乙烯醇(PV A)时,加入催化剂后在甲醇中即可直接进行醇解。
醋酸乙烯(V Ac)在聚合过程中,容易发生向聚合物链的链转移反应。
聚合物浓度越大,支化越容易发生。
聚合物活性自由基链除了向聚醋酸乙烯酯(PV Ac)主链上的α、β氢处链转移,形成水解不掉的支链,还会向乙酰基上活泼氢原子转移,在乙酰基上形成支链。
这部分支链容易水解脱掉,导致聚合度降低。
在聚合反应的同时,可能存在副反应:(2)在单体浓度为85%时聚合得聚醋酸乙烯酯(PVAc),醇解后聚合度下降38.15%。
单体浓度为67%时醇解后只降低了6.89%。
因此,要降低溶液中单体浓度。
但单体浓度过低,会影响产物的最终聚合度。
表1 60℃甲醇中不同单体浓度溶液聚合得到PVAc和PVA的聚合度单体浓度/% 聚合时间/h 转化率/% PVAc聚合度PVA聚合度聚合度降低/%85 16 96.2 1903 1177 38.1567 17 96.6 668 622 6.89聚醋酸乙烯酯(PVAc)的醇解可以在酸性或碱性的催化下进行,用酸性醇解时,由于痕量级的酸很难从PVA中除去,而残留的酸可加速PVA的脱水作用,使产物变黄或不溶于水,所以一般均采用碱性醇解法。
另外,甲醇中的水对醇解会产生阻碍作用。
因为水的存在使反应体系内产生CH3COONa,消耗了NaOH,而NaOH在此起的是催化作用。
因此,一定要严格控制甲醇中的水的含量。