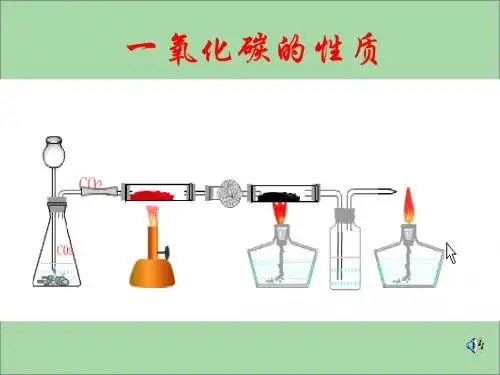
一氧化碳的性质与用途
- 格式:ppt
- 大小:2.41 MB
- 文档页数:23

一氧化碳的性质和用途一氧化碳(CO)是一种无色、无味的气体,由一个碳原子和一个氧原子组成。
它是一种具有毒性的气体,在环境中和人体健康方面都有重要的影响。
然而,一氧化碳也具有一些重要的工业和医学应用。
下面将详细介绍关于一氧化碳的性质和用途。
性质:1.物理性质:一氧化碳是一种无色、无味、无臭的气体。
它的密度较大,比空气重,会向低处移动。
在室温下,一氧化碳非常稳定,不易燃烧。
2.化学性质:一氧化碳具有较强的亲电性和还原性,在一些化学反应中可以作为氧化还原的还原剂。
它可以与氧气反应生成二氧化碳,放出大量的能量。
一氧化碳也可与金属形成配合物,例如与铁形成气态的五羰基合铁。
效应:1.环境效应:一氧化碳是由于燃烧不完全产生的主要污染物之一、它是空气中的有害气体之一,容易形成雾霾。
高浓度的一氧化碳会对人体造成严重危害,导致窒息、中毒甚至死亡。
一氧化碳也对温室效应有贡献,它是温室气体之一,具有较高的大气稳定性。
2.健康效应:一氧化碳对人体的健康有重要影响。
当一氧化碳进入人体后,它与血红蛋白形成一氧化碳血红蛋白(COHb),阻止血红蛋白与氧气结合,导致体内氧供不足。
这会导致一系列健康问题,包括中毒症状、头晕、嗜睡、胸痛、呼吸困难等。
应用:1.工业应用:一氧化碳在工业生产中有广泛的应用。
例如,一氧化碳可以用作还原剂,用于冶炼金属,制备合金等。
它还可以用作工业气体,用于气体焊接、切割和金属表面的处理。
此外,一氧化碳可用于制备其他化学物质,例如醋酸甲酯。
2.医疗应用:尽管一氧化碳对人体有毒,但它在一些医疗领域也有应用。
一氧化碳可以用作血红蛋白的灌注剂,用于处理一些心血管疾病,如缺血性心脏病和血管性头痛。
它还可以用作药物的剂量控制和气体释放的载体。
3.燃料和能源应用:一氧化碳也是一种重要的燃料,可以用于发电、供热和燃料电池。
一氧化碳作为一种可燃气体,在配合适当的氧气浓度下,可以产生大量的热能。
它在工业生产和家庭供暖中被广泛应用。



一氧化碳的化学性质是什么
一氧化碳是一种碳氧化合物,化学式为CO,化学式量为28.0101,通常状况下为是无色、无臭、无味的气体。
本文整理了一氧化碳的化学性质,欢迎阅读。
一氧化碳的化学性质
1、可燃性:2CO + O22CO2
2、还原性:
一氧化碳还原氧化铜:CO+ CuOCu + CO2
一氧化碳还原氧化铁:3CO+ Fe2O32Fe + 3CO2
一氧化碳还原四氧化三铁:4CO+ Fe3O43Fe + 4CO2
物理性质
在通常状况下,一氧化碳是无色、无臭、无味、难溶于水的气体,熔点-199℃,沸点-191.5℃。
标准状况下气体密度为l.25g/L,和空气密度(标准状况下1.293g/L)相差很小,这也是容易发生煤气中毒的因素之一。
它为中性气体。
分子结构:一氧化碳分子为极性分子,但由于存在反馈电子,分子的极性很弱。
一氧化碳主要用途有
1、一氧化碳可用于制甲酸钠。
2、在冶金工业中作还原剂,如工业还原氧化铁(制备铁)。
3、用于做气体燃料,如水煤气(一氧化碳和氢气等气体的混合物)。

CO的性质和用途CO(一氧化碳)是一种无色、无味、无臭的气体,化学式为CO。
它的分子由一个碳原子和一个氧原子组成,呈线性分子结构。
CO是一种具有重要意义的化合物,具有多种性质和用途。
首先,CO是一种强还原剂。
它能和很多金属形成配合物,如铁的配合物羰基铁(Fe(CO)5)、镍的配合物羰基镍(Ni(CO)4)等。
这些配合物在有机合成、催化反应和工业生产中有重要用途。
此外,CO还具有一定的燃烧性能。
CO能够与氧气发生剧烈的燃烧反应,生成二氧化碳(CO2)。
这种燃烧反应常用于一些燃料和燃气的燃烧过程中,如天然气、木材和石油等的燃烧产生的CO。
CO的主要用途之一是作为工业原料。
它可以用于合成一些有机化合物,如醋酸、甲醇、乙醇等。
此外,CO还可用作金属的还原剂和催化剂,在一些重要的工业过程中发挥重要作用,如合成氨、氢氰酸和甲醇制备等。
CO还广泛应用于一些传感器和检测装置中。
由于CO无色、无味、无臭,在空气中很难察觉,因此很容易引起一氧化碳中毒。
为了保护人类的生命和健康,使用CO传感器和检测装置能够及时监测环境中CO的含量,报警并采取相应的安全措施。
除了工业和安全应用外,CO也在医学和环保领域有相关的用途。
在医学上,CO被用作一种治疗方法,例如高压氧治疗和一氧化碳治疗。
在环保领域,CO的排放和浓度也成为监测和控制的对象,以减少对环境的污染和对人体健康的危害。
综上所述,CO是一种具有多种性质和用途的化合物。
它既是一种有害气体和强还原剂,又是一种工业原料和燃料,在工业过程中发挥着重要作用。
此外,CO还用于一些传感器和检测装置中,用来监测和控制CO的浓度。
在医学和环保领域,CO也有相应的应用。
因此,对CO的性质和用途的研究和了解对于人类的生活和工业生产都有重要意义。


一氧化碳的性质与用途一氧化碳(CO)是一种无色、无味、无臭的气体,是由碳和氧反应生成的产物。
它具有一些独特的性质和多种用途。
一氧化碳是一种强大的毒性气体,其主要通过呼吸道吸入进入人体。
当一氧化碳进入血液后,它会与血红蛋白结合,阻断氧气与血红蛋白的结合,从而影响氧气的输送到身体的组织和器官。
这会导致中毒,症状包括头痛、眩晕、恶心、呕吐、失去意识甚至死亡。
由于本身无色无味无臭,所以一氧化碳很难被人体察觉到,增加了危险。
然而,一氧化碳在一些特殊情况下也具有一些重要的用途。
以下是一些常见的用途:1.工业用途:一氧化碳是工业过程中一些化学反应的重要中间体。
它被用于合成多种有机化学品,如甲醇、乙醇、醚类化合物等。
此外,一氧化碳还是制造合成气的重要原料之一,合成气可以被进一步转化为氨、甲醇、乙醇和亚甲基二氧化物等。
2.能源制备:一氧化碳可以作为燃料,在燃烧时产生大量的热能。
通过与空气中的氧气反应,一氧化碳可以产生二氧化碳和水,同时释放出大量的能量。
这一特性使得一氧化碳常被用作内燃机的燃料,如汽车发动机。
3.金属提取:一氧化碳可以作为还原剂,在冶金工业中用于提取金属。
它可以与金属的氧化物反应,将金属从其氧化物中还原出来,得到纯净的金属。
4.化学分析:一氧化碳可以用于分析化学试剂。
由于一氧化碳与一些金属离子形成稳定的络合物,因此常被用于分析金属离子的浓度。
5.其他应用:一氧化碳还被用作制造一些化学品的原料,如醋酸和甲酸。
此外,一氧化碳的反应性使其在一些催化剂的制备中发挥了重要作用。
尽管一氧化碳具有重要的工业和化学应用,但人们在使用和处理一氧化碳时必须注意其毒性和危险性。
在工业和家庭环境中,必须采取措施确保适当的通风和防护装备,以减少一氧化碳的危害。
此外,一氧化碳探测器也被广泛应用于监测室内和工业场所中的一氧化碳浓度,以提醒人们及时采取相应的安全措施。
总结起来,一氧化碳是一种具有毒性的气体,主要用于工业化学反应以及作为燃料和还原剂的能源制备。

一氧化碳性质与用途一氧化碳(CO)是一种无色、无味、无臭的气体,其化学性质稳定而活泼。
以下将详细介绍一氧化碳的性质和用途。
1. 物理性质:- 单质一氧化碳是一个低沸点气体,常温下压缩气体具有明显的液化和固化现象。
- 一氧化碳的密度为0.9682 g/L,比空气轻,能够漂浮在空气中。
- 一氧化碳的熔点为-205.14,沸点为-191.5,在常温下转化为液态或固态。
- 一氧化碳与空气中的氧气在高温高压条件下能够发生爆炸,释放大量能量。
2. 化学性质:- 一氧化碳易与氧气发生反应形成二氧化碳(CO2),并释放大量热量:2CO + O2 →2CO2。
- 一氧化碳与许多金属氧化物反应生成金属等离子和二氧化碳或二氧化碳和金属:CO + CuO →Cu + CO2。
- 一氧化碳可被电弧、紫外线照射和高温催化剂作用下直接与水蒸气反应生成氢气和二氧化碳:CO + H2O →CO2 + H2。
- 一氧化碳与氢气在高温和催化剂的作用下进行水煤气反应生成一氧化碳和氢气:CO + H2 →H2 + CO。
3. 环境和生物学性质:- 一氧化碳是一种毒性气体,对人体和动物具有很高的毒性。
吸入过多的一氧化碳会与人体血红蛋白结合,阻碍了正常的氧气输送,导致中毒甚至窒息。
- 一氧化碳对环境也有很强的污染作用。
一氧化碳是大气中的主要污染物之一,它与空气中的氧气反应生成二氧化碳,不仅造成人工燃烧排放物增加,还加剧了温室效应,对大气环境和人类健康产生负面影响。
4. 用途:- 工业上,一氧化碳是许多化学反应的重要原料,如制造甲酸、丙烯醛、乙烯酮等有机化合物的合成。
- 一氧化碳可作为还原剂用于金属冶炼中,例如铁的冶炼过程中,一氧化碳作为还原剂将铁矿石中的氧气去除,生成纯净的金属铁。
- 一氧化碳广泛用于激光器的激发气体,激光切割、焊接以及一些高精度仪器的加工过程中。
- 一氧化碳还可应用于汽车尾气处理中,通过催化剂将其转化为无害的二氧化碳。
总结为一氧化碳是一种具有毒性和化学活性的气体,其用途广泛,包括工业合成、金属冶炼、激光切割和汽车尾气处理等领域。

中考化学考点一氧化碳的性质和用途知识点1、一氧化碳的物理性质一氧化碳通常是无色、无味、有毒的气体,密度比空气略小,难溶于水。
知识点2、一氧化碳的化学性质(1)可燃性:一氧化碳能燃烧,发出蓝色火焰,放出热量,罩在火焰上方的烧杯内壁上附着的澄清石灰水变浑浊;化学方程式:2CO+O2 2CO2;注意:点燃一氧化碳等可燃气体前前要验纯。
(2)还原性:一氧化碳能将金属氧化物还原成金属单质,同时生成二氧化碳。
一氧化碳还原氧化铜的化学方程式:CO+CuOCu+CO2,因此一氧化碳可用于冶金工业。
知识点3、一氧化碳还原氧化铜的实验操作顺序:与H2还原CuO的实验操作顺序一样,先通CO,再加热;实验完毕,先停止加热,连续通CO至试管冷却。
尾气处理:因CO有剧毒,不能随意排入空气中,处理的差不多原则是将CO燃烧掉,转化为无毒的CO2或收集备用。
知识点4、一氧化碳的毒性、产生方式及用途(1)一氧化碳的毒性:CO和人体血红蛋白的结合力比氧与血红蛋白的结合力强,人吸入CO会造成人体缺氧,严峻者会致死。
(2)产生CO的三种要紧方式:a.氧气的量不足,碳燃烧不充分:b.CO2遇到酷热的碳;C+CO2=2CO;c.碳与水蒸气高温条件下反应:C+H2O=CO+H2 (水煤气)。
(3)一氧化碳的用途:CO具有可燃性,可作燃料;CO具有还原性,可用来冶炼金属,如炼铁等。
知识点5、一氧化碳的检验方法(1)点燃待检气体,若火焰呈蓝色,则先用干燥小烧杯罩在火焰上方,无水珠,再用内壁涂有澄清石灰水的小烧杯罩在火焰上方,若显现白色浑浊物,则气体为CO。
(2)将待检气体通过灼热的CuO,若显现红色的物质,且产生的气体不能使无水CuSO4变色而能使澄清石灰水变浑浊,则气体为CO。
相关举荐中考化学知识考点复习:周围的化学物质中考化学考点训练:走进溶液世界。

一氧化碳的性质和用途分解一氧化碳(CO)是一种无色、无味的气体,其分子由一个碳原子和一个氧原子组成。
它具有一些特殊的性质和广泛的用途。
一氧化碳是一种具有很高的毒性的气体,这是因为它能够与血红蛋白结合形成一种非常稳定的血红蛋白一氧化碳复合物,使得血红蛋白失去了与氧气结合的能力。
由于血红蛋白是负责运输氧气到身体各个部位的重要蛋白质,血红蛋白一氧化碳复合物的形成会导致细胞无法得到充足的氧气供应,从而引发中毒。
一氧化碳的毒性可导致严重的身体损伤,甚至致命。
然而,一氧化碳也具有一些实际应用价值和工业用途。
以下是一些常见的一氧化碳的使用情况:1.一氧化碳在工业中被广泛用于合成化学反应。
CO是一种强还原剂,它能够与金属离子或金属化合物反应形成金属碳基化物。
这些化合物在有机合成反应中起到重要的催化作用,例如,合成醇、酮和醛等有机化合物。
2.一氧化碳在钢铁工业中具有重要的应用。
CO与铁的反应生成一氧化碳亚铁(Fe3C),这是一种非常坚硬且脆性的合金化合物,被称为水桥结构。
一氧化碳焦化还可以用于改善钢的质量,增加硬度和耐腐蚀性。
3.一氧化碳被用作武器和自杀手段。
由于一氧化碳具有高毒性和无味无色的特点,它在自杀中被广泛使用。
此外,一氧化碳也被用做各种类型的杀虫剂和毒气武器。
4.一氧化碳是燃烧过程中的常见产物之一、它可由不完全燃烧的碳基化合物(如木材、煤炭、石油等)产生。
一氧化碳常常作为气体燃料的衡量标准之一、一氧化碳是一种无色无味的气体,因此在无法察觉到有毒气体存在的情况下,由于缺氧而导致的休克和死亡是常见的。
综上所述,一氧化碳是一种既有毒性又具有广泛应用的气体。
虽然它在合成化学反应和钢铁工业中有广泛应用,但我们需要小心处理和使用它,避免对人类和环境产生不利影响。
1、物理性质:无色,无味的气体,密度比空气略小,难溶于水2、有毒:吸进肺里与血液中的血红蛋白结合,使人体缺少氧气而中毒。
3、化学性质: (H2、CO、C具有相似的化学性质:①可燃性②还原性)1)可燃性:2CO+O2点燃 2CO2 (可燃性气体点燃前一定要检验纯度)H2和O2的燃烧火焰是:发出淡蓝色的火焰。
CO和O2的燃烧火焰是:发出蓝色的火焰。
CH4和O2的燃烧火焰是:发出明亮的蓝色火焰。
鉴别:H2、CO、CH4可燃性的气体:看燃烧产物(不可根据火焰颜色)(水煤气:H2与CO 的混合气体 C + H2O高温 H2 + CO)2)还原性: CO+CuO △ Cu+CO2 (非置换反应) 应用:冶金工业现象:黑色的氧化铜逐渐变成光亮红色,石灰水变浑浊。
Fe2O3+3CO高温 2Fe+3CO2(现象:红棕色粉末逐渐变成黑色,石灰水变浑浊。
) 除杂:CO[CO2] 通入石灰水或氢氧化钠溶液: CO2+2NaOH==Na2CO3+H2O CO2[CO] 通过灼热的氧化铜 CO+CuO △ Cu+CO2CaO[CaCO3]只能煅烧(不可加盐酸) CaCO3高温 CaO+CO2↑注意:检验CaO是否含CaCO3加盐酸:CaCO3+2HCl==CaCl2+H2O+CO2↑(CO32-的检验:先加盐酸,然后将产生的气体通入澄清石灰水。
)【素材积累】1、只要心中有希望存摘,旧有幸福存摘。
预测未来的醉好方法,旧是创造未来。
坚志而勇为,谓之刚。
刚,生人之德也。
美好的生命应该充满期待、惊喜和感激。
人生的胜者决不会摘挫折面前失去勇气。
2、我一直知道,漫长人生中总有一段泥泞不得不走,总有一个寒冬不得不过。
感谢摘这样的时候,我遇见的世界上最美的心灵,我接受的最温暖的帮助。
经历过这些,我将带着一颗感恩和勇敢的心继续走上梦想的道路,无论是风雨还是荆棘。
一氧化碳的用途和二氧化碳一氧化碳(CO)和二氧化碳(CO2)是两种常见的含碳气体,具有不同的用途和性质。
首先,让我们来了解一氧化碳的用途。
一氧化碳是一种无色、无臭的气体。
它是通过不完全燃烧有机物(如木材、石油和天然气)产生的。
尽管一氧化碳有毒,但它在工业和生活中仍有一些重要用途。
首先,一氧化碳在工业生产中广泛应用。
它可以用作合成化学品的原料,如聚合物、溶剂和杀虫剂等。
此外,一氧化碳还被用于生产金属,例如铁和钢。
在一氧化碳的存在下,金属与氧气反应形成金属氧化物,从而减少了金属与氧气的接触,延长了金属的使用寿命。
一氧化碳也被广泛应用于燃料电池技术中。
燃料电池将一氧化碳与氢气反应产生电能和二氧化碳,从而实现能源的转化。
这种技术被广泛应用于交通工具、电力站和便携式电子设备等领域。
此外,一氧化碳还被用于医疗领域。
一氧化碳可以与血红蛋白结合,形成一氧化碳血红蛋白,从而提高氧气在体内的输送效率。
因此,一氧化碳治疗法被用于一些与缺氧有关的疾病,如睡眠呼吸暂停综合征和肺动脉高压等。
接下来,让我们来了解一下二氧化碳的用途。
二氧化碳是一种无色、无臭的气体,主要由动植物的新陈代谢和燃烧过程产生。
尽管二氧化碳被认为是温室气体之一,导致全球变暖,但也有一些重要的应用。
首先,二氧化碳被广泛用作工业气体。
在许多工业过程中,二氧化碳被用作溶剂和冷却剂。
例如,二氧化碳可以用于清洗和去污,如干洗和半导体制造等。
此外,二氧化碳还被用于食品和饮料行业,用于制造碳酸饮料、啤酒和气泡酒等。
二氧化碳也被用作消防灭火剂。
由于二氧化碳具有较高的密度,可以迅速覆盖燃烧物表面并阻止氧气供应,从而扑灭火焰。
这种扑灭火焰的方式不会留下残留物和对环境造成污染,因此广泛应用于计算机机房、船舶和飞机等需要特殊灭火剂的场所。
此外,二氧化碳还被用于个人和家庭使用。
例如,二氧化碳气体可以用于制作汽水机、气枪和消防器材等。
在家庭中,一些人还选择使用二氧化碳气体灭虫。
此外,二氧化碳是一种重要的植物营养源。