生物化学维生素与辅酶章节考点总结
- 格式:doc
- 大小:148.50 KB
- 文档页数:24

第三章酶与辅酶一、知识要点在生物体的活细胞中每分每秒都进行着成千上万的大量生物化学反应,而这些反应却能有条不紊地进行且速度非常快,使细胞能同时进行各种降解代谢及合成代谢,以满足生命活动的需要。
生物细胞之所以能在常温常压下以极高的速度和很大的专一性进行化学反应,这是由于生物细胞中存在着生物催化剂——酶。
酶是生物体活细胞产生的具有特殊催化能力的蛋白质。
酶作为一种生物催化剂不同于一般的催化剂,它具有条件温和、催化效率高、高度专一性和酶活可调控性等催化特点。
酶可分为氧化还原酶类、转移酶类、水解酶类、裂解酶类、异构酶类和合成酶类六大类。
酶的专一性可分为相对专一性、绝对专一性和立体异构专一性,其中相对专一性又分为基团专一性和键专一性,立体异构专一性又分为旋光异构专一性、几何异构专一性和潜手性专一性。
影响酶促反应速度的因素有底物浓度(S)、酶液浓度(E)、反应温度(T)、反应pH值、激活剂(A)和抑制剂(I)等。
其中底物浓度与酶反应速度之间有一个重要的关系为米氏方程,米氏常数(K m)是酶的特征性常数,它的物理意义是当酶反应速度达到最大反应速度一半时的底物浓度。
竞争性抑制作用、非竞争性抑制作用和反竞争性抑制作用分别对Km 值与V max的影响是各不相同的。
酶的活性中心有两个功能部位,即结合部位和催化部位。
酶的催化机理包括过渡态学说、邻近和定向效应、锁钥学说、诱导楔合学说、酸碱催化和共价催化等,每个学说都有其各自的理论依据,其中过渡态学说或中间产物学说为大家所公认,诱导楔合学说也为对酶的研究做了大量贡献。
胰凝乳蛋白酶是胰脏中合成的一种蛋白水解酶,其活性中心由Asp102、His57及Ser195构成一个电荷转接系统,即电荷中继网。
其催化机理包括两个阶段,第一阶段为水解反应的酰化阶段,第二阶段为水解反应的脱酰阶段。
同工酶和变构酶是两种重要的酶。
同工酶是指有机体内能催化相同的化学反应,但其酶蛋白本身的理化性质及生物学功能不完全相同的一组酶;变构酶是利用构象的改变来调节其催化活性的酶,是一个关键酶,催化限速步骤。

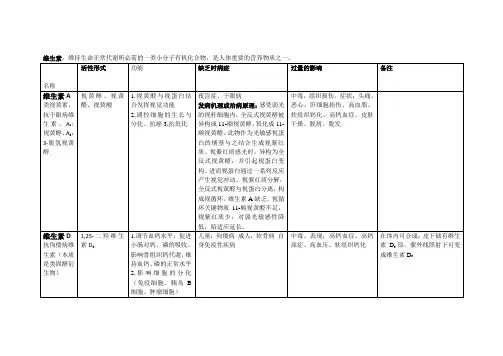
维生素与辅酶一、教学大纲基本要求4种脂溶性维生维生素即:维生素A与胡萝卜素,维生素D,维生素E和维生素K;10种水溶性维生素及其辅酶即:维生素B1,维生素B2,维生素B3,维生素B5,维生素B6,维生素B7,维生素B11,维生素B12,硫辛酸和维生素C。
二、本章知识要点(一)维生素(Vitamin)的概念1.维生素(Vitamin)的概念:维生素是维持机体正常代谢和健康所必需的,但体内不能合成或合成量不足,必须靠食物供给的一类小分子有机化合物。
2.维生素的分类:根据维生素溶解的性质可分为脂溶性维生素和水溶性维生素两大类。
(1)脂溶性维生素(Lipid-Soluble Vitamin)包括维生素A、D、E、K。
(2)水溶性维生素(Water-Soluble Vitamin)包括B族维生素和维生素C,B族维生素又包括维生素B1、B2、PP、B6、泛酸、生物素、叶酸、B12等。
3.维生素缺乏原因: (1)摄入量不足。
(2)吸收障碍。
(3)需要量增加。
(4)长期服用某些药物。
(二)脂溶性维生素脂溶性维生素的特点:都是亲脂性的非极性分子或者衍生物,可伴随脂类吸收(可大量在体内储存)若吸收障碍就易产生缺乏病。
此类维生素各自发挥不同的生理功用。
l. 维生素A(1)化学本质与性质:维生素A是β—白芷酮环的不饱和一元醇。
化学性质活泼,对氧、酸及紫外线敏感。
在避氧情况下可耐高温。
(2)维生素A原及转变:自然界一些红黄色植物(如胡萝卜素、红辣椒、黄玉米、茄等)含有类胡萝卜素。
(3)生化作用及缺乏症:①11—顺视黄醛构成视角细胞内感受弱光或暗光的物质——视紫红质。
②参与糖蛋白的合成,维持上皮细胞的完整与健全。
③β胡萝卜素是抗氧化剂,在氧分压低时直接消灭自由基。
④维生素A具有类固醇样作用,促进生长发育。
⑤维生素A缺乏时可导致夜盲症,干眼病.角膜软化症等。
2.维生素D(1)化学本质与性质:维生素D属于类固醇的衍生物,主要有VD2(麦角钙化醇,)和VD3(胆钙化醇,)两种。


第三章酶与辅酶一、知识要点在生物体的活细胞中每分每秒都进行着成千上万的大量生物化学反应,而这些反应却能有条不紊地进行且速度非常快,使细胞能同时进行各种降解代谢及合成代谢,以满足生命活动的需要。
生物细胞之所以能在常温常压下以极高的速度和很大的专一性进行化学反应,这是由于生物细胞中存在着生物催化剂——酶。
酶是生物体活细胞产生的具有特殊催化能力的蛋白质。
酶作为一种生物催化剂不同于一般的催化剂,它具有条件温和、催化效率高、高度专一性和酶活可调控性等催化特点。
酶可分为氧化还原酶类、转移酶类、水解酶类、裂解酶类、异构酶类和合成酶类六大类。
酶的专一性可分为相对专一性、绝对专一性和立体异构专一性,其中相对专一性又分为基团专一性和键专一性,立体异构专一性又分为旋光异构专一性、几何异构专一性和潜手性专一性。
影响酶促反应速度的因素有底物浓度(S)、酶液浓度(E)、反应温度(T)、反应pH值、激活剂(A)和抑制剂(I)等。
其中底物浓度与酶反应速度之间有一个重要的关系为米氏方程,米氏常数(K m)是酶的特征性常数,它的物理意义是当酶反应速度达到最大反应速度一半时的底物浓度。
竞争性抑制作用、非竞争性抑制作用和反竞争性抑制作用分别对Km 值与V max的影响是各不相同的。
酶的活性中心有两个功能部位,即结合部位和催化部位。
酶的催化机理包括过渡态学说、邻近和定向效应、锁钥学说、诱导楔合学说、酸碱催化和共价催化等,每个学说都有其各自的理论依据,其中过渡态学说或中间产物学说为大家所公认,诱导楔合学说也为对酶的研究做了大量贡献。
胰凝乳蛋白酶是胰脏中合成的一种蛋白水解酶,其活性中心由Asp102、His57及Ser195构成一个电荷转接系统,即电荷中继网。
其催化机理包括两个阶段,第一阶段为水解反应的酰化阶段,第二阶段为水解反应的脱酰阶段。
同工酶和变构酶是两种重要的酶。
同工酶是指有机体内能催化相同的化学反应,但其酶蛋白本身的理化性质及生物学功能不完全相同的一组酶;变构酶是利用构象的改变来调节其催化活性的酶,是一个关键酶,催化限速步骤。





第十一章维生素与辅酶提要维生素是维持生物体正常生长发育和代谢所必需的异类微量有机物质,不能由机体合成,或合成量不足,必须靠食物供给。
由于维生素缺乏而引起的疾病称为维生素缺乏症。
维生素都是小分子有机化合物,在结构上无共同性。
通常根据其溶解性质分为脂溶性维生素和水溶性维生素两大类。
脂溶性维生素由维生素A、D、E、K等,水溶性维生素有维生素B1、B2、B6、B12、烟酸、烟酰胺、泛酸、生物素、叶酸、硫辛酸和维生素C等。
现已知绝大多数维生素作为酶的辅酶或辅基的组成成分,在物质代谢中起重要作用。
维生素A的活性形式是11-顺视磺醛,参与视紫红质的合成,与暗视觉有关。
此外维生素A还参与糖蛋白的合成,在刺激组织生长分化中也起重要作用。
维生素D为类淄醇衍生物,1,25-二羟维生素D3是其活性形式,用以调节钙磷代谢,促进新骨的生成与钙化。
维生素E是体内最重要的抗氧化剂,可保护生物膜的结构和功能,维生素E还可促进血红素的合成。
维生素K与肝脏合成凝血因子Ⅱ、Ⅶ、Ⅸ和Ⅹ有关,作为谷氨酰羧化酶的辅助因子参与凝血因子前体转变活性凝血因子所必须的。
除维生素C外,水溶性维生素主要为B族维生素,以辅酶和辅基的形式存在,参与物质代谢。
硫胺素的辅酶形式为硫胺素焦磷酸(TPP),是α-酮酸脱羧酶、转酮酶及磷酸酮酶的辅酶,在α-裂解反应、α-缩合反应及α-酮转移反应中起重要作用。
核黄素和烟酰胺是氧化还原酶类的重要辅酶,核黄素以FMN和FAD是形式作为黄素蛋白酶的辅基;而烟酰胺以NAD+和NADP+形式作为许多脱氢酶的辅酶,至少催化6种不同类型的反应。
泛酸是构成CoA和ACP的成分,CoA起传递酰基的作用,是各种酰化反应的辅酶,而ACP与脂肪酸的合成关系密切。
磷酸吡哆醛是氨基酸代谢种多种酶的辅酶,参加催化涉及氨基酸的转氨作用,α-和β-脱羧作用,β-和γ-消除作用,消旋作用和醛醇裂解反应。
生物素是几种羧化酶的辅酶,包括乙酰CoA羧化酶和丙酮酸羧化酶,参与CO2的固定作用。
第五章维生素与辅酶3学时定义:维持生物正常生命过程必需的一类小分子有机化合物,它在生物体内含量极少,大多数由食物供给,人体自身不能合成它们。
脂溶性:A、D、E、K,单独具有生理功能。
水溶性:B1、B2、B6、B12、C等,辅酶。
第一节脂溶性维生素一、维生素A和胡萝卜素P3601、结构化学名称:视黄醇,包括两种:A1、A22、维生素A的来源β-胡萝卜素、α-胡萝卜素、γ-胡萝卜素、黄玉米色素在肝脏、肠粘膜内转化成A。
β-胡萝卜素转化成二个维生素A(一切有色蔬菜)α-胡萝卜素γ-胡萝卜素转化成一个维生素A黄玉米色素3、功能与视觉有关。
缺乏症:夜盲症。
活性形式:11-顺式视黄醛P361 视循环视紫红质为弱光感受物,当弱光射到视网膜上时,视紫红质分解,并刺激视神经而发生光觉。
11-顺式视黄醛,在暗光下经视网膜圆柱细胞作用后,与视蛋白结合成视紫红质,形成一个视循环。
当全反视黄醛变成11-顺式视黄醛时,部分全反视黄醛被分解为无用物质,故必需随时补充维生素A,每日补充量1 mg。
二、维生素D(D1、D3,还有D4、D5)P361有两种:D3(又名胆钙化醇),D2(又名麦角钙化固醇)。
植物体内不含维生素D(但有维生素D原)1、来源鱼肝油、蛋黄、牛奶、肝、肾、皮肤组织等富含维生素D。
酵母、真菌、植物中:麦角固醇(D2原)动物体内:7一脱氢胆固醇(D3原)2、结构P362反应式:麦角固醇→维生素D2 (麦角钙化固醇)7-脱氢胆固醇(皮肤)→维生素D3 (胆钙化固醇)3、功能调节钙磷代谢,维持血中钙磷正常水平,促进骨骼正常生长。
缺乏症:佝偻症等。
活性形式:1,25一二羟基胆钙固醇。
维生素D3 (胆钙化固醇)→25-羟基胆钙固醇(肝脏)→1,25一二羟基胆钙固醇(肾脏)→小肠(促进Ca2+ 的吸收、运输)及骨骼(促进Ca2+的沉积)中,参与调节钙磷代谢。
三、维生素E P363化学名称:生育酚,共有8种,直接具有活性。
1、结构P363 结构式:α-生育酚2、来源动、植物油、麦胚油、玉米油、花生油、棉子油、蛋黄、牛奶、水果等。
3、功能(抗氧剂—油脂氧化)生理功能:抗生殖不育、肌肉委缩、贫血、血细胞形态异常机理:有抗氧化活性,能防止不饱和脂肪酸自动氧化,保护细胞膜,延长细胞寿命,还可保护巯基酶的活性。
四、维生素K(K1、K2、K3)P3641、结构2、来源食物和肠道微生物合成;绿色蔬菜、动物肝脏、牛奶、大豆,大肠杆菌、乳酸菌3、功能促进凝血。
缺乏症:肌肉出血、凝血时间延长。
凝血过程中,许多凝血因子的生成与维生K有关。
①凝血酶原,即因子II②转变加速因子前体,因子VII③血浆凝血酶激酶因子IX④司徒氏因子因子X第二节水溶性维生素与辅酶主要是B族维生素,绝大多数都是辅酶。
一、维生B1与焦磷酸硫胺素(TPP)P367化学名称:硫胺素,活性形式:焦磷酸硫胺素(TPP)1、结构P367 结构式:硫胺素活性形式:TPP硫胺素+ ATP Mg2+ TPP + AMP硫胺素激酶2、来源:瘦肉、酵母、谷类的胚芽、皮层。
3、功能(TPP)脱羧辅酶。
缺乏症:脚气病、多发性神经炎。
TPP是催化丙酮酸、α-酮戊二酸脱羧反应的辅酶。
噻唑环C-2上氢解离,使C-2变成负碳离子,可以和α-酮酸的羧基碳结合,形成中间复合物脱CHOH。
二、维生素B2与黄素辅酶(FAD、FMN)P368化学名称:核黄素1、结构P368 结构式:VB2、FMN、FAD活性形式:FMN(还原型FMNH2),FAD (还原型FADH2)核黄素+ATP→FMN+ADP,FMN+ATP→FAD+ppi2、来源肝脏、酵母、大豆和米糠等3、功能FMN、FAD作为氧化还原型黄素辅酶,可分别与酶蛋白结合(称黄素蛋白),构成脱氢酶,辅酶传递2H酶底物产物辅酶D-a.a氧化酶D-a.a α-酮酸FAD羟基乙酸氧化酶羟基乙酸乙醛酸FMN琥珀酸脱氢酶琥珀酸反丁烯二酸FAD三、维生素B3—泛酸与辅酶A(CoA)P370维生素B3也称泛酸,是辅酶A的组成成分1、结构P370 结构式VB3(泛酸)、辅酶AVB3(泛酸):泛解酸、β-丙氨酸腺苷-3’-磷酸辅酶A(CoA-SH)磷酸泛酸巯基乙胺泛酰巯基乙胺活性位点:-SH2、功能:脂酰基载体,乙酰辅酶A是糖代谢、脂肪代谢氨基酸代谢的枢纽。
四、维生素B5与烟酰胺辅酶P369维生素B5包括烟酸(尼克酸)、烟酰胺(尼克酰胺)烟酰胺是合成NAD、NADP的前体P369 结构式:烟酸、烟酰胺、NAD、NADPNAD、NADP是各种脱氢酶的辅酶。
MH2+NAD+→M+NADH+H+酶底物产物辅酶醇脱氢酶乙醇乙醛NAD+异柠檬酸脱氢酶异柠檬酸α-酮戊二酸NAD+或NADP+五、维生素B6与磷酸吡哆醛辅酶维生素B6包括:吡哆醛、吡哆胺、吡哆醇P375 结构式活性形式:磷酸吡哆胺、磷酸吡哆醛功能:磷酸吡哆醛转氨酶、磷酸吡哆胺转氨酶P376 转氨反应过程转氨、脱羧、消旋六、维生素B7 生物素与羧化辅酶P373化学名称:生物素P373 生物素的结构生物素是多种羧化酶的辅酶酶蛋白的Lysε—NH2与生物素的羧基结合,生成Enz-biotin复合体丙酮酸的羧化:E-Biotin+HCO3- + ATP →E-Biotin-COO- + ADP + PiE-Biotin-COO- + 丙酮酸→草酰乙酸+ E-Biotin活性位点:N-1P374 N-1羧化生素素七、维生素B11 叶酸P371维生素B11又名叶酸,喋血谷氨酸P372 结构式:叶酸活性形式:四氢叶酸(THF),传递一碳单位的辅酶传递的一碳单位有:甲基、亚甲基(甲叉)、甲川基、甲酰基、亚胺甲基活性位点:N5、N10举例:P373 甲硫氨酸的合成八、维生素B12 钴胺素化学名称:钴胺素。
5’—脱氧腺嘌呤核苷酸钴胺素是甲基丙二酸单酰辅酶A变位酶的辅酶九、硫辛酸丙酮酸脱羧酶复合体中的辅酶(硫辛酰氨转乙酰酶和二氢硫辛酰氨脱氢酶的辅酶)十、维生素C1、结构化学名称:抗坏血酸2、来源:食物。
3、功能:抗氧化剂缺乏症:坏血病,毛细血管脆弱,牙龈发炎出血P378 表:组成辅酶的B族维生素第六章核酸核酸是遗传物质1868年瑞士Miesher.从脓细胞的细胞核中分离出可溶于碱而不溶于稀酸的酸性物质。
间接证据:同一种生物的不同种类的不同生长期的细胞,DNA含量基本恒定。
直接证据:T2噬菌体DNA感染E.coli用35S标记噬菌体蛋白质,感染E.coli,又用32P标记噬菌体核酸,感染E.coliDNA、RNA的分布(DNA在核内,RNA在核外)。
第一节核酸的化学组成核酸是一种线形多聚核苷酸,基本组成单位是核苷酸。
结构层次:核酸核苷酸磷酸核苷碱基组成核酸的戊糖有两种::D-核糖和D-2-脱氧核糖,据此,可以将核酸分为两种:核糖核酸(RNA)和脱氧核糖核酸(DNA)P330 表5-1 两类核酸的基本化学组成一、碱基1. 嘌呤碱:腺嘌呤鸟嘌呤2. 嘧啶碱:胞嘧啶尿嘧啶胸腺嘧啶P331 结构式3. 修饰碱基植物中有大量5-甲基胞嘧啶。
E.coli噬菌体中,5-羟甲基胞嘧啶代替C。
稀有碱基:100余种,多数是甲基化的产物。
DNA由A、G、C、T碱基构成。
RNA由A、G、C、U碱基构成。
二、核苷核苷由戊糖和碱基缩合而成,糖环上C1与嘧啶碱的N1或与嘌呤碱的N9连接。
核酸中的核苷均为β-型核苷P332 结构式腺嘌呤核苷胞嘧啶脱氧核苷DNA 的戊糖是:脱氧核糖RNA 的戊糖是:核糖三、核苷酸核苷中戊糖C3、C5羟基被磷酸酯化,生成核苷酸。
1、构成DNA、RNA的核苷酸P333表5-32、细胞内游离核苷酸及其衍生物①核苷5’-多磷酸化合物ATP、GTP、CTP、ppppA、ppppG在能量代谢和物质代谢及调控中起重要作用。
②环核苷酸cAMP(3’,5’-cAMP)cGMP(3’,5’-cGMP)它们作为质膜的激素的第二信使起作用,cAMP调节细胞的糖代谢、脂代谢。
③核苷5’多磷酸3’多磷酸化合物ppGpp pppGpp ppApp④核苷酸衍生物HSCoA、NAD+、NADP+、FAD等辅助因子。
GDP-半乳糖、GDP-葡萄糖等是糖蛋白生物合成的活性糖基供体。
第二节DNA的结构一级:脱氧核苷酸分子间连接方式及排列顺序。
二级:DNA的两条多聚核苷酸链间通过氢键形成的双螺旋结构。
三级:DNA双链进一步折叠卷曲形成的构象。
一、DNA的一级结构DNA的一级结构是4种脱氧核苷酸(dAMP、dGMP、dCMP、dTMP)通过3/、5/-磷酸二酯键连接起来的线形多聚体。
3/、5/-磷酸二酯键是DNA、RNA的主链结构。
P334 图5-1书写方法:5/ →3/:5’-pApCpTpG-3’,或5’…ACTG…3’(在DNA中,3/-OH一般是游离的)在DNA分子中,不变的骨架成分磷酸二酯键被逐渐省略,真正代表DNA生物学意义的是碱基的排列顺序。
遗传信息贮存在DNA的碱基排列顺序中,生物界生物的多样性即寓于DNA分子4种核苷酸千变万化的精确的排列顺序中。
二、DNA的二级结构1953年,Watson和Crick根据Chargaff 规律和DNA Na盐纤维的X光衍射数据提出了DNA的双螺旋结构模型。
1、Watson-Crick双螺旋结构建立的根据①Chargaff 规律1950年a. 所有DNA中,A=T,G=C 且A+G=C+T。
P334表5—4。
b. DNA的碱基组成具有种的特异性,即不同生物的DNA皆有自己独特的碱基组成。
c. DNA碱基组成没有组织和器官的特异性。
d. 年龄、营养状况、环境等因素不影响DNA的碱基组成。
②DNA的Na盐纤维和DNA晶体的X光衍射分析。
相对湿度92%,DNA钠盐结晶,B—DNA。
相对湿度75%,DNA钠盐结晶,A—DNA。
Z—DNA。
生物体内DNA均为B—DNA。
Franklin 的工作2、Watson-Crick双螺旋结构模型P335 图5—2a.两条反平行的多核苷酸链绕同一中心轴相缠绕,形成右手双股螺旋,一条5’→3’,另一条3’→5’b.嘌呤与嘧啶碱位于双螺旋的内侧,磷酸与脱氧核糖在外侧。
磷酸与脱氧核糖彼此通过3/、5/-磷酸二酯键相连接,构成DNA分子的骨架。
宽1.2 nm 宽0.6nm大沟小沟深0.85nm 深0.75nmc.螺旋平均直径2nm每圈螺旋含10个核苷酸碱基堆积距离:0.34nm螺距:3.4nmd.两条核苷酸链,依靠彼此碱基间形成的氢链结合在一起。
碱基平面垂直于螺旋轴。
A=T、G=CP336 图5—4碱基互补原则具有极重要的生物学意义,DNA的复制、转录、反转录等的分子基础都是碱基互补。
3、稳定双螺旋结构的因素①碱基堆积力(主要因素)形成疏水环境。
②碱基配对的氢键。
GC含量越多,越稳定。