第四章炔烃二烯烃
- 格式:ppt
- 大小:1.60 MB
- 文档页数:37
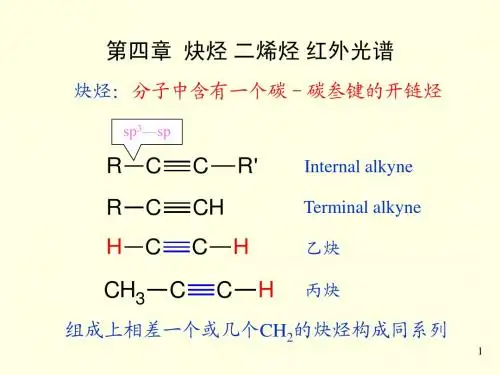

第四章炔烃二烯烃红外光谱(一)炔烃▪分子中具有一个碳碳叁键的开链不饱和烃——炔烃。
▪通式为CnH2n-2,碳碳叁键是炔烃的官能基。
4.1 炔烃的构造异构和命名1.炔烃的构造异构▪从丁炔开始,除碳链异构外,碳碳叁键位置的不同(位置异构)也可引起同分异构现象。
1-丁炔2-丁炔2. 炔烃的命名炔烃的系统命名法规则1)选含有碳碳叁键的最长碳链为主链。
2)从靠近叁键的一端开始编号,使叁键的位次尽可能小。
命名时要标出叁键的位置。
3) 其余取代基按烷烃的系统命名规则来命名。
4) 含有双键的炔烃命名时,一般先命名烯再命名炔,碳链编号以表示双键与叁键位置的两个数字之和取最小的原则。
1-戊炔2-戊炔3-甲基-1-丁炔4.2 炔烃的结构▪X光衍射和电子衍射等物理方法证明,乙炔分子是一个线性分子,所有碳原子和氢原子都分布在同一条直线上。
•sp杂化:由一个s轨道和一个p轨道参加的杂化,其结果形成了处于同一直线上的两个sp杂化轨道。
0.120 nm180 o C0.106 nmH乙炔分子中σ键的形成▪乙炔分子中,每个碳原子与另外两个原子形成了一个C sp-H s σ键和一个C sp-C sp σ键,在同一直线上,方向相反,故乙炔分子为线性分子。
乙炔分子中的π键▪每个碳原子上还各有两个未参加杂化的p轨道,互相平行,故这两个p轨道可侧面相互交盖而形成了两个π键,这两个π键并不是孤立分离的,其电子云对称分布在碳碳σ键键轴周围,类似圆筒性状。
参见图4-3。
▪碳碳叁键由一个σ键和两个π键组成。
乙炔键长缩短的原因1)s轨道的电子较p电子接近原子核,故杂化轨道的s成分越多,则在杂化轨道上的电子越接近原子核。
乙炔分子中的C sp-H s σ键,因sp杂化轨道的s成分大(50%),其电子云更靠近原子核。
2)乙炔分子中有两个形成π键,且sp杂化轨道参与了碳碳σ键的组成。
4.3 炔烃的物理性质∙炔烃的物理性质和烷烃、烯烃基本相似。
∙低级的炔烃常温常压下为气体,但沸点比相同碳原子数的烯烃略高。

第四章炔烃和二烯烃(I )炔烃一、定义、通式和同分异构体定义:分子中含有碳碳叁键的不饱和烃。
通式:C n H 2n-2同分异构体:与烯烃相同。
二、结构在乙炔分子中,两个碳原子采用SP 杂化方式,即一个 2S 轨道与一个2P 轨道杂化, 组成两个等同的 SP 杂化轨道,SP 杂化轨道的形状与 SP 2、SP 3杂化轨道相似,两个SP 杂化 轨道的对称轴在一条直线上。
两个以SP 杂化的碳原子,各以一个杂化轨道相互结合形成碳碳6键,另一个杂化轨道各与一个氢原子结合,形成碳氢 6键,三个6键的键轴在一条直线上,即乙炔分子为直线型分子。
每个碳原子还有两个末参加杂化的P 轨道,它们的轴互相垂直。
当两个碳原子的两P轨道分别平行时,两两侧面重叠,形成两个相互垂直的 n 键。
三、命名炔烃的命名原则与烯烃相同,即选择包含叁键的最长碳链作主链,碳原子的编号从 距叁键最近的一端开始。
若分子中即含有双键又含有叁键时,则应选择含有双键和叁键的最长碳链为主链, 并将其命名为烯炔(烯在前、炔在后)。
编号时,应使烯、炔所在位次的和为最小。
例如:CfCfCHCHDHC 三 CH3-甲基-4-庚烯-1-炔CH 3但是,当双键和叁键处在相同的位次时,即烯、炔两碳原子编号之和相等时,则从 靠近双键一端开始编号。
如:Cf 二C 比三CH1-丁烯-3-炔四、 物理性质与烯烃相似,乙炔、丙炔和丁炔为气体,戊炔以上的低级炔烃为液体,高级炔烃为 固体。
简单炔烃的沸点、熔点和相对密度比相应的烯烃要高。
炔烃难溶于水而易溶于有机溶剂。
五、 化学性质 (一)加成反应1、催化加氢炔烃的催化加氢分两步进行,第一步加一个氢分子,生成烯烃;第二步再与一个氢分加成,生成烷烃。
催化剂HC 三 CH + H 2 —CH2、加卤素炔烃与卤素的加成也是分两步进行的。
先加一分子氯或溴,生成二卤代烯,在过量 的氯或溴的存在下,再进一步与一分子卤素加成,生成四卤代烷。
HC 三CH + Br2 -------- Br=CHBrCHB 广2CHB 2虽然炔烃比烯烃更不饱和,但炔烃进行亲电加成却比烯烃难。



第四章炔烃二烯烃学习要点:本章学习在了解炔烃和二烯烃结构的基础上,重点掌握这两类化合物的化学性质以及由共轭二烯烃的结构特征所引起的共轭效应及其对化学性质的影响。
第一节炔烃不饱和烃除了烯烃外还有炔烃。
例如气割气焊用的乙炔(HC≡CH),就是一个炔烃,凡含有碳碳叁键的不饱和烃均称为炔烃,碳碳叁键(-C≡C-)是它的官能团,它的通式为C n H2n-2,与碳原子数相同的二烯烃,环烯烃为同分异构体。
一、炔烃的结构以炔烃中结构最简单的乙炔为例,在乙炔中两个叁键碳原子都是只和两个原子相结合,因此它只需要用两个价电子来构成两个σ键,亦即炔碳原子中的s电子轨道只要和一个p电子轨道进行sp杂化就可以了,形成了两个相等的sp杂化轨道,如图4-1所示。
图4-1 碳原子轨道的sp杂化每个sp杂化轨道包含1/2s轨道成分和1/2p轨道成分,其形状与sp3,sp2杂化轨道相似,只是更“胖”些,两个sp杂化轨道对称地分布在碳的两侧,成为一条直线,两者之间的夹角为180º。
如图4-2所示。
所以在乙炔中每一个碳都以一个sp杂化电子轨道与氢的1s电子轨道相互重迭成为一个C-H键,两个碳又各以一个sp杂化轨道相重迭,形成C-C键,这些都是σ键。
图4-2 碳原子的sp杂化电子轨道两个C原子尚各余两个p电子轨道,它们的对称轴都与sp杂化轨道的对称轴互相垂直,这两个p轨道可以在各自侧面重迭形成两个π键,所以炔键叁键中一个是σ键,两个是π键。
实际上叁键中四个π电子的电子云是混合在一起,它们围绕着连接两个碳核的直线成圆筒形分布。
如图4-3所示。
图4-3 乙炔分子的圆筒形π电子云其他炔烃的碳碳叁键与乙炔相同,也是由一个σ键和两个π键组成。
二、炔烃的同分异构和命名炔烃中除了乙炔和丙炔没有异构体外,从丁炔开始有构造异构现象,但由于叁键碳上只有一个取代基,因此炔烃的构造异构体比烯烃少,也无顺反异构体。
例如丁烯有三个构造异构体,但丁炔只有两个构造异构体,如下:CH3CH2C CH CH3C CCH31-丁炔2-丁炔简单的炔烃可采用衍生物命名法,即以乙炔作母体,将其它基团看成取代基,而复杂的炔烃必须采用系统命名法,炔烃的命名与烯烃相似,只须将“烯”改为“炔”即可。



