元素结合规律与赋存状态4
- 格式:ppt
- 大小:13.17 MB
- 文档页数:71



煤中微量元素的赋存状态煤中微量元素是一类具有重要环境和生物学意义的组分。
在这些微量元素的赋存状态上,存在着关键的化学、物理和生物学影响,这种影响可能会影响煤的质量、热值、可燃性和毒性。
为了提高煤资源的经济价值,必须准确地测定煤中微量元素的赋存状态,以便合理地利用煤资源,保护环境并实现煤的可持续利用。
煤是一种自然的有机质材料,它的组成有很多种元素,其中微量元素包括碳(C),氢(H),氧(O),硫(S),氮(N),氟(F),磷(P),硒(Se),锰(Mn),铁(Fe),锌(Zn)和铜(Cu)等。
这些微量元素在煤体中的赋存状态有三种:元素,元素的混合物或元素的有机化合物,形成了多层次、复杂的赋存状态。
元素赋存状态是指元素自身在煤体中的存在形式,它主要有晶体和液体两种形式,这两种形式的元素具有不同的耐受性和迁移性,会影响煤的性质。
晶体元素,如铁、锰和锌,除了处于原子状态外,很容易形成氧化物,水解物或沉淀物,对其他元素有较大的分解、改变和稳定作用;液体元素,如氢、氧和氮,它们在煤体中一般少有极大的变化,但它们在煤体中具有迁移性,会影响煤体中其他元素的形成和运动。
元素混合物赋存状态是指元素形成包裹体,其中宿主支撑了元素的主要活性,从而形成特定的化学和物理组合。
这种混合物的存在,可以赋予煤体一定的比表面积和活性,体现出煤的性质,如热值、着火温度、煤气峰值等。
例如,燃烧过程中释放氮气,归因于煤体中FeN和SiN混合物;另外,锰、铁、锌和硫的混合物也能够影响煤的热值。
元素有机化合物的赋存状态指的是元素被有机物所包裹,形成特定的有机化合物,这些有机物可能是有机磷酸盐、羧酸盐、酰胺类化合物、含氮有机物等。
它们的存在会影响煤的可燃性和毒性,在煤的燃烧过程中,这些有机化合物也会形成有害的物质,如硫氧化物、氮氧化物等,从而对环境造成污染。
综上所述,煤中微量元素的赋存状态对煤的质量、热值、可燃性和毒性具有重要影响。
因此,为了更加合理地利用煤资源,保护环境并实现煤的可持续性利用,必须准确地测定煤中微量元素的赋存状态,以期提高煤资源的经济价值。



绪论:1. 地球化学:地球化学是研究地球及其子系统(含部分宇宙)的化学组成、化学作用和化学演化的科学.2. 地球化学研究的基本问题:①元素(同位素)在地球及各子系统中的组成②元素的共生组合和存在形式③研究元素的迁移④研究元素(同位素)的行为⑤元素的地球化学演化3. 地球化学的研究思路:"见微而知著"。
通过观察原子、研究元素(同位素),以求认识地球和地质作用地球化学现象。
4. 简述地球化学的研究方法:A. 野外工作方法:①宏观地质调研②运用地球化学思维观察、认识地质现象③在地质地球化学观察的基础上,根据目标任务采集各种地球化学样品B.室内研究方法:④量的测定,应用精密灵敏的分析测试方法,以取得元素在各种地质体中的含量值⑤质的研究,也就是元素结合形态和赋存状态的研究⑥动的研究,地球化学作用过程物理化学条件的测定和计算。
包括测定和计算两大类。
⑦模拟地球化学过程,进行模拟实验。
⑧测试数据的多元统计处理和计算。
第一章:基本概念1. 地球化学体系:我们把所要研究的对象看作是一个地球化学体系,每个地球化学体系都有一定的时间连续,具有一定的空间,都处于特定的物理化学状态(T、P 等)2. 丰度:一般指的是元素在这个体系中的相对含量(平均含量)。
3. 分布:元素的分布指的是元素在一个化学体系中(太阳、陨石、地球、地壳、某地区)整体的总的含量特征。
4. 分配:元素的分配指的是元素在各地球化学体系内各个区域、各个区段中的含量。
5. 研究元素丰度的意义:①元素丰度是每一个地球化学体系的基本数据以在同一体系中或不同体系中用元素的含量值来进行比较,通过纵向(时间)、横向(空间)上的比较,了解元素基本特征和动态情况,从而建立起元素集中、分散、迁移等系列的地球化学概念。
是研究地球、研究矿产的重要手段之一。
②研究元素丰度是研究地球化学基础理论问题的重要素材之一。
宇宙天体是怎样起源的?地球又是如何形成的?地壳中主要元素为什么与地幔中的主要元素不一样?生命是怎么产生和演化的?这些研究都离不开地球化学体系中元素丰度分布特征和分布规律。
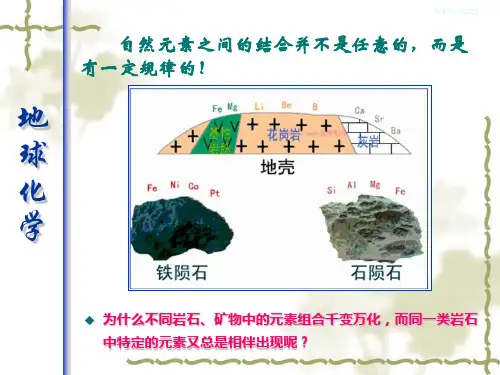


元素赋存状态
元素赋存状态是指元素在其地球化学迁移历史的某个阶段所处的物理化学状态及与共生元素的结合特征。
包括该元素所处的物态、形成化合物的种类和形式、价态、键态、配位位置等多方面的物理化学特征。
元素赋存状态是化学反应的结果,与作用条件有关。
已观测到的元素在自然固结相中的赋存状态,大多能反映其形成的物理化学条件。
因此,元素赋存状态有地质成因意义。
元素的主要赋存状态有:①元素的集中状态。
元素形成独立矿物的能力与其丰度有关。
常量元素在地壳中主要以独立矿物形式存在。
②类质同象状态。
元素以离子或原子置换形式进入其他元素的晶格,构成固溶体。
是元素的分散状态。
③超显微包体。
元素呈极细小颗粒(粒径小于0.001毫米)的独立化合物或其原子和分子存在。
又称超显微非结构混入物。
主要特征是不进入主要矿物晶格,但又不形成可以进行矿物学研究的颗粒化合物。
④吸附状态。
元素以离子或化合物分子形式被胶体颗粒表面、矿物晶面、解理面所吸附,是一种非独立化合物形式。
⑤与有机质结合的形式。
主要有金属有机化合物、金属有机络合物或螯合物、以及有机胶体吸附态离子等。
以上为元素在凝固相中的赋存状态。
当元素处于流体相迁移时,其活动形式有气体状态、溶解状态、熔融状态、各种胶体态、悬浮态等。


元素的赋存形态元素是构成物质的基本单位,它们以不同的形态存在于自然界中。
元素的赋存形态指的是元素在自然界中所呈现的不同物质形态和状态。
这些赋存形态的差异,对我们了解元素的性质和应用具有重要意义。
首先,元素可以以自由形态存在。
自由元素是指元素以单质形式存在,不与其他元素形成化合物。
例如,氧气和氮气就是自由元素的典型代表。
氧气以O2的形式存在于空气中,是我们呼吸的必需气体。
氮气以N2的形式存在于空气中,是植物和动物体内重要的成分。
其次,元素可以以化合物的形态存在。
化合物是由两种或多种不同元素通过化学反应结合而成的物质。
在自然界中,元素与其他元素形成化合物的形态非常普遍。
例如,氧气与氢气反应生成水,这是氧的一种赋存形态。
氧化铁是由铁与氧气反应形成的化合物,是自然界中常见的铁矿石。
化合物的形态不仅帮助我们了解元素之间的相互作用,还为我们提供了利用元素的途径。
另外,元素还可以以离子的形态存在。
离子是带电的原子或原子团,它们形成的化合物被称为离子化合物。
离子化合物包括金属离子化合物和非金属离子化合物。
金属离子化合物是由金属元素和非金属元素通过电子转移形成的化合物,例如氯化钠。
非金属离子化合物是由两种或多种非金属元素通过共价键结合形成的化合物,例如二氧化碳。
离子的形态在化学反应中起着重要的作用,也是化学反应能够进行的基础。
此外,元素还可以以同素异形体的形态存在。
同素异形体是指同一种元素在结构上存在不同的形式。
这种形态的存在使得元素在化学反应中具有不同的性质。
例如,碳可以以钻石和石墨的形式存在,它们的结构和性质都不相同。
同素异形体的存在丰富了元素的化学性质,也为我们的生活和工业应用提供了更多的选择。
总结起来,元素的赋存形态包括自由形态、化合物形态、离子形态和同素异形体。
这些形态的存在使得元素在自然界中展现出丰富多样的性质和应用价值。
通过深入了解和研究元素的赋存形态,我们能够更好地利用元素的特性,推动科学技术的发展,并为人类的生活带来更多的福祉。
二、查瓦里茨基分类1)、以展开式周期表为基础2)、分类依据和参数:01.外层电子数02.电子层数03.原子半径和离子半径3)、查瓦里茨基分类01.氢族02.惰性气体族03.造岩元素族(岩石主要元素族)04.矿化剂或挥发元素族(岩浆射气元素族)05.铁族元素06.稀有稀土元素族07.放射性元素族08.钨钼族09.硫化矿床成矿元素族10.铂族元素11.半金属和重矿化剂12.重卤素族4、优点:较好地反映了元素在成矿和成岩作用中的意义。
5、不足:01.稀有元素作为一个分类范围不够准确,目前对稀有元素的理解和划分很不一致02.造岩元素的性质和行为比较笼统03.重卤素族和钨、钼族作为单独一族又嫌太窄04.Cu 、Ag、Au 在自然界中既可呈自然金属产出、又可以与Se、Te形成化合物,兼具铂族元素和硫化物成矿元素两族性质,但查氏却把它们分开了。
4)费尔斯曼分类(普通场、硫化物场、酸性场)5)北大分类(强调元素的化学特性)6)涂先生关于矿产元素分类(元素的活动性)7)微量元素地球化学分类地球化学中常用的元素分类名称01.主量元素和微量元素02.造岩元素03.稀土元素04.高温成矿元素05.第一过渡族06.金属成矿元素07.阴离子族08.放射性元素09.地球挥发份键参数及其地球化学意义1、键是在晶体中各种原子及离子间相互作用的结合力,而所谓键参数也就是用以表示这种结合力的一些参数,在地球化学中常碰到的键参数有以下几类:01.半径02.化学键03.电离和电价04.电离能与电子亲合能05.电负性06.离子电位半径(原子或离子的半径)1、半径的概念、分类2、半径的计算方法3、影响半径的因素4、周期表中半径的变化规律01.镧系和锕系收缩原子或离子的半径:原子或离子在晶格中形成一个有一定范围的电磁场,即电子云的分布范围,其半径即称为原子或离子的半径分类:01.绝对半径02.有效半径有效半径又包括(原子半径、共价半径、离子半径)绝对半径:单纯根据原子的内部结构,不考虑外界环境影响而计算出的半径有效半径:为原子或离子在晶格中的半径,即受到周围原子或离子的相互影响而表现出来的真正范围。
第2章 元素的结合规律与赋存形式一、元素的赋存状态① 形成独立矿物;指形成能够用肉眼或仪器进行矿物学研究的颗粒(粒径一般大于0.001毫米)。
元素形成独立矿物的能力与其丰度有关。
常量元素在地壳中主要以独立矿物形式存在,而微量元素如稀有元素只有总量的极少部分形成独立矿物,而绝大部分处于各种形式的分散状态。
元素形成矿物的数目(N)与其原子克拉克值(K)呈正相关关系。
② 呈类质同像状态,由于元素与矿物中主要元素地球化学性质相近,加入矿物晶格。
类质同象是矿物结晶时,其晶体结构中一种位置被两种或两种以上的不同元素(或基团)占据而形成混晶的现象。
③ 以超显微的微粒包体,又称超显微非结构混入物。
元素呈极细小颗粒(粒径<0.001毫米)的独立化合物或其原子和分子存在。
主要特征是不进入主要矿物晶格,但又不形成可以进行研究的颗粒的化合物。
具有独立的化学性质,一般可应用化学处理的方法使之分离和进行研究。
元素的超显微包体形式可有不同的地质成因,如在岩浆岩特别是喷发岩中呈微细分散的成矿元素的硫化物或氧化物,如铀、钍的氧化物,以及呈原子分散状态存在的金、银等。
其他如中的共沉淀物质、土壤中的微细次生矿物、中的交代残余包体等都属此类④ 呈离子附吸状态,元素以离子或离子团被胶体颗粒表面吸附,为一种非独立化合物形式。
元素以离子态或单独分子存在,又不参加寄主矿物的晶格构造,因此是一种结合力较弱的、易于交换和分离的赋存状态,亦称活性状态。
粘土矿物、土壤和其他胶体物质对元素的吸附作用最常见,对元素的迁移和富集有重要影响。
⑤ 与有机质结合,形成金属有机化合物,络合物或螯合物以及有机胶体吸附态离子等。
生物和各种有机质除集中了亲生物元素,如碳、氢、氧、氮、硫、磷、钙等外,还吸收大量金属和非金属元素,构成其次要的或微量的元素组分。
这些元素在有机质体系中的存在,无论对有机质的性质和它们的生物功能,以及对元素本身的迁移活动和富集分散都有极重要的影响。