聚酮合酶
- 格式:doc
- 大小:26.50 KB
- 文档页数:2

聚酮化合物及其组合生物合成一、本文概述聚酮化合物是一类由聚酮合酶催化合成的重要天然产物,广泛存在于生物界中,并表现出多种生物活性,如抗菌、抗病毒、抗肿瘤等。
聚酮化合物的生物合成过程是一种复杂而精细的化学反应,涉及多个酶和辅因子的协同作用。
本文旨在深入探讨聚酮化合物及其组合生物合成的机制、方法与应用,以期为进一步理解和利用这类天然产物提供理论支持和实践指导。
文章首先将对聚酮化合物的结构特点、分类及生物活性进行概述,为后续研究奠定基础。
接着,将详细介绍聚酮合酶的结构与功能,以及其在聚酮化合物生物合成中的关键作用。
在此基础上,文章将重点探讨聚酮化合物组合生物合成的策略与方法,包括基因工程、代谢工程等手段在聚酮化合物合成中的应用。
文章还将对聚酮化合物及其组合生物合成的未来发展趋势进行展望,以期为推动该领域的研究与发展提供有益参考。
二、聚酮化合物的结构与性质聚酮化合物是一类具有广泛生物活性的天然产物,其结构多样性和生物活性使得它们在医药、农业、材料科学等领域具有广泛的应用前景。
聚酮化合物的结构特点主要由一系列线性或环状的酮基团组成,这些酮基团通过碳碳键连接,形成复杂的碳骨架。
在结构上,聚酮化合物可以根据其碳骨架的类型分为线性聚酮、环状聚酮以及大环内酯等。
线性聚酮通常具有长链结构,其碳骨架呈现出一定的柔性;环状聚酮则具有闭合的环状结构,具有较高的稳定性;大环内酯则是一类特殊的环状聚酮,其中包含一个或多个内酯键,使得分子呈现出独特的空间构象。
在性质上,聚酮化合物通常具有较好的热稳定性和化学稳定性,这使得它们在各种条件下都能保持稳定的生物活性。
聚酮化合物的生物活性往往与其结构中的特定官能团密切相关,如酮基、羟基、羧基等。
这些官能团的存在使得聚酮化合物能够与生物体内的靶标分子发生特异性相互作用,从而表现出抗菌、抗病毒、抗肿瘤等多种生物活性。
为了深入研究聚酮化合物的结构与性质之间的关系,科学家们采用了多种现代分析方法,如核磁共振、质谱、射线晶体衍射等。


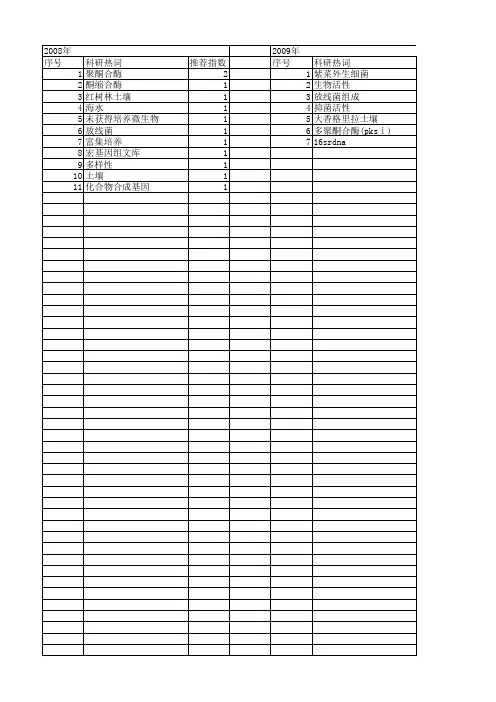
聚酮类化合物聚酮类化合物与聚酮合酶生物基地81 1038126 徐冉芳1.属于聚酮类化合物的药物抗细菌:红霉素、利福霉素、四环素抗真菌:两性霉素、灰黄霉素兽药:泰乐菌素抗寄生虫药剂:除虫菌素、南吕霉素、奈马克丁免疫抑制剂:雷帕霉素、FK506抗癌药:多柔比星、mithramycin降血脂药物:洛伐他丁、普伐他丁2.聚酮合酶的结构功能聚酮合酶(PKS)分为三种类型:Ⅰ型,又称为模件型;Ⅱ型,又称为迭代型;Ⅲ型,又称为査尔酮型。
Ⅰ型PKS是以模块形式存在的多功能酶,每一模块含有一套独特的、非重复使用的催化功能域。
其非重复使用的催化功能域与聚酮生物合成的反应顺序呈线性对应。
主要催化合成大环内酯类、聚烯及聚醚类化合物。
.Ⅱ型PKS是一个多功能酶复合体,只包含一套可重复使用的结构域,每一结构域在重复的反应步骤中都多次地用来催化相同的反应。
Ⅲ型PKS是一种类似苯基苯乙烯酮合成酶的PKS。
这种类型的PKS 和其它两种PKS迥然不同,它在不需要ACP的情况下直接催化泛酰辅酶A间的缩合,主要负责单环或双环芳香类聚酮化合物的生物合成。
3.聚酮合酶合成聚酮化合物的分子机制聚酮化合物是通过聚酮合酶催化形成的,其催化过程类似于脂肪酸合酶(FAS)催化的脂肪酸生物合成,即通过酰基-CoA活化的底物之间的重复脱羧缩合而合成,但两者在合成单位的选择(包括起始单位和延伸单位)、链装配过程中每个酮基还原程度的控制、以及芳香聚酮或复合聚酮链长的决定等方面也存在着明显的差异,主要体现在:(1)FAS一般以乙酸作为起始单位,而PKS往往使用不同的起始单位,最为常用的有乙酸、丙酸,此外还有丁酸,杀假丝菌素使用的对氨基苯甲酸等;(2)FAS一般只用乙酸为链延伸单位,而PKS除了利用乙酸作为链伸长单位外,还可利用丙酸或丁酸,在终产物中相应生成甲基或乙基侧链;(3)PKS可以通过酮基选择性地还原和脱水,从而在终产物的相应位置形成酮基、羟基、双键或亚甲基等功能团,同时也决定了手性中心的立体化学构型。





聚酮化合物及其生物合成摘要:聚酮化合物的生物合成是当前国际化学与生物学交叉学科研究的热点之一,也正在发展成为药物创新超常规的重要手段。
合成聚酮类化合物的方法有很多,但应用最多的是组合生物合成方法,因而本文主要是对这种方法的介绍,特别是I型聚酮化合物的组合生物合成的常用技术和方法学发展进行了详细解说。
关键词:聚酮化合物;聚酮合酶;生物合成一、聚酮化合物及其聚酮合酶聚酮化合物是一大类由细菌、真菌和植物将低级羧酸通过连续的缩合反应产生的天然产物,它包括许许多多具有抑制细菌(如红霉素、四环素)、真菌(如灰黄霉素、两性霉素)、寄生虫(如avermectin、奈马克丁)、癌症(如多柔比星、enediynes)等活性的化合物,有些抗真菌聚酮化合物同时还具有免疫抑制剂的活性(如雷帕霉素、FK506),它被广泛地应用于医药、畜牧和农业。
如今,这一化合物越来越为人们所重视,这主要是由于该化合物具有:(1)无可比拟的生物学活性使之具有巨大的新药物开发潜力和商业价值,聚酮化合物所形成的药物已用于几乎所有重要的疾病治疗,每年的销售额超过了100亿美元;(2)独特的结构和合成机制为人们研究酶催化的分子机制、分子识别和蛋白质的相互作用提供了空前的契机;(3)聚酮合酶所具有的可塑性可以使人们方便地通过组合生物合成手段来获得新的化合物。
目前已发现了不少于10000种聚酮化合物,而由之衍生出的新产物更是难以记数。
聚酮化合物是功能和结构最多样化的天然产物之一,它们的合成包括酰基辅酶A活化羧酸的一系列重复的醇醛缩合而形成有一定长度的聚酮链骨架,然后经过环化或者芳香化、或者与脱氧糖等结构单位连接等过程。
尽管聚酮化合物的结构和特性千差万别,总的来说它可以分为两大类:芳香族聚酮化合物和复合聚酮化合物。
前者是乙酸通过缩合(起始单位除外)形成的大部分β-酮基在酰基链的延伸和完成后都一直保持非还原状态,经过折叠和醇醛缩合形成六元环,芳香环随后被脱水还原,如放线紫红素、柔红霉素、四环素。
聚酮类化合物与聚酮合酶生物基地81 1038126 徐冉芳1.属于聚酮类化合物的药物抗细菌:红霉素、利福霉素、四环素抗真菌:两性霉素、灰黄霉素兽药:泰乐菌素抗寄生虫药剂:除虫菌素、南吕霉素、奈马克丁免疫抑制剂:雷帕霉素、FK506抗癌药:多柔比星、mithramycin降血脂药物:洛伐他丁、普伐他丁2.聚酮合酶的结构功能聚酮合酶(PKS)分为三种类型:Ⅰ型,又称为模件型;Ⅱ型,又称为迭代型;Ⅲ型,又称为査尔酮型。
Ⅰ型PKS是以模块形式存在的多功能酶,每一模块含有一套独特的、非重复使用的催化功能域。
其非重复使用的催化功能域与聚酮生物合成的反应顺序呈线性对应。
主要催化合成大环内酯类、聚烯及聚醚类化合物。
.Ⅱ型PKS是一个多功能酶复合体,只包含一套可重复使用的结构域,每一结构域在重复的反应步骤中都多次地用来催化相同的反应。
Ⅲ型PKS是一种类似苯基苯乙烯酮合成酶的PKS。
这种类型的PKS和其它两种PKS迥然不同,它在不需要ACP的情况下直接催化泛酰辅酶A间的缩合,主要负责单环或双环芳香类聚酮化合物的生物合成。
3.聚酮合酶合成聚酮化合物的分子机制聚酮化合物是通过聚酮合酶催化形成的,其催化过程类似于脂肪酸合酶(FAS)催化的脂肪酸生物合成,即通过酰基-CoA活化的底物之间的重复脱羧缩合而合成,但两者在合成单位的选择(包括起始单位和延伸单位)、链装配过程中每个酮基还原程度的控制、以及芳香聚酮或复合聚酮链长的决定等方面也存在着明显的差异,主要体现在:(1)FAS一般以乙酸作为起始单位,而PKS往往使用不同的起始单位,最为常用的有乙酸、丙酸,此外还有丁酸,杀假丝菌素使用的对氨基苯甲酸等;(2)FAS一般只用乙酸为链延伸单位,而PKS除了利用乙酸作为链伸长单位外,还可利用丙酸或丁酸,在终产物中相应生成甲基或乙基侧链;(3)PKS可以通过酮基选择性地还原和脱水,从而在终产物的相应位置形成酮基、羟基、双键或亚甲基等功能团,同时也决定了手性中心的立体化学构型。
第50卷第2期2021年3月福建农林大学学报(自然科学版)Journal of Fujian Agriculture and Forestry University ( Natural Science Edition )青头菌(Russula virescens )聚酮合酶基因的克隆及碳源对该基因表达的影响原晓龙,王毅,杨文忠(云南省林业和草原科学院,云南省森林培育与开发利用重点实验室/国家林业和草原局云南珍稀濒特森林植物保护和繁育重点实验室,云南 昆明650201)摘要:为了解青头菌中具体的聚酮合酶基因,从青头菌(Russula virescens )基因组挖掘并克隆到一个聚酮合酶(polyketide synthase, PKS)基因(RvPKS),通过生物信息学分析预期其功能,并检测了不同浓度碳源添加物对该基因表达的影响.结果 表明:R q PKS 基因(GenBank 登录号:MT655136)的cDNA 长度为6039 bp,编码2 012个氨基酸,结构域组织顺序为SAT-KS- AT-ACP-TE ,各结构域的保守活性氨基酸序列为 SAT(GIIGFSSGII)、KS( DTACSSSL). AT( NWEAHGTGTQ) .ACP(WGH- SLGEYVA)和 TE( LGGWSLGGIIA);预测的 RvPKS 编码蛋白与火丝菌(Pyronema omphalodes )、鸡枞菌属(Termitomyces sp.)、 白环菇属(Leucoagaricus sp.)、乌氏曲霉(Aspergillus udagawae )、丝曲霉(Aspergillus lentulus )、Penicillium subrubescens 等相关聚 酮合酶蛋白聚为一支,该蛋白可能催化合成一种新型的分生抱子色素.此外,2%山梨醇和10%蔗糖能强烈诱导RvPKS 基因的表达.关键词:青头菌;聚酮合酶;聚类分析;基因表达中图分类号:Q939.95 文献标识码:A文章编号:1671-5470( 2021) 02-0250-07DOI :10.13323/ki.j.fafu( nat.sci.) .2021.02.015开放科学(资源服务)标识码(OSID )Cloning of a polyketide synthetase gene from Russula virescens andthe effects of carbon sources on its expressionYUAN Xiaolong, WANG Yi, YANG Wenzhong(Laboratory of Forest Plant Cultivation and Utilization/Key Laboratory of Rare and Endangered Forest Plants of StateForestry Administration , Yunnan Academy of Forestry and Grassland , Kunming , Yunnan , 650201, China)Abstract : In order to comprehend the specific polyketide synthetase gene of Russula virescens , a polyketide synthetase gene (RvPKS) was cloned from the genome of R.virescens by genome mining. The function of the gene was analyzed by bioinformatics. The expression of the RvPKS gene in R. virescens was investigated under different concentrations of carbon sources. The results showed that the cDNA of the RvPKS gene was 6 039 bp in full length, encoding 2 012 amino acids. Its conserved domain was SAT-KS-AT-ACP- TE in sequence , with its conserved active amino acid sites being SAT ( GIIGFSSGII ) , KS ( DTACSSSL) , AT ( NVVEAHGTGTQ ), ACP ( VVGHSLGEYVA) and TE ( LGGWSLGGIIA) , respectively. The proteins encoded by RvPKS were clustered with those from Pyronema omphalodes , Termitomyces sp , Leucoagaricus sp., Aspergillus udagawae , Aspergillus lentulus and Penicillium sub- rubescens , suggesting that RvPKS might catalyze a new type of conidial pigment. The expression of the RvPKS gene was intensively induced by 2% sorbitol and 10% sucrose.Key words : Russula virescens ; polyketide synthetase ; phylogenetic analysis ; gene expression食用菌因其上佳的口感、柔软的质地和丰富的营养而广泛地被人们所喜爱.青头菌[Russula virescens (Schff. ex Zart.) Fr.]是其中一种重要的野生食用菌.青头菌又名绿菇,是一种红菇科(Russulaceae )红菇属 (Russula )担子菌类真菌⑴,通常着生在阔叶或针叶树种(如云南松等)根部形成外生菌根⑵,其子实体较 大,味道浓郁鲜美、营养丰富⑶,长期以来被用作传统中药的民间药方⑷•目前关于青头菌的分子生物学研收稿日期:2020-05-13 修回日期:2020-06-29基金项目:国家自然科学基金项目(31860177);2019中央引导地方发展专项基金(云南松研究开发中心建设);云南省林业和草原科学院创 新基金项目(MS2019-09).作者简介:原晓龙(1986-),男,助理研究员.研究方向:分子生物学.Email :xiaolony@ .通信作者王毅(1981-),男,副研究员.研究方 向:分子生物学.Email :22825818@ .第2期原晓龙等:青头菌(Russula virescens)聚酮合酶基因的克隆及碳源对该基因表达的影响-251-究大多集中在系统进化、ITS鉴定[5]和DNA条形码等⑷方面.青头菌在成长过程中会产生戊基咲喃、辛酮和丁烯酮等聚酮类挥发性产物[3],目前尚未发现有关青头菌聚酮类化合物相关基因研究的报道.大环内酯类、蔥环类、四环素类和聚醚类天然聚酮化合物具抗感染、抗真菌、抗肿瘤和免疫抑制等活性,这些聚酮类化合物在临床上被广泛应用[7];聚酮类是由聚酮合酶(polyketide synthase,PKS)催化合成的,聚酮合酶通过催化前体物质进行反复的缩合反应,可以形成多种聚酮体,再经过甲基化、氧化还原、糖基化等修饰反应形成各种各样结构复杂的聚酮类化合物⑻.本研究通过对青头菌转录组数据的BLAST比对分析,获得了一条PKS基因,通过RT-PCR克隆获得该基因全长,并检测了其在含不同碳氮源添加物培养基上的具体表达情况,以期为青头菌品质研究、及具生物活性聚酮类生物合成提供基础材料.1材料与方法1.1青头菌菌株分离将采集于云南省宜良县的青头菌带回实验室后,采用组织分离法,在无菌环境下将新鲜子实体的菌柄、菌盖等不同部位的组织分离出来,切成小块,置于PDA斜面培养基上,25弋恒温环境培养.长满管后,转接2次平板,纯化菌丝.纯化后的菌丝经形态鉴定,及ITS(GenBank登录号MW307354),p-tubulin(Gen-Bank登录号MW307355)和elongation factor1a(GenBank登录号:MW307356)鉴定后,该菌种为青头菌(R. virescens),并将该菌株命名为Rv-yaf-001.1.2试剂与仪器真菌RNA提取试剂盒(康为世纪公司),高保真DNA聚合酶(TaKaRa公司),NanoDrop TM2000紫外分光光度计(赛默飞世尔科技公司),真菌总RNA提取试剂盒(TaKaRa公司),反转录试剂盒(赛默飞世尔科技公司),DNA纯化试剂盒(Qiagen公司),无缝克隆试剂盒(Biomiga公司).1.3RvPKS基因的挖掘和分离首先以曲霉中已报道过的PKS基因为模板,利用本地BLAST对青头菌基因组进行扫描,获得可能含有PKS基因的contigs,然后利用antiSMASH(https://antismash.secondarymetabolites.o r g/)软件进行验证,并利用GENEFISH对contigs进行开放阅读框扫描,通过生物信息学分析获得青头菌基因组中RvPKS基因的 DNA序列以及蛋白序列.根据DNA序列设计含起始密码子的特异引物RvPKSF:5'-ATGGAACATCTGAATATCCC-3',及含终止密码子的特异引物RvPKSR:5'-ACGGCCTCTGCAATAATTGA-3',以青头菌cDNA为模板,用HiFi高保真DNA聚合酶用于RvPKS基因全长cDNA的克隆;经DNA纯化试剂盒将该片段纯化后,并将其连接到克隆载体Peasy-T3上,转化到Trans-T1感受态细胞中.37X培养24h,进行菌落PCR后选择含有插入片段的阳性克隆送到上海生工进行测序.1.4生物信息学分析应用ExPASy数据库(https:///)中的ProtParam、SignalP、TargetP、Prosite和TMHMM对RvPKS蛋白对其理化性质、信号肽、细胞定位、保守结构域和跨膜结构域进行分析.并从美国生物技术信息中心(NCBI)上选择功能已知且鉴定过化合物的蛋白序列用于聚类分析,采用MEGA7.0中的Clustal W程序对所选择的PKS蛋白序列和青头菌中的RvPKS蛋白序列进行比对后,采用邻位相接法(Neighbor-joining),自检举1000次,其余采用默认参数构建分子系统进化树.依据聚类结果,从基因起源与功能分化的角度预测该基因功能,并进一步推测该基因产生的聚酮化合物.1.5RvPKS基因在不同培养基上的表达根据RvPKS基因的DNA序列设计特异检测引物(TRvPKSF:5'-AGAATCGCTTCAGAGTTG-3‘,TRvPK-SR:5'-ATGAACACCGAGTATCAC-3').然后将青头菌菌种培养在不同含量的碳源添加物培养基上,37X恒温培养箱中培养14d后,从每种培养基上收获0.5g菌丝体,重复3次取样,提取总RNA并选择完整性较好和浓度合适的转录成cDNA.以MYA为基本培养基,分别添加2%和10%的葡萄糖、山梨醇、蔗糖、肌醇、麦芽糖、甘露醇和可溶性淀粉.然后以actin为阳性对照,采用RT-PCR以特异引物TRvPKSF和TRvPKSR-252 -福建农林大学学报(自然科学版)第50卷检测该基因的具体表达情况.2结果与分析2.1 RvPKS 基因的全长cDNA 克隆RvPKS 基因的克隆测序结果(图1)显示,该基因(GenBank 登录号 MT655136)的全长 cDNA 含有 6 039bp,可编码氨基酸2 012个;保守结构域分析显示该基因 的蛋白结构域组织为:ACP 酰基转移酶(SAT )中酮基合成酶(KS )-酰基转移酶(AT )-酰基载体蛋白(ACP )-硫酯 酶释放结构域(TE ).将该基因的cDNA 全长于NCBI 上进行BLASTN 比对,未发现与该基因同源的基因;将其蛋白序列进行BLASTP 比对发现,该蛋白与易碎软齿菌 (Dentipellis fragilis )的 PKS ( TFY72602.1)蛋白序列拥有最高的相似性,但其相似度仅为49.03%,说明该基因为尚未报道的PKS 基因.2.2 RvPKS 蛋白的生物信息学分析RvPKS 蛋白分子质量为219.03 ku,理论等电点(pl ) 5.89,分子式为 C 9748H 15372N 2656O 2910S 8,其由 2 012 个氨基10 000 ——7 500bp 15 0005 0002 5001 000250M RvPKS bp6 039M : maker.图1 RvPKS 基因全长cDNA 的琼脂糖凝胶电泳图Fig.1 Agarose gel electrophoresis of the full-length cDNA ofthe RvPKS gene 酸残基组成,其中亮氨酸(Leu )、丝氨酸(Ser )和丙氨酸(Ala )为该蛋白中含量最高的3个氨基酸,酸性氨 基酸数量191个,碱性氨基酸155个;该蛋白的不稳定系数(II )是41.02,属于不稳定蛋白;其脂肪族氨基 酸系数为97.09,亲水性平均系数(GRAVY )为0.061.经保守结构域分析表明,该蛋白含有SAT-KS-AT- ACP-TE 等结构域,其中各结构域的保守活性氨基酸序列(图2)为SAT (GIIGFSSGII ) ,KS ( DTACSSSL )、AT (NVVEAHGTGTQ )、ACP ( VVGHSLGEYVA )和 TE ( LGGWSLGGIIA )(粗体字代表高度保守氨基酸).Sig- nalP-5.0预测显示RvPKS 蛋白无信号肽存在,TargetP 2.0预测结果显示该蛋白定位于细胞质基质;SOP- MA 预测显示该蛋白组成a 螺旋的氨基酸有813个*折叠289个、R 转角87个、无规则卷曲823个,分别 占蛋白质氨基酸总数的40.41%、14.36%、4.32%和40.90%(图3).青头菌RvPKS 蛋白与其他真菌PKS 蛋 白的聚类分析结果显示(图4),该聚类树分为5个分支,其中火丝菌(Pyronema omphalodes , GenBank 登录 号:CCX04910)、鸡枞菌属(Termitomyces sp., GenBank 登录号:KNZ72615 )、白环菇属(Leucoagaricus sp., GenBank 登录号:KXN83388 )、乌氏曲霉(Aspergillus udagawae , GenBank 登录号:GAO84443 )、丝曲霉(As pergillus lentulus , GenBank 登录号:GFG17843 )、Penicillium subrubescens ( GenBank 登录号:OKP10856)和青 头菌PKS 蛋白聚为一支,其结构域组织顺序为SAT-KS-AT-ACP-TE,含有非还原型PKS 的结构域SAT,即 该蛋白编码非还原型PKS ;该分支中乌氏曲霉的PKS ( GenBank 登录号:GAO84443)⑼、火丝菌的PKS (GenBank 登录号:CCX04910) [10]其蛋白产物为聚酮合酶,生物合成的产物为分生抱子色素,青头菌 RvPKS 基因的终产物可能为分生抱子色素.2.3 RvPKS 基因的表达分析RT-PCR 结果显示(图5):该基因在2%碳源含量条件下,添加山梨醇的培养基中,该基因表达量最 高,后面从高到低依次为麦芽糖>葡萄糖〉肌醇>蔗糖〉甘露醇〉可溶性淀粉;RvPKS 基因在10%碳源含量条 件下,表达量从高到低依次为蔗糖〉葡萄糖 > 山梨醇 > 麦芽糖 > 甘露醇 > 肌醇 > 可溶性淀粉.说明该基因受不 同含量糖类的诱导表达程度不同,但可溶性淀粉均不能强烈诱导该基因表达.3讨论目前,关于青头菌的研究主要集中在青头菌冷冻工艺[11]、化学成分[12,13]、子实体多糖的理化性质[14]、 系统发育和ITS 鉴定[15,16]、系统分类等方面,而关于青头菌中聚酮类化合物及其基因的研究尚未见报道. 本研究以青头菌的基因组数据为基础,分离获得一条PKS 基因,生物信息学分析显示该基因的蛋白序列第2期原晓龙等:青头菌(Russula virescens )聚酮合酶基因的克隆及碳源对该基因表达的影响-253 -含有SAT-KS-AT-ACP-TE,其中SAT 结构域为非还原型PKS 特有的结构域[17];与其它真菌进行比较,发现 各结构域含有保守氨基酸序列,分别为 SAT [ G( I/V) (I/L)GFSSGI(I/L) ] ,KS(DTACSSS)、AT( HGTGT)、 ACP(VVGHSLGEY)和TE(GGWSLGG) [18,19];同时该蛋白含有KS-AT-ACP 这3个聚酮合酶的最基本结构 域[20];分子系统进化树显示与青头菌RvPKS 蛋白聚为一支的其他真菌,其结构域组织顺序均为SAT-KS- AT-ACP-TE ;且其中乌氏曲霉的PKS(GenBank 登录号:GAO84443)[9]、火丝菌的PKS ( GenBank 登录号 CCX04910)[10]的终产物为分生抱子色素.这些证据均表明青头菌RvPKS 基因编码非还原型PKS 酶,其终 产物可能为分生抱子色素.SAT domam 鉅始单位:脱基蛋白转移酶)RvPKS QVLIYFKWATSIVG —DSQDAFASLLERNRQNG1GIIGFSSGIISACITGTSATLLDFLDePKS QTLRYLAFIESYL —ASTSQPFASVLASNRAHSI.GrvTGFSSGILIACWGTSISTLEFIGtPKS HsPKS QSLRYLAHIESLS-TEKKTSPFADYLKSNAAQGLGTvTGFSSGILIACWGTSNTTVSYIQSLRYLAHVESQASAE KSAAPF FDYLKKNVEHGI ,GVLGFSSGm ACWGT SKNTLAYVAgPKSQTLRYLAYIDASVASNGSLTPFSDVLKPNSVHG^ ^TGFSSGILIAAWATSFSSVS FL % * * * * * W it 4r itKS domain (p 翩基合成酶)RvPKS DePKS GtPKSHsPKS AgPKS★★★★★★IDVYYSTGNLRAFLSGRISYAMGFGGPSMV" 7DTACSSSL VAIYQACRALLSGDCNAALAGIDVYYSTGTLRAFLSGRISYAMKLSGPSW : DTACSSSI gVYQACRALMNRDCNAAMAGIDVYYSTGTLRAFLSGRISYAFQWSGPSLV : DTACSSSK VAIYQACRALMNRDCNAALAG IDVYYSTGTLRAFLSGRISYAMQWSGPSIV .DTACSGSIIAVYQACRALMNRDCNAALAGIDVYYSTGTLKAFLSGRLSYSMQLSGPSIV fDTACSSSG VAVYQGARALMNGDCNAAIVG★ ★★★★★★★ ★ ★★ it it * * * * * * * it * * * * * * * w w AT domam 〔酰基转移酶)RvPKS LGIIRGIEVNQSAEARSITQPHIPTQIKLFRQLLETS^ZAPETl^ATAHGTGTQ :•GDIGDePKS GtPKSMGVIRGVEVNQSGLAHSITHPHPPTQEVLFKaVLDKTGIDPRRiN\7T v 7EAHGTGT MGVIRGIDVNQSGNAHSITHPHAPTQATLFKRVLEATGIDPTRINWEAHGTGT ;l GDPNl GDPN HsPKS LGVIRGIEVNQSGNAHSITHPHAPTQATLFHRVLAQTGIDPHRprATAHGTGT ;l GDPNAgPKS WGVIRGIEVNQSGLAHSITHPHAPTQITLFKQLLENTGV^ATRib^TAHGTGTQ * *** n * *** ** *** ** * * ]** *********l GDPN **ACP domain (酰基载体蛋白)RvPKSDePKS WGHSLGET/A ;WGHSLGEYAA^p^G\TTLQDALLLVANRARLMAQKCTSSSTGM14AVNLCAATIGRILT k^IAG^TTLKGALTLIANRVRFMVTKCAVETTGMIAINRGSEAIAELLA GtPKS WGHSLGEYAA HsPKS WGHSLGEYAA \T :AGVLTLKGALTIVANRVRLMVTKCATESTGMIAINQGPAAVKDILQOTAGVLTVKGALAIIAHRVRLMVTKCATDATSMIAINQGPAAIED HRAgPKSWGHSLGEYAA T vT :ANVLSLRGALTI IAHRVRLMVTKCAVSSTSMIAVNLAQSLLQDILK ********* %* * **TE domam (硫酉:酶释放结构域)RvPKS SMAIEYAKYTIKAVGLGPV : LGGWSLGGIIAI ,EVARHLLKLDVPVKGWLI DSPSPLNHVDePKS GtPKS SMAAEYSEFATKTT-S EPL] ,LGGWSFGGWAI EAARQLMKKGVaVKGVLLI DSPSPVNHVAMASEYADLITKTA-SGPIJIGGWSFGGVAAIEIARQLLRKGVPVKGVLLI DSPSPVNHVHsPKSSMASEYADFVTKTS-SGPL1 ,LGGWSFGGVAAI 'ELARQLMRKGVaVKGWLI DSPSPVNHV AgPKS EMSQAYAKVISQVS-KGPL1 .LGGWSFGG\7^:***** **ETALQLQKQGITVKGILLVDSPNPINHV * * * *** 4r *** * **** **★ ★★ ★ ★ ★RvPKS :青头菌 PKS (Russula virescens ) ; DePKS :软齿菌属 PKS (Dentipellis sp., GenBank 登录号:KAA1469652.1) ; GtPKS :密褐褶孔菌PKS( Gloeophyllum trabeum , GenBank 登录号:XP_007866703.1) ; HsPKS :小侧沟香菇(Heliocybe sulcata , GenBank 登录号:TFK52663.1) ;AgPKS :法国蜜环菌(Armillaria gallica , GenBank 登录号:PBK92884.1) , * 表示竖列中的氨基酸完全一致,表示竖列中的氨基酸有3个以下的差异.图2青头菌RvPKS 蛋白各结构域的保守活性位点Fig.2 Conserved active amino acids sites of the RvPKS proteins in R.virescens-254 -福建农林大学学报(自然科学版)第50卷图3 RvPKS 蛋白的三级结构预测结果Fig.3 Prediction of the RvPKS protein tertiary structure—Talarontyces mameffei EEA24206.1—PenidUium chiysogenum KZN89197.1Lepidopterellapalustris OCK80349.1 Aspergillus lentulus GFF79351.1一 Tolypocladiwn ophioglossoides KND95254.1-Tdlaroniyces marneffei KFX44829.1Aspergillus niger XP_001390425.2—Beaiiveria bassiana KGQ04250.1SAT-KS-AT-ACP-PT-PP-TESAT-KS-AT-ACP-PT-PP-PP-TESAT-KS-AT-ACP-PT-PP-PP-TESAT-KS-AT-ACP-TESAT-KS-AT-ACP-PP-TE--------Pestalotiopsis malicola AGT 56219.1---------Diaporthe helianthi POS73626.1----------Scedosporium apiospermuin KEZ40717.1Verticillium alfalfae EEY 14472.1Colletotrichum trifolii TDZ67169.1Aspergillus udagawae GAO84443.1-Aspergillus lentulus GFG17843.1-----Pyivnema omphalodes CCX04910.1Russula virescens PKS Termitomyces sp. KNZ72615.1Leucoagaiicus sp. KXN83388.1一 Pyricularia otyzae ELQ70531.1—Penicillium chiysogenum KZN88913.1-Cotynespora cassiicola PSN68461.1Pyrenophora tiitici-repemis EDU47223.1图4青头菌RvPKS 蛋白与其他真菌PKS 蛋白的聚类分析Fig.4 Phylogenic analysis of the RvPKS in R.virescens and PKS proteins from otherfungus第2期原晓龙等:青头菌(Russula virescens)聚酮合酶基因的克隆及碳源对该基因表达的影响・255・图5RvPKS基因在含不同碳源添加物培养基上的基因表达情况Fig.5Relative expression of the RvPKS gene under mediums supplemented with various carbon sources 青头菌是一种与阔叶树或针叶树的根部共生的外生菌根菌,需要供给其合适的营养成分和生长条件才能使其抱子萌发、菌丝生长[21].离体培养时,不同的培养基会影响青头菌菌种的菌丝生长速度[22],青头菌子实体中多糖含量成分较高,其单糖组分主要包括葡萄糖、甘露糖和果糖等[⑷;同时渗透压、不同碳氮源和不同含量的碳氮源添加物能影响真菌中聚酮类次生代谢产物和PKS基因的表达,如10%含量的山梨醇、2%和10%含量的蔗糖均能够促使长松萝中UlPKS基因的大量表达[23].因此,本研究在基础培养基上,添加不同种类和浓度的碳源添加物以研究碳源添加物对RvPKS基因表达的影响.结果表明,不同含量的碳源添加物对该基因表达影响差异显著,其中在2%碳源含量条件下,山梨醇对该基因的表达的影响最为强烈;在10%碳源含量条件下,蔗糖对该基因表达的影响最为强烈.这种同一基因在不同培养条件下表达量明显差异的现象是因其受到渗透压、培养基成分和酶抑制剂等的影响,使同一蛋白酶受到正或负反馈,进而进入不同的代谢通路,产生不同的次级代谢产物,是一种通过微生物基因组数据挖掘获得骨架新颖、活性不同的次级代谢产物的有效途径[24,25].本研究以基因组数据为基础,结合生物信息学分析成功分离得到一条青头菌的RvPKS基因,并对其功能进行预测分析,并检测该基因在不同碳源条件下的具体表达,为鉴定和异源表达青头菌中聚酮合酶基因提供依据.参考文献[1]黄萍,沈孝善•绿菇子实体菌株的原生质体分离及再生菌株的获得[J].西南农业学报,2001,14(1):91-95.[2]朱启顺,杨大智.绿菇与云南松共生关系的研究[J].中国食用菌,1999,18(5):19-20.[3]王勃,周文忠,董胜强,等.青头菌子实体发育进程中挥发性成分分析[J].食品与发酵工业,2014,40(8):178-183.[4]SUN Z,ZHANG L,ZHANG B,et al.Structural characterisation and antioxidant properties of polysaccharides from the fruitingbodies of Russula virescens[J].Food Chemistry,2010,118(3):675-680.[5]马红英,杨明挚,张汉波,等.青头菌的分离纯化及ITS序列鉴定[J].中国食用菌,2013,32(3):41-43.[6]LI GJ,ZHAO R L,ZHANG CL,et al.A preliminary DNA barcode selection for the genus Russula(Russulales,Basidiomyco-ta)[J].Mycology,2019,10(2):61-74.[7]TAE H,SOHNG J K,PARK K.MapsiDB:an integrated web database for type I polyketide synthases[J].Bioprocess and Biosystems Engineering,2009,32(6):723-727.[8]朱峰,乔建军.聚酮合成酶底物专一性的研究进展[J].中国抗生素杂志,2006,31(11):641-645,664.[9]KUSUYA Y,TAKAHASHINAKAGUCHI A,TAKAHASHI H,et al.Draft genome sequence of the pathogenic filamentous fungus Aspergillus udagawae strain IFM46973T[J].Genome Announcements,2015,3(4).DOI:10.1128/genomeA.00834-15. [10]TRAEGER S,ALTEGOER F,FREITAG M,et al.The genome and development-dependent transcriptomes of Pyronema con-fluens:a window into fungal evolution[J].PLOS Genetics,2013,9(9).DOI:10.1371/journal.pgen.1003820.[11]汤建国.变绿红菇化学成分研究[J].中草药,2008,39(12):1776-1778.[12]徐丹先,林佶,段志敏,等.云南野生青头菌的化学成分分析[J].现代预防医学,2012,39(21):37-38.[13]王婷婷,樊建,赵天瑞.青头菌汁液对香蕉果酒发酵的影响[J].中国食用菌,2012,31(2):54-56.[14]孙忠伟,张丽香,王愈,等.变绿红菇子实体多糖的理化性质及其抗肿瘤活性[J].农产品加工学刊,2009(7):77-81.[15]MILLER S L,BUYCK B.Molecular phylogeny of the genus Russula in Europe with a comparison of modern infrageneric clas--256-福建农林大学学报(自然科学版)第50卷sifications[J].Mycological Research,2002,106(3):259-276.[16]SHIMONO Y,KATO M,TAKAMATSU S.Molecular phylogeny of Russulaceae(Basidiomycetes;Russulales)inferred fromthe nucleotide sequences of nuclear large subunit Rdna[J].Mycoscience,2004,45(5):303-316.[17]CRAWFORD J,DANCY B,HILL E,et al.Identification of a starter unit acyl-carrier protein transacylase domain in an iterative type I polyketide synthase[J].Proceedings of the National Academy of Ences of the United States of America,2006,103(45):16728-16733.[18]BUKELSKIS D,DABKEVICIENE D,LUKOSEVICIUTE L,et al.Screening and transcriptional analysis of polyketide synthases and non-ribosomal peptide synthetases in bacterial strains from Krubera-Voronja Cave[J].Frontiers in Microbiology, 2019,10:2149.DOI:10.3389/fmicb.2019.02149.[19]PARK H,MIN B,JANG Y,et prehensive genomic and transcriptomic analysis of polycyclic aromatic hydrocarbondegradation by a mycoremediation fungus,Dentipellis sp.KUC8613[J].Applied Microbiology and Biotechnology,2019,103(6):8145-8155.[20]KOMAKI H,SAKURAI K,HOSOYAMA A,et al.Diversity of nonribosomal peptide synthetase and polyketide synthase geneclusters among taxonomically close Streptomyces strains[J].Scientific Reports,2018,8(1):6888.DOI:10.1038/s41598—018-24921-y.[21]才晓玲,何伟,安福全•青头菌研究进展[J].现代农业科技,2014(17):122-125.[22]马红英•云南常见食用菌分离、培养及鉴定[D].昆明:云南大学,2013.[23]王毅,周旭,许宰铣,等•长松萝中一个聚酮合酶基因簇的克隆和鉴定[J].微生物学报,2014,54(7):770-777.[24]WANG W J,LI D Y,LI Y C,et al.Caryophyllene sesquiterpenes from the marine-derived Fungus Ascotricha sp.ZJ-M-5bythe one strain-many compounds strategy[J].Journal of Natural Products,2014,77(6):1367-1371.[25]VALARMATHI R,HARIHARAN G N,VENKATARAMAN G,et al.Characterization of a non-reducing polyketide synthasegene from lichen Dirinaria applanata[J].Phytochemistry,2009,70(6):721-729.(责任编辑:吴显达)。
非核糖体肽合成酶和聚酮合酶
非核糖体肽合成酶和聚酮合酶是两个重要的酶类,它们在蛋白质合成和DNA修复中起着关键作用。
非核糖体肽合成酶是一种复合酶,由不同的蛋白质和RNA组成。
它的主要功能是将氨基酸与tRNA结合,形成带有氨基酸的tRNA,为蛋白质合成提供基础。
非核糖体肽合成酶的缺陷会导致蛋白质合成异常,甚至致死。
聚酮合酶是一种酶家族,包括多个亚型。
它们的主要功能是修复DNA中的氧化损伤和单链断裂。
聚酮合酶在DNA修复中发挥重要作用,缺陷会导致DNA损伤的积累和细胞死亡。
研究非核糖体肽合成酶和聚酮合酶的结构和功能,对于理解蛋白质合成和DNA修复的机理具有重要意义。
同时,这些酶也是开发新型药物和治疗癌症的重要靶点。
- 1 -。
非核糖体肽合成酶和聚酮合酶
非核糖体肽合成酶和聚酮合酶是两种重要的酶类,它们在生物合成中起着不可替代的作用。
非核糖体肽合成酶是一种在蛋白质合成过程中起着关键作用的酶。
它通过将氨基酸与tRNA结合,从而将氨基酸带入到正在合成的蛋白质链中。
非核糖体肽合成酶还能够保证蛋白质链的正确性和稳定性,避免其受到蛋白酶的降解。
聚酮合酶是一种能够催化多种有机化合物合成的酶。
它能够将简单的有机化合物聚合成更复杂的化合物,包括多肽、多糖等。
聚酮合酶在生物合成中的作用十分广泛,包括合成DNA、RNA、蛋白质等。
这两种酶的作用不仅在生物合成中具有重要作用,在生物医学、生物工程等领域中也有广泛应用。
对这两种酶的深入研究将有助于揭示生物合成的机制,推动生物工程技术的发展。
- 1 -。
聚酮合类药物和聚酮合酶
一、聚酮类药物
聚酮类化合物是由简单脂肪酸在聚酮合酶催化下经过类似长链脂肪酸的合成途径生成的,其中心骨架是通过丙二酸(或有取代基的丙二酸)硫酯重复的脱羧缩合而形成的。
包括聚次甲基酮基团( (CH2一CO)n)化合物及其加水、脱水或者脱羧的衍生物。
常见的聚酮类药物主要有洛伐他汀、阿霉素、红霉素、四环素、两性霉素、南昌霉素、普拉固(普伐他汀)等
二、聚酮合酶
聚酮合成酶通过催化前体物质进行反复的缩合反应,可以形成多种聚酮体,再经过甲基化、氧化还原、糖基化等修饰反应形成各种各样结构复杂的聚酮类化合物。
尽管聚酮类化合物在结构上是多样的,但其生物合成有其共同的机制,其核心结构均由聚酮合酶催化合成。
根据聚酮合酶的结构及其它性质,聚酮合酶被分成Ⅰ型(typeⅠPKS,又称模件型)、Ⅱ型(typeⅡPKS,又称迭代型)和Ⅲ型(typeⅢPKS,查尔酮型)3大类。
Ⅰ型PKSⅠ型PKS是以模块形式存在的多功能酶,每一模块含有一套独特的、非重复使用的催化功能域,其非重复使用的催化功能域与聚酮生物合成的反应顺序呈线性对应,主要催化合成大环内酯类、聚烯及聚醚类化合物。
Ⅱ型PKS 1984年Malpartida和Hopwood首次报道了Ⅱ型PKS是一个多功能酶复合体,只包含一套可重复使用的结构域,每一结构域在重复的反应步骤中都多次地用来催化相同的反应。
Ⅲ型PKSⅢ型聚酮合酶(TypeⅢPKSs)以植物中的查耳酮合酶为代表(chalcone synthases)。
1999年,Funa等发现了一种类似苯基苯乙烯酮合成酶的PKS(chalcone synthase-like PKS)———Rp-pA,后来被称为Ⅲ型PKS。
Ⅲ型PKS和其它两种PKS迥然不同,它在不需要ACP的情况下直接催化泛酰辅酶A间的缩合,主要负责单环或双环芳香类聚酮化合物的生物合成。
全球现在已有两个聚酮合酶数据库,一个是印度国家免疫学研究所的Yadav G等人于2003年构建的PKSDB数据库;另一个是在PKSDB数据库基础上,韩国SmallSoft公司Tae H等人对PKSDB数据库加以改进和补充,在2007年构建的ASMPKS数据库。
三、聚酮合酶与组合生物药物
3.1聚酮化合物的组合生物合成的理论依据
组合生物合成(eombinatorial biosynthesis)或组合生物学(eombinatorial biology)是近年发展起来的技术,是在微生物次级代谢产物生物合成基因和酶学研究基础上形成的。
是指应用基因重组技术重新组合微生物药物的基因簇(duster),产生一些新的非天然的基因簇,从而合成许多新的非天然的化合物,为微生物药物的筛选提供丰富的化合物资源。
负责延伸1个二碳单位的所有结构域称为1个模块,I型聚酮合酶包括多个模块。
每个模块上分别携带有参与聚酮生物合成所必需的各种具有不同催化功能的结构域(Domain),包括酰基转移酶、酰基载体蛋白、β-酮酰-ACP合酶、酮还原酶、脱水酶、烯酰还原酶、硫酯酶等。
利用组合生物合成技术进行非天然聚酮类化合物的理论依据是:这些模块是线性排列的,在不同的PKS中都能发挥各自相应的酶活性,催化相应的底物进行合成,并且对底物的特异性要求并不十分严格。
这为聚酮化合物的组合生物合成的发展奠定了基础。
利用组合生物合成技术使PKS中的某些模块互换、插入或缺失就可以得到许多“非天然”具有活性
的聚酮类化合物。
3.2聚酮化合物组合生物合成面临的困难
PKS全酶基因簇的异源表达还有比较大的难度,这是由于PKS的异源表达对宿主提出许多要求:遗传背景清楚、有成熟的遗传操作方法、有成熟的培养方法、宿主的生长不受PKS蛋白表达的影响、有能力表达高分子量的PKS(约100~10000 kDa)、可以对PKS进行翻译后修饰、自身可产生足够的合成前体(如脂酰CoA或衍生物)、对聚酮化合物的修饰、宿主不受聚酮产物毒害、具有某些必需的细胞因子等等。
目前组合生物合成聚酮产物种类非常多,2008年在PubMed上已发表论文中报道的组合生物合成聚酮已经超过200多种,但是这些新产物的生物活性都没有能够超过原来的聚酮化合物,商品化的组合生物合成聚酮产物也没有出现。
参考文献:
1、顾觉奋,祝兴伟。
组合生物合成聚酮类药物研究进展。
Chinese Journal of New Drugs 2006,15(19):
1620
2、刘炳辉,曹远银,闫建芳,齐小辉,程浩,黄盼盼,刘秋。
聚酮类化合物生物合成基因簇与药物筛选。
Biotechnology Bulletin,2008,4:31
3、朱峰乔建军。
聚酮合成酶底物专一性的研究进展。
中国抗生素杂志,2006年3月,11:641
4、王翠玲。
聚酮合酶数据库初步构建及多烯类聚酮合酶系统发育分析。
李云涛
生命基地82班
2010-10-16。