氧化铝-
- 格式:ppt
- 大小:2.70 MB
- 文档页数:30

氧化铝(Al2O3)是一种广泛应用的陶瓷材料,具有优异的物理化学性质和热稳定性。
但是,传统的氧化铝在催化剂和吸附剂等领域的应用受到制约,主要是因为其表面活性较低,难以与目标分子发生有效的化学反应。
为了克服这一局限,研究人员提出了利用特定方法来活化氧化铝的想法,从而提高其表面活性和催化效率。
1. 氧化铝的活化原理氧化铝的活化主要是通过改变其表面结构和化学性质来增强其表面活性。
常见的活化方法包括物理活化和化学活化两种。
- 物理活化:主要是通过改变氧化铝的晶体结构或孔隙结构来提高其表面积和孔隙率,从而增加其吸附能力和活性位点密度。
常用的物理活化方法包括煅烧、球磨、超声处理等。
- 化学活化:主要是通过引入活性位点或表面功能团来改变氧化铝的化学性质,从而增强其与目标分子的相互作用能力。
常用的化学活化方法包括表面改性、负载金属催化剂、酸碱处理等。
2. 氧化铝的活化技术对于氧化铝的活化,研究人员提出了多种技术和方法,其中一些技术已经在实际生产中得到了应用。
- 煅烧活化:通过高温煅烧氧化铝样品,可以使其结晶度提高,晶格畸变减小,晶体尺寸变大,从而提高其比表面积和孔隙率。
同时还可以改善氧化铝的结晶性质和物理化学性能,增强其与目标分子的相互作用能力。
- 表面改性活化:通过引入金属或非金属元素,改变氧化铝的表面化学性质,增强其与目标分子的吸附和催化能力。
负载金属催化剂可以增加氧化铝的活性位点密度,提高其催化性能。
- 酸碱处理活化:通过酸碱处理,可以改变氧化铝的表面酸碱性质,增强其与目标分子的化学反应能力。
酸处理可以引入强酸性位点,增强氧化铝的酸性;碱处理可以引入强碱性位点,增强氧化铝的碱性。
3. 氧化铝活化的应用领域活化后的氧化铝可以在多个领域得到应用,包括催化剂、吸附剂、分离膜等。
- 催化剂应用:活化后的氧化铝具有更高的表面活性和催化效率,可以应用于催化反应中,如重油加氢、醇醚化、氧化反应等。
- 吸附剂应用:活化后的氧化铝具有更高的吸附能力和选择性,可以应用于气体吸附、废水处理、有机物分离等领域。
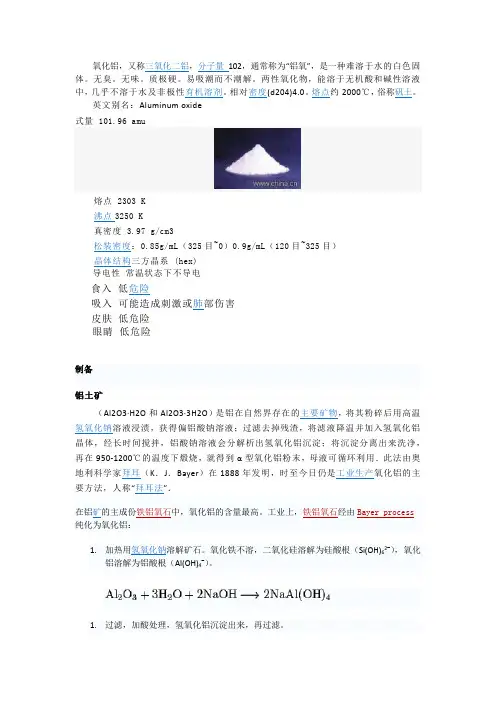
氧化铝,又称三氧化二铝,分子量102,通常称为“铝氧”,是一种难溶于水的白色固体。
无臭。
无味。
质极硬。
易吸潮而不潮解。
两性氧化物,能溶于无机酸和碱性溶液中,几乎不溶于水及非极性有机溶剂。
相对密度(d204)4.0。
熔点约2000℃,俗称矾土。
英文别名:Aluminum oxide式量 101.96 amu导电性常温状态下不导电1.加热用氢氧化钠溶解矿石。
氧化铁不溶,二氧化硅溶解为硅酸根(Si(OH)62−),氧化铝溶解为铝酸根(Al(OH)4−)。
1.过滤,加酸处理,氢氧化铝沉淀出来,再过滤。
再由Hall-Heroult法转变为铝金属。
再由Hall-Heroult法转变为铝金属。
α型氧化铝在α型氧化铝的晶格中,氧离子为六方紧密堆积,Al3+对称地分布在氧离子围成的八面体配位中心,晶格能很大,故熔点、沸点很高.α型氧化铝不溶于水和酸,工业上也称铝氧,是制金属铝的基本原料;也用于制各种耐火砖、耐火坩埚、耐火管、耐高温实验仪器;还可作研磨剂、阻燃剂、填充料等;高纯的α型氧化铝还是生产人造刚玉、人造红宝石和蓝宝石的原料;还用于生产现代大规模集成电路的板基.γ型氧化铝γ型氧化铝是氢氧化铝在140-150℃的低温环境下脱水制得,工业上也叫活性氧化铝、铝胶.其结构中氧离子近似为立方面心紧密堆积,Al3+不规则地分布在由氧离子围成的八面体和四面体空隙之中.γ型氧化铝不溶于水,能溶于强酸或强碱溶液,将它加热至1200℃就全部转化为α型氧化铝.γ型氧化铝是一种多孔性物质,每克的内表面积高达数百平方米,活性高吸附能力强.工业品常为无色或微带粉红的圆柱型颗粒,耐压性好.在石油炼制和石油化工中是常用的吸附剂、催化剂和催化剂载体;在工业上是变压器油、透平油的脱酸剂,还用于色层分析;在实验室是中性强干燥剂,其干燥能力不亚于五氧化二磷,使用后在175℃以下加热6-8h还能再生重复使用.目前世界上用拜耳法生产的氧化铝要占到总产量的90%以上,氧化铝大部分用于制金属铝,用作其它用途的不到10%.电解氧化铝工业化大规模生产电解铝的主要工艺过程是一个熔盐电化学过程,用简单的化学式可表示如下:熔盐电解主反应:Al2O3+2C ——————→ 2Al+CO2↑+CO↑ (1)阳极960~990℃阴极副反应:AlF3+C→Al+CF3 (2)Na3AlF3+C →Al+NaF+CF4+F2 (3)NaF+C → Na+CF4 (4)β型氧化铝还有一种β-Al2O3,它有离子传导能力(允许Na通过),以β-铝矾土为电解质制成钠-硫蓄电池。

氧化铝,又称三氧化二铝1,分子量102,通常称为“铝氧”,是一种白色无定形粉状物,俗称矾土,属原子晶体,成键为共价键,熔点为2050℃,沸点为3000℃,真密度为3.6g/c m。
它的流动性好,不溶于水,能溶解在熔融的冰晶石中。
它是铝电解生产的中的主要原料。
有四种同素异构体β-氧化铝δ-氧化铝v-氧化铝 a-氧化铝,主要有α型和γ型两种变体,工业上可从铝土矿中提取。
名称氧化铝;刚玉;白玉;红宝石;蓝宝石;刚玉粉;cor undum化学式 Al?O?外观白色晶状粉末或固体物理属性式量101.96 amu熔点 2303 K 沸点3250K密度 3.97 kg/m..晶体结构三方晶系 (h ex) 热化学属性ΔfH0liqui d ?1620.57 kJ/m olΔfH0solid?1675.69kJ/mo lS0liq uid,1 bar 67.24 J/m ol?KS0solid 50.9 J/mo l?K 安全性食入低危险吸入可能造成刺激或肺部伤害皮肤低危险眼睛低危险在没有特别注明的情况下,使用SI单位和标准气温和气压。
氧化铝是铝和氧的化合物,分子式为A l2O3。
在矿业、制陶业和材料科学上又被称为矾土。
应急处理隔离泄漏污染区,限制出入。
建议应急处理人员戴防尘面具(全面罩),穿防毒服。
避免扬尘,小心扫起,置于袋中转移至安全场所。
若大量泄漏,用塑料布、帆布覆盖。
收集回收或运至废物处理场所处置。
制备强热氢氧化铝,可得无定形之白色氧化铝粉末。
2Al(O H) 3→ Al2 O 3 +3H2 O 用途1.红宝石、蓝宝石的主成份皆为氧化铝,因为其它杂质而呈现不同的色泽。

有关氧化铝知识氧化铝、刚玉、红宝石和蓝宝石虽然名称各异,其形态、硬度、性质、用途也不相同,贵贱更是相距甚远,但是它们的化学成份却完全相同,皆是氧化铝。
一.氧化铝纯净的氧化铝是白色无定形粉末,俗称矾土,密度3.9-4.0g/cm3,熔点2050℃、沸点2980℃,不溶于水,氧化铝主要有α型和γ型两种变体,工业上可从铝土矿中提取。
铝土矿(Al2O3·H2O和Al2O3·3H2O)是铝在自然界存在的主要矿物,将其粉碎后用高温氢氧化钠溶液浸渍,获得铝酸钠溶液;过滤去掉残渣,将滤液降温并加入氢氧化铝晶体,经长时间搅拌,铝酸钠溶液会分解析出氢氧化铝沉淀;将沉淀分离出来洗净,再在950-1200℃的温度下煅烧,就得到α型氧化铝粉末,母液可循环利用.此法由奥地利科学家拜耳(K.J.Bayer)在1888年发明,时至今日仍是工业生产氧化铝的主要方法,人称“拜耳法”.在α型氧化铝的晶格中,氧离子为六方紧密堆积,Al3+对称地分布在氧离子围成的八面体配位中心,晶格能很大,故熔点、沸点很高.α型氧化铝不溶于水和酸,工业上也称铝氧,是制金属铝的基本原料;也用于制各种耐火砖、耐火坩埚、耐火管、耐高温实验仪器;还可作研磨剂、阻燃剂、填充料等;高纯的α型氧化铝还是生产人造刚玉、人造红宝石和蓝宝石的原料;还用于生产现代大规模集成电路的板基.γ型氧化铝是氢氧化铝在140-150℃的低温环境下脱水制得,工业上也叫活性氧化铝、铝胶.其结构中氧离子近似为立方面心紧密堆积,Al3+不规则地分布在由氧离子围成的八面体和四面体空隙之中.γ型氧化铝不溶于水,能溶于强酸或强碱溶液,将它加热至1200℃就全部转化为α型氧化铝.γ型氧化铝是一种多孔性物质,每克的内表面积高达数百平方米,活性高吸附能力强.工业品常为无色或微带粉红的圆柱型颗粒,耐压性好.在石油炼制和石油化工中是常用的吸附剂、催化剂和催化剂载体;在工业上是变压器油、透平油的脱酸剂,还用于色层分析;在实验室是中性强干燥剂,其干燥能力不亚于五氧化二磷,使用后在175℃以下加热6-8h还能再生重复使用.目前世界上用拜耳法生产的氧化铝要占到总产量的90%以上,氧化铝大部分用于制金属铝,用作其它用途的不到10%.二.刚玉自然界天然存在的α型氧化铝晶体叫做刚玉,常因含有不同的杂质而呈现不同的颜色.刚玉一般呈带蓝或带黄的灰色,有玻璃或金刚光泽,密度在3.9-4.1g/cm3,硬度8.8,仅次于金刚石和碳化硅,能耐高温.含有铁的氧化物的刚玉砂叫金刚砂,呈暗灰色、暗黑色,常作研磨材料,用于制各种研磨纸、砂轮、研磨石,也用于加工光学仪器和某些金属制品.因天然刚玉产量供不应求,工业上常将纯α型氧化铝粉末在高温电炉中烧结制成人造刚玉,也称电熔刚玉.它能耐1800℃以上的高温,是制造高级特殊耐火材料的原料,有高温下机械强度大,抗热震性好,抗侵蚀性强,热膨胀系数小等特点,用于制火箭发动机燃烧室内衬、喷咀,雷达天线保护罩,原子能反应堆材料,高级高频绝缘陶瓷,冶炼纯金属和合金的坩埚,高温发热原件,热电偶保护管,各种高温炉的炉衬等.人造刚玉还用于制精密仪表轴承和金属丝的拉丝模具.我国自1958年起就能产生人造刚玉了.三.红宝石和蓝宝石混有少量不同氧化物杂质的优质刚玉就是大名鼎鼎的红宝石和蓝宝石,是制作名贵首饰的材料,其微粒可制精密仪表和手表的轴承.红宝石是天然产的透明红色刚玉,颜色从淡玫瑰红至深胭脂红,有的还略带紫色色调,有的有星光,以呈鸽子血红色最具有商业价值.红色是晶体中含少量氧化铬之故.红宝石是宝石中的珍品,七月生石.红宝石英语为Ruby,源出拉丁语ruber意为红色,硬度为9,密度常为4g/cm3,有金刚光泽.天然红宝石重量达1克拉的不多,超过5克拉已属罕见,世界上每年开采的红宝石其中品质最优者仅占千分之一.世界天然红宝石迄今发现最大的重3450克拉产自缅甸,世界著名的巨大星光红宝石重138.7克拉,著名的鸽血红宝石重55克拉.世界红宝石最有名的产地是缅甸曼德拉的东北部,还有泰国、斯里兰卡、柬寨.1973年在非洲肯尼亚的恩干加,1978年在澳大利亚中部阿利斯波利,70年代末在巴基斯担的罕萨先后发现大型红宝石矿藏,以上发现被誉为70年代世界红宝石矿三大发现.我国红宝石主要产地为云南、青海,数量不多质量也不大理想.蓝宝石因其在自然界存在比红宝石数量要多,故早在公元前800年就被人类当作宝石.它也是天然的α型氧化铝晶体.因含有少量铁和钛杂质,颜色从很淡的蓝色至深靛蓝,尤以中等程度的蓝色最为珍贵.天然刚玉晶体中若含少量铁、钴呈绿色,含钒呈翠绿,含镍、镁呈黄色,含锰、铁呈褐色,这些有色刚玉一般也归入蓝宝石.蓝宝石的硬度、密度、类似红宝石,也有金刚光泽,少数有星光效果,它是九月生辰石.我国蓝宝石主要产地为山东省昌乐县和海南省文昌县,此外江苏、福建也有出产,虽然数量比红宝石要大,但质量也不甚理想.世界蓝宝石主要产自澳大利亚和斯里兰卡,两国约集中了世界蓝宝石资源的80%,其中澳大利亚就占60%,此外印度、缅甸、泰国、柬埔寨、马达加斯加、俄国、南非、美国也有出产.美国某博物馆藏有一颗重563克拉的印度星光蓝宝石,色泽稍暗淡,星光完美几乎无瑕疵.1984年在澳大利亚发现著名昆土兰星光蓝宝石,为历来发现的最大星光刚玉,原石重1156克拉,琢磨后重733克拉,呈椭圆形如鸡蛋,后为美国洛杉矶一家私人宝石公司所收藏.1996年下半年一批泰国宝石学家在非洲马达加斯加发现了迄今世界上最大的一串绿石.他们化了一周时间挖掘一块巨大的云母,在云母下面发现了一串绿宝石,共有127块,重达数十千克,价值5千万美元.泰国的曼谷是日前世界上最大的红、蓝宝石加工中心,宝石的改色、雕琢工艺技术水平居世界前茅,宝石加工业是该国的支柱产业.四.人造红宝石、蓝宝石1877年法国化学家弗雷米将纯氧化铝粉末、碳酸钾、氟化钡和少量重铬酸钾作原料,在坩埚中经高温熔融8天,获得小颗粒红宝石晶体,这是人造红宝石的开端.1885年在瑞士日内瓦出现一些品质优良的人造红宝石,据说是有天然红宝石碎片,加上增强红色的重铬酸钾等经高温熔融制成,和天然品性质相同.然而真正实现人工制造宝石并能投入规模化生产的要归功于法国化学家维尔纳叶.维尔纳叶在1891年发明火焰熔融法,并用该法试制人造宝石,成功后又用纯净的氧化铝试验.在高温马弗炉中用倒置的氢氧吹管进行试验,含有少量氧化铬的纯净氧化铝细末慢慢落入火焰中熔化,滴在基座上冷凝结晶.经过十年的努力,1904年维尔纳叶正式制造出了人造红宝石,以后火焰熔融法逐渐完善,生产出的红宝石和天然品几乎无差别.该法一直沿用到现代,至今仍是世界生产人造宝石的主要方法,人称“维尔纳叶法”。

氧化铝种类氧化铝是一种常见的无机化合物,具有多种不同的种类和用途。
以下将介绍几种常见的氧化铝种类及其特点和应用。
1. α-氧化铝α-氧化铝是一种高纯度的氧化铝,具有良好的晶体结构和高热稳定性。
它通常以白色粉末的形式存在,具有优良的抗腐蚀性和绝缘性能。
α-氧化铝被广泛应用于电子元件、高温陶瓷、耐火材料等领域,如电容器、绝缘子、瓷砖等。
2. β-氧化铝β-氧化铝是一种具有较高比表面积的氧化铝,因其微米级的颗粒大小和多孔性结构而广泛应用于催化剂和吸附剂等领域。
β-氧化铝具有较大的比表面积和孔隙容积,能够提供更多的活性表面和吸附空间,因此在催化剂制备和废气处理等过程中发挥重要作用。
3. γ-氧化铝γ-氧化铝是一种具有高度活性和较大孔隙的氧化铝,常以无定形粉末的形式存在。
γ-氧化铝具有优异的吸附性能和催化活性,广泛应用于吸附剂、催化剂和催化载体等领域。
在吸附剂中,γ-氧化铝可用于气体和液体的吸附和分离;在催化剂中,γ-氧化铝可用作载体,提供活性金属的分散和稳定性。
4. δ-氧化铝δ-氧化铝是一种中间相态的氧化铝,具有介于α-氧化铝和γ-氧化铝之间的晶体结构和性质。
它通常以胶状或凝胶状的形式存在,具有较高的比表面积和孔隙度。
δ-氧化铝具有良好的吸附性能和催化活性,可用于催化剂的制备、催化反应和吸附分离等方面。
5. 高纯氧化铝高纯氧化铝是指纯度超过99.99%的氧化铝,具有极低的杂质含量和优异的物理化学性质。
高纯氧化铝常用于集成电路制备和高温陶瓷制备等高科技领域,如半导体材料、人工蓝宝石晶体、高压钠灯等。
高纯氧化铝的制备过程需要严格控制原料和工艺条件,以确保最终产品的纯度和质量。
氧化铝具有多种不同的种类和用途,每种种类都具有独特的特点和应用领域。
了解和掌握这些氧化铝种类的特性和用途,对于相关领域的科学研究和工业应用具有重要意义。
通过不断的研究和创新,氧化铝的应用领域将会不断扩展和深化,为人类的生活和工业发展带来更多的便利和可能性。

氧化铝氧化铝,又称三氧化二铝,俗称“矾土”。
是一种白色无定形粉状物。
与氧化铝有关的基本知识因氧化铝有不同的晶形,它可能属于不同的晶体类型:刚玉型晶体接近于原子晶体,其它晶型的基本上是离子晶体。
熔点为2050℃,沸点为3000℃,真密度为3.6g/cm。
它难溶于水,能溶解在熔融的冰晶石中。
它是铝电解生产中的主要原料,化学反应方程式为:2Al2O3=4Al+3O2。
工业上可从铝土矿中提取,化学方程式:溶解:将铝土矿溶于NaOH:Al2O3+2NaOH=2NaAlO2+H2O,过滤:除去残渣氧化铁,铝硅酸钠等酸化:向滤液中通入CO2.NaAlO2+CO2+H2O=Al(OH)3+NaHCO3.过滤,灼烧Al(OH)32Al(OH)3=Al2O3+3H2O.注释:电解时为使氧化铝融熔温度减低,在其中添加冰晶石电解:2Al2O3=4Al+3O2。
它有四种同素异构体β-氧化铝δ-氧化铝γ-氧化铝α-氧化铝,主要有α型和γ型两种变体,α型氧化铝熔点、沸点很高,不溶于水和酸,工业上也称铝氧,是制金属铝的基本原料;也用于制各种耐火砖、耐火坩埚、耐火管、耐高温实验仪器;还可作研磨剂、阻燃剂、填充料等;高纯的α型氧化铝还是生产人造刚玉、人造红宝石和蓝宝石的原料;还用于生产现代大规模集成电路的板基.γ型氧化铝是氢氧化铝在140-150℃的低温环境下脱水制得,工业上也叫活性氧化铝、铝胶.γ型氧化铝不溶于水,能溶于强酸或强碱溶液,将它加热至1200℃就全部转化为α型氧化铝.γ型氧化铝活性高吸附能力强,耐压性好.在石油炼制和石油化工中是常用的吸附剂、催化剂和催化剂载体;在工业上是变压器油、透平油的脱酸剂,还用于色层分析;在实验室是中性强干燥剂,其干燥能力不亚于五氧化二磷,使用后在175℃以下加热6-8h还能再生重复使用.我们所熟知的纯净的金属铝与空气中的氧气所生成的一层致密的氧化铝薄膜便是α型氧化铝。
我们所熟知的红宝石、蓝宝石的主成份也为氧化铝,但因为其它杂质而呈现不同的色泽。


展开编辑本段概要管制信息本品不受管制名称中文名称:铝氧,三氧化二铝英文别名:Aluminum oxide化学式Al2O3相对分子质量101.96性状白色结晶性粉末。
无臭。
无味。
质极硬。
易吸潮而不潮解。
溶于浓硫酸,缓慢溶于碱液中形成氢氧化物,几乎不溶于水及非极性有机溶剂。
相对密度(d204)4.0。
熔点约2000℃。
储存密封干燥保存。
SCRC100009用途用作分析试剂。
有机溶剂的脱水。
吸附剂。
有机反应催化剂。
研磨剂。
抛光剂。
质检信息质检项目指标值水中溶解物,% ≤0.5硅酸盐(SiO3) 合格碱金属及碱士金属,% ≤0.50重金属(以Pb计),% ≤0.005氯化物(Cl),% ≤0.01硫酸盐(SO4),% ≤0.05灼烧失量,% ≤5.0铁(Fe),% ≤0.01编辑本段物理性质式量 101.96 amu熔点 2303 K沸点 3250 K真密度 3.97 g/cm3松装密度:0.85g/mL(325目~0)0.9g/mL(120目~325目)晶体结构三方晶系 (hex)导电性常温状态下不导电热化学属性ΔfH0liquid ?1620.57 kJ/molΔfH0solid ?1675.69 kJ/molS0liquid, 1 bar 67.24 J/mol·KS0solid 50.9 J/mol·K编辑本段安全性食入低危险吸入可能造成刺激或肺部伤害皮肤低危险眼睛低危险在没有特别注明的情况下,使用SI单位和标准气温和气压。
氧化铝是铝和氧的化合物,分子式为Al2O3。
在矿业、制陶业和材料科学上又被称为矾土。
编辑本段应急处理隔离泄漏污染区,限制出入。
建议应急处理人员戴防尘面具(全面罩),穿防毒服。
避免扬尘,小心扫起,置于袋中转移至安全场所。
若大量泄漏,用塑料布、帆布覆盖。
收集回收或运至废物处理场所处置。
编辑本段中国工业概况我国具有较丰富的铝土矿资源,迄今已探明保守储量23亿吨,位居世界第4,具备发展氧化铝工业的资源条件。

氧化铝的基本概念及相关知识Alumina(氧化铝)一词可能来源于Alumen(明矾)而明矾一词最早的文字记载出现在公元前五世纪。
纯氧化铝是1746年J.H.波特(Pott)首先从明矾中提取出来的。
1786年L.B.莫维约(De Morveau)认为明矾的主要成份是Alumina(矾土),约到1820年英国才将Alum译成Alumina,格来维尔(Grevule)于1799年提出的一种矿物中含有AL2O3成分,称这种矿物为“刚玉”刚玉又称为(α-AL2O3)是唯一一种纯氧化铝天然矿物。
1858年苏打-铝土矿烧结法由(法国)路易.勒萨斯提出,1902年帕卡尔提出了生料配比,使其完善,1868~1892年奥地利化学家K.J.拜耳发明了生产氧化铝的拜耳法,用它处理高品位铝土矿。
每生产一吨金属铝消耗近两吨氧化铝(1.91~1.92吨)我厂2002年1.939吨。
我国于1950年开始建设山东铝厂,用碱――石灰烧结法生产氧化铝,该厂于1954年7月1日投产,从此拉开了我国氧化铝工业生产的序幕,继山东铝厂之后,郑州铝厂于1965年、贵州铝厂1978年、山西铝厂1987年,中州铝厂1993年、平果铝厂1995年相继投产。
1、氧化铝的物理化学性质及主要用途氧化铝是一种白色的结晶体,不溶于水,但可溶于酸和碱溶液,它的碱性和酸性都很弱,是一种典型的两性化学物。
氧化铝主要是供电解炼铝用,(90%以上),但是电子、石油、化工、耐火材料、陶瓷、塑料、纺织、磨料、造纸以及制药等许多部门也需要各种特殊性能的氧化铝和氢氧化铝。
并且国内外不少氧化铝厂都重视发展多品种氧化铝生产,例如活性氧化铝、低钠氧化铝、喷涂氧化铝、γ-AL2O3、超α-AL2O3、高纯氧化铝和氢氧化铝,拟薄水铝石以及铝胶等,这些非冶金级的多品种氧化铝占整个氧化铝产量的8~10%左右,品种在200种以上。
2、氧化铝的生产方法分类及细分氧化铝生产方法分为碱法、酸法、酸碱联合法、热法,其中碱法中包括拜耳法、烧结法、拜-烧联合法1、串联法、2、并联法、3、混联法。

(完整版)氧化铝msds(完整版)氧化铝MSDS1. 产品标识- 产品名称:氧化铝- 英文名称:Aluminum Oxide- CAS号:1344-28-12. 成分/组分信息- 化学名称:氧化铝- 化学式:Al2O3- 分子量:101.96 g/mol- 外观:白色结晶粉末- 熔点:2,072°C- 沸点:不适用3. 危险性识别- 健康危害:经皮肤接触可引起轻度刺激,吸入粉尘可引起呼吸道刺激。
- 环境危害:对环境无明显危害。
- 火灾危险:不易燃,但在高温下与可燃物接触可引起燃烧。
- 爆炸危险:在堆积过密、受潮等情况下可能发生剧烈爆炸。
- 急救措施:接触皮肤后,用大量流动清水冲洗至少15分钟。
如有不适,就医治疗。
4. 安全措施- 防护措施:- 呼吸系统防护:操作时应佩戴防尘口罩。
- 眼睛防护:操作时应佩戴防护眼镜或护目镜。
- 体触防护:穿戴适当的防护服,避免长时间接触。
- 其他防护措施:操作结束后及时洗手,更换干净的工作衣服。
- 储存要求:- 仓储条件:存放在干燥、通风良好的库房中,避免阳光直射。
- 储存注意事项:避免与酸性物质接触,防止受潮。
- 应急处理:- 泄露处置:密封,转移至专用集装器,以防止进一步泄露。
- 泄露清理:用堤坝材料围堵,收集到溢出的物质并将其转移到安全中。
5. 食品接触说明- 不适用于食品接触。
6. 运输信息- 联合国编号:UN3077- 包装类别:III- 危险等级:9- 运输注意事项:按照货物类别和数量选择合适的运输工具及包装。
7. 法规信息- 化学品货物安全技术说明书(MSDS)的编制依据:GB/T -2008- 特别注意事项:需遵守当地法规法规的要求,注意个人防护和环境保护。
8. 体检生物学效应- 毒性状况:低毒。
- 慢性毒性:长期接触可引起呼吸道不适,可导致哮喘等呼吸系统疾病。
9. 稳定性和反应活性- 稳定性:稳定。
- 危险性反应:与酸性物质接触可能产生有害气体。

氧化铝标准溶液-概述说明以及解释1.引言1.1 概述氧化铝标准溶液是一种被广泛应用于科学研究和工业生产中的重要实验试剂。
该溶液是由纯净的氧化铝粉末和溶剂按一定比例配制而成的稳定溶液。
氧化铝标准溶液具有高纯度、稳定性好、可重复性高等特点,因此被广泛用于各个领域的分析和实验中。
通过精确地调整溶液中氧化铝的浓度,可以满足不同实验或分析的要求。
在化学分析领域,氧化铝标准溶液常被用作溶液标定的参考物质。
由于氧化铝的成分和性质稳定,可以通过对溶液中氧化铝浓度的准确测量,来验证和校正实验过程中的测量误差,从而提高实验结果的准确性和可靠性。
此外,由于氧化铝本身具有较高的抗腐蚀性和热稳定性,氧化铝标准溶液还常被用于材料表面处理、陶瓷材料生产等工业领域中。
总之,氧化铝标准溶液作为一种重要的实验试剂,不仅在科学研究中发挥了关键作用,还在工业生产中具有重要的应用价值。
在未来的研究中,进一步探索氧化铝标准溶液的制备方法、性质调控和应用场景的拓展,将有助于更好地满足科学研究和工业生产的需求。
提高氧化铝标准溶液的稳定性和可重复性,将为相关领域的研究和实验提供更准确、可靠的基准。
1.2 文章结构文章结构部分的内容应该是对整篇文章的结构进行介绍和概括。
以下是一种可能的写作方式:在本文中,将对氧化铝标准溶液进行全面的介绍和分析。
文章将按照以下结构展开:引言部分将首先给出对氧化铝标准溶液的概述,介绍其基本概念和重要性。
接着,会介绍文章的结构,即本文将包含正文部分和结论部分。
最后,会明确本文的目的,即通过深入分析氧化铝标准溶液的制备方法、性质与特点以及应用领域,揭示其在实际应用中的重要性,并为未来研究方向提供展望。
正文部分将包括两个主要内容:首先,将详细介绍氧化铝标准溶液的制备方法,包括常用的制备工艺和具体步骤。
其次,将深入分析氧化铝标准溶液的性质与特点,包括化学性质、物理性质以及其他相关特性的研究成果。
结论部分将对全文进行总结,并强调氧化铝标准溶液在实际应用中的重要性。
氧化铝分类
氧化铝可以根据其粒径、晶型和用途进行分类。
根据粒径,氧化铝可分为三种类型:
1. 细粉:粒径小于10微米的氧化铝,常用于涂料、油漆、塑料等领域。
2. 中等粉:粒径在10-50微米之间的氧化铝,常用于陶瓷、橡胶、磨料等领域。
3. 粗粉:粒径大于50微米的氧化铝,常用于铝制品的生产、耐火材料等领域。
根据晶型,氧化铝可分为以下几种:
1. α-Al2O3:也称为α氧化铝,具有高结晶度和高热稳定性,广泛应用于陶瓷、磨料和耐火材料等领域。
2. γ-Al2O3:也称为γ氧化铝,具有较高的比表面积和孔隙度,常用于催化剂和吸附剂等领域。
3. δ-Al2O3:也称为δ氧化铝,具有较低的比表面积和孔隙度,常用于填充剂和增塑剂等领域。
根据用途,氧化铝可分为:
1. 工业级氧化铝:主要用于陶瓷、磨料、耐火材料、催化剂等工业领域。
2. 医疗级氧化铝:经过特殊处理和纯化的氧化铝,用于医疗领域,如牙科材料和人工关节等。
3. 食品级氧化铝:经过特殊处理和纯化的氧化铝,符合食品
卫生标准,常用于食品添加剂中,如稳定剂、酸度调节剂等。
以上是对氧化铝分类的简单介绍,如果需要更详细的信息,请告诉我具体的需求。
氧化铝化学结构-概述说明以及解释1.引言1.1 概述:氧化铝(Aluminum Oxide,简称Alumina)是一种重要的无机化合物,具有广泛的应用和重要的化学性质。
作为一种重要的陶瓷材料,氧化铝在工业和科学领域中起着至关重要的作用。
本文将对氧化铝的化学性质、晶体结构及在工业上的应用进行深入探讨。
通过对氧化铝的综合了解,可以更好地认识和理解这一化合物在材料科学和工业生产中的重要性和潜力。
1.2 文章结构文章结构部分的内容:本文将分为引言、正文和结论三部分。
在引言部分,我们将概述氧化铝的化学结构,并介绍本文的目的和结构。
在正文部分,我们将重点讨论氧化铝的化学性质、晶体结构以及在工业上的应用。
最后,在结论部分,我们将总结氧化铝在工业和科学研究中的重要性,并展望氧化铝在未来的发展前景。
部分的内容文章1.3 目的部分的内容:本文旨在深入探讨氧化铝的化学结构及其相关性质,以及其在工业上的应用。
通过对氧化铝的化学性质及晶体结构的介绍,读者能够更好地了解氧化铝在材料科学中的重要性和广泛应用。
同时,通过对氧化铝在工业上的应用领域进行分析,可以更好地了解氧化铝在现代工业生产中的重要作用。
最后,通过总结氧化铝的重要性,并展望其在未来的发展趋势,可以为读者提供对氧化铝相关领域的全面认识和理解。
因此,本文的目的在于全面介绍氧化铝的化学结构及其应用,以期为读者提供有益的信息和知识。
2.正文2.1 氧化铝的化学性质氧化铝是一种无机化合物,化学式为Al2O3,在化学性质上表现出一些重要特点。
首先,氧化铝具有很高的化学稳定性,能够抵抗大部分酸碱腐蚀,这使得它成为一种重要的耐火材料。
其次,氧化铝在高温下能够与金属发生还原反应,从而被用于冶金工业中。
此外,氧化铝还具有很强的吸附性,可以用于吸附水和有机物质。
在工业上,氧化铝通常被用作催化剂、填料和吸附剂等。
另外,由于氧化铝具有良好的电绝缘性能和耐高温性,因此在电子工业和航天航空等领域也有广泛的应用。
氧化铝行业现状一、氧化铝行业概况(一)氧化铝简介氧化铝是由铝土矿经过加工后的一种工业原料,90%主要用于电解铝的生产。
通常每2吨左右铝土矿可以生产出1吨氧化铝,约2吨左右氧化铝可以生产出1吨电解铝。
氧化铝的生产方法主要有酸法和碱法,酸法有盐酸法、硫酸法、硝酸法,由于酸法存在耐酸设备造价昂贵、铝盐溶液除铁困难、溶解单位质量AL2O3需要大量酸、多数酸具有挥发性污染环境、产品物理性质难以达到电解制铝的要求等原因,导致酸法没有得到广泛应用。
碱法有拜耳法、烧结法和联合法。
世界上90%以上氧化铝都是由拜耳法生产的,拜耳法适用于处理品味比较高的铝土矿;烧结法主要用来处理品位低的含硅高的一水硬铝石矿,也可以烧结赤泥;联合法是对于A/S为4-7的铝土矿,采用拜耳法和烧结法联合处理,取长补短,可得到比单纯的拜耳法或烧结法更好的经济效果。
而联合法需要在拜耳法生产的基础上配套烧结法的设备,前期投资较大,所以没有得到广泛应用。
(二)行业产业链铝工业广泛采取的产业链是,铝土矿-氧化铝-电解铝-铝加工材(合金)-各种铝产品的终端消费品。
生产1吨氧化铝将消耗2吨铝土矿、0.3~1.6吨石灰石、1.5吨煤炭、25公斤碱、2~7吨新鲜水,而生产1吨原铝将消耗2吨氧化铝、22~25公斤氟化盐、12-14MWh电力、碳素阳极(毛耗,由石油焦和煤沥青制成)500~550公斤。
每生产1吨氧化铝,产生0.9~1.7吨赤泥。
铝制品主要用于建筑行业(如建筑铝型材)、交通运输、电力行业(主要是电力电缆和变压器)、耐用消费(家用五金如铝锅,灯具)、包装等行业(铝箔)。
铝行业产业链二、我国铝行业政策国家发改委根据国家有关法律法规和产业政策,制定铝行业准入条件如下:(一)企业规模新建铝土矿开采项目总投资5亿元及以上的由国务院投资主管部门核准,其他矿山开发项目由省级政府投资主管部门核准。
申请核准的矿山投资项目,总生产建设规模不得低于30万吨/年,服务年限为15年以上。
氧化铝的生产原理和方法氧化铝(Al2O3)是一种重要的无机化合物,广泛应用于冶金、建材、化工、电子等众多领域。
其生产原理和方法有以下几种。
1.工业熔融法工业熔融法是最常用的氧化铝生产方法之一、其流程包括氧化铝的原料准备、炉料的装载、熔炼和冷却过程。
首先,将氧化铝的原料(例如铝土矿)经过破碎、磨细等处理,得到适当粒度的矿石粉末。
然后,将矿石粉末与适量的草酸溶液混合,形成湿糊状的矿浆。
此时,矿浆中的铝沉降到底部,与草酸反应生成沉淀物。
接下来,将沉淀物进行过滤、洗涤和干燥,得到氢氧化铝粉末。
最后,将氢氧化铝粉末装入电阻炉中,进行高温熔炼。
熔炼过程中,氢氧化铝分解为氧化铝和水蒸气。
氧化铝蒸发,通过冷却设备冷凝后收集,得到氧化铝产品。
2.氧化铝的溶胶-凝胶法溶胶-凝胶法是一种常用于制备高纯度氧化铝粉体的方法。
该方法的流程包括溶解、凝胶化、热解和焙烧等步骤。
首先,将铝盐(如硝酸铝)加入溶剂(如水),形成溶胶。
通过加热、搅拌等操作,使溶剂中的铝盐完全溶解。
然后,将溶胶放置一段时间,使其逐渐转化为凝胶。
凝胶形成的过程中,溶胶中的铝离子逐渐聚集形成固体颗粒。
接下来,将凝胶进行热解,即将凝胶中的溶剂蒸发掉,得到凝胶固体。
最后,将凝胶固体进行焙烧,即加热到一定温度下进行处理。
焙烧可以进一步提高氧化铝的结晶度和纯度,得到高质量的氧化铝颗粒。
3.硅铝材料的水热法水热法是一种制备氧化铝的新兴方法,主要通过水热反应在硅铝材料上形成氧化铝颗粒。
首先,将硅铝材料(如硅铝合成凝胶)与适量的氢氧化钠溶液混合,并添加少量的有机物催化剂。
然后,将混合物加入反应釜中,在高温高压的条件下进行水热反应。
在水热过程中,硅铝材料逐渐转化为氧化铝颗粒。
最后,将反应产物进行过滤、洗涤和干燥,得到氧化铝产品。
此方法制备的氧化铝具有良好的分散性和高比表面积,适用于一些特殊领域的应用。
综上所述,氧化铝的生产原理和方法包括工业熔融法、溶胶-凝胶法和硅铝材料的水热法等多种途径。
氧化铝的化合价氧化铝是一种具有重要用途的化学物质,它的化合价有多种不同类型。
1、2价氧化铝:二价氧化铝包含一个氧原子和两个氧化铝的离子,其化合价为Al2O3,即氧化铝的基本形式,即氧化铝(II)酸盐。
2、3价氧化铝:三价氧化铝包含三个氧化铝的离子,它的化合价为Al3O3,也称为氧化铝(III)离子,即氧化铝(III)氰酸盐。
3、4价氧化铝:四价氧化铝包含四个氧原子和四个氧化铝的离子,其化合价为Al4O4,即氧化铝(IV)离子,即氧化铝(IV)羧酸盐。
4、5价氧化铝:五价氧化铝包含五个氧原子和五个氧化铝的离子,其化合价为Al5O5,也称为铝氧合物(V),即氧化铝(V)羧基盐。
5、6价氧化铝:六价氧化铝包含六个氧原子和六个氧化铝的离子,它的化合价为Al6O6,也称为铝离子(VI),即氧化铝(VI)羟基盐。
除此之外,氧化铝还有其他不同在配体数目,以及它们组成氧化铝化合物的配体结构不同而存在不同类型的化合价。
这些不同类型的配体结构分别来自:水合酸,盐基酸,还原性酸,羧化酸,酯化酸,碱酸,醛酸以及羧酸。
例如,氧化铝的水合酸形式,如铝氢氧化酸、硫酸铝、氢氧化铝等,的化合价分别为Al(H2O)3^3+,AlSO4^3-和Al(OH)3^3-。
硫酸铝的化合价是一种维吉石晶体,它的组成离子形式为Al3+和SO4^2-。
此外,另一中常见的氧化铝配体是氧化铝钠,它的化合价为AlNaO2-,以及氧化铝铬,其化合价为AlCrO2-。
总之,氧化铝是一种具有活跃的化学用途的化学物质,它的化合价有多种不同类型,从2-6价不等,根据它们的结构不同,可分为水合酸,盐基酸,还原性酸,羧化酸,酯化酸,碱酸,醛酸以及羧酸等。
尽管有不同的形式,但它们的共同点在于,都具有显著的活性特性和多种良好的用途。
氧化铝力学参数氧化铝是一种重要的无机材料,具有广泛的应用领域,包括陶瓷、电子材料、催化剂、磨料等。
其力学参数是指描述氧化铝材料力学性能的物理量,包括弹性模量、屈服强度、抗拉强度、断裂韧性等参数。
本文将对氧化铝的力学参数进行详细介绍。
1. 弹性模量弹性模量是衡量材料在受力作用下产生弹性形变的能力的物理量,通常用符号E表示。
对于氧化铝而言,其弹性模量在常温下大约为380-400 GPa。
这意味着氧化铝在受力作用下可以产生较小的弹性形变,具有较好的抗拉伸性和抗压缩性。
2. 屈服强度屈服强度是材料在受力作用下开始产生塑性变形的临界点。
对于氧化铝而言,其屈服强度在常温下通常在200-300 MPa左右。
这说明在这个应力范围内,氧化铝会开始产生可逆的塑性变形,从而形成永久变形。
3. 抗拉强度抗拉强度是材料在拉伸状态下抵抗破坏的能力。
对于氧化铝而言,其抗拉强度通常在300-400 MPa之间。
这意味着氧化铝具有较高的抗拉破坏能力,适用于承受拉应力的工程应用。
4. 断裂韧性断裂韧性是材料抗裂纹扩展和抵抗断裂的能力。
对于氧化铝而言,其断裂韧性较高,通常在3-4 MPa·m^0.5左右。
这说明氧化铝在受到冲击或者弯曲载荷时,具有较好的抗断裂性能。
氧化铝作为一种重要的无机材料,具有良好的力学性能,诸如较高的弹性模量、适当的屈服强度、较高的抗拉强度和断裂韧性,这些性能使其在各个领域有着广泛的应用前景。
希望本文能够对氧化铝力学参数有所了解,并对相关领域的科研工作者和工程技术人员有所帮助。