非经典碳正离子简介
- 格式:ppt
- 大小:54.00 KB
- 文档页数:1

有机化学基本理论主讲人:史达清4. 碳正离子与碳负离子碳正离子、碳负离子是有机化学中非常重要的两类活性中间体,我们有必要掌握这两类活性中间体的结构、生成方法及影响稳定性的因素。
(1)碳正离子碳正离子是指碳原子带有正电荷的三价化合物,对碳正离子的研究是最早且最深入的,被称为物理有机化学的基础,许多有机反应历程的研究概念和方法都起始于碳正离子的研究工作。
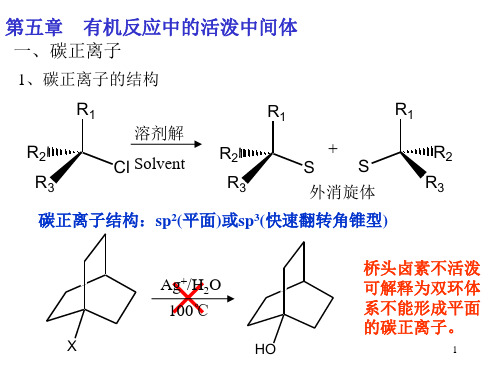
(a)碳正离子的结构碳正离子的中心碳原子是sp2 杂化的平面型结构,正电荷在p 轨道中:例外:下面的几个实例是例外,这是由于它们都不能形成空的p 轨道形式,如乙烯正离子,乙炔正离子是线型结构,有一个空的sp 杂化轨道,苯基正离子C6H5+则有一个空的sp2杂化轨道,但它们都很难生成,因为空轨道与π 体系相互垂直,正电荷得不到分散。
(b)碳正离子的生成方法离解是形成碳正离子的一个主要方法,离解时,与碳原子相连的基团带着一对对子离去。
苯磺酸根离子和卤离子是常用的较好的离去基团。
卤代物中的卤离子还可以在Ag+ 或Lewis 酸存在下脱去而生成碳正离子。
例如:醇一般是在酸作用下,将不容易离去的羟基转变成易离去的水离去,可以形成碳正离子:伯胺一般先用亚硝酸重氮化得到重氮盐,再脱氮得到碳正离子:如果生成的碳正离子具有芳香性,那么这些碳正离子就比较容易生成。
例如:另一类产生碳正离子的方法是质子或其它带正电荷的原子团或Lewis 酸对不饱和体系的加成。
例如:(c)碳正离子的稳定性凡是能够使碳正离子的正电荷得到分散的,则碳正离子比较稳定;相反,如果使碳正离子的正电荷集中,则碳正离子更不稳定。
其影响因素主要有:(i) 诱导效应给电子的诱导效应(+I)使碳正离子稳定;而吸引电子的诱导效应(-I),使碳正离子不稳定。
例如:(ii) 共轭效应给电子的共轭效应(+C)使碳正离子稳定;而吸电子的共轭效应(-C)使碳正离子不稳定。
例如:(iii) 空间效应由于碳正离子是平面型结构,如果正电荷在桥头碳原子上,由于桥的刚性结构,难以形成平面型,所以该碳正离子的稳定性比较差,例如:1-氯双环[2.2.1]庚烷的乙醇解速度比叔丁基氯慢1013倍。

碳正离子综述碳正离子是一种带正电的极不稳定的碳氢化合物。
分析这种物质对发现能廉价制造几十种当代必需的化工产品是至关重要的。
欧拉教授发现了利用超强酸使碳正离子保持稳定的方法,能够配制高浓度的碳正离子和仔细研究它。
他的发现已用于提高炼油的效率、生产无铅汽油和研制新药物。
碳正离子与自由基一样,是一个活波的中间体。
碳正离子有一个正电荷,最外层有6个电子。
带正电荷的碳原子以SP2杂化轨道与3个原子(或原子团)结合,形成3个σ键,与碳原子处于同一个平面。
碳原子剩余的P 轨道与这个平面垂直。
碳正离子是平面结构。
1963年有报道,直接观察到简单的碳正离子,证明了它的平面结构,为它的存在及其结构提供了实验依据。
根据带正电荷的碳原子的位置,可分为一级碳正离子,二级碳正离子和三级碳正离子。
碳正离子的结构与稳定性直接受到与之相连接的基团的影响。
它们稳定性的一般规律如下:(1)苄基型或烯丙型一般较稳定;(2)其它碳正离子是:3°>2°>1°;碳正离子越稳定,能量越低,形成越容易,加成速度也越快,可见碳正离子的稳定性决定烯烃加成的取向。
碳正离子根据结构特点不同可分为:经典碳正离子和非经典碳正离子下面着重讨论经典碳正离子:碳正离子化学是有机化学非常重要的组成部分,Olah由于发现在超强酸中稳定存在的碳正离子,获得了1994年的诺贝尔化学奖。
碳正离子是带有正电荷的含碳离子,是一类重要的活性中间体,可用R3C+表示(R为烷基)。
碳正离子及其反应于20世纪20年代由C.K.英戈尔德等提出的。
碳正离子可以认为是通过共价C-C单键中一对电子的异裂反应而产生,式中X为卤素。
R3C:X →R3C++X-所形成的碳正离子R3C+,一个正电荷,配位数为3,中心原子以三个sp2杂化轨道和三个原子成键,三个键轴构成平面,空着的p轨道垂直于平面,正电荷集中在p 轨道上。
取代基R 的共轭效应,诱导效应和立体效应,以及烷基的超共轭效应都能对碳正离子其稳定作用。


非经典碳正离子简介樊宇成;孙泽昊;张睿;张一航;朱家祺【摘要】非经典碳正离子作为一种特殊的反应中间体,具有重要的理论和实际研究的意义.本文以碳正离子理论的发展为主线,以历史上非经典碳正离子(特别是降冰片基正离子)之争为中心,简要综述了Winstein、Brown和Olah三人的观点,并结合最新进展进行评述.此外,还对除降冰片基正离子之外的非经典碳正离子进行了适当的讨论.【期刊名称】《大学化学》【年(卷),期】2017(032)009【总页数】13页(P66-78)【关键词】非经典碳正离子;降冰片基正离子;理论发展历史【作者】樊宇成;孙泽昊;张睿;张一航;朱家祺【作者单位】北京大学化学与分子工程学院,北京100871;北京大学化学与分子工程学院,北京100871;北京大学化学与分子工程学院,北京100871;北京大学化学与分子工程学院,北京100871;北京大学化学与分子工程学院,北京100871【正文语种】中文【中图分类】G64;O6碳正离子是有机化学理论的重要组成部分。
1901年,Norris[1]与Kehrmann、Wentzel[2]各自独立地发现将三苯甲醇与浓硫酸混合可得深黄色产物;1922年,Meerwein和van Emster[3]第一次将碳正离子认为是反应的活性中间体;1939年,Wilson等[4]提出了非经典碳正离子的概念。
之后,碳正离子理论不断发展完善,却也引发了不少争论。
尤其是围绕非经典碳正离子这一问题,几十年来一直争论不断。
最终,在争论推动下的广泛研究工作终于将非经典碳正离子从一个猜想变为广为接受的完备理论。
本文就其中的争论与理论发展作一些简要介绍。
1899年,Wagner等[5]在研究萜类化合物时发现,冰片1在质量分数为50%的硫酸作用下脱水会经历碳架重排生成莰烯2,而并非生成直接消除产物冰片烯3。
虽然在当时无法对该反应做出任何解释,但Wagner将该反应与甲基叔丁基甲醇4在酸性条件下脱水重排得到四甲基乙烯5的反应进行类比(图1),认为二者在某种程度上具有一定的相似性。

非经典碳正离子简介非经典碳正离子是一种碳正离子,它们不包含传统的正三角形碳原子骨架,而是由六个中心碳原子和若干氢、氧或其他外来原子组成的环或类环结构组成。
它们不仅具有碳正离子特有的特性,而且还具有独特的新功能。
由于它们具有独特的化学活性和热力学性质,因此被广泛用作高分子化学的重要原料,以及药物的靶向和可视化药物,甚至是氢能源的催化剂。
非经典碳正离子相比传统的碳正离子,其结构更加复杂,因此具有更高的反应活性,能够改变环境中物质的结构和功能。
它们可以用来合成各种复杂的有机物质,例如有机硅烷、芳烃类酸酯、烷酸酯等,也可以用来制备纳米材料、生物反应器和修饰剂等。
此外,非经典碳正离子还可以用来催化一些烯烃和炔烃的反应,改善有机物的催化效率,以及对不同的化合物进行分离等。
同时,由于非经典碳正离子的结构是动态的,因此可以更有效地利用外来物质,从而改善材料及抗微生物性能。
由此可见,非经典碳正离子在化学领域已经发挥着重要的作用,其在未来的发展也将更加迅速和广泛。
非经典碳正离子也可以应用于构建自组装结构,利用动态的非经典碳正离子衬底,可以让金属簇和酶活性体由溶液状态自发移植到表面,从而构建有机/无机杂化材料。
此外,还可以应用于构建多孔材料,可以在液体环境中实现有机/无机杂化材料的分子尺度合成,从而构建具有高比表面积和多种功能的多孔材料。
此外,非经典碳正离子还可以用于构建光催化剂和能量转换材料,如光催化活性水处理剂、太阳能电池材料、储能材料等。
总之,非经典碳正离子作为一种具有新型功能的碳正离子,其应用前景非常广阔。
它们在高分子材料、有机/无机杂化材料、光催化剂、能量转换材料和药物靶向及可视化药物等领域都具有很大的发展潜力。
它们将给无数领域带来新的技术和新的创新,为人类社会建设做出重要贡献。
非经典碳正离子也应用于生物系统,由于其独特的结构,可以增强生物分子的特性,例如可以增强药物的靶向性和活性,从而提高药物的疗效。
此外,非经典碳正离子还可以应用于生物传感器,利用它们可以对生物体进行快速检测,可以实时监测药物的吸收、代谢和排泄情况,从而更好地控制药物的使用效果。