燃烧的条件(实验)
- 格式:doc
- 大小:43.00 KB
- 文档页数:11

“燃烧的条件”实验的另类设计燃烧是一种化学反应,当一种物质与氧气发生反应时,产生了能量、二氧化碳和水蒸气。
按照常规实验设计,我们通常使用蜡烛、纸张或者木棍进行燃烧实验。
为了增加趣味性和吸引学生的兴趣,我们可以设计一些另类的燃烧实验。
下面将介绍两个另类实验设计。
第一个实验设计是“燃烧的条件与花火的关系”。
在这个实验中,我们将探究不同条件下的燃烧情况,并与花火的原理进行对比。
实验设备和材料:1. 长长的竹子(可以是竹竿或竹条)2. 果汁盒子3. 盐和糖4. 火柴或打火机5. 火箭糖(代表花火)实验步骤:1. 将竹子固定在果汁盒子上,使其竖直放置。
2. 将竹子切成不同长度的小段,分别为A、B、C、D。
3. 在A段竹子上撒上盐粉,B段竹子上撒上糖粉,C段竹子上撒上盐和糖的混合粉末,D段不撒任何粉末。
4. 用火柴或打火机点燃各段竹子的顶端。
5. 观察不同条件下的燃烧情况。
预期结果:A段竹子燃烧时可能会发出噼啪声,燃烧比较旺盛,类似花火爆炸声。
B段竹子燃烧时可能会发出噗噗声,燃烧比较缓慢,产生比较多的黑烟。
C段竹子燃烧时可能会产生彩虹色的火焰。
D段竹子燃烧时与常规情况下的燃烧没有明显差异。
实验原理:A段竹子上的盐使燃烧条件更加充分,燃烧速度更快,产生更多能量,类似于花火爆炸的效果。
B段竹子上的糖使燃烧速度减慢,产生更多的黑烟。
C段竹子上的盐和糖的混合物使燃烧温度升高,发出彩虹色的火焰。
D段竹子作为对照组,用于比较其他条件下的燃烧情况。
实验设备和材料:1. 铁丝网2. 纸张3. 木棍4. 火柴或打火机实验步骤:1. 将铁丝网固定在一个台子上,使其竖直放置。
2. 在铁丝网上平铺一张纸张,并将纸张的上方固定在一个木棍上,使纸张与铁丝网保持一定的距离。
3. 在纸张下方平铺另一张纸张,并用火柴或打火机点燃纸张的下方。
4. 同时点燃纸张下方的火焰和纸张上方的纸张,观察燃烧情况。
5. 将纸张移除,换成木棍,并重复步骤4。

初中化学燃烧的条件实验
初中化学燃烧的条件实验可以通过以下步骤进行:
1. 准备实验材料:取适量MnO2于广口瓶,用注射器取5ml双氧水,连接好制氧装置。
2. 设定实验组:取带气球的具支试管倒入适量热水,再取一小块绿豆粒般大小的白磷放入具支试管中,放入大烧杯左边。
3. 设定对照组:另取一支干燥试管放入一小块绿豆粒般大小的红磷,塞上带气球橡皮塞,放入大烧杯右边,观察记录实验现象。
4. 实验操作:将制氧装置和具支试管连接,缓缓推动注射器活塞通入氧气,观察记录实验现象。
5. 实验现象分析:干燥试管中白磷燃烧红磷不燃烧,说明燃烧需达到可燃物着火点。
具支试管里热水中白磷不燃烧,通氧气后燃烧,说明燃烧需要氧气(或空气)。
通过以上步骤,可以清晰地观察到燃烧的条件,增强对燃烧条件的理解。
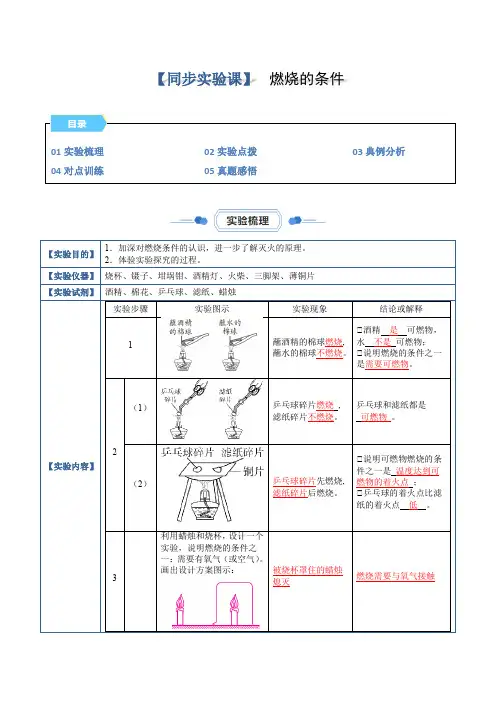
【同步实验课】 燃烧的条件【实验目的】1.加深对燃烧条件的认识,进一步了解灭火的原理。
2.体验实验探究的过程。
【实验仪器】 烧杯、镊子、坩埚钳、酒精灯、火柴、三脚架、薄铜片 【实验试剂】 酒精、棉花、乒乓球、滤纸、蜡烛【实验内容】实验步骤实验图示实验现象结论或解释1蘸酒精的棉球燃烧, 蘸水的棉球不燃烧。
①酒精 是 可燃物,水 不是 可燃物; ①说明燃烧的条件之一是需要可燃物。
2(1)乒乓球碎片燃烧 , 滤纸碎片不燃烧。
乒乓球和滤纸都是可燃物 。
(2)乒乓球碎片先燃烧, 滤纸碎片后燃烧。
①说明可燃物燃烧的条件之一是 温度达到可燃物的着火点 ;①乒乓球的着火点比滤纸的着火点 低 。
3利用蜡烛和烧杯,设计一个实验,说明燃烧的条件之一:需要有氧气(或空气)。
画出设计方案图示:被烧杯罩住的蜡烛熄灭燃烧需要与氧气接触01实验梳理 02实验点拨 03典例分析 04对点训练 05真题感悟1. 物质燃烧的条件物质燃烧一般需要同时满足三个条件:(1)物质具有可燃性。
(2)可燃物与氧气接触。
(3)可燃物达到燃烧所需要的最低温度。
2. 着火点某种可燃物燃烧所需要的最低温度,称为该物质的着火点。
【注意】(1)物质燃烧一般需要三个条件同时满足,缺少其中任何一个,燃烧就不能发生。
(2)不同物质着火点一般不同,着火点是物质本身的固有属性,一般不随外界条件的变化而变化。
3. 灭火的原理和方法(1)满足清除可燃物、隔绝空气(或氧气)、降低温度到可燃物的着火点以下三种方法中的任何一种,就能达到灭火的目的。
(2)使用冷却剂是为了降低可燃物的温度,而不是降低可燃物的着火点。
(3)电器设备或电线着火,应先切断电源,再用干粉或液态二氧化碳灭火器灭火,不可用水直接灭火。
(4)油、酒精着火时不能用水灭火,否则易引起火势蔓延。
【典例01】用如图所示装置探究燃烧的条件。
下列说法正确的是()A.铜片上的白磷不燃烧,红磷燃烧B.向热水中的白磷通氧气,白磷会燃烧C.热水的作用只是提供热量D.该实验只能得出燃烧需要氧气这一结论【答案】B【详解】A、铜片上的白磷:与氧气接触,且温度达到着火点,具备燃烧的三个条件燃烧;铜片上的红磷:与氧气接触,但温度没有达到着火点,不同时具备燃烧的三个条件不燃烧,说法不正确;B、热水中的白磷:温度达到着火点,但不能与氧气接触,不能燃烧,向水中通氧气,燃烧的三个条件同时具备,白磷会燃烧,说法正确;C、热水的作用除了提供热量,还起到隔绝氧气的作用,说法不正确;D、该实验中:铜片上的白磷燃烧,红磷不燃烧,可以得出燃烧需要温度达到着火点;铜片上白磷燃烧,热水中的白磷不燃烧,可以得出燃烧需要氧气,说法不正确。


第1篇一、实验目的1. 探究燃烧的条件。
2. 验证可燃物、助燃物和点火温度对燃烧的影响。
二、实验原理燃烧是一种化学反应,通常需要三个条件:可燃物、助燃物和点火温度。
本实验通过控制变量法,分别探究这三个条件对燃烧的影响。
三、实验材料1. 可燃物:酒精、纸张、棉花等。
2. 助燃物:氧气、空气等。
3. 点火温度:打火机、酒精灯等。
4. 实验器材:实验台、试管、烧杯、玻璃棒、酒精灯、打火机等。
四、实验步骤1. 准备实验材料,将可燃物、助燃物和点火温度分别放置在实验台上。
2. 分别进行以下实验:(1)可燃物实验:将酒精、纸张、棉花等可燃物分别放置在试管中,用打火机点燃,观察燃烧现象。
(2)助燃物实验:将酒精、纸张、棉花等可燃物分别放置在烧杯中,用酒精灯加热至点火温度,观察燃烧现象。
(3)点火温度实验:将酒精、纸张、棉花等可燃物分别放置在实验台上,用打火机加热至不同温度,观察燃烧现象。
3. 记录实验数据,分析实验结果。
五、实验结果与分析1. 可燃物实验:酒精、纸张、棉花等可燃物在点火温度下均可燃烧,说明可燃物是燃烧的必要条件。
2. 助燃物实验:在氧气充足的情况下,酒精、纸张、棉花等可燃物燃烧更加旺盛;在空气条件下,燃烧现象相对较弱。
这说明助燃物对燃烧有重要影响。
3. 点火温度实验:酒精、纸张、棉花等可燃物在点火温度下均可燃烧,但随着点火温度的升高,燃烧现象逐渐减弱。
这说明点火温度对燃烧有影响。
六、实验结论1. 燃烧需要满足三个条件:可燃物、助燃物和点火温度。
2. 可燃物是燃烧的必要条件,助燃物和点火温度对燃烧有重要影响。
3. 在实际生活中,要确保燃烧过程安全,需严格控制可燃物、助燃物和点火温度。
七、实验注意事项1. 实验过程中,注意安全,避免火灾事故。
2. 实验操作要规范,确保实验结果的准确性。
3. 实验结束后,及时清理实验场地,回收实验材料。
八、实验总结本次实验通过对燃烧条件的探究,验证了可燃物、助燃物和点火温度对燃烧的影响。
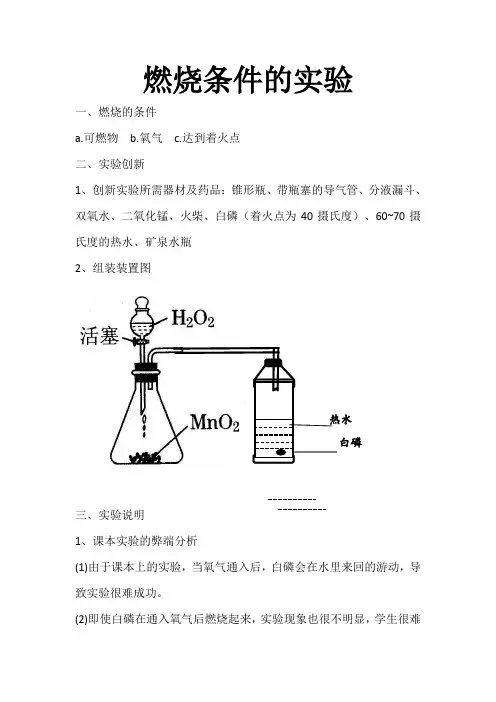
燃烧条件的实验一、燃烧的条件a.可燃物b.氧气c.达到着火点二、实验创新1、创新实验所需器材及药品:锥形瓶、带瓶塞的导气管、分液漏斗、双氧水、二氧化锰、火柴、白磷(着火点为40摄氏度)、60~70摄氏度的热水、矿泉水瓶2、组装装置图热水白磷三、实验说明1、课本实验的弊端分析(1)由于课本上的实验,当氧气通入后,白磷会在水里来回的游动,导致实验很难成功。
(2)即使白磷在通入氧气后燃烧起来,实验现象也很不明显,学生很难看到明显的实验现象(3)燃烧的火焰很容易喷出来,非常危险,学生就非常害怕,进而使学生对实验退避三舍,从而失去对实验的兴趣。
(4)实验后会产生大量的五氧化二磷白烟,不仅对身体有一定的危害作用,而且还污染环境。
(5)操作起来复杂,如需要成功需要一定的运气。
2、创新实验的优点总结(1)操作上:首先操作简单,装置图组装更容易(2)安全上:a、不会有火花冲出来,学生不会害怕,就导致学生愿意来观察实验,动手进行实验。
b、燃烧装置为密闭装置,五氧化二磷不会跑出来,不会危害师生的身体健康。
(3)现象上:a、在矿泉水瓶里面可以看见大量的火光,能明显的看到燃烧的现象。
学生更明显的、直观的观察到了燃烧的实验现象。
瓶子内燃烧结束后可以看到瓶子里面充满了白色的浓烟,最后可以看到水里的固体,再次回顾了磷燃烧的产物是烟而不是雾。
(4)环保上:燃烧装置为密闭装置,就使白磷燃烧后的产物五氧化二磷不会跑出来污染环境,从而达到保护环境,倡导环保的作用。
四、实验过程:1,将白磷放在60~70摄氏度的热水中。
2,接着向热水中通入氧气,直至装满矿泉水瓶(注意验满)。
3,上下振荡矿泉水瓶,可以看见明显的实验现象,白磷燃烧并产生大量的白烟。
4,达到探究燃烧的三个条件的目的。
芦山县太平中学:雷秋梅。


燃烧的条件笔记一、燃烧的定义。
燃烧是一种发光、放热的剧烈的氧化反应。
二、燃烧的条件。
(一)可燃物。
1. 概念。
- 能与空气中的氧或其他氧化剂起燃烧反应的物质称为可燃物。
- 例如:木材、纸张、汽油、酒精等都是可燃物。
2. 举例说明。
- 木材中含有纤维素等有机物质,在有氧气存在的条件下,达到一定温度就可以燃烧。
纸张主要由植物纤维制成,也是常见的可燃物。
汽油是由多种碳氢化合物组成的混合物,挥发性强,极易燃烧,是机动车常用的燃料。
酒精(乙醇)具有可燃性,在实验室中常用作燃料。
(二)氧气(或空气)1. 燃烧与氧气的关系。
- 氧气是燃烧过程中常见的氧化剂。
大多数燃烧反应都需要氧气参与。
- 在空气中,氧气约占21%,足够支持许多物质的燃烧。
2. 实验证明。
- 例如,将一根点燃的蜡烛放在一个密封的玻璃罩内。
随着蜡烛的燃烧,玻璃罩内的氧气逐渐被消耗。
当氧气消耗到一定程度时,蜡烛就会熄灭。
这表明蜡烛燃烧需要氧气。
(三)达到燃烧所需的最低温度(着火点)1. 着火点的概念。
- 着火点是指可燃物燃烧所需的最低温度。
不同的可燃物着火点不同。
2. 举例。
- 白磷的着火点很低,约为40℃。
在室温(一般高于20℃)下,如果将白磷暴露在空气中,它就会缓慢氧化并产生热量,当热量积累到一定程度,温度达到40℃时,白磷就会自燃。
而红磷的着火点约为240℃,相对较高。
- 纸张的着火点一般在130 - 255℃之间。
如果用打火机火焰(温度可达几百摄氏度)去点燃纸张,纸张会达到着火点而燃烧起来。
三、燃烧条件的探究实验。
1. 实验装置及步骤。
- 实验器材:铜片、白磷、红磷、热水、导管、气球等。
- 步骤:- 在铜片上放置一小块白磷和一小块红磷,将铜片放在盛有热水的烧杯上。
可以观察到白磷燃烧起来,产生大量白烟,而红磷没有燃烧。
这是因为热水的温度达到了白磷的着火点(40℃),但没有达到红磷的着火点(240℃),同时白磷和红磷都与空气(氧气)接触。
- 然后将导管一端插入热水中的白磷上方,另一端连接一个气球,通过导管向热水中的白磷鼓入空气,可以看到白磷在水下燃烧起来。
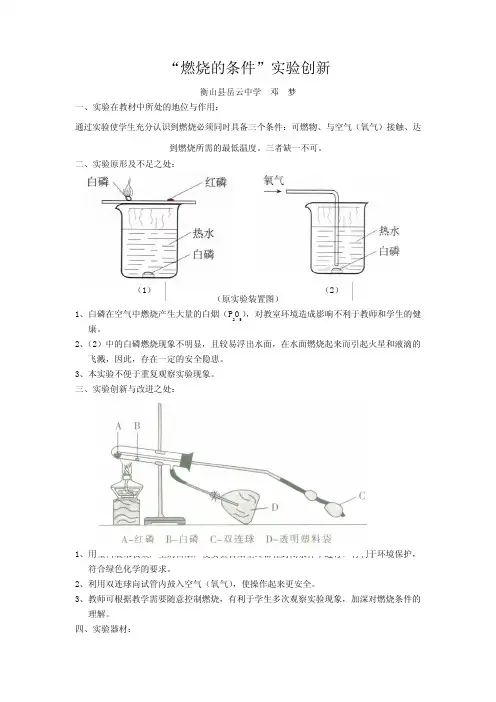
“燃烧的条件”实验创新衡山县岳云中学 邓 梦一、实验在教材中所处的地位与作用:通过实验使学生充分认识到燃烧必须同时具备三个条件:可燃物、与空气(氧气)接触、达到燃烧所需的最低温度。
三者缺一不可。
二、实验原形及不足之处:(原实验装置图)1、白磷在空气中燃烧产生大量的白烟(P 2O 5),对教室环境造成影响不利于教师和学生的健康。
2、(2)中的白磷燃烧现象不明显,且较易浮出水面,在水面燃烧起来而引起火星和液滴的飞溅,因此,存在一定的安全隐患。
3、本实验不便于重复观察实验现象。
三、实验创新与改进之处:1、用塑料袋来收集产生的白烟,使实验自始至终都在封闭条件下进行,有利于环境保护,符合绿色化学的要求。
2、利用双连球向试管内鼓入空气(氧气),使操作起来更安全。
3、教师可根据教学需要随意控制燃烧,有利于学生多次观察实验现象,加深对燃烧条件的理解。
四、实验器材:(1)(2)仪器:具支试管、铁架台、酒精灯、带导管的橡皮塞、双连球、塑料袋、药匙、镊子、试管架药品:红磷、白磷五、实验原理及装置说明:原理:利用酒精灯给红磷和白磷加热,利用双连球向具支试管中鼓入空气(氧气),随着温度的上升,白磷先燃烧起来(白磷的着火点为40℃)如果继续加热,温度上升至240℃或240℃以上,则红磷也能燃烧起来,说明燃烧必须同时具备的三个条件:可燃物、与空气(氧气)接触、达到燃烧的最低温度。
六、实验过程:1、加入0.2g红磷于具支试管底部,距其2cm初放一米粒大小的白磷,并将试管固定在铁架台上,导管口离试管底部0.5cm左右。
2、由双连球鼓入空气,发现无明显现象(说明可燃物虽与氧气接触,但温度达不到着火点,也不会燃烧)。
3、先用酒精灯均匀预热,然后对准红磷与白磷的中间部位集中加热,(温度在40℃或之上)同时挤压双连球,使进入的空气先通过红磷,再到白磷。
此时可观察到红磷无明显变化,而白磷却剧烈燃烧;(说明可燃物在温度达到着火点,且有氧气存在时能够燃烧),若停止鼓气,则白磷停止燃烧(说明仅温度达到着火点,但没有氧气时,可燃物不能燃烧)。


一、实验目的1. 探究燃烧的条件,验证燃烧需要满足的三个条件:有可燃物、可燃物与氧气接触、温度达到可燃物的着火点。
2. 通过实验观察不同条件下燃烧现象,加深对燃烧条件理解。
二、实验原理燃烧是可燃物与氧气在一定的温度下发生的一种剧烈的氧化反应,放出大量的热和光。
燃烧的条件有三个:有可燃物、可燃物与氧气接触、温度达到可燃物的着火点。
三、实验材料与仪器1. 实验材料:酒精、水、小棉球、小木条、煤、蜡烛、烧杯、玻璃杯、滤纸等。
2. 实验仪器:酒精灯、火柴、铁夹、铁架台、温度计等。
四、实验步骤1. 将分别蘸有酒精、水的小棉球放到酒精灯火焰上加热片刻,观察现象。
2. 同时将一根小木条和一小块煤放在酒精灯火焰上灼烧,观察现象。
3. 点燃两支小蜡烛,其中一支用烧杯罩住,观察现象。
4. 将一小块金属钠放入氯气中,观察现象。
5. 将一小块镁放入二氧化碳中,观察现象。
五、实验现象1. 蘸有酒精的小棉球能被点燃,而蘸有水的小棉球不能被点燃。
2. 小木条容易被点燃,而煤不易被点燃。
3. 未罩烧杯的小蜡烛能继续燃烧,罩烧杯的小蜡烛一会儿熄灭。
4. 金属钠在氯气中剧烈燃烧,产生大量白烟。
5. 镁在二氧化碳中剧烈燃烧,产生大量白烟。
六、实验结论1. 燃烧需要满足三个条件:有可燃物、可燃物与氧气接触、温度达到可燃物的着火点。
2. 不同物质的着火点不同,有些物质在氧气中也能燃烧。
3. 用玻璃杯罩住蜡烛,隔绝氧气,蜡烛会熄灭。
七、实验讨论1. 实验过程中,为什么蘸有酒精的小棉球能被点燃,而蘸有水的小棉球不能被点燃?答:因为酒精具有可燃性,而水不具有可燃性。
2. 实验过程中,为什么小木条容易被点燃,而煤不易被点燃?答:因为小木条的着火点低于煤的着火点。
3. 实验过程中,为什么用玻璃杯罩住蜡烛,蜡烛会熄灭?答:因为玻璃杯隔绝了蜡烛与氧气的接触,导致蜡烛熄灭。
八、实验总结本次实验通过观察不同条件下燃烧现象,验证了燃烧需要满足的三个条件。
同时,实验过程中发现了一些特殊现象,如金属钠在氯气中燃烧、镁在二氧化碳中燃烧等,进一步加深了对燃烧条件的理解。
一、实验目的通过本次实验,了解燃烧的条件,探究不同条件下物质燃烧的特性,为今后的安全用火提供理论依据。
二、实验原理燃烧是一种氧化反应,需要满足以下条件:1. 物质具有可燃性;2. 可燃物与氧气接触;3. 可燃物温度达到着火点。
三、实验器材1. 酒精灯;2. 酒精;3. 小木块;4. 小铁块;5. 烧杯;6. 氧气瓶;7. 温度计;8. 秒表;9. 火柴;10. 实验记录表。
四、实验步骤1. 将酒精倒入酒精灯中,点燃酒精灯,观察火焰颜色和形状;2. 将小木块放在酒精灯火焰上加热,记录木块燃烧的时间;3. 将小铁块放在酒精灯火焰上加热,观察铁块表面现象;4. 将烧杯罩在酒精灯火焰上,观察火焰熄灭时间;5. 将氧气瓶打开,用酒精灯加热氧气瓶,观察氧气燃烧现象;6. 记录实验数据,分析燃烧条件。
五、实验现象1. 酒精灯火焰呈蓝色,温度较高;2. 小木块在酒精灯火焰上燃烧,燃烧时间为10秒;3. 小铁块在酒精灯火焰上加热,表面出现红色;4. 烧杯罩在酒精灯火焰上,火焰熄灭时间为30秒;5. 氧气瓶打开后,加热氧气瓶,火焰迅速熄灭。
六、实验结论1. 物质具有可燃性,酒精、木块、铁块均具有可燃性;2. 可燃物与氧气接触,酒精、木块、铁块在氧气中均能燃烧;3. 可燃物温度达到着火点,酒精、木块、铁块在酒精灯火焰上加热后能燃烧;4. 燃烧条件满足时,燃烧现象明显,如火焰颜色、形状、温度等;5. 燃烧条件不满足时,燃烧现象不明显或无法燃烧。
七、实验注意事项1. 实验过程中注意安全,避免酒精灯火焰烧伤;2. 实验过程中注意观察实验现象,准确记录实验数据;3. 实验结束后,将实验器材整理归位。
八、实验拓展1. 探究不同可燃物的燃烧特性;2. 研究燃烧过程中产生的热量;3. 探究燃烧过程中产生的有害气体;4. 研究燃烧条件对燃烧速度的影响。
九、实验总结通过本次实验,我们了解了燃烧的条件,掌握了不同条件下物质燃烧的特性。
在今后的学习和生活中,我们要注意安全用火,避免火灾事故的发生。
一、实验目的1. 掌握燃烧的基本概念和条件;2. 了解不同燃烧条件下火焰、烟尘、气味等现象;3. 分析燃烧过程中物质的变化和能量转换。
二、实验原理燃烧是指可燃物质与氧气在一定条件下发生的放热反应,产生火焰、烟尘、气味等现象。
燃烧的条件包括:可燃物质、氧气和点火源。
本实验通过改变燃烧条件,观察火焰、烟尘、气味等现象,分析燃烧过程中的物质变化和能量转换。
三、实验材料与仪器1. 实验材料:蜡烛、火柴、酒精灯、酒精、氧气瓶、铁夹、烧杯、量筒、试管等;2. 实验仪器:酒精灯、铁夹、烧杯、量筒、试管等。
四、实验步骤1. 点燃蜡烛,观察火焰颜色、形状、大小等;2. 将蜡烛放入烧杯中,观察火焰与氧气接触面积的变化;3. 在烧杯中加入少量酒精,观察火焰与酒精接触面积的变化;4. 将氧气瓶连接铁夹,将蜡烛放入氧气瓶中,观察火焰的变化;5. 在氧气瓶中加入少量酒精,观察火焰的变化;6. 点燃酒精灯,观察火焰颜色、形状、大小等;7. 将酒精灯火焰吹灭,观察火焰熄灭后的现象;8. 分析实验现象,得出结论。
五、实验现象1. 点燃蜡烛,火焰呈黄色,形状为锥形,大小适中;2. 将蜡烛放入烧杯中,火焰与氧气接触面积减小,火焰逐渐变暗;3. 在烧杯中加入少量酒精,火焰与酒精接触面积增大,火焰变亮;4. 将蜡烛放入氧气瓶中,火焰变得明亮,颜色呈蓝紫色;5. 在氧气瓶中加入少量酒精,火焰变得更加明亮,颜色呈蓝紫色;6. 点燃酒精灯,火焰呈黄色,形状为锥形,大小适中;7. 将酒精灯火焰吹灭,火焰熄灭,留下少量烟尘;8. 火焰熄灭后,烧杯底部有少量水滴,酒精灯底部有少量酒精残留。
六、实验分析1. 火焰颜色、形状、大小与可燃物质和氧气接触面积有关。
蜡烛和酒精的燃烧过程中,火焰颜色、形状、大小发生变化,说明燃烧条件对火焰特征有影响;2. 氧气浓度对燃烧有重要影响。
在氧气瓶中,火焰变得更加明亮,颜色呈蓝紫色,说明氧气浓度越高,燃烧越充分;3. 燃烧过程中,物质发生化学变化,释放出热量和能量。
一、创新实验名称燃烧条件的探究
青岛莱西市绕岭中学初四一班张雅宁
指导教师:柳志中
二、创新实验目的运用控制变量,对比试验的方法探究燃烧条件
三、实验仪器及用品
红磷、白磷、氧气、试管、小气球、带导管的单孔塞、烧杯、水槽、胶塞、锥形瓶
四、实验装置图及说明
五、实验操作
1、将白磷直接放在热水中。
2、将红磷、白磷放入装有氧气的试管中,用一端系有小气球的带导管的单孔塞塞住试管口,
完全封闭后将两试管同时浸入热水中进行对比实验,使产生的P2O5白烟外泄污染环境的问题得到解决,如上图。
3、水下白磷燃烧:在水槽中放置胶塞,白磷放在上面,将盛有氧气的锥形瓶快速倒扣在白
磷上,进行实验。
六、实验创新点及意义
1、能较长时间观察到白磷燃烧时产生的黄色火焰,这样既可观察到白磷在热水下燃烧,又可控制白磷不“乱跑”,还可以把产生的白烟消灭在锥形瓶内。
2、简化实验操作,不但使实验产生的效果更明显,而且把实验中产生的污染物尽量消灭在实验过程中,注重环保教育,培养可持续发展的素质。
燃烧的条件实验报告燃烧的条件实验报告引言:燃烧是我们日常生活中常见的现象之一,它是指物质在与氧气接触时产生火焰、释放能量的化学反应。
然而,燃烧并非所有物质都能进行的,它需要一定的条件才能发生。
为了深入了解燃烧的条件,我们进行了一系列的实验。
实验一:氧气的必要性为了验证氧气在燃烧过程中的重要性,我们选取了两个物质进行实验:木炭和蜡烛。
首先,我们点燃一块木炭,观察到它迅速燃烧,并产生出明亮的火焰和热量。
然后,我们将另一块木炭放入一个密闭容器中,再次点燃。
这一次,由于缺乏氧气,木炭只是慢慢地燃烧,没有明亮的火焰产生。
类似地,我们点燃了一支蜡烛,它也迅速燃烧并产生火焰。
接着,我们将蜡烛放入一个密闭容器中,结果同样是缺乏氧气导致蜡烛燃烧缓慢,没有明亮的火焰。
通过这些实验,我们可以得出结论:氧气是燃烧发生的必要条件之一。
实验二:可燃物质的存在为了验证可燃物质的存在对燃烧的影响,我们选取了两个物质进行实验:纸张和水。
首先,我们点燃一张纸,观察到它迅速燃烧并产生明亮的火焰。
然后,我们将纸张放入一个密闭容器中,再次点燃。
这一次,由于缺乏可燃物质,纸张只是燃烧一小段时间后熄灭。
接着,我们将水倒入一个容器中,再点燃一张纸。
结果是纸张无法燃烧,因为水的存在阻碍了燃烧反应的进行。
通过这些实验,我们可以得出结论:可燃物质的存在是燃烧发生的必要条件之一。
实验三:点燃温度的影响为了验证点燃温度对燃烧的影响,我们选取了两个物质进行实验:纸张和木片。
首先,我们将一张纸张放在火焰附近,观察到纸张开始燃烧。
然后,我们将另一张纸张放在冰箱中冷却一段时间后再接近火焰,结果是纸张无法点燃。
类似地,我们将一块木片放在火焰附近,观察到木片开始燃烧。
然后,我们将另一块木片放在冰箱中冷却一段时间后再接近火焰,结果是木片无法点燃。
通过这些实验,我们可以得出结论:点燃温度是燃烧发生的必要条件之一。
结论:通过以上实验,我们可以总结出燃烧的三个基本条件:氧气的存在、可燃物质的存在和适当的点燃温度。
燃烧的实验报告燃烧的实验报告燃烧是我们日常生活中经常遇到的现象,无论是烧火做饭,还是汽车的燃油燃烧,都离不开燃烧的过程。
为了更好地了解燃烧的原理和特性,我们进行了一系列的实验。
实验一:燃烧的基本原理在这个实验中,我们使用了一根蜡烛作为燃烧的样本。
首先,我们点燃了蜡烛的蜡烛芯,然后观察了燃烧的过程。
通过观察,我们发现蜡烛的蜡烛芯燃烧后会产生明亮的火焰,并伴有一定的热量释放。
这是因为蜡烛芯中的蜡燃烧时与空气中的氧气反应,产生了二氧化碳和水蒸气。
同时,燃烧产生的热量也使蜡烛芯继续燃烧,形成了一个循环。
实验二:燃烧的条件在这个实验中,我们探究了燃烧所需的条件。
我们分别取了一根蜡烛和一根木棍,将它们分别放在两个密闭的容器中,并点燃两者。
结果令人惊讶的是,蜡烛在密闭容器中燃烧了一段时间后熄灭了,而木棍却一直燃烧下去。
我们分析得出,这是因为燃烧需要氧气的供应,而密闭容器中的氧气被燃烧过程中产生的二氧化碳所取代,导致蜡烛燃烧不了。
实验三:燃烧的种类在这个实验中,我们研究了不同物质的燃烧特性。
我们选取了纸张、木头和塑料作为研究对象,并分别点燃它们。
纸张燃烧时产生了明亮的火焰,燃烧速度较快,并伴有明显的黑烟。
木头的燃烧速度较慢,形成的火焰较小,但燃烧的时间较长。
而塑料的燃烧则产生了黑烟和有毒气体,燃烧速度也非常快。
通过这个实验,我们可以得出结论:不同物质的燃烧特性不同,这是由其化学成分和结构所决定的。
因此,在日常生活中,我们要注意选择正确的燃料,避免对环境和健康造成不良影响。
实验四:燃烧的应用燃烧不仅仅是一种化学反应,还有许多实际应用。
我们以火箭发动机为例,探究了燃烧在航天领域的应用。
火箭发动机的燃烧过程是通过燃料和氧化剂的反应来产生高温和高压气体,从而产生推力。
这种推力可以使火箭脱离地球引力,实现航天任务。
通过这个实验,我们深刻认识到燃烧的应用不仅仅局限于日常生活,还涉及到科学技术的前沿领域。
燃烧的研究不仅可以帮助我们更好地理解自然界的现象,还可以为人类的发展做出贡献。
探究燃烧的条件实验教案
一、实验目的
(1)了解燃烧的必要条件;
(2)掌握燃烧过程中物质数量守恒的定律。
二、实验原理
燃烧是一种无机物质中氧元素和其它化学元素的化学反应,它包含一个也可以称作火的热量耗散的过程。
需要燃烧的四个条件是氧气、高温、燃料和火花(或其它火源)。
三、实验准备
(1)准备实验用具:安全桶、安全帽、橡胶瓶、蜡烛、棉花、餐巾纸、打火机等;
(2)准备实验台:放置橡胶瓶,让其位于安全桶中,将蜡烛放置在安全桶内;
四、实验步骤
(1)将一片棉花放置在橡胶瓶内;
(2)将橡胶瓶装入安全桶中;
(3)将蜡烛放置在安全桶中;
(4)将餐巾纸放置在安全桶中;
(5)用打火机点燃蜡烛的蜡油;
(6)在安全桶中关闭盖子;
(7)观察棉花是否燃烧。
五、安全须知
(1)本实验必须年满18岁或以上;
(2)本实验应在室外空气节奏或有良好通风的室内进行;
(3)实验时应佩戴口罩;
(4)实验时禁止吸烟;
(5)实验时应注意安全,使用安全桶。
六、结果分析
经过上述实验,可以发现棉花燃烧的过程中氧气能够使燃料(棉花)燃烧,而高温和火花(打火机)则是辅助燃烧发生的必要条件。
从而可以得出:燃烧是一种物质加热使之分解成另一些物质的化学反应,要使物质燃烧,必须具备四个条件:氧气、高温、燃料和火花(或其它火源)。
同时,这也验证了物质守恒定律。