溶质质量分数与溶解度的关系
- 格式:ppt
- 大小:351.50 KB
- 文档页数:10



溶液溶质的质量分数一、溶液组成的表示方法------溶质的质量分数1、概念:溶质质量与溶液质量之比注:溶质的质量分数的理解应注意以下几点:①、所指溶液可以是饱和溶液,也可以是不饱和溶液;可以是浓溶液,也可以是稀溶液。
②、溶质的质量分数是质量之比,一般情况下与温度无关。
③、由于溶液的组成是指溶质在溶解度的范围内,所以溶质的质量分数最大不能超过溶解度/(100g+溶解度)×100%④、运用公式时,必须分清溶质质量、溶剂质量、溶液质量。
2、公式:溶液质量=溶质质量+溶剂质量饱和溶液中:溶质的质量分数=溶解度÷(100g+溶解度)×100%3、变换公式:溶质质量=溶液质量×溶质的质量分数溶液质量=溶质质量÷溶质的质量分数4、溶解度与溶质的质量分数的关系:溶解度= 100g×溶质的质量分数/(1-溶质的质量分数)5、含义:(溶质的质量分数为B%的溶液)(1)、每100g溶液中含溶质B g( 2 )、该溶液中, 溶质的质量:溶剂的质量:溶液的质量==B :100 : (100 +B) 计算时注意:(1)溶质的质量分数是质量比而不是体积比,若是体积,必须先用物理公式ρ=m/v进行换算,然后计算;(2)在运算过程中,质量的单位要统一;(3)因为通常溶液均为水溶液,所以溶质应为无水的物质;能与水反应的物质,其溶质应是反应后的生成物,而不是原来加入的物质,因此计算时应先算出反应后的生成物的质量。
二、计算(一)、基本公式的计算例1:某溶液50g,完全蒸干后,得到溶质15g,求该溶液中溶质的质量分数?例2:某溶液中,20g溶质完全溶解在80g溶剂中,求该溶液中溶质的质量分数?例3:20℃的某饱和溶液1000g,求该溶液中溶质的质量分数?(20℃时,该溶质的溶解度为36g)(二)、变换公式的计算例4:某农场,需要16%的氯化钠溶液100Kg,则需要氯化钠和水各多少Kg?例5:200g稀硫酸与足量锌反应,生成0.4g氢气.求:①原硫酸溶液中溶质的质量分数.②所得溶液中溶质质量分数.(三)、溶液稀释的计算1、方法:加入水或加入低浓度溶液。

溶解度和溶质的质量分数【学习目标】1.掌握饱和溶液、不饱和溶液、溶解度等概念及相互关系;掌握溶解度曲线的意义及应用。
2.认识一种溶液组成的表示方法——溶质的质量分数;掌握溶质质量分数的有关计算。
3.初步学会配制一定溶质质量分数的溶液。
【要点梳理】要点一、饱和溶液、不饱和溶液(专题课堂《溶解度》一)1.饱和溶液:在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得到的溶液叫做饱和溶液。
2.不饱和溶液:在一定温度下,向一定量溶剂里加入某种溶质,当溶质还能继续溶解时的溶液,叫做不饱和溶液。
3.饱和溶液、不饱和溶液的转化方法:大多数情况下饱和溶液和不饱和溶液存在以下转化关系(溶质为固体):4.判断溶液是否饱和的方法:一般说来,可以向原溶液中再加入少量原溶质,如果溶解的量不再增大则说明原溶液是饱和溶液,如果溶解的量还能增大则说明原溶液是不饱和溶液。
【要点诠释】1.饱和溶液、不饱和溶液概念的理解(1)首先要明确“一定条件”、“一定量的溶剂”。
在某一温度和一定量的溶剂里,对某种固态溶质来说饱和了,但若改变温度或改变溶剂的量,就可能使溶液不饱和了。
如室温下,100 g水中溶解31.6 g KNO3达到饱和,若升高温度或增大溶剂(水)量,原来饱和溶液就变为不饱和溶液。
所以溶液饱和与否,首先必须明确“一定条件”和“一定量的溶剂”。
(2)必须明确是某种溶质的饱和溶液或不饱和溶液。
如:在一定条件下不能再溶解食盐的溶液,可能还能继续溶解蔗糖,此时的溶液对于食盐来说是饱和溶液,但是对于蔗搪来说就是不饱和溶液。
2.由于Ca(OH)2的溶解度在一定范围内随温度的升高而减小,因此将Ca(OH)2的不饱和溶液转化为饱和溶液,在改变温度时应该是升高温度;将熟石灰的饱和溶液转化为不饱和溶液,在改变温度时应该是降低温度。
要点二、溶解度、溶解度曲线1.固体的溶解度:(专题课堂《溶解度》二)在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。



第 1 页 共 1 页 物质的量浓度、质量分数、溶解度间的换算
由定义出发,运用公式:c =n V 、质量分数=溶质的质量溶液的质量
×100%进行推理,注意密度的桥梁作用,不要死记公式。
(1)物质的量浓度(c )与溶质质量分数(w )的换算
体积为V ,密度为ρ g·cm -3的溶液,含有摩尔质量为M g·mol -1的溶质m g ,溶质的质量分
数为w ,则溶质的物质的量浓度c 与溶质的质量分数w 的关系是:c =n V =m M V =m MV =1 000ρw V MV
=1 000ρw M ,反之,w =cM 1 000ρ。
(2)物质的量浓度(c )与溶解度(S )的换算
若某饱和溶液的密度为ρ g·cm -3,溶质的摩尔质量为M g·mol -
1,溶解度为S g ,则溶解度与
物质的量浓度的表达式分别为:S =100cM 1 000ρ-cM
,c =n V =S M 100+S 1 000ρ= 1 000ρS M (100+S )。



第八讲 溶解度计算【知识梳理】1、溶液由溶质和溶剂组成,所以:m(溶液)=m( )+m( )2、溶质的质量百分数溶质的质量占全部溶液质量的百分比来表示的溶液的浓度。
溶质的质量百分数(c %)= _______________________________3、溶解度溶解度基本关系式:溶解度S ——100g 溶剂——+溶解度100(溶质质量) (溶剂质量) (饱和溶液质量) 计算公式:()=()100m S m 溶质(1)溶剂 ()2=()100m S m S 溶质()饱和溶液 (2)相同温度下,溶解度(S )与饱和溶液中溶质的质量分数(w%)的关系:(3)温度不变,蒸发饱和溶液中的溶剂(水),析出晶体的质量m 的计算:(4)降低热饱和溶液的温度,析出晶体的质量m 的计算:【相关考点】1、有关溶解度的计算(1)计算溶解度:已知饱和溶液中溶剂的质量(或溶液的质量)和溶质的质量,能正确计算溶解度。
(2)已知溶解度,计算溶质、溶剂或溶液的质量。
已知溶解度,能正确计算一定饱和溶液(溶剂)的质量。
2、有关溶液中溶质和质量分数的计算(1)溶液中溶质的质量分数的计算:已知溶质和溶液(或溶剂)的质量,能正确计算溶液中溶质的质量分数;已知溶液中溶质的质量分数,能正确计算溶质(或溶剂)的质量;能正确计算不同温度下,溶质、溶剂的质量及溶液中溶质的质量分数。
(2)溶解度跟饱和溶液中溶质的质量分数的换算:掌握一定温度下溶解度和饱和溶液中溶质的质量分数的换算。
【题型归纳】1、已知一定温度下某物质饱和溶液里的溶质和溶剂的质量,求溶解度【例1】在一定温度下,ng某物质恰好溶于一定量的水中形成mg饱和溶液,求该物质在此温度下的溶解度。
2、已知一定温度下某物质的溶解度,求此温度下一定量的饱和溶液中含溶质和溶剂的质量【例2】已知在20℃时KNO3的溶解度为31.6g。
现要在20℃时配制20gKNO3饱和溶液,需KNO3和H2O各几克?3、已知一定温度下某物质的溶解度,求一定量溶质配制成饱和溶液时,所需溶剂的质量【例3】已知氯化钠在20℃的溶解度是36g,在20℃时要把40g氯化钠配制成饱和溶液,需要水多少克?4、计算不饱和溶液恒温变成饱和溶溶需要蒸发溶剂或加入溶质的质量【例4】已知硝酸钾在20℃的溶解度为31.6g,现有150g20%的硝酸钾溶液,欲想使其恰好饱和,应加入几克硝酸钾或蒸发几克水?5、计算温度升高时变成饱和溶液需加入溶质或蒸发溶剂的质量【例5】将20℃时263.2g硝酸钾饱和溶液温度升至60℃需加入几克硝酸钾或蒸发几克水才能变为饱和溶液?(20℃硝酸钾溶解度为31.6g,60℃为110g)6、饱和溶液的溶质质量分数与溶解度的相互换算【例6】20℃时氯化钠的溶解度为36g,求此温度下氯化钠饱和溶液中氯化钠的质量分数。
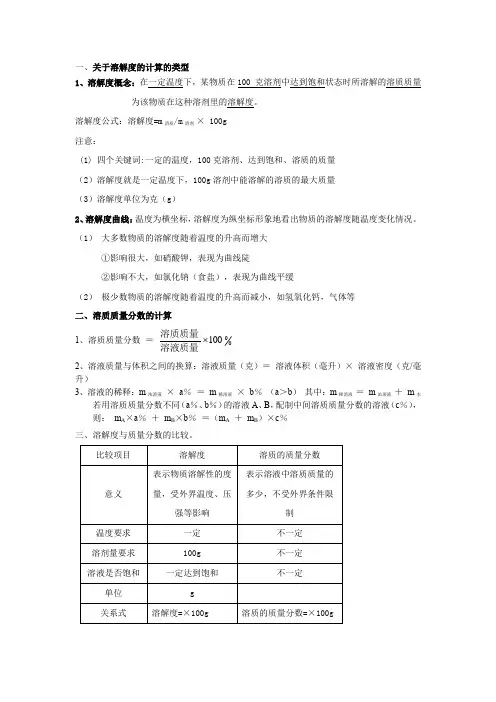
一、关于溶解度的计算的类型1、溶解度概念:在一定温度下,某物质在100 克溶剂中达到饱和状态时所溶解的溶质质量为该物质在这种溶剂里的溶解度。
溶解度公式:溶解度=m 溶质/m 溶剂 × 100g 注意:(1) 四个关键词:一定的温度,100克溶剂、达到饱和、溶质的质量 (2)溶解度就是一定温度下,100g 溶剂中能溶解的溶质的最大质量 (3)溶解度单位为克(g )2、溶解度曲线:温度为横坐标,溶解度为纵坐标形象地看出物质的溶解度随温度变化情况。
(1) 大多数物质的溶解度随着温度的升高而增大①影响很大,如硝酸钾,表现为曲线陡②影响不大,如氯化钠(食盐),表现为曲线平缓(2) 极少数物质的溶解度随着温度的升高而减小,如氢氧化钙,气体等 二、溶质质量分数的计算 1、溶质质量分数 =0100 溶液质量溶质质量2、溶液质量与体积之间的换算:溶液质量(克)= 溶液体积(毫升)× 溶液密度(克/毫升)3、溶液的稀释:m 浓溶液 × a % = m 稀溶液 × b % (a >b ) 其中:m 稀溶液 = m 浓溶液 + m 水若用溶质质量分数不同(a %、b %)的溶液A 、B ,配制中间溶质质量分数的溶液(c %), 则: m A ×a % + m B ×b % =(m A + m B )×c % 三、溶解度与质量分数的比较。
甲乙溶解度 g0 t 1 t 2 温度/℃305020 40 10初中化学总复习溶解度曲线专题练习9.右图所示曲线a 、b 、c 分别代表A 、B 、C 三种物质的溶解度曲线。
下列说法错误的是( )A .t 1 ℃时,三种物质溶解度大小的顺序是B >C >AB .t 2℃时,A 和B 两种物质的饱和溶液中溶质质量相同C .t 3℃时,在100g 水里分别加入三种物质各mg ,只有b 能形成饱和溶液D .从混有少量C 的A 物质中提取较纯净的A ,最适宜用蒸发溶剂的方法 10.右图是a 、b 、c 三种固体的溶解度曲线,下列说法正确的是( ) A .b 的溶解度一定小于a 的溶解度B .当a 中含有少量b 时,可以用降温结晶的方法提纯aC .通过降低温度可将c 的不饱和溶液变为饱和溶液D .a 的饱和溶液从t 2℃降温至t 1℃时变为不饱和溶液11.有关a 、b 两种物质的溶解度曲线如图所示,下列叙述不正确的是( ) A .a 物质的溶解度随着温度的升高而增大B .在t 2℃时,a 、b 两种物质的溶液中溶质的质量分数一定相等C .将a 、b 两种物质的饱和溶液从t 3℃降温至t 1℃,a 有晶体析出,bD .t 3℃时,a 物质的溶解度大于b 物质的溶解度 12.a 、b 、c 三种物质的溶解度曲线如右图所示。
溶质的质量分数与溶解度的关系
溶质的质量分数与溶解度之间存在着一定的关系。
溶解度是指单位温度和压力下,溶液中最多可以溶解的物质的量,通常用摩尔/升或克/升表示。
而溶质的质量分数则是指单位溶液中溶质质量与溶液总质量之比,通常用百分比表示。
当溶质的质量分数小于溶解度时,溶液处于不饱和状态,此时溶质可以继续溶解。
当溶质的质量分数等于溶解度时,溶液处于饱和状态,此时溶质不再溶解,但可以继续溶解剂和溶质之间的物质交换。
当溶质的质量分数大于溶解度时,溶液处于过饱和状态,此时溶质会发生析出,形成固体沉淀。
因此,溶质的质量分数与溶解度之间的关系可以用来判断溶液的状态,以及调节溶液中溶质的含量。
在化学实验和工业生产中,了解这种关系对于正确选择反应条件和操作方法是非常重要的。
- 1 -。
2021届中考化学压轴题专项练习溶解度【考点一】固体溶解度及其影响因素【要点梳理】1.固体溶解度的概念在一定的温度下,某物质在100克溶剂里达到饱和状态时所溶解的质量,其单位是克(符号为g)。
在未注明溶剂的情况下,通常溶解度指的是物质在水里的溶解度。
2.固体溶解度的意义对于溶解度的意义的表达一般有两种方式:一种是在某温度时,100g水里最多能溶解多少克某物质;另一种是在某温度时,100g水里溶解多少克某物质,溶液达到饱和状态。
例如:在20℃时,100g水里最多能溶36g氯化钠(这时溶液达到饱和状态),我们就说在20℃时,氯化钠在水里的溶解度是36g。
3.固体溶解度的影响因素主要是指温度。
大部分固体随温度升高溶解度增大,如硝酸钾;少部分固体溶解度受温度影响不大,如食盐(氯化钠);极少数物质溶解度随温度升高反而减小,如熟石灰.【典型例题】下表是KC1、NH4Cl、KNO3三种物质在不同温度时的溶解度。
温度/℃020*********溶解度/gKC127.634.040.045.551.156.7 NH4C129.437.245.855.265.677.3 KNO313.331.663.9110169246根据表格信息,可以推知()A.三种物质中溶解度最小的是KClB.40℃时,100g KNO3饱和溶液中含有63.9g KNO3C.三种物质中,溶解度受温度变化影响最大的是KNO3D.在0℃﹣100℃以内的相同温度下,KCl和NH4Cl的溶解度可能相等【答案】C【解答】解:A.比较物质溶解度大小的时候。
要指明温度,否则没有意义,故A错误;B.在一定温度下,某物质在100g溶剂里达到饱和状态时所溶解的质量。
40℃时,KNO3的溶解度是63;40℃时,应该是163.9g KNO3饱和溶液中才含有63.9g KNO3,故B错误;C.根据三种物质的溶解度的表格可以看出:三种物质中,溶解度受温度变化影响最大的是KNO3,故C正确;D.根据从表格中获取的信息可知:在0℃﹣100℃以内的相同温度下,KCl和NH4Cl的溶解度不可能相等,故D错误。