高中物理封闭气体压强的计算
- 格式:docx
- 大小:417.45 KB
- 文档页数:13

压强高中公式
压强高中公式是一个重要的物理公式,它用于计算物体在单位面积上所受到的压力。
这个公式通常表示为p=F/S,其中p代表压强,F代表施加在物体上的力,S代表物体的受力面积。
这个公式可以应用于许多不同的场景,例如在工程学中计算建筑物或机械部件的承载能力,在气象学中计算大气压强等等。
在应用这个公式时,需要注意的是,压强和力是向量,即它们有方向和大小,而受力面积必须是垂直于力的方向上的面积。
在解决具体的压强问题时,还需要考虑一些其他的因素,例如液体的密度、重力加速度等。
例如,在计算液体内部的压强时,可以使用公式p=ρgh,其中ρ代表液体的密度,g代表重力加速度,h代表液体的高度。
此外,还有一些其他的压强公式可以用于解决不同类型的问题。
例如,在计算气体压强时,可以使用玻意耳定律和查理
定律等气体实验定律来解决问题。
这些公式可以根据不同的气体状态和条件进行选择和运用。
总之,压强是一个非常重要的物理量,它可以影响物体的机械性能、能量传递和热力学性质等多个方面。
通过掌握这些压强公式,我们可以更好地理解和应用这些物理原理,为我们的生活和工业生产带来更多的便利和效益。




第2节气体的等容变化和等压变化1.查理定律:一定质量的某种气体,在体积不变的情况下,压强p 与热力学温度T 成正比,即p T=C 。
2.盖-吕萨克定律:一定质量的某种气体,在压强不变的情况下,其体积V 与热力学温度T 成正比,即V T=C 。
3.玻意耳定律、查理定律、盖-吕萨克定律的适用条件均为一定质量的某种气体。
一、气体的等容变化 1.等容变化一定质量的某种气体,在体积不变时,压强随温度的变化。
2.查理定律 (1)内容:一定质量的某种气体,在体积不变的情况下,压强p 与热力学温度T 成正比。
(2)表达式:p T =C 或p 1T 1=p 2T 2。
(3)适用条件:①气体的质量不变;②气体的体积不变。
3.等容线一定质量的气体,在体积不变时,其p T 图像是一条过原点的直线,这条直线叫做等容线。
二、气体的等压变化 1.等压变化一定质量的某种气体,在压强不变时,体积随温度的变化。
2.盖-吕萨克定律 (1)内容:一定质量的某种气体,在压强不变的情况下,体积V 与热力学温度T 成正比。
(2)表达式:V =CT 或V T =C 或V 1T 1=V 2T 2。
(3)适用条件:①气体的质量不变;②气体的压强不变。
3.等压线一定质量的气体,在压强不变时,其V T 图像是一条过原点的直线,这条直线叫做等压线。
1.自主思考——判一判(1)气体的温度升高,气体体积一定增大。
(×)(2)一定质量的气体,在压强不变时体积与温度成正比。
(×)(3)一定质量的某种气体,在压强不变时,其V T 图像是过原点的直线。
(√) (4)一定质量的气体在体积不变的情况下,气体的压强与摄氏温度成正比。
(×) (5)pV =C 、p T =C 、V T=C ,三个公式中的常数C 是同一个值。
(×) 2.合作探究——议一议(1)某登山运动员在一次攀登珠穆朗玛峰的过程中,在接近山顶时他裸露在手腕上的防水手表的表盘玻璃突然爆裂了,而手表没有受到任何撞击,你知道其中的原因吗?提示:手表表壳可以看成一个密闭容器,出厂时封闭着一定质量的气体,登山过程中气体发生等容变化,因为高山山顶附近的压强比山脚处小很多,内外压力差超过表盘玻璃的承受限度,便会发生爆裂。


气体气压的计算公式气体压强是指气体分子在单位面积上对物体施加的压力,是一种物体受力的表现。
气体压强的计算公式可以根据不同的情况有所不同,下面将介绍几种常见的计算气体压强的公式。
1.理想气体状态方程理想气体状态方程描述了气体的状态与温度、压强、体积之间的关系,其公式如下:PV=nRT其中P表示气体压强(单位为帕斯卡Pa),V表示气体体积(单位为立方米m³),n表示气体物质的摩尔数,R表示气体常数(约为8.314J/(mol·K)),T表示气体的绝对温度(单位为开尔文K)。
通过此公式,可以根据已知条件计算气体的压强。
2.玻意耳-马略特定律玻意耳-马略特定律是描述气体在恒温下压强与体积之间的关系的定律,其公式为:P₁V₁=P₂V₂其中P₁和P₂分别表示气体的初始压强和最终压强,V₁和V₂分别表示气体的初始体积和最终体积。
该定律适用于恒温过程中,通过已知初始状态和改变的体积来计算气体的压强。
3.爱德瓦·沃泽定律爱德瓦·沃泽定律描述了温度和压强之间的关系,其公式为:P₁/T₁=P₂/T₂其中P₁和P₂分别表示气体的初始压强和最终压强,T₁和T₂分别表示气体的初始温度和最终温度。
该定律适用于等容过程中,通过已知初始状态和改变的温度来计算气体的压强。
4.高斯定理高斯定理是描述封闭容器内气体压强与容器内总分子数的关系的定律,其公式为:P=(n/V)kT其中P表示气体的压强,n表示气体内分子数,V表示容器的体积,k表示玻尔兹曼常数(约为1.38×10⁻²³J/K),T表示气体的温度。
通过此公式,可以根据已知条件计算气体的压强。
5.狄朗-珀蒂定律狄朗-珀蒂定律描述了气体压强与气体的密度和温度之间的关系,其公式如下:P=ρRT其中P表示气体的压强,ρ表示气体的密度(单位为千克/立方米kg/m³),R表示气体常数(约为8.314J/(mol·K)),T表示气体的绝对温度(单位为开尔文K)。


第1节气体的等温变化1.一定质量的气体,在温度不变的条件下,其压强与体积变化时的关系,叫做气体的等温变化。
2.玻意耳定律:一定质量的某种气体,在温度不变的情况下,压强p 与体积V 成反比,即pV =C 。
3.等温线:在p -V 图像中,用来表示温度不变时,压强和体积关系的图像,它们是一些双曲线。
在p -1V 图像中,等温线是倾斜直线。
一、探究气体等温变化的规律 1.状态参量研究气体性质时,常用气体的温度、体积、压强来描述气体的状态。
2.实验探究二、玻意耳定律1.内容一定质量的某种气体,在温度不变的情况下,压强与体积成反比。
2.公式pV=C或p1V1=p2V2。
3.条件气体的质量一定,温度不变。
4.气体等温变化的p -V图像气体的压强p随体积V的变化关系如图8-1-1所示,图线的形状为双曲线,它描述的是温度不变时的p -V关系,称为等温线。
一定质量的气体,不同温度下的等温线是不同的。
图8-1-11.自主思考——判一判(1)一定质量的气体压强跟体积成反比。
(×)(2)一定质量的气体压强跟体积成正比。
(×)(3)一定质量的气体在温度不变时,压强跟体积成反比。
(√)(4)在探究气体压强、体积、温度三个状态参量之间关系时采用控制变量法。
(√)(5)玻意耳定律适用于质量不变、温度变化的气体。
(×)(6)在公式pV=C中,C是一个与气体无关的参量。
(×)2.合作探究——议一议(1)用注射器对封闭气体进行等温变化的实验时,在改变封闭气体的体积时为什么要缓慢进行?提示:该实验的条件是气体的质量一定,温度不变,体积变化时封闭气体自身的温度会发生变化,为保证温度不变,应给封闭气体以足够的时间进行热交换,以保证气体的温度不变。
(2)玻意耳定律成立的条件是气体的温度不太低、压强不太大,那么为什么在压强很大、温度很低的情况下玻意耳定律就不成立了呢?提示:①在气体的温度不太低、压强不太大时,气体分子之间的距离很大,气体分子之间除碰撞外可以认为无作用力,并且气体分子本身的大小也可以忽略不计,这样由玻意耳定律计算得到的结果与实际的实验结果基本吻合,玻意耳定律成立。
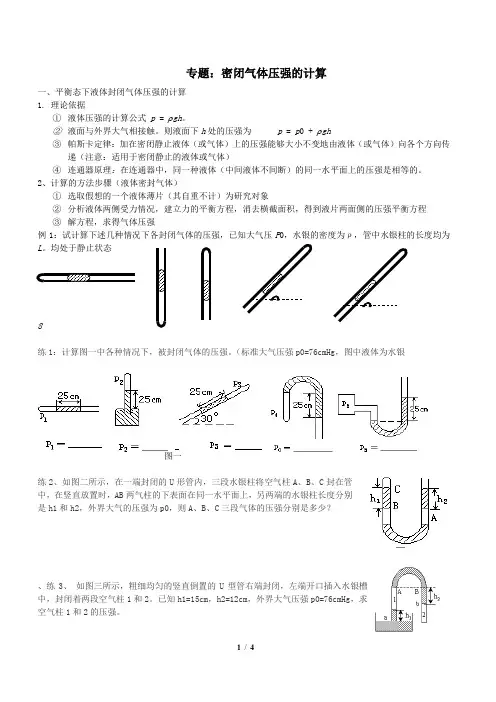
专题:密闭气体压强的计算一、平衡态下液体封闭气体压强的计算1. 理论依据①液体压强的计算公式p = ρgh。
②液面与外界大气相接触。
则液面下h处的压强为p = p0 + ρgh③帕斯卡定律:加在密闭静止液体(或气体)上的压强能够大小不变地由液体(或气体)向各个方向传递(注意:适用于密闭静止的液体或气体)④连通器原理:在连通器中,同一种液体(中间液体不间断)的同一水平面上的压强是相等的。
2、计算的方法步骤(液体密封气体)①选取假想的一个液体薄片(其自重不计)为研究对象②分析液体两侧受力情况,建立力的平衡方程,消去横截面积,得到液片两面侧的压强平衡方程③解方程,求得气体压强例1:试计算下述几种情况下各封闭气体的压强,已知大气压P 0,水银的密度为ρ,管中水银柱的长度均为L。
均处于静止状态θθ8练1:计算图一中各种情况下,被封闭气体的压强。
(标准大气压强p0=76cmHg,图中液体为水银图一练2、如图二所示,在一端封闭的U形管内,三段水银柱将空气柱A、B、C封在管中,在竖直放置时,AB两气柱的下表面在同一水平面上,另两端的水银柱长度分别是h1和h2,外界大气的压强为p0,则A、B、C三段气体的压强分别是多少?、练3、如图三所示,粗细均匀的竖直倒置的U型管右端封闭,左端开口插入水银槽中,封闭着两段空气柱1和2。
已知h1=15cm,h2=12cm,外界大气压强p0=76cmHg,求空气柱1和2的压强。
二、平衡态下活塞、气缸密闭气体压强的计算1. 解题的基本思路(1)对活塞(或气缸)进行受力分析,画出受力示意图;(2)列出活塞(或气缸)的平衡方程,求出未知量。
注意:不要忘记气缸底部和活塞外面的大气压。
例2 如图四所示,一个横截面积为S 的圆筒形容器竖直放置,金属圆板A 的上表面是水平的,下表面是倾斜的,下表面与水平面的夹角为θ,圆板的质量为M 。
不计圆板与容器内壁之间的摩擦。
若大气压强为P 0,则被圆板封闭在容器中的气体压强P 等于( ) A. P Mg S 0+cos θ B. P Mg S 0cos cos θθ+ C.P Mg S 02+cos θ D. P Mg S 0+图四练习4:三个长方体容器中被光滑的活塞封闭一定质量的气体。
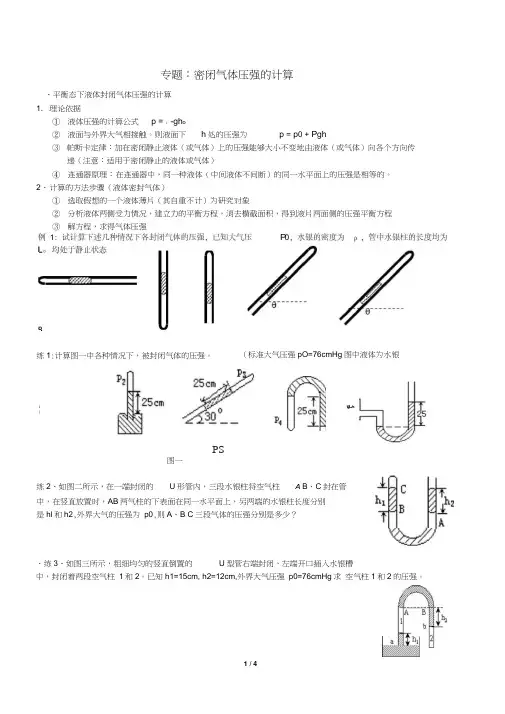
专题:密闭气体压强的计算、平衡态下液体封闭气体压强的计算1. 理论依据①液体压强的计算公式p = ;-gh o②液面与外界大气相接触。
则液面下h处的压强为p = p0 + Pgh③帕斯卡定律:加在密闭静止液体(或气体)上的压强能够大小不变地由液体(或气体)向各个方向传递(注意:适用于密闭静止的液体或气体)④连通器原理:在连通器中,同一种液体(中间液体不间断)的同一水平面上的压强是相等的。
2、计算的方法步骤(液体密封气体)①选取假想的一个液体薄片(其自重不计)为研究对象②分析液体两侧受力情况,建立力的平衡方程,消去横截面积,得到液片两面侧的压强平衡方程③解方程,求得气体压强PS图一练2、如图二所示,在一端封闭的U形管内,三段水银柱将空气柱A B、C封在管中,在竖直放置时,AB两气柱的下表面在同一水平面上,另两端的水银柱长度分别是hl和h2,外界大气的压强为p0,则A、B C三段气体的压强分别是多少?、练3、如图三所示,粗细均匀的竖直倒置的U型管右端封闭,左端开口插入水银槽中,封闭着两段空气柱1和2。
已知h1=15cm, h2=12cm,外界大气压强p0=76cmHg求空气柱1和2的压强。
练1:计算图一中各种情况下,被封闭气体的压强。
(标准大气压强pO=76cmHg图中液体为水银nr 5 P二、平衡态下活塞、气缸密闭气体压强的计算 1. 解题的基本思路(1)对活塞(或气缸)进行受力分析,画出受力示意图;(2 )列出活塞(或气缸)的平衡方程,求出未知量。
注意:不要忘记气缸底部和活塞外面的大气压。
例2如图四所示,一个横截面积为 S 的圆筒形容器竖直放置,金属圆板A 的上表面是水平的,下表面是倾斜的,下表面与水平面的夹角为 0,圆板的质量为 M 。
不计圆板与容器内壁之间的摩擦。
若大气压强为P o ,则被圆板封闭在容器中的气体压强P 等于()练习5、如图六所示,活塞质量为 m 缸套质量为 M 通过弹簧吊在天花板上,气缸内封住了一定质量的 空气,而活塞与缸套间无摩擦 ,活塞面积为S,则下列说法正确的是(P o 为大气压强)() A 、 内外空气对缸套的总作用力方向向上,大小为 Mg B 、 内外空气对缸套的总作用力方向向下,大小为 mg C 、 气缸内空气压强为 P o -Mg/S D 气缸内空气压强为 P o +mg/S练习6、所示,水平放置的气缸 A 和B 的活塞面积分别为 S a 和S b 且S a S b ,它们可以无摩擦地沿器壁自由滑 动,气缸内圭寸有气体。
8.1 气体的等温变化学习目标1.了解玻意耳定律的内容、表达式及适用条件。
2.了解p-V图象的物理意义。
重点:1.掌握玻意耳定律的内容和公式。
2.理解气体等温变化的p-V图象的物理意义。
难点:1.理解气体等温变化的p-V图象的物理意义。
2.会用玻意耳定律计算有关的问题。
知识点一、等温变化1.气体的状态和状态参量:用以描述气体宏观性质的物理量,叫状态参量。
对于一定质量的某种气体来说,描述其宏观性质的物理量有温度、体积、压强三个。
(1)体积:指气体分子所能达到的空间,即气体所能充满的容器的容积。
(2)温度:从宏观角度看表示物体的冷热程度。
从微观角度看,温度是物体分子热运动的平均动能的标志。
(3)压强:垂直作用于容器壁单位面积上的压力。
单位:帕Pa。
2.气体的状态由状态参量决定,对一定质量的气体来说,当三个状态参量都不变时,我们就说气体的状态一定,否则气体的状态就发生了变化。
对于一定质量的气体,压强、温度、体积三个状态参量中只有一个量变而其他量不变是不可能的,起码其中的两个量变或三个量都发生变化。
3.等温变化:一定质量的气体,在温度不变的条件下其压强与体积变化时的关系。
【题1】下列过程可能发生的是A.气体的温度变化,但压强、体积保持不变B.气体的温度、压强保持不变,而体积发生变化C.气体的温度保持不变,而压强、体积发生变化D.气体的温度、压强、体积都发生变化【答案】CD【解析】p、V、T三个量中,可以两个量发生变化,一个量恒定;也可以三个量同时发生变化;一个量变化的情况是不存在的,故C、D选项正确。
【题2】(多选)一定质量的气体,在等温变化过程中,下列物理量中发生改变的有A.分子的平均速率B.单位体积内的分子数C.气体的压强D.分子总数【答案】BC【解析】温度不变,对于一定质量的气体,分子的平均动能不变,分子的平均速率也不会变;但体积和压强可以发生变化,故选B、C。
知识点二、实验:探究等温变化的规律1.实验器材:如图所示,有铁架台,带压力表的注射器、铁夹等。
第2课时气体的等温变化[学习目标] 1.知道玻意耳定律的内容、表达式及适用条件.2.能运用玻意耳定律对有关问题进行分析、计算.玻意耳定律1.内容一定质量的某种气体,在温度不变的情况下,压强p与体积V成反比.2.公式pV=C或p1V1=p2V2.3.条件气体的质量一定,温度不变.1.判断下列说法的正误.(1)一定质量的气体,在温度不变时,压强跟体积成反比.(√)(2)公式pV=C中的C是常量,指当p、V变化时C的值不变.(√)(3)一定质量的某种气体等温变化的p-V图像是通过原点的倾斜直线.(×)2.一定质量的某种气体发生等温变化时,若体积增大了n倍,则压强变为原来的.答案1 n+1一、封闭气体压强的计算导学探究(1)如图1甲所示,C、D液面水平且等高,液体密度为ρ,重力加速度为g,其他条件已标于图上,试求封闭气体A的压强.(2)在图乙中,汽缸置于水平地面上,汽缸横截面积为S,活塞质量为m,汽缸与活塞之间无摩擦,设大气压强为p0,重力加速度为g,试求封闭气体的压强.图1答案 (1)同一水平液面C 、D 处压强相同,可得p A =p 0+ρgh .(2)以活塞为研究对象,受力分析如图所示,由平衡条件得mg +p 0S =pS则p =p 0+mg S. 知识深化1.取等压面法同种液体在同一深度向各个方向的压强相等,在连通器中,灵活选取等压面,利用同一液面压强相等求解气体压强.如图2甲所示,同一液面C 、D 两处压强相等,故p A =p 0+p h ;如图乙所示,M 、N 两处压强相等,从左侧管看有p B =p A +p h 2,从右侧管看,有p B =p 0+p h 1.图22.力平衡法选与封闭气体接触的活塞、汽缸或液体为研究对象进行受力分析,由平衡条件列式求气体压强.说明:容器加速运动时,可由牛顿第二定律列方程求解.如图3所示,活塞的质量为m ,缸套的质量为M ,通过弹簧静止吊在天花板上,汽缸内封住一定质量的气体,缸套和活塞间无摩擦,活塞横截面积为S ,大气压强为p 0,重力加速度为g ,则封闭气体的压强p 为( )图3A .p 0+Mg SB .p 0+(M +m )g SC .p 0-Mg S D.mg S答案 C解析 以缸套为研究对象,有pS +Mg =p 0S ,所以封闭气体的压强p =p 0-Mg S,故应选C. 如图4所示,竖直静止放置的U 形管,左端开口,右端封闭,管内有a 、b 两段水银柱,将A 、B 两段空气柱封闭在管内.已知水银柱a 长h 1为10 cm ,水银柱b 两个液面间的高度差h 2为5 cm ,大气压强为75 cmHg ,求空气柱A 、B 的压强分别是多少.图4答案 65 cmHg 60 cmHg解析 设管的横截面积为S ,选a 的下端面为参考液面,它受向下的压力为(p A +p h 1)S ,受向上的大气压力为p 0S ,由于系统处于静止状态,则(p A +p h 1)S =p 0S ,所以p A =p 0-p h 1=(75-10) cmHg =65 cmHg ,再选b 的左下端面为参考液面,由连通器原理知:液柱h 2的上表面处的压强等于p B ,则(p B +p h 2)S =p A S ,所以p B =p A -p h 2=(65-5) cmHg =60 cmHg.二、玻意耳定律导学探究 如图5所示,在一个恒温池中,一串串气泡由池底慢慢升到水面,有趣的是气泡在上升过程中,体积逐渐变大,到水面时就会破裂.问:图5(1)上升过程中,气泡内气体的压强如何改变?(2)气泡在上升过程中体积为何会变大?(3)为什么到达水面会破?答案 (1)变小.(2)由玻意耳定律pV =C 可知,压强变小,气体的体积增大.(3)内外压强不相等,气泡内压强大于外部压强.知识深化1.常量的意义p 1V 1=p 2V 2=C ,该常量C 与气体的种类、质量、温度有关,对一定质量的气体,温度越高,则常量C越大.2.应用玻意耳定律解题的一般步骤(1)确定研究对象,并判断是否满足玻意耳定律的条件.(2)确定初、末状态及状态参量(p1、V1;p2、V2).(3)根据玻意耳定律列方程求解.(注意统一单位)(4)注意分析隐含条件,作出必要的判断和说明.特别提醒确定气体压强或体积时,只要初、末状态的单位统一即可,没有必要都转换成国际单位制.如图6所示,在长为57 cm且一端封闭、另一端开口向上的竖直玻璃管内,用4 cm 高的水银柱封闭着51 cm长的气体,管内外气体的温度相同.现将水银从管侧壁缓慢地注入管中,直到水银面与管口相平.外界大气压强p0=76 cmHg,且温度不变.求此时管中封闭气体的压强.图6答案85 cmHg解析设玻璃管的横截面积为S,以玻璃管内封闭的气体为研究对象,初状态p1=p0+p h1=80 cmHg,V1=51 cm×S,末状态p2=p0+p h=(76+h) cmHg,V2=(57 cm-h)S,气体发生等温变化,由玻意耳定律得p1V1=p2V2,代入数据解得h=9 cm,则p2=85 cmHg.如图7所示,高为H的导热汽缸竖直固定在水平地面上,汽缸的横截面积为S,重力为G的“⊥”形活塞封闭着一定质量的气体,活塞离缸底高为h,现手持“⊥”形活塞上端,缓慢竖直上提活塞,当活塞上升到汽缸上端口时,求竖直上提的力F的大小.已知大气压强为p0,不考虑活塞与汽缸之间的摩擦及温度的变化,不计活塞及汽缸壁的厚度.图7答案 (H -h )(p 0S +G )H解析 以密闭气体为研究对象,初状态:压强p 1=p 0+G S,体积V 1=hS ,末状态:压强p 2=p 0+G -F S ,体积V 2=HS .由玻意耳定律得p 1V 1=p 2V 2,即⎝⎛⎭⎫p 0+G S hS =⎝⎛⎭⎫p 0+G -F S HS ,解得F =(H -h )(p 0S +G )H.1.(压强的计算)求图8中被封闭气体A 的压强.其中(1)、(2)、(3)图中的玻璃管内都装有水银,(4)图中的小玻璃管浸没在水中.大气压强p 0=76 cmHg.(p 0=1.01×105 Pa ,g =10 m/s 2,ρ水=1×103 kg/m 3)图8答案 (1)66 cmHg (2)71 cmHg (3)81 cmHg (4)1.13×105 Pa解析 (1)p A =p 0-p h =76 cmHg -10 cmHg =66 cmHg.(2)p A =p 0-p h =76 cmHg -10sin 30° cmHg =71 cmHg.(3)p B =p 0+p h 2=76 cmHg +10 cmHg =86 cmHg ,p A =p B -p h 1=86 cmHg -5 cmHg =81 cmHg.(4)p A =p 0+ρ水gh =1.01×105 Pa +1×103×10×1.2 Pa =1.13×105 Pa.2.(压强的计算)如图9所示,活塞质量为M ,上表面横截面积为S ,上表面水平,下表面与水平面成α角,摩擦不计,外界大气压为p 0,则被封闭气体的压强为(重力加速度为g )( )图9A.p 0-Mg cos αSB.p 0cos αMg SC .p 0-Mg SD.p 0-Mg cos 2αS答案 C解析 以活塞为研究对象,对活塞受力分析如图所示外界对活塞的压力为F =p 0S cos α, 由平衡条件有F cos α=Mg +pS ,解得p =p 0-Mg S,C 正确. 3.(玻意耳定律)(2020·吉林高二期末)如图10所示,马桶吸由皮吸和汽缸两部分组成,下方半球形皮吸空间的容积为1 000 cm 3,上方汽缸的长度为40 cm ,横截面积为50 cm 2.小明在试用时,用手柄将皮吸压在水平地面上,皮吸中气体的压强等于大气压.皮吸与地面及活塞与汽缸间密封完好不漏气,不考虑皮吸与汽缸的形状变化,环境温度保持不变,汽缸内薄活塞、连杆及手柄的质量忽略不计,已知大气压强p 0=1.0×105 Pa ,g =10 m/s 2.图10(1)若初始状态下活塞位于汽缸顶部,当活塞缓慢下压到汽缸底部时,求皮吸中气体的压强;(2)若初始状态下活塞位于汽缸底部,小明用竖直向上的力将活塞缓慢向上提起20 cm 高度保持静止,求此时小明作用力的大小.答案 (1)3.0×105 Pa (2)250 N解析 (1)以汽缸和皮吸内的气体为研究对象,初始状态下封闭气体的压强为p 0, 体积:V 1=1 000 cm 3+40×50 cm 3=3 000 cm 3当活塞下压到汽缸底部时,设封闭气体的压强为p2,体积为V2=1 000 cm3,由玻意耳定律:p0V1=p2V2解得:p2=3p0=3.0×105 Pa(2)以皮吸内的气体为研究对象,初始状态下封闭气体的压强为p0,体积为V2=1 000 cm3,活塞缓慢向上提起20 cm高度保持静止时,设小明作用力的大小为F,封闭气体的压强为p3,体积为:V3=1 000 cm3+20×50 cm3=2 000 cm3由玻意耳定律有:p0V2=p3V3又有:F+p3S=p0S解得:F=250 N.考点一气体压强的计算1.如图1所示,U形管封闭端内有一部分气体被水银封住,已知大气压强为p0,封闭部分气体的压强p(以汞柱为单位)为()图1A.p0+h2B.p0-h1C.p0-(h1+h2)D.p0+(h2-h1)答案 B解析选右边液面为研究对象,右边液面受到向下的大气压强p0,在相同高度的左边液面受到液柱h1向下的压强和液柱h1上面气体向下的压强p,根据连通器原理可知:p+h1=p0,所以p=p0-h1,B正确.2.(2020·莱州一中高二月考)如图2所示,内壁光滑的汽缸竖直放置在水平地面上,T形活塞的质量为M,下底面积为S,上底面积为4S,若大气压强为p0,重力加速度为g,则被封闭气体的压强p等于()图2A .4p 0+Mg SB .3p 0+Mg SC .p 0+Mg SD .条件不够,无法判断答案 C解析 以活塞为研究对象,活塞受重力、大气压力和封闭气体的支持力,根据受力平衡得Mg +p 0S =pS ,解得p =p 0+Mg S ,C 正确. 3.如图3所示,两端开口的足够长的均匀U 形管竖直放置,用两段汞柱封闭了一段空气柱.若在右端再注入2 cm 的汞柱,则封闭气体的压强为 cmHg ;若在左端再注入2 cm 的汞柱,则封闭气体的压强为 cmHg.(大气压为76 cmHg)图3答案 88 86考点二 玻意耳定律4.各种卡通形状的氢气球,受到孩子们的喜欢,小孩一不小心松手,氢气球会飞向天空,上升到一定高度会胀破,是因为( )A .球内氢气温度升高B .球内氢气压强增大C .球外空气压强减小D .以上说法均不正确答案 C解析 气球上升时,由于高空处空气稀薄,球外气体的压强减小,球内气体发生膨胀,到一定程度时,气球就会胀破,故C 正确.5.如图4所示,某种自动洗衣机进水时,与洗衣缸相连的细管中会封闭一定质量的空气,通过压力传感器感知管中的空气压力,从而控制进水量.设温度不变,洗衣缸内水位升高,则细管中被封闭的空气( )图4A .体积不变,压强变小B .体积变小,压强变大C .体积不变,压强变大D .体积变小,压强变小答案 B解析 由题图可知空气被封闭在细管内,洗衣缸内水位升高时,被封闭的空气体积减小,根据玻意耳定律可知,压强增大,B 选项正确.6.一定质量的气体,压强为3 atm ,保持温度不变,当压强减小了2 atm 时,体积变化了4 L ,则该气体原来的体积为( )A.43 L B .2 L C.83L D .3 L 答案 B解析 设该气体原来的体积为V 1,由玻意耳定律知压强减小时,气体体积增大,即3V 1=(3-2)·(V 1+4 L),解得V 1=2 L ,B 正确.7.一个气泡由湖面下20 m 深处缓慢上升到湖面下10 m 深处,不考虑气泡温度的变化,它的体积约变为原来体积的( )A .3倍B .2倍C .1.5倍 D.710答案 C解析 由于气泡缓慢上升,在湖面下20 m 处,气泡的压强p 1≈3 atm(1 atm 即1个标准大气压p 0=1.01×105 Pa ,湖面上的大气压强为1 atm);在湖面下10 m 深处,气泡的压强p 2≈2 atm.由玻意耳定律得p 1V 1=p 2V 2,因此V 2V 1=p 1p 2≈3 atm 2 atm =1.5,故C 正确.8.如图5所示,下端用橡皮管连接的两根粗细相同的玻璃管竖直放置,右管开口,左管内被封闭一段气体,水银面比右管低,现保持左管不动,为了使两管内水银面一样高,下面采取的措施可行的是( )图5A .减小外界气压B .从U 形管的右管向内加水银C .把U 形管的右管向上移动D .把U 形管的右管向下移动答案 D解析 为使两管内水银面一样高,左管中气体的压强减小,由玻意耳定律知,气体的体积要增大,右管必须向下移动,D 正确.9.质量为M 的汽缸口朝上静置于水平地面上(如图6甲),用质量为m 的活塞封闭一定量的气体(气体的质量忽略不计),活塞的横截面积为S .将汽缸倒扣水在水平地面上(如图乙),静止时活塞没有接触地面.已知大气压强为p 0,重力加速度为g ,不计一切摩擦,则下列分析正确的是( )图6A .甲图中,汽缸对地面的压力为MgB .甲图中,封闭气体压强为p 0+mg SC .乙图中,地面对汽缸的支持力为Mg +p 0SD .乙图中,封闭气体压强为p 0-Mg S答案 B解析 题图甲中对活塞受力分析可知,p 0S +mg =pS ,则封闭气体压强为p =p 0+mg S,选项B 正确;题图甲、乙中,对活塞和汽缸整体受力分析可知,地面对汽缸的支持力为Mg +mg ,则汽缸对地面的压力为Mg +mg ,选项A 、C 错误;题图乙中,对活塞受力分析可知,p ′S+mg =p 0S ,则封闭气体压强为p ′=p 0-mg S,选项D 错误. 10.(多选)(2021·辽宁沈阳市高二期中)如图7所示,两端开口的均匀玻璃管竖直插入水根槽中,管中有一段高为h 1的水银柱封闭一定质量的气体,这时管下端开口处内、外水银面高度差为h 2,若保持环境温度不变,当外界压强增大时,下列分析正确的是( )图7A.h2变长B.h2不变C.水银柱上升D.水银柱下降答案BD解析对于管内封闭的气体,其压强为p=p0+ρ水银gh1也可以有p=p0+ρ水银gh2则知h1=h2h1不变则h2不变.当外界压强增大时,管内封闭气体压强p增大,根据玻意耳定律pV=C可以知道气体的体积减小,则水银柱下降.故选B、D.11.(2020·西安中学高二期末)粗细均匀的U形管中装有水银,左管上端开口与大气相连,右管上端封闭,如图8所示.开始时两管内水银柱等高,两管内空气柱长均为l=90 cm,此时两管内空气柱温度均为27 ℃,外界大气压为p0=76 cmHg.现在左管上端开口处缓慢注入水银压缩空气柱,直至右管内水银面上升14 cm,在注入水银过程中,左管内温度缓慢下降到-23 ℃,右管内温度保持在27 ℃.求:图8(1)注入水银柱的长度;(2)左管注入的水银柱上表面离左管开口的距离.答案(1)42 cm(2)62 cm解析(1)只对右管封闭气体研究,发生了等温变化p1V1=p2V2即76×90S=p2(90-14)S解得p2=90 cmHg故注入水银柱的长度L=28 cm+(90-76) cm=42 cm(2)左管注入的水银柱上表面离左管开口的距离h=(90+14) cm-42 cm=62 cm.12.(多选)如图9所示,内径均匀、两端开口的V形管,B支管竖直插入水银槽中,A支管与B支管之间的夹角为θ,A支管中有一段长为h的水银柱保持静止,下列说法中正确的是()图9A.B管内水银面比管外水银面高hB.B管内水银面比管外水银面高h cos θC.B管内水银面比管外水银面低h cos θD.管内封闭气体的压强比大气压强小h cos θ高的水银柱产生的压强答案BD解析以A管中的水银柱为研究对象,则有pS+ρ水银h cos θ·S=p0S,管内封闭气体压强p=p0-ρ水银h cos θ,显然p<p0,且B管内水银面要比管外水银面高h cos θ,故B、D正确.13.如图10,玻璃管内封闭了一段气体,气柱长度为l,管内外水银面高度差为h.若温度保持不变,把玻璃管稍向上提起一段距离,则()图10A.h、l均变大B.h、l均变小C.h变大,l变小D.h变小,l变大答案 A解析水银柱产生的压强加上封闭气体产生的压强等于外界大气压.如果将玻璃管向上提,假设水银柱不动,则管内水银柱上方气体的体积增大,因为温度保持不变,所以压强减小,而此时外界的大气压不变,根据上述等量关系,管内水银柱的压强须增大才能重新平衡,故管内水银柱的高度增大,故选A.。
高二物理理想气体状态方程、气体压强的计算知识精讲气体的体积、压强、温度间的关系,气体分子运动的特点,气体压强的微观意义(A 级要求)。
这期复习内容比高考要求要高,多讲理想气体状态方程,气体压强的计算。
求封闭气体的压强,本质还是力学问题,求解思路一般以被封闭气体的液柱或活塞为研究对象,进行受力分析,再利用平衡条件或牛顿第二定律列方程求解。
在用气态方程解决多部分气体或多过程问题时,要先隔离各部分气体,确定每部分气体的多个不同状态、及状态参量,再找出体积或压强联系,然后联立方程求解。
一. 气体的状态参量:1. 体积V :描述气体的几何参量宏观角度:气体没有固定的体积,通常说气体体积是指一定质量气体所占据的容器的容积。
由于气体分子之间有间隙,气体体积并不是气体分子体积的总和。
微观角度:气体分子做无规则热运动所能到达空间。
2. 温度(T 和t ):气体的热学参量宏观意义:表示物体冷热程度,决定热传递过程中内能传递的数量与方向。
微观意义:是大量分子无规则热运动平均动能的标志,反映大量分子无规则热运动的剧烈程度。
数值表示法:(1)摄氏温标t :单位℃。
(2)热力学温标T :单位K ,把-273℃作为0K 。
(3)两种温标关系:T t =+273就每一度大小来说,热力学温度和摄氏温度相等∆∆T t =,只是零值的起点不同而已。
(4)绝对零度0K 是低温的极限,不可能达到。
3. 压强:描述气体的力学参量。
宏观意义:气体作用在器壁单位面积上的压力,大小取决于气体的密度和温度。
微观意义:是由大量气体分子无规则热运动对器壁的碰撞产生的,大小取决于单位体积内的分子数和分子平均速率。
单位:atm Pa cmHg mmHg ,,, 1760101105atm mmHg Pa ==⨯.4. 三参量关系:一定质量的气体,p 和T 、V 有关,只有一个状态,参量改变是不可能的,至少两个或三个参量同时改变。
二. 理想气体状态方程:1. 理想气体:理想气体是一种理想化模型,指能严格遵守三个实验定律的气体,气体分子间无作用力,分子势能为零。
高中物理大气压强公式
大气压强公式:P=ρgh
p表示:压强,单位:帕斯卡(pa),ρ表示:液体密度,单位:千克每立方米(kg/m³),g表示:重力加速度,g=9.8N/kg,h表示:深度,单位:米(m)。
大气压强不但随高度变化,在同一地点也不是固定不变的,通常把1.01325×10^5Pa的大气压强叫做标准大气压强。
它相当于760mm水银柱所产生的压强。
标准大气压也可以叫做760mm水银柱大气压。
标准大气压强的值在一般计算中常取1.01×10^5Pa(101KPa),在粗略计算中还可以取作10^5Pa(100KPa)。
大气压强:
1、大气压强是指地球上某个位置的空气产生的压强,地球表面的空气受到重力作用,由此而产生了大气压强。
2、气体和液体都具有流动性,它们的压强有相似之处、大气压向各个方向都有,在同一位置各个方向的大气压强相等。
但是由于大气的密度不是均匀的,所以大气压强的计算不能应用液体压强公式。
3、被密封在某种容器中的气体,其压强是大量的做无规则运动的气体分子对容器壁不断碰撞而产生的。
它的大小不是由被封闭气体的重力所决定的。
专题:密闭气体压强的计算一、平衡态下液体封闭气体压强的计算1.理论依据① 液体压强的计算公式p =?gh 。
② 液面与外界大气相接触。
则液面下h 处的压强为p =p 0+?gh③ 帕斯卡定律:加在密闭静止液体(或气体)上的压强能够大小不变地由液体(或气体)向各个方向传递(注意:适用于密闭静止的液体或气体)④ 连通器原理:在连通器中,同一种液体(中间液体不间断)的同一水平面上的压强是相等的。
下表A.P Mg S 0+cos θ B.P Mg S 0cos cos θθ+ C.P Mg S 02+cos θD.P Mg S 0+ 图四练习4:三个长方体容器中被光滑的活塞封闭一定质量的气体。
如图五所示,M 为重物质量,F 是外力,p0为大气压,S 为活塞面积,G 为活塞重,则压强各为:练习5、如图六所示,活塞质量为m ,缸套质量为M ,通过弹簧吊在天花板上,气缸内封住了一定质量的空气,而活塞与缸套间无摩擦,活塞面积为S ,则下列说法正确的是(P 0为大气压强)()A 、内外空气对缸套的总作用力方向向上,大小为MgB 、内外空气对缸套的总作用力方向向下,大小为mgC 、气缸内空气压强为P 0-Mg/SD 、气缸内空气压强为P 0+mg/S练习6、所示,水平放置的气缸A 和B 的活塞面积分别为S S a b 和且S S a b >,它们可以无摩擦地沿器壁自由滑动,气缸内封有气体。
当活塞处于平衡状态时,气缸A 、B 内气体的压强分别为P P a b 和(大气压不为零),则下列正确的是()A.P a C.P a 1. (1析;(22.典例例3上,()。
练7面积为S ,若在活塞上加一1.温度不变,试管截面积为s ,水银密度为ρ).2.如图所示,水平放置的一根玻璃管和几个竖直放置的U 形管内都有一段水银柱,封闭端里有一定质量的气体,图(a)中的水银柱长度和图(b)、(c)、(d)中U 形管两臂内水银柱高度差均为h=10cm,外界大气压强p 0=76cmHg,则四部分气体的压强分别为p a =________cmHg,p b =__________cmHg,p c =_______cmHg,p d =_________cmHg.3如图所示,两端开口的U 形管内有两段水柱AB 、CD 封住一段空气柱BC ,已知CD 高为1h ,AB 高度差为2h ,大气压强为0p 。
高中物理封闭气体压强的计算公司内部档案编码:[OPPTR-OPPT28-OPPTL98-难点突破:用气体实验定律解题的思路1.基本解题思路(1)选取研究对象:它可以是由两个或多个物体组成的系统,也可以是全部气体和某一部分气体(状态变化时质量必须一定).(2)确定状态参量:找出状态变化前后的p、V、T数值或表达式.(3)认识变化过程:除题设条件已指明外,常需通过研究对象跟周围环境的相互关系来确定.(4)列出相关方程.封闭气体压强的计算1.系统处于平衡状态的气体压强的计算方法(1)液体封闭的气体压强的确定①平衡法:选与气体接触的液柱为研究对象进行受力分析,利用它的受力平衡,求出气体的压强.②取等压面法:根据同种液体在同一水平液面处压强相等,在连通器内灵活选取等压面,由两侧压强相等建立方程求出压强.液体内部深度为h 处的总压强p =p 0+ρgh ,例如,图中同一水平液面C 、D 处压强相等,则p A =p 0+ρgh .(2)固体(活塞或汽缸)封闭的气体压强的确定:由于该固体必定受到被封闭气体的压力,可通过对该固体进行受力分析,由平衡条件建立方程来找出气体压强与其他各力的关系.2.加速运动系统中封闭气体压强的计算方法一般选与气体接触的液柱或活塞、汽缸为研究对象,进行受力分析,利用牛顿第二定律列方程求出封闭气体的压强.如图所示,当竖直放置的玻璃管向上加速时,对液柱受力分析有:pS -p 0S -mg =ma ,S 为玻璃管横截面积,得p =p 0+S m (g +a ).3.分析压强时的注意点(1)气体压强与大气压强不同,大气压强由于重力而产生,随高度增大而减小,气体压强是由大量气体分子频繁碰撞器壁而产生的,大小不随高度而变化;封闭气体对器壁的压强处处相等.(2)求解液体内部深度为h 处的总压强时,不要忘记液面上方气体的压强.用气体实验定律解题的思路1.基本解题思路(1)选取研究对象:它可以是由两个或多个物体组成的系统,也可以是全部气体和某一部分气体(状态变化时质量必须一定).(2)确定状态参量:找出状态变化前后的p、V、T数值或表达式.(3)认识变化过程:除题设条件已指明外,常需通过研究对象跟周围环境的相互关系来确定.(4)列出相关方程.2.对两部分气体的状态变化问题总结多个系统相互联系的定质量气体问题,往往以压强建立起系统间的关系,各系统独立进行状态分析,要确定每个研究对象的变化性质,分别应用相应的实验定律,并充分应用各研究对象之间的压强、体积、温度等量的有效关联.若活塞可自由移动,一般要根据活塞平衡确定两部分气体的压强关系.变质量气体问题的分析方法这类问题的关键是巧妙地选择研究对象,把变质量转化为定质量问题.常见变质量气体问题有:(1)打气问题:选择原有气体和即将充入的气体作为研究对象,就可把充气过程中的气体质量变化问题转化为定质量气体的状态变化问题.(2)抽气问题:将每次抽气过程中抽出的气体和剩余气体作为研究对象,质量不变,故抽气过程可以看成是等温膨胀过程.(3)灌气问题:把大容器中的剩余气体和多个小容器中的气体整体作为研究对象,可将变质量问题转化为定质量问题.(4)漏气问题:选容器内剩余气体和漏出气体整体作为研究对象,便可使问题变成一定质量气体的状态变化,可用理想气体的状态方程求解.液柱(活塞)的移动问题的分析方法此类问题的特点是气体的状态参量p 、V 、T 都发生了变化,直接判断液柱或活塞的移动方向比较困难,通常先进行气体状态的假设,然后应用查理定律可以简单地求解.其一般思路为:(1)先假设液柱或活塞不发生移动,两部分气体均做等容变化.(2)对两部分气体分别应用查理定律,求出每部分气体压强的变化量Δp =T ΔTp ,并加以比较.①如果液柱或活塞两端的横截面积相等,则若Δp 均大于零,意味着两部分气体的压强均增大,则液柱或活塞向Δp 值较小的一方移动;若Δp 均小于零,意味着两部分气体的压强均减小,则液柱或活塞向压强减小量较大的一方(即|Δp |较大的一方)移动;若Δp 相等,则液柱或活塞不移动.②如果液柱或活塞两端的横截面积不相等,则应考虑液柱或活塞两端的受力变化(ΔpS),若Δp均大于零,则液柱或活塞向ΔpS较小的一方移动;若Δp均小于零,则液柱或活塞向|ΔpS|较大的一方移动;若ΔpS相等,则液柱或活塞不移动.气体图象问题的分析要点对气体状态变化图象的理解应注意两点:(1)图象上的一个点表示一定质量气体的一个平衡状态,它对应着三个状态参量;图象上的某一条直线或曲线表示一定质量气体状态变化的一个过程.(2)熟练掌握同一过程的p—V、V—T、p—T图象之间的转化,必要时能作出辅助的状态变化图线.如在V—T或p—T图象中,比较两个状态的压强或体积大小,可以用这两个状态到原点连线的斜率大小来判断.斜率越大,压强或体积越小;斜率越小,压强或体积越大.计算气体压强的常用方法气体压强的计算问题,可以转化为力学问题进行处理。
具体如下:参考液面法(1)主要依据是液体静力学知识:①静止(或匀速)液面下深h处的压强为。
注意h 是液体的竖直深度。
②若静止(或匀速)液面与外界大气接触,则液面下深h处的压强为,为外界大气压强。
③帕斯卡定律:加在密闭静止液体(或气体)上的压强能够大小不变地由液体(或气体)向各个方向传递。
④连通器原理:在连通器中,同一种液体(中间液体不间断)的同一平面上时压强是相等的。
(2)计算压强的步骤:①选取假想的一个液体薄片(不计自身重力)为研究对象;②分析液片两侧受力情况,建立平衡方程,消去横截面积,得到薄片两侧的压强平衡方程;③解方程,求得气体压强。
【典例】如图(a)所示,水平放置的均匀玻璃管内,一段长为h=25 cm的水银柱封闭了长为L0=20 cm、温度为t0=27 ℃的理想气体,大气压强p0=75cmHg,将玻璃管缓慢地转过90°角,使它开口向上,并将封闭端浸入热水中,如图(b)所示,待稳定后,测得玻璃管内封闭气柱的长度L1= cm。
问:(1)此时管内封闭气体的温度t1是多少(2)若用薄塞将管口封闭,此时水银上部封闭气柱的长度为L2=10 cm。
保持水银上部封闭气体的温度不变,对水银下面的气体加热,当上面气柱长度的减少量ΔL= cm时,下面气体的温度是多少1.如图所示,玻璃管A上端封闭,B上端开口且足够长,两管下端用橡皮管连接起来,A管上端被一段水银柱封闭了一段长为6 cm的气体,外界大气压为75 cmHg,左右两水银面高度差为5 cm,温度为t1=27℃。
(1)保持温度不变,上下移动B管,使A管中气体长度变为5 cm,稳定后的压强为多少(2)稳定后保持B不动,为了让A管中气体体积回复到6 cm,则温度应变为多少2.如图乙所示,两端开口、粗细均匀的足够长玻璃管插在大水银槽中,管的上部有一定长度的水银柱,两段空气柱被封闭在左右两侧的竖直管中。
开启上部连通左右水银的阀门A ,当温度为300 K,平衡时水银柱的位置如图(h1=h2=5 cm,L1=50 cm),大气压为75 cmHg。
求:(1)右管内气柱的长度L2。
(2)关闭阀门A,当温度升至405 K时,左侧竖直管内气柱的长度L3(大气压强保持不变)。
平衡条件法对于用固体(或活塞)封闭静止容器内的气体,要求气体的压强,可对固体(或活塞)进行受力分析,然后根据平衡条件列式求解。
【典例】如图所示,透热的气缸内封有一定质量的理想气体,缸体质量M=200 kg,活塞质量m=10 kg,活塞面积S=100 cm2,活塞与气缸壁无摩擦且不漏气,此时缸内气体的温度为27 ℃,活塞刚好位于气缸正中间,整个装置都静止,已知大气压恒为p0=×105 Pa,重力加速度为g=10 m/s2,,求:(1)缸内气体的压强p1;(2)缸内气体的温度升高到多少摄氏度时,活塞恰好会静止在气缸缸口AB处1.圆柱形气缸固定放置在水平地面上,其截面如图所示,用硬杆连接的两个活塞在气缸的左右两侧分别封闭了两部分气体A、B,活塞可自由移动。
两侧的横截面积S A<S B,两活塞间的C部分可通过阀门K 实现与外界的连通或断开。
开始时两边气体温度相同,活塞处于平衡状态。
现使两边气体缓慢升高相同的温度,重新平衡后两边气体压强的增量分别为△p A和△p B。
下列判断正确的是A.若C部分是真空,则在温度升高的过程中活塞始终不动B.若C部分是真空,则最终平衡时△p A=△p BC.若C部分与外界大气连通,则活塞向右移D.若C部分与外界大气连通,则最终平衡时△p A>△p B2.两端开口、内表面光滑的U形管处于竖直平面内,如图所示质量均为m=10 kg的活塞A、B在外力作用下静止于左右管中同一高度h 处,将管内空气封闭,此时管内外空气的压强均为p0=×105 Pa,左管和水平管横截面积S1=10 cm2,右管横截面积S2 =20 cm2,水平管长为3h,现撤去外力让活塞在管中下降,求两活塞稳定后所处的高度。
(活塞厚度均大于水平管直径,管内气体初末状态温度相同,g取10 m/s2)动力学法当与气体相连的系统加速运动时,要求气体的压强,可以选择与气体相连的合适的研究对象(如活塞、气缸等),对其进行受力分析,然后根据牛顿第二定律列动力学方程进行求解。
在对系统进行分析时,可针对具体情况选用整体法或隔离法。
【典例】如图,在沿水平方向以加速度a=1 m/s2匀加速行驶的车厢中,斜靠着与水平方向成α=37°角的气缸。
一质量m=2 kg、横截面积S=10 cm2的光滑活塞,将一定质量的气体封闭在气缸内,并与气缸保持相对静止。
已知大气压强为p0=1×105 Pa。
下列说法正确的是A.气缸对活塞的弹力为16 NB.气缸对活塞的弹力为 NC.气缸内气体的压强为×105 PaD.气缸内气体的压强为×105 Pa1.高空试验火箭起飞前,仪器舱内气体的压强p0=1 atm,温度t=27 ℃。
在火箭竖直上升的过程中,加速度的大小等于重力加速度g,仪器舱内水银气压计的读数为p=,已知仪器舱是密封的,那么,该过程中舱里的温度是多少2.如图所示,倾斜的玻璃管长L=57 cm,一端封闭、另一端开口向上,倾角θ=30°。
有4 cm长的水银柱封闭着45 cm长的理想气体,管内外气体的温度均为33 ℃,大气压强p0=76 cmHg。
(1)将璃管缓慢加热,若有2 cm水银柱逸出,则温度需要升高到多少(2)若让玻璃管沿倾斜方向向上以a=2 m/s2做匀加速直线运动,则空气柱长度为多少。