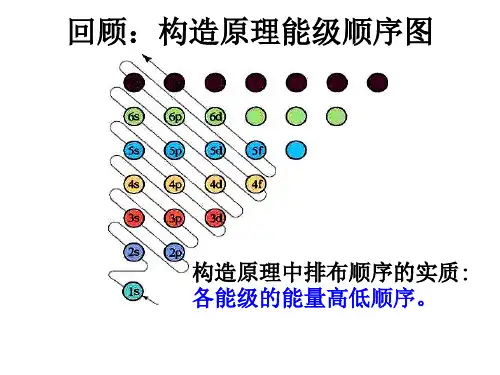
能量最低原理电子云原子轨道
- 格式:ppt
- 大小:1.57 MB
- 文档页数:20

《2021-2022学年高二化学同步精品学案(新人教版选择性必修2)》第一章原子结构与性质第一节原子结构第2课时电子云与原子轨道泡利原理、洪特规则、能量最低原理四.电子云与原子轨道由于核外电子的概率密度分布看起来像一片云雾,因而被形象地称为电子云。
,注:(1)同一能层中,p能级的原子轨道空间伸展方向不同但原子轨道的能量相同;(2)人们把同一能级的几个能量相同的原子轨道称为简并轨道。
【思考讨论】分析同一原子的s电子的电子云轮廓图,请解释为什么同一原子的能层越高,s电子云半径越大?同一原子的s电子的电子云轮廓图【回顾与展望】各能级所含有原子轨道数目能级符号 n s n p n d n f 最多电子数 能级轨道数目能层轨道数目电子层为n 的状态含有 个原子轨道。
五、泡利原理、洪特规则、能量最低原理:基态电子排布遵循的三个原理1、电子的运动状态⎩⎪⎨⎪⎧空间运动状态:一个空间运动状态即一个原子轨道自旋状态:一个原子轨道内的两个电子有顺时针和逆时针两种取向【深刻理解】电子自旋(1)内在属性:自旋是微观粒子普遍存在的一种如同电荷、质量一样的内在属性; (2)两种取向:电子自旋在空间有顺时针和逆时针两种取向,简称 ; (3)表示方法:常用上下箭头(↑和↓)表示自旋相反的电子。
2、轨道表示式(电子排布图)(1)用方框(或圆圈)表示原子轨道,能量相同的原子轨道(简并轨道)的方框相连;(2)箭头表示一种自旋状态的电子,“↑↓”称 ,“↑”或“↓”称 (或称未成对电子); (3)能直观反映出电子的排布情况及电子的自旋状态。
【资料卡片】常见原子的电子排布图原子类别 电子排布式电子排布图 氢原子 1s 1 1s↑ 氦原子1s 21s ↑↓ 氮原子 1s 22s 22p 31s ↑↓ 2s ↑↓ 2p ↑ ↑ ↑ 氧原子 1s 22s 22p 41s ↑↓ 2s ↑↓ 2p ↑↓ ↑ ↑ 钠原子1s 22s 22p 63s 11s ↑↓ 2s ↑↓ 2p ↑↓ ↑↓ ↑↓ 3s ↑〔思考讨论〕(1)在钠原子中,有 种空间运动状态,有 种运动状态不同的电子。


第2课时能量最低原理电子云与原子轨道1.了解能量最低原理,知道基态与激发态。
2.知道原子核外电子在一定条件下会发生跃迁产生原子光谱。
3.了解原子核外电子的运动状态,知道电子云和原子轨道,掌握泡利原理和洪特规则。
(重难点)[基础·初探]1.能量最低原理原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,简称能量最低原理。
2.基态原子与激发态原子(1)基态原子:处于最低能量的原子。
(2)激发态原子:基态原子的电子吸收能量后,电子跃迁到较高能级,变成激发态原子。
(3)基态、激发态相互转化的能量变化3.光谱与光谱分析(1)光谱形成原因不同元素的原子发生跃迁时会吸收或释放不同的光。
(2)光谱分类(3)光谱分析在现代化学中,利用原子光谱上的特征谱线来鉴定元素的分析方法。
[探究·升华][思考探究](1)在国庆节、元旦、春节,我们经常放焰火来庆祝,请你思考这与原子结构有什么关系呢?【提示】这与原子核外电子发生跃迁释放能量有关。
(2)对充有氖气的霓虹灯管通电,灯管发出红色光。
产生这一现象的主要原因是什么?【提示】在电流作用下,基态氖原子的电子吸收能量跃迁到较高的能级,变为激发态原子,这一过程要吸收能量,不会发出红色光;而电子从较高能量的激发态跃迁到较低能量的激发态或基态原子时,将释放能量,从而产生红光。
[认知升华]1.光(辐射)是电子释放能量的重要形式之一。
电子从较高能量的激发态跃迁到较低能量的激发态乃至基态时,将以光的形式释放能量。
2.日常生活中看到的灯光、激光、焰火等可见光,都与原子核外电子发生跃迁释放能量有关。
[题组·冲关]题组1基态、激发态1.下列关于同一原子中的基态和激发态说法中,正确的是()A.基态时的能量比激发态时高B.激发态时比较稳定C.由基态转化为激发态过程中吸收能量D.电子仅在激发态跃迁到基态时才会产生原子光谱【解析】激发态时能量较高,较不稳定,A、B不正确。

第02讲电子云与原子轨道泡利原理、洪特规则、能量最低原理考点导航知识精讲知识点一:一、电子云与原子轨道1.电子云由于核外电子的看起来像一片云雾,因而被形象地称作电子云。
2.电子云轮廓图为了表示电子云轮廓的形状,对核外电子的有一个形象化的简便描述。
把电子在原子核外空间出现概率P=的空间圈出来,即电子云轮廓图。
3.原子轨道(1)定义:量子力学把电子在原子核外的称为一个原子轨道。
(2)形状①s电子的原子轨道呈形,能层序数越大,原子轨道的半径越。
②除s电子云外,其他电子云轮廓图都不是球形的。
例如,p电子云轮廓图是呈状的。
(3)各能级所含有原子轨道数目能级符号n s n p n d n f轨道数目微点拨原子轨道与能层序数的关系①不同能层的同种能级的原子轨道形状相同,只是半径不同。
能层序数n越大,原子轨道的半径越大。
如:同一原子的s电子的电子云轮廓图②s能级只有1个原子轨道。
p能级有3个原子轨道,它们互相垂直,分别以p x、p y、p z表示。
在同一能层中p x、p y、p z的能量相同。
【即学即练1】1.以下关于原子核外电子的叙述正确的是A.在同一原子轨道上的不同电子的电子云是相同的B.电子云的小黑点表示电子曾在该处出现过一次C.所有原子的电子云都是球形的D.原子核外电子的运动无法作规律性描述2.下列有关电子云和原子轨道的说法正确的是A.s、p、d能级所含原子轨道数分别为1,3,5B.s能级的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动C.p能级的原子轨道呈纺锤形,随着能层的增加,p能级原子轨道数也增多D.原子核外的电子像云雾一样笼罩在原子核周围,故称电子云3.下列关于电子云和原子轨道的说法中正确的是A.电子云图中一个小点表示1个自由运动的电子B.s电子云呈球形,表示电子绕原子核做圆周运动C.电子云图中的小点密度大,说明该原子核外空间电子数目多D.ns能级的轨道呈球形,有无数对称轴4.下列说法正确的是A.原子核外的电子像云雾一样笼罩在原子核周围,故称电子云B.s能级的电子云呈球形,处在该轨道上的电子只能在球壳内运动C.p电子云轮廓图呈哑铃形,在空间有两个伸展方向D.2s轨道与1s轨道都是球形,但2s轨道的球形半径更大知识点二:二、泡利原理、洪特规则、能量最低原理1.电子自旋与泡利原理(1)自旋是微观粒子普遍存在的一种如同电荷、质量一样的内在属性,电子自旋在空间有和两种取向,简称自旋相反,常用上下箭头(↑和↓)表示自旋相反的电子。


第2课时 原子的基态与激发态、电子云与原子轨道[目标定位] 1.知道原子的基态、激发态与光谱之间的关系。
2.了解核外电子运动、电子云轮廓图和核外电子运动的状态。
一、能量最低原理和原子的基态与激发态1.原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,简称能量最低原理。
(1)处于最低能量的原子叫做基态原子。
(2)当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子。
(3)基态、激发态相互间转化的能量变化基态原子 吸收能量释放能量,主要形式为光激发态原子 2.不同元素的原子发生跃迁时会吸收或释放不同的光,若用光谱仪摄取各种元素的电子的吸收光谱或发射光谱,则可确立某种元素的原子,这些光谱总称原子光谱。
(1)玻尔原子结构模型证明氢原子光谱为线状光谱。
(2)氢原子光谱为线状光谱,多电子原子光谱比较复杂。
3.可见光,如灯光、霓虹灯光、激光、焰火……都与原子核外电子发生跃迁释放能量有关。
(1)基态原子电子按照构造原理排布(即电子优先排布在能量最低的能级里,然后依次排布在能量逐渐升高的能级里),会使整个原子的能量处于最低状态,此时为基态原子。
(2)光谱分析不同元素的原子光谱都是特定的,在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析。
1.下列说法正确的是( )A .自然界中的所有原子都处于基态B .同一原子处于激发态时的能量一定高于基态时的能量C.无论原子种类是否相同,基态原子的能量总是低于激发态原子的能量D.激发态原子的能量较高,极易失去电子,表现出较强的还原性答案 B解析处于最低能量的原子叫做基态原子。
电子由较低能级向较高能级跃迁,叫激发。
激发态原子的能量只是比原来基态原子的能量高。
如果电子仅在内层激发,电子未获得足够的能量,不会失去。
2.对充有氖气的霓虹灯管通电,灯管发出红色光。
产生这一现象的主要原因是() A.电子由激发态向基态跃迁时以光的形式释放能量B.电子由基态向激发态跃迁时吸收除红光以外的光线C.氖原子获得电子后转变成发出红光的物质D.在电流的作用下,氖原子与构成灯管的物质发生反应答案 A解析解答该题的关键是明确基态原子与激发态原子的相互转化及其转化过程中的能量变化及现象。

第一章原子结构与性质第一节原子结构狂做03 电子云与原子轨道泡利原理与洪特规则能量最低原理1.图①和图②分别是1s电子的概率密度分布图和电子云轮廓图。
下列认识正确的是( )A.图①中的每个小黑点表示1个电子B.图②表明1s电子云呈球形,有无数条对称轴C.图②表示1s电子只能在球体内出现D.不同能层的s电子云的半径相等【答案】B【分析】电子的概率密度分布图是用小黑点形象地描述电子在原子核外空间各处出现的概率;电子云轮廓图是按某一标准(如出现概率为90%)将空间圈出来形成的图形。
【详解】A.1s能级只有1个原子轨道,最多排2个电子,所以图①中的每个小黑点表示1个电子是错误的,小黑点的作用是通过其疏密来形象地描述电子在原子核外空间各处出现的概率,A选项错误;B.由图②可知,1s电子云轮廓图呈球形,球形对称图形有无数条对称轴,B选项正确;C.1s电子电子云轮廓图为球形,代表1s电子出现概率大的区域呈球形对称,但1s电子也可能在其它区域出现,只是出现的概率小,C选项错误;D.能层越大,s电子云的半径越大,D选项错误;答案选B。
【点睛】电子云中的小黑点:电子云中,小黑点不是电子本身。
电子云中的小黑点是电子在原子核外出现的概率密度的形象描述。
小黑点越密,表明概率密度越大。
2.描述硅原子核外电子运动说法错误的是A.有4种不同的伸展方向B.有14种不同运动状态的电子C.有5种不同能量的电子D.有5种不同的空间运动状态【答案】D【详解】A.Si原子的核外电子排布式是1s22s22p63s23p2,电子占据的是s、p能级,s能级有1个轨道,是球形,p能级有3个轨道,所以Si原子核外电子由4种不同的伸展方向,A正确;B.Si原子核外有14个电子,每个电子的运动状态都不相同,因此有14种不同运动状态的电子,B正确;C.根据核外电子的排布式可知,Si原子的核外电子占据5个能级,所以有5种不同能量的电子,C正确;D.s能级有1个轨道,p能级有3个轨道,Si原子的核外电子轨道数为8,因此有8种不同的空间运动状态,D错误;答案选D。

第一章原子结构与性质第一节原子结构第二课时电子云与原子轨道泡利原理、洪特规则、能量最低原理【必备知识基础练】1.下列原子或离子核外电子排布式不属于基态排布的是()A.Na:1s22s22p53s2B.S2-:1s22s22p63s23p6C.N:1s22s22p3D.P:1s22s22p63s23p3【答案】A【解析】根据能量最低原理,基态Na原子的电子排布式应为1s22s22p63s1,故A项不是基态Na原子的电子排布式,故选A。
2.下列说法正确的是()A.每个能层s能级的原子轨道的形状均相同,能层序数越大,轨道半径越大,电子能量越高B.原子核外电子云是核外电子运动后留下的痕迹C.教材中说“核外电子的概率密度分布看起来像一片云雾,因而被形象地称作电子云”,这说明原子核外电子云是实际存在的D.每个能层都有p能级,p能级都有3个原子轨道【答案】A【解析】s能级的原子轨道的形状都是球形的,且能层序数越大,轨道半径也越大,电子能量越高,A正确;电子云是用小点的疏密来表示空间电子出现的概率密度大小的一种图形,B错误;“核外电子的概率密度分布看起来像一片云雾,因而被形象地称作电子云”,但电子云不是实际存在的,C错误;第一能层没有p能级,D错误。
3.将n d能级中的电子排布成,而不排布成,其最直接的根据是()A.能量最低原理B.泡利原理C.构造原理D.洪特规则【答案】D【解析】洪特规则表明,基态原子中,填入简并轨道的电子总是先单独分占,且自旋方向相同。
4.下列说法中正确的是()A.1s电子云呈球形,表示电子绕原子核做圆周运动B.基态氢原子的电子云是圆形的C.n s能级的原子轨道图可表示为D.3d3表示3d能级有3个原子轨道【答案】C【解析】电子云是用小点表示电子在原子核外空间出现的概率,小点不代表电子,小点的疏密表示电子出现概率的大小,A项错误;基态氢原子的电子云是球形而不是圆形的,B项错误;3d3表示第三能层d能级有3个电子,d能级有5个原子轨道,D项错误。
实蹲市安分阳光实验学校课时跟踪检测(二)能量最低原理电子云与原子轨道1.下列有关电子原子轨道的说法正确的是( )A.原子核外的电子像云雾一样笼罩在原子核周围,故称电子云B.s能级的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动C.p能级的原子轨道呈哑铃形,随着能层的增加,p能级原子轨道也增多D.与s电子原子轨道相同,p电子原子轨道的平均半径随能层的增大而增大解析:选D A项,电子云只是一种对核外电子运动的“形象”描述;B项,核外电子并不像宏观物体的运动那样具有一的轨道;C项,p能级在任何能层均只有3个轨道。
2.当碳原子的核外电子排布由转变为时,下列说法正确的是( )①碳原子由基态变为激发态②碳原子由激发态变为基态③碳原子要从外界环境中吸收能量④碳原子要向外界环境中释放能量A.①② B.②③C.①③ D.②④解析:选C 核外电子排布由2s22p2转变为2s12p3,碳原子体系能量升高,由基态变为激发态,要从外界环境中吸收能量。
3.观察1s轨道电子云示意图,判断下列说法正确的是( )A.一个小黑点表示1个的电子B.1s轨道的电子云形状为圆形的面C.电子在1s轨道上运动像地球围绕太阳旋转D.1s轨道电子云的点的疏密表示电子在某一位置出现机会的多少解析:选D 由电子云图可知,处于1s轨道上的电子在空间出现的概率分布呈球形对称,而且电子在原子核附近出现的概率最大,离核越远,出现的概率越小。
图中的小黑点不表示电子,而表示电子曾经出现过的位置。
4.基态硅原子的最外能层的各能级中,电子排布的方式正确的是( )解析:选C 基态硅原子的电子排布遵循能量最低原理、泡利原理、洪特规则,只有C选项正确。
5.对于Fe的下列电子排布,正确的是( )解析:选A Fe原子的核外电子排布为1s22s22p63s23p63d64s2,据洪特规则可知A正确。
6.某原子核外电子排布为n s2n p7,它违背了( )A.泡利原理 B.能量最低原理C.洪特规则 D.洪特规则特例解析:选A p能级有三个轨道,根据泡利原理,每个轨道最多排2个电子,故p能级最多排6个电子,不可能排7个,故违背泡利原理。