最新溶液 溶解度知识点(大全)
- 格式:doc
- 大小:245.50 KB
- 文档页数:15

高考化学溶解度知识点归纳一、溶解度的定义和影响因素溶解度是指在一定温度下,单位体积溶剂中可以溶解的最大溶质量。
溶解度的大小与温度、压力和溶质种类有关。
随着温度的升高,溶解度通常增大;但对于少数溶质如氢气等,随着温度升高,溶解度反而减小。
溶解度还受压力的影响,但对于一般的固体和液体溶质,压力的变化对溶解度的影响较小。
二、饱和溶液和过饱和溶液饱和溶液是指在一定温度下,溶质溶解度达到最大且保持稳定的溶液。
当溶质继续加入时,不再溶解而形成沉淀,此时溶液处于饱和状态。
过饱和溶液是指在一定条件下,溶质溶解度超过饱和溶液的溶解度,但仍保持溶解的不稳定状态。
过饱和溶液具有较高的浓度,一旦触发条件改变,如温度下降或添加晶核,在短时间内会迅速结晶析出。
三、溶解度曲线溶解度曲线是描述溶质的溶解度和温度关系的曲线图。
通常,固体溶质在液体溶剂中的溶解度随温度的升高而增大,溶解度曲线呈现上升趋势。
液体溶质在液体溶剂中的溶解度通常不受温度的显著影响,溶解度曲线呈水平趋势。
气体溶质在液体溶剂中的溶解度随温度的升高而减小,溶解度曲线呈下降趋势。
四、共存溶液共存溶液指的是两种或多种溶质在同一溶剂中共存的溶液。
共存溶液可以分为两类:共存饱和溶液和共存非饱和溶液。
共存饱和溶液是指两种或多种溶质在同一溶剂中达到饱和状态的溶液。
在共存饱和溶液中,各组分的溶解度均达到最大值,不再溶解或析出。
共存非饱和溶液是指两种或多种溶质在同一溶剂中没有达到饱和状态的溶液。
在共存非饱和溶液中,各组分的溶解度还未达到最大值,可以继续溶解或析出。
五、晶体的溶解晶体的溶解是指将固体溶质溶解到溶剂中的过程。
晶体的溶解通常具有放热,可以通过增加温度、搅拌溶液、细化晶体等方式促进溶解速度。
晶体的溶解速度与多个因素有关,包括溶质的颗粒大小、晶体的形状、温度、溶液的饱和度等。
一般来说,溶质颗粒越细小,晶体越细碎,溶解速度越快。
溶液的饱和度越低,溶解速度越快。
六、溶液稀释溶液稀释是指通过添加溶剂降低溶液的浓度。

《溶液》知识点一、溶液的形成二、溶解度1、固体的溶解度(1)溶解度定义:在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量四要素:①条件:一定温度②标准:100g溶剂③状态:达到饱和④质量:单位:克(2)溶解度的含义:20℃时NaCl的溶液度为36g含义:在20℃时,在100克水中最多能溶解36克NaCl或在20℃时,NaCl在100克水中达到饱和状态时所溶解的质量为36克(3)影响固体溶解度的因素:①溶质、溶剂的性质(种类)②温度大多数固体物的溶解度随温度升高而升高;如KNO3少数固体物质的溶解度受温度的影响很小;如NaCl极少数物质溶解度随温度升高而降低。
如Ca(OH)2(4)溶解度曲线℃时A的溶解度为 80g例:(1)t3(2)P点的含义在该温度时,A和C的溶解度相同(3)N点为 t℃时A的不饱和溶液,可通过加3入A物质,降温,蒸发溶剂的方法使它变为饱和(4)t℃时A、B、C、溶解度由大到小的顺序C>B>A1(5)从A溶液中获取A晶体可用降温结晶的方法获取晶体。
(6)从B的溶液中获取晶体,适宜采用蒸发结晶的方法获取晶体。
(7)t2℃时A、B、C的饱和溶液各W克,降温到t1℃ 会析出晶体的有A和B 无晶体析出的有 C,所得溶液中溶质的质量分数由小到大依次为 A<C<B(8)除去A中的泥沙用过滤法;分离A与B(含量少)的混合物,用结晶法2、气体的溶解度(1)气体溶解度的定义:在压强为101kPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积。
(2)影响因素:①气体的性质②温度(温度越高,气体溶解度越小)③压强(压强越大,气体溶解度越大)3、混合物的分离(1)过滤法:分离可溶物 + 难溶物(2)结晶法:分离几种可溶性物质结晶的两种方法蒸发溶剂,如NaCl(海水晒盐)降低温度(冷却热的饱和溶液,如KNO3)三、溶质质量分数(1)、溶质的质量分数溶液中溶质的质量分数是溶质质量与溶液质量之比。

溶解度知识点溶解度是指在特定温度和压力下,溶质在溶剂中所能溶解的最大数量。
溶解度是溶液中溶质的浓度的度量,它对于理解溶液的性质以及溶液的制备和应用具有重要意义。
溶解度与溶质和溶剂之间的相互作用力有关。
溶解过程中,溶质分子与溶剂分子之间的相互作用力必须克服溶质分子之间的相互作用力,才能使溶质溶解在溶剂中。
溶解度的大小取决于溶质和溶剂之间的相互作用力的强弱。
如果溶质分子与溶剂分子之间的相互作用力较强,溶质在溶剂中的溶解度就较低;相反,如果溶质分子与溶剂分子之间的相互作用力较弱,溶质在溶剂中的溶解度就较高。
溶解度与温度的关系是一个重要的溶解度规律。
一般来说,溶解度随着温度的升高而增大。
这是因为随着温度的升高,溶液中的分子热运动加剧,分子间的距离增大,溶质分子与溶剂分子之间的相互作用力减弱,从而使溶质的溶解度增大。
然而,并非所有的溶质都遵循这个规律,有些溶质的溶解度随着温度的升高而减小。
除了温度,溶解度还受到压力和溶液的组成等因素的影响。
在一定温度下,气体溶质的溶解度随着压力的增加而增大,这是因为增加压力可以增加气体分子与溶剂分子之间的相互作用力。
而对于固体溶质来说,压力的变化对溶解度影响较小。
此外,溶质的溶解度还与溶液的组成有关。
例如,某些溶质在饱和溶液中的溶解度与溶液的浓度成正比,而某些溶质则与溶液的浓度无关。
溶解度的测定方法有多种,常用的方法包括重量法、体积法和电导率法等。
重量法是通过测量溶质在一定量的溶剂中的质量,计算出溶质的溶解度。
体积法则是通过测量溶质在一定体积的溶剂中的体积,计算出溶质的溶解度。
电导率法是通过测量溶液的电导率来间接推算出溶质的溶解度。
这些测定方法都有其适用的范围和条件,需要根据实际情况选择合适的方法。
溶解度的应用非常广泛。
在化学实验中,溶解度是溶液制备和反应条件控制的重要参考。
在工业生产中,溶解度的了解可以帮助优化工艺条件,提高产品质量和产量。
在药物研发中,溶解度是评价药物溶解性能的重要指标。

初中化学知识点归纳溶液的浓度和溶解度初中化学知识点归纳:溶液的浓度和溶解度一、浓度的概念和计算浓度是指溶液中溶质溶解在溶剂中的比例大小,常用的表示方法有质量浓度、体积浓度和摩尔浓度等。
1. 质量浓度(C)的计算质量浓度是指单位体积(或单位质量)的溶液中溶质的质量,计算公式为:C = m/V其中,C为质量浓度,m为溶质的质量,V为溶液的体积。
举例:若将10g的NaCl溶解在100mL的水中,求NaCl溶液的质量浓度。
解:C = m/V = 10g/100mL = 0.1g/mL2. 体积浓度(C)的计算体积浓度是指单位体积的溶液中溶质的体积,计算公式为:C = V1/V2其中,C为体积浓度,V1为溶质的体积,V2为溶液的体积。
举例:若将20mL的乙醇溶解在100mL的水中,求乙醇溶液的体积浓度。
解:C = V1/V2 = 20mL/100mL = 0.23. 摩尔浓度(C)的计算摩尔浓度是指单位体积的溶液中溶质的物质的量,计算公式为:C = n/V其中,C为摩尔浓度,n为溶质的物质的量,V为溶液的体积。
举例:若将0.5mol的NaOH溶解在500mL的水中,求NaOH溶液的摩尔浓度。
解:C = n/V = 0.5mol/0.5L = 1mol/L二、溶解度的概念和影响因素溶解度是指溶质在给定温度下在一定量的溶剂中能够溶解的最大物质的量,通常用单位质量溶剂中能够溶解的溶质的质量来表示。
1. 影响溶解度的因素溶解度受以下因素的影响:- 温度:一般情况下,溶解度随温度升高而增加,但对于部分物质如Ca(OH)2等,溶解度随温度的升高而降低。
- 压强:对固体和液体溶质影响较小,但对气体溶质有较大影响。
- 溶剂的性质:不同溶剂对溶质的溶解度有差异。
- 其他:如溶质的结构、溶液的饱和度等。
三、浓溶液的稀释计算浓溶液的稀释是指通过增加溶剂的体积来降低溶液的浓度,使其达到所需浓度的过程。
1. 稀释计算的公式根据稀释计算公式可以计算出稀释后溶液的浓度:C1V1 = C2V2其中,C1为初始溶液的浓度,V1为初始溶液的体积,C2为稀释后溶液的浓度,V2为稀释后溶液的体积。

高中化学重要知识点解析溶液与溶解度溶液是在溶剂中溶解了一定量的溶质的混合物。
在化学中,溶解度是描述溶质在溶剂中溶解程度的重要参数。
了解溶液与溶解度的相关知识对于理解化学反应、溶解现象和溶液中的平衡体系至关重要。
本文将深入解析溶液与溶解度的相关知识点。
一、溶液的概念和组成溶液是由溶剂和溶质组成的,其中溶剂是溶解度较大的组分,而溶质是溶解度较小的组分。
比如我们常见的盐水,其中水是溶剂,盐是溶质。
二、溶解度的定义和影响因素溶解度是指在特定温度下单位体积(或单位质量)的溶剂中能够溶解的溶质的最大量。
溶解度与温度、压力等因素密切相关,不同溶质在不同溶剂中的溶解度也有所差异。
以下是影响溶解度的几个主要因素:1. 温度:在一定压力下,大多数固体在溶液中的溶解度随温度升高而增大,而气体在溶液中的溶解度随温度升高而减小。
2. 压力:只对气体溶质在溶液中的溶解度有显著影响。
3. 溶质和溶剂的性质:如极性、分子大小等因素也会影响溶解度。
极性相近的物质通常具有更高的相容性,溶解度也相对较大。
三、饱和溶液和过饱和溶液饱和溶液是指在一定温度下,溶剂中已经溶解了最大量的溶质,此时溶解度达到了最大值。
过饱和溶液是指在饱和溶液的基础上,通过方法调节,使溶质的溶解度超过了饱和溶液的溶解度。
过饱和溶液相对不稳定,会因为微小扰动而发生结晶。
四、溶液浓度的表示方法溶液浓度是指单位体积(或单位质量)的溶剂中溶质的含量。
常用的溶液浓度表示方法有以下几种:1. 质量分数:指溶质质量与溶液总质量的比值,通常用百分数表示。
2. 体积分数:指溶质体积与溶液总体积的比值,通常用百分数表示。
3. 摩尔浓度:指溶质的摩尔数与溶液的体积之比,单位为mol/L。
4. 摩尔分数:指溶质的摩尔数与溶液中所有组成物的摩尔数之和的比值。
五、溶解过程和溶解热溶解是一个吸热过程,其中需要消耗热量,称为溶解热。
不同物质的溶解热也有所差异,溶解热可以通过实验测定得到。
溶解热的大小与溶质和溶剂之间的相互作用力有关。
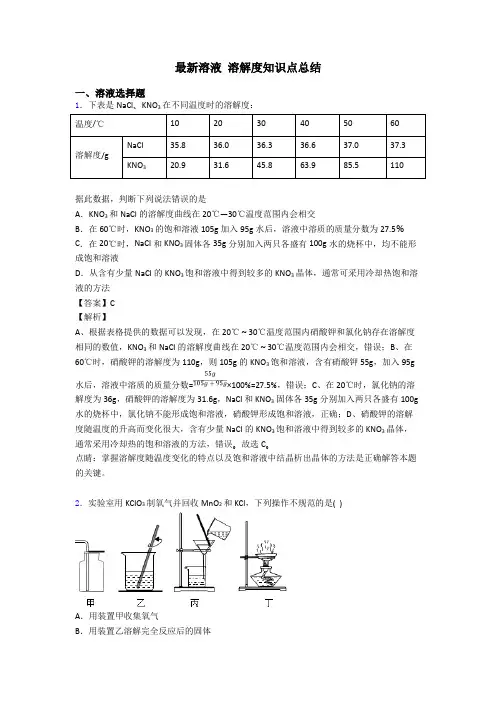
最新溶液溶解度知识点总结一、溶液选择题1.下表是NaCl、KNO3在不同温度时的溶解度:温度/℃102030405060 NaCl35.836.036.336.637.037.3溶解度/gKNO320.931.645.863.985.5110据此数据,判断下列说法错误的是A.KNO3和NaCl的溶解度曲线在20℃—30℃温度范围内会相交B.在60℃时,KNO3的饱和溶液105g加入95g水后,溶液中溶质的质量分数为27.5%C.在20℃时,NaCl和KNO3固体各35g分别加入两只各盛有100g水的烧杯中,均不能形成饱和溶液D.从含有少量NaCl的KNO3饱和溶液中得到较多的KNO3晶体,通常可采用冷却热饱和溶液的方法【答案】C【解析】A、根据表格提供的数据可以发现,在20℃~30℃温度范围内硝酸钾和氯化钠存在溶解度相同的数值,KNO3和NaCl的溶解度曲线在20℃~30℃温度范围内会相交,错误;B、在60℃时,硝酸钾的溶解度为110g,则105g的KNO3饱和溶液,含有硝酸钾55g,加入95g水后,溶液中溶质的质量分数=×100%=27.5%,错误;C、在20℃时,氯化钠的溶解度为36g,硝酸钾的溶解度为31.6g,NaCl 和KNO3固体各35g分别加入两只各盛有100g 水的烧杯中,氯化钠不能形成饱和溶液,硝酸钾形成饱和溶液,正确;D、硝酸钾的溶解度随温度的升高而变化很大,含有少量NaCl的KNO3饱和溶液中得到较多的KNO3晶体,通常采用冷却热的饱和溶液的方法,错误。
故选C。
点睛:掌握溶解度随温度变化的特点以及饱和溶液中结晶析出晶体的方法是正确解答本题的关键。
2.实验室用KClO3制氧气并回收MnO2和KCl,下列操作不规范的是( )A.用装置甲收集氧气B.用装置乙溶解完全反应后的固体C.用装置丙分离MnO2和KCl溶液D.用装置丁蒸发分离后的溶液得KCl晶体【答案】D【解析】【分析】【详解】A、氧气的密度比空气大,可用向上排空气法收集,故A正确;B、氯化钾易溶于水,二氧化锰难溶于水,溶解用玻璃棒搅拌以加快溶解速率,故B正确;C、过滤时要用玻璃棒引流,故C正确;D、蒸发时要变加热边搅拌,故D不正确。

化学中的溶液与溶解度(化学知识点)溶液是化学中常见的一种物质状态,它由溶质和溶剂组成。
在化学反应和研究中,溶液的溶解度是一个重要的概念。
本文将介绍溶液和溶解度的相关知识点。
一、溶液的定义和分类溶液是由两种或多种物质混合而成的均匀体系,其中溶解物质称为溶质,溶解介质称为溶剂。
溶液可以分为固体溶液、液体溶液和气体溶液等多种类型。
溶液的形成是由于溶质的分子或离子与溶剂中的分子之间发生了相互作用。
二、溶解度的概念与影响因素溶解度是指在一定温度下,单位体积溶剂中所能溶解的最大溶质量。
溶解度可以用质量分数、摩尔分数和摩尔浓度等方式来表示。
影响溶解度的因素包括温度、压力、溶质和溶剂的性质。
1. 温度对溶解度的影响一般来说,溶解度随温度升高而增加。
这是因为温度升高会使溶质和溶剂的分子运动加快,从而增强它们之间的相互作用力,有利于溶解过程的进行。
但有些物质的溶解度在升温过程中会出现异常变化,例如碳酸钠在25℃时溶解度最大,超过该温度后溶解度反而下降。
2. 压力对溶解度的影响对于固体和液体溶质来说,压力对溶解度的影响通常可以忽略不计。
而对于气体溶质来说,溶解度随压力的增加而增加。
根据亨利定律,气体溶质在液体中的溶解度与气体的分压成正比。
3. 溶质和溶剂的性质对溶解度的影响溶质和溶剂之间的相互作用力对溶解度起着决定性的作用。
相互作用力较强的溶质和溶剂能够更好地相互吸引,从而有利于溶解。
例如极性溶质在极性溶剂中的溶解度往往较高,而非极性溶质则偏好溶解于非极性溶剂中。
三、饱和溶液和过饱和溶液当溶剂已经溶解了尽可能多的溶质时,称为饱和溶液。
饱和溶液的溶解度是恒定的,并且在一定温度下与溶质的种类无关。
相反,如果溶液中含有超过饱和度的溶质,称为过饱和溶液。
过饱和溶液的形成常常需要某种条件,例如快速冷却或加入适量的其他物质。
四、溶解度曲线和溶解度积溶解度曲线是指在一定温度范围内,溶质在单位体积溶剂中的溶解度随溶质浓度变化的曲线。

溶解化学知识点总结一、溶解度1. 溶解度的定义溶解度是指在一定条件下,单位溶剂中溶解物质的最大量。
溶解度受温度、压强和溶剂种类等因素的影响。
2. 影响溶解度的因素(1)温度:大多数固体在增加温度下其溶解度增大,但对有些固体的溶解度则随温度升高而下降。
(2)压力:对气体溶解度的影响非常显著,呈直接比例关系。
(3)溶剂种类:不同溶剂的溶解度是不同的。
3. 溶解度的单位通常情况下,溶解度用溶质在100g水或g溶剂中的溶解量表示,单位是g/100g水或g/100g溶剂。
4. 溶解度曲线溶解度曲线是在一定温度下,溶质在单位溶剂中的溶解量随溶剂中溶质溶解比例的关系曲线。
二、溶液的稀释1. 稀释液的定义在化学中,稀释是指将一个浓度较高的溶液加入适量的溶剂,使溶液的浓度减小的过程。
2. 稀释的原理添加溶剂到溶液中时,溶剂分子与溶质分子相互作用,使得溶质分子之间的相互作用减少,从而使溶质分子的浓度减小。
3. 稀释公式根据溶液的浓度和体积,可以用以下公式计算稀释后的溶液浓度:c1v1=c2v2。
三、溶解的过程1. 溶解的过程溶解是指溶质和溶剂之间发生的相互作用,使得溶质分子散布在溶剂中,形成均匀的溶液的过程。
2. 溶解的热效应(1)溶解吸热:当溶解的过程中吸收了热量,溶解过程即是吸热的过程。
(2)溶解放热:当溶解过程中释放了热量,溶解过程即是放热的过程。
四、离子在溶液中的行为1. 离子的电解当离子型物质溶于水时,其分子将分解为离子,这个过程被称为电解。
2. 电解实验通过电解实验可以发现,在电解质的溶液中,会在电极上产生气体和发生化学反应。
3. 离子浓度变化(1)阳离子的浓度增加:阴极处发生还原反应。
(2)阴离子的浓度增加:阳极处发生氧化反应。
五、溶液的浓度1. 溶液的浓度定义溶液的浓度是指单位体积或单位质量的溶液中所含溶质的质量或物质的量。
2. 溶液的浓度计算(1)质量分数:溶质的质量与溶液的质量之比。
(2)体积分数:溶质的体积与溶液的体积之比。

溶解化学知识点总结大全一、溶解的定义和基本概念1. 溶解的定义溶解是指溶质在溶剂中分散并与其相互作用的过程。
在溶解过程中,溶质分子或离子被溶剂分子包围,并形成溶液。
溶解是一个平衡过程,溶质在溶解的同时也可能发生逆向的析出过程,而平衡时的溶质浓度称为溶解度。
2. 溶液的表示方法溶液可以使用浓溶液、稀溶液、饱和溶液等多种方式进行分类和表示。
其中,浓溶液指溶质在溶剂中的浓度较高,稀溶液指溶质在溶剂中的浓度较低,而饱和溶液则指在一定温度下,溶质在溶剂中达到最大溶解度的溶液。
3. 溶解度和溶度溶解度是指在一定温度下,单位溶剂中单位物质的饱和溶解度。
而溶度是指在一定条件下的溶质在溶剂中的浓度。
二、溶解的动力学1. 溶解过程的速率在溶解过程中,溶质分子或离子需要克服各种障碍才能与溶剂分子发生相互作用。
因此,溶解过程的速率与溶质的性质、溶剂的性质、温度和压力等因素有关。
2. 离子溶解的动力学在离子溶解的过程中,溶质中的离子在溶液中的浓度是随时间变化的。
离子溶解的速率可通过动力学方程进行描述,而离子溶解的速率与温度、离子浓度、电场强度等因素相关。
3. 溶解热溶解过程中释放或吸收的热量称为溶解热。
溶解热的大小与溶质和溶剂之间相互作用的性质有关,可以通过热力学方程来描述。
三、溶解度和溶解度曲线1. 溶解度的影响因素溶解度与溶质、溶剂之间的相互作用、温度和压力等因素有关。
通常情况下,随着温度的升高,溶解度会增大,而对气体溶解来说,随温度升高,溶解度会减小。
2. 溶解度曲线溶解度曲线是描述一定温度下溶质在溶剂中的溶解度随溶质浓度变化的曲线。
对于非电解质来说,溶解度曲线呈正比例曲线;对于一些电解质来说,溶解度曲线可能呈现出“S”型曲线。
3. 饱和溶解度饱和溶解度是指在一定温度下,单位溶剂中最大量溶质的溶解度,具有固定的数值。
饱和溶解度在化学反应、制备溶液等方面有着重要的应用。
四、溶解的应用1. 化学反应中的溶解在各种化学反应中,溶解都起着重要的作用。

化学反应中的溶解度和溶液浓度知识点总结化学反应中的溶解度和溶液浓度是重要的概念,对于理解溶解过程和溶液中溶质和溶剂的相互关系至关重要。
本文将总结化学反应中与溶解度和溶液浓度相关的主要知识点。
一、溶解度和饱和溶解度溶解度是指在一定温度下,在溶剂中最多可溶解的溶质物质的量。
通常以溶质物质的质量(g)或摩尔数(mol)来表示。
溶解度与溶质和溶剂种类、温度和压力等因素有关。
饱和溶解度是指在特定温度下,溶剂中所能容纳的最大溶质物质的量。
当溶质物质的添加超过饱和溶解度时,会出现剩余物质无法溶解的情况。
二、溶解度曲线溶解度曲线是指在一定温度下,溶质物质的溶解度与溶质物质的质量或摩尔数的关系曲线。
通常以图像的形式表示。
溶解度曲线可以帮助我们了解溶质物质在不同条件下的溶解度变化规律。
在溶解度曲线中,饱和溶解度点可以确定溶质物质在该温度下的饱和溶解度。
曲线的斜率可以反映溶质物质的溶解度随溶质质量或摩尔数的变化速率。
三、溶解度和温度的关系溶解度与温度之间存在一定的关系,一般情况下可以总结为:溶解度随温度的升高而增加。
这是由于在较高温度下分子的动能增加,使得溶质分子能够克服相互作用力而更容易分散在溶剂中。
但是,也存在一些特殊情况的溶解度和温度的关系。
例如,某些溶解反应是伴随着释放热量(放热),则溶解度随温度升高而减小;而某些溶解反应是吸收热量(吸热),则溶解度随温度升高而增大。
四、溶解度和压力的关系一般情况下,溶质在液体溶剂中的溶解度与压力无关。
但是,一些气体溶质在液体溶剂中的溶解度与压力存在一定的关系,即亨利定律。
亨利定律表示气体溶质在液体溶剂中的溶解度与其压力成正比。
亨利定律的数学表达式为:C = kP,其中C表示溶质气体在溶液中的摩尔浓度,k为亨利常数,P为溶质气体的分压。
五、溶液浓度的表示方式溶液浓度是指单位容积或质量的溶剂中溶质的含量。
常用的溶液浓度表示方式包括质量分数、体积分数、摩尔浓度、溶解度等。
质量分数是指溶液中溶质质量与溶液总质量之比。

溶解度知识点溶解度是描述物质在溶液中的溶解性质的重要参数,它是指在一定温度下,单位体积溶剂中最多可以溶解的物质的量,通常用克/升(g/L)表示。
溶解度不仅与物质本身的性质有关,还与溶剂的性质和温度有关。
1. 影响溶解度的因素1.1 物质的性质物质的极性是影响溶解度的重要因素之一。
极性分子之间的相互作用力较强,容易溶解,而非极性分子的溶解度较低。
此外,分子间的键合方式、晶格结构等也会影响溶解度。
1.2 溶剂的性质溶剂的极性与溶解度密切相关。
通常,极性溶质易溶于极性溶剂,非极性溶质易溶于非极性溶剂。
另外,溶剂的溶解度也与溶剂的饱和蒸汽压、溶剂分子大小等因素有关。
1.3 温度温度对溶解度的影响因物质而异,一般来说,大多数固体在溶解时需吸收热量,因此随着温度的升高,溶解度会增加。
而对于气体溶解于液体中,溶解度随温度升高而降低。
2. 溶解度的表示方法2.1 饱和溶解度饱和溶解度是指在特定温度下,溶液与未溶解物质之间的平衡状态达到一定的浓度。
当溶液中加入更多的溶质时,将无法再溶解,此时称为饱和溶液。
2.2 饱和溶解度曲线饱和溶解度曲线是描述溶质在不同温度下溶解度随溶质质量分数的变化关系的曲线。
通常是在坐标轴上绘制溶质质量分数和温度,通过实验测定得出。
3. 应用3.1 药学药物的溶解度是评价其溶解性的重要指标之一。
药物的溶解度决定了它在体内的吸收速度和效果。
通过研究药物的溶解度,可以优化药物的给药方式和剂型。
3.2 化学工程在化学反应和工业生产过程中,溶解度对原料溶解、反应速度、反应平衡等有重要影响。
通过研究溶解度,可以指导工程师合理设计设备和控制条件,提高生产效率。
3.3 环境科学溶解度对环境中的污染物迁移和转化过程具有重要影响。
了解溶解度可以帮助科学家预测污染物在水体、土壤中的分布和迁移规律,为环境保护和污染治理提供理论依据。
总结:溶解度是描述物质在溶液中溶解性质的重要参数,受到物质本身、溶剂和温度等因素的影响。
溶解度和溶液浓度的计算知识点总结溶解度和溶液浓度是化学中非常重要的概念,用于描述溶质在溶剂中的溶解程度以及溶液中溶质的相对含量。
正确理解和计算溶解度和溶液浓度对于化学实验和实际应用具有重要意义。
本文将总结溶解度和溶液浓度的定义、计算方法以及相关的知识点。
一、溶解度的定义和计算溶解度是指溶质在一定温度下在溶剂中达到饱和时的溶解质量。
其计量单位可以是克/升(g/L),摩尔/升(mol/L)等。
溶解度与溶质的溶性和温度相关。
通常情况下,溶解度随着温度的升高而增加,但对于部分溶质来说,随温度的升高而减小。
溶解度的计算方法:1. 溶解度可通过实验测量得到。
实验中,取一定量的溶剂,逐渐加入溶质,直到观察到溶质无法再溶解为止。
记录此时溶质的质量,并按照溶剂的体积计算溶解度。
2. 某些情况下,可以通过公式计算溶解度。
例如,钙离子在水中的溶解度可以利用下式计算:溶解度 = [Ca2+] × V其中[Ca2+]表示溶液中钙离子的浓度,V表示溶剂的体积。
二、溶液浓度的定义和计算溶液浓度是指溶液中溶质的相对含量,可以通过溶质的质量或摩尔数与溶剂的体积来计算。
常见的溶液浓度表示方法包括质量浓度、摩尔浓度、体积分数等。
1. 质量浓度(或称质量百分比浓度)表示单位体积(一般为升)的溶液中所含溶质的质量。
其计算公式如下:质量浓度 = (溶质质量 / 溶剂体积) × 100%2. 摩尔浓度是指单位体积溶液中溶质的物质的量。
其计算公式如下:摩尔浓度 = 溶质的物质的量 / 溶剂的体积3. 体积分数是指溶质的体积与溶液总体积之比。
其计算公式如下:体积分数 = (溶质的体积 / 溶液总体积) × 100%三、其他相关知识点1. 溶解度曲线:表达了溶质在不同温度下的溶解度。
使用溶解度曲线可以预测随温度变化时的溶解度情况。
2. 饱和溶液:指在一定温度下,溶液中已经溶解了最大量的溶质,无法再溶解更多溶质的溶液。
溶液部分知识点总结1. 溶解度与溶解度曲线溶解度是指溶质在给定温度下,在一定量溶剂中能溶解的最大量。
通常用单位质量溶剂中最大溶质量来表示,单位是mol/L。
溶解度受温度、压力和溶质种类等因素影响。
在溶解度与温度之间有一定的关系,即溶解度随着温度的升高而增大或减小。
溶解度随温度升高而增加的情况多见于固体在液体中的溶解,而气体在液体中的溶解则随温度升高而减小。
当随着温度的升高溶解度增大并达到一定的饱和值时,再升温不会再增大溶解度,而会出现饱和溶液变成过饱和溶液的现象。
溶解度曲线是描绘溶解度与温度之间的关系曲线,通常在温度和溶解度坐标系中绘制。
溶解度曲线的形状通常与该溶质的性质有关,常见的有对称型、不对称型和温度不变型等。
对称型的溶解度曲线常见于一些晶型变化规则性较好的化合物,可以通过溶解度曲线研究物质晶型结构的变化。
不对称型的溶解度曲线则多见于各种不同晶型形成菱形相图的化合物。
温度不变型溶解度曲线则见于常见的无机化合物中,特别是在溶解度曲线的中间部分温度范围内。
2. 溶液的稀释与浓缩溶液的稀释是指在保持溶质质量不变的情况下,加入更多的溶剂以减少溶质的浓度。
溶质的质量不变,但是溶液的体积增大,浓度减小。
稀释常用于化学实验中,通过稀释可以调整溶液的浓度,使实验过程更好地进行。
稀释的过程中,溶质的质量是不变的,遵循质量守恒定律。
溶液的浓缩是指在不加溶剂的情况下,增加溶质质量以增大溶液的浓度。
溶液的浓度增大时,溶质的质量也增加。
浓缩的方法有很多种,如蒸发法、结晶法等。
浓缩是化学工业制备一些化合物的常用方法,也是溶液处理和回收的重要手段。
3. 溶解过程中的热效应溶解过程中通常会伴随有吸热或放热的现象。
吸热现象是指溶解过程中需要吸收热量才能进行的现象,这样的溶解过程通常会使溶液温度下降。
而放热现象则是指溶解过程中放出热量的现象,这样的溶解过程通常会使溶液温度升高。
吸热和放热现象对于控制溶解过程和预测溶解过程中的温度变化都具有重要的意义。
初三化学溶液知识点总结完整版一、溶液的性质1. 溶解度:溶解度是指在给定的温度和压力下溶质质量被溶解的速率的度量。
溶解度亦称溶质的溶解度或溶质的溶解率。
溶解度越大,表明溶质越容易溶解;溶解度越小,表明溶质越不容易溶解。
一定条件下,相同物质的溶解度是一定的,是不随外界因素改变的。
2. 极性:极性是指由原子或分子组成的物质中,具有电荷不均匀分布的性质。
每个原子或分子都有一些电子充电,它们可以表示为正电荷或负电荷。
极性决定了沉淀物的稳定性,极性更强的物质的溶液的稳定性更低;极性更弱的物质的溶液的稳定性更高。
3. 气味:气味是指一定条件下溶液可以很明显地闻到的气体的气味。
气味的性质主要取决于溶质的特性,而不是溶液的性质,所以要判断溶液是苦味还是咸味,就可以闻一闻溶液的气味。
二、化学反应1. 前置反应:前置反应是指在溶液中发生前,必须准备好充分配分的物质,以促使反应发生的反应。
这类一般是可逆反应,反应产物可以再次发生反应,结果产生新的产物,多用于改变溶液的参数,如酸碱度、Ph值等。
2. 溶解反应:溶解反应是指在溶液中离子或分子被完全拆分的反应。
这种反应的特点是不可逆的,也就是说不可能通过另一对反应引起游离离子或原子的重新组合,只能提供单一离子或原子。
3. 水解反应:水解反应是指某些化合物与水反应,当化合物与水反应时,会引起改变,因此得到新的有机物或无机物的反应。
这类反应一般是可逆的,可以表示为水的添加或分解的形式。
三、物质的溶解过程1. 吸收:当溶质溶解在溶剂中时,溶质与溶剂之间会发生电荷的传递,溶质的电荷会被溶剂的电荷所吸收,从而使溶质分子更加稳定、更容易进行溶解。
2. 团簇化:当溶质在溶剂中溶解时,溶解过程会随着溶剂量、温度、压强等参数的改变而改变。
当溶质质量足够时,溶质分子之间会形成团簇,从而促进溶解过程。
3. 渗入:溶质分子吸收溶剂后,会分子局部溶质分子结构发生变化,以促进其质量的渗入溶剂中,使溶质稳定溶解在溶剂中,完成溶质的溶解过程。
【化学】溶液溶解度知识点(大全)经典一、溶液选择题1.配制一定质量分数的氯化钠溶液,下列操作正确的是A.称量固体时,左盘放砝码,右盘放氯化钠B.将配好的溶液倒入细口瓶中,盖紧瓶塞,并贴上标签C.量取液体时,手持量筒,视线与液体的凹液面的最低处保持水平D.称量固体时,发现指针向左偏,应该用镊子将游码向右移动直至天平平衡【答案】B【解析】A、称量固体药品的质量时要注意“左物右码”,错误;B、溶于配制好后需要标明溶液的名称和溶质的质量分数,正确;C、量取液体体积时,量筒应放在水平桌面上,错误;D、定量称量固体质量时,指针向左偏,说明左盘重了,应该减少药品的质量直至天平平衡,错误。
故选B。
2.如图是甲、乙两种固体物质在水中的溶解度曲线。
下列说法正确的是A.t1℃时,甲、乙两种物质的饱和溶液中溶质的质量分数相等B.由t2℃降温到t1℃,甲饱和溶液比乙饱和溶液析出晶体的质量多C.t2℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为90gD.t2℃时,用甲、乙配制等质量的饱和溶液,甲所需要水的质量比乙多【答案】A【解析】A、一定温度下,饱和溶液溶质的质量分数=s100g s+×100%。
t1℃时,甲、乙的溶解度相等,甲、乙两种饱和溶液的溶质质量分数相等,正确;B、没有确定溶液的质量无法比较甲、乙饱和溶液析出晶体的质量,错误;C、t2℃时,甲的溶解度为50g,即100g水中最多溶解50g的甲,40g甲加入50g水中,充分溶解后只能溶解25g,所得的溶液质量为75g,错误;D、t2℃时,甲的溶解度大于乙的溶解度,配制等质量饱和溶液,甲所需要水的质量比乙少,错误。
故选A。
点睛:一定温度下,饱和溶液溶质的质量分数=s100g s+×100%。
3.下图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是A.P点表示甲、丙两种物质的饱和溶液质量相等B.t1℃时,乙物质的饱和溶液,升温至t2℃时仍是饱和溶液C.t1℃时,甲物质的饱和溶液中溶质和溶剂的质量比为1∶4D.将三种物质的溶液从t2℃降至t1℃,溶质质量分数最小的一定是丙物质【答案】C【解析】【详解】A、由题中信息知,A. P点表示甲、丙两种物质溶解度相等,故错误。