苯亚甲基苯乙酮的制备
- 格式:doc
- 大小:82.50 KB
- 文档页数:3



功能化离子液体催化合成苯亚甲基苯乙酮
胡晓允;韦丽艳;钟诗诗;陈玉;周忠强
【期刊名称】《实验室科学》
【年(卷),期】2015(018)003
【摘要】设计合成了功能化离子液体乙醇胺乙酸盐,并考察了该功能化离子液体催化苯甲醛和苯乙酮的反应.发现在无溶剂条件下,10%的催化剂用量就可以有效促进反应进行,在90℃下加热反应1.5小时就可以89%的产率制得苯亚甲基苯乙酮.与传统方法相比,乙醇胺乙酸盐离子液体催化合成苯亚甲基苯乙酮减少了碱液的使用和排放,简化了实验的分离纯化过程,具有高效性、易纯化且合成绿色化等特点,体现了化学实验教学绿色化的改革目标.
【总页数】3页(P48-50)
【作者】胡晓允;韦丽艳;钟诗诗;陈玉;周忠强
【作者单位】中南民族大学化学与材料科学学院,湖北武汉430074;中南民族大学化学与材料科学学院,湖北武汉430074;中南民族大学化学与材料科学学院,湖北武汉430074;中南民族大学化学与材料科学学院,湖北武汉430074;中南民族大学化学与材料科学学院,湖北武汉430074
【正文语种】中文
【中图分类】O621.3
【相关文献】
1.超声辐射技术合成苯亚甲基苯乙酮 [J], 王振华;李记太;杨文智;孙汉文
2.苯亚甲基苯乙酮合成方法的改进 [J], 胡晓允;周忠强;单自兴
3.超声辐射合成苯亚甲基苯乙酮的研究 [J], 阿布力米提·阿布都卡德尔;孙亚栋;张永红;张增鹏
4.苯亚甲基苯乙酮-4-氯苯甲酰腙的合成、晶体结勾及荧光性质 [J], 王亮;刘娟;郑长征;任立娣
5.功能化离子液体[C3SO3Hnhm] HSO4催化合成苯并氧杂蒽 [J], 汤小芳;刘显明;周思言;李双
因版权原因,仅展示原文概要,查看原文内容请购买。

苯亚甲基苯乙酮相对原子质量苯亚甲基苯乙酮,化学式为C9H10O,是一种有机化合物。
下面,我们将从不同角度来探讨苯亚甲基苯乙酮的相对原子质量。
1. 苯亚甲基苯乙酮的结构苯亚甲基苯乙酮的分子结构由苯环和乙酮基团组成。
苯环是由六个碳原子和六个氢原子构成的环状结构,而乙酮基团则由三个碳原子、五个氢原子和一个氧原子组成。
这两部分通过碳碳键连接在一起,形成了苯亚甲基苯乙酮的分子结构。
2. 相对原子质量的计算方法相对原子质量是指一个元素的原子质量与碳-12同位素的原子质量的比值。
苯亚甲基苯乙酮的相对原子质量可以通过将各个原子的质量相加得到。
根据元素周期表,碳的相对原子质量为12,氢的相对原子质量为1,氧的相对原子质量为16。
因此,苯亚甲基苯乙酮的相对原子质量可以计算为:(6 × 12) + (5 × 1) + (1 × 16) = 983. 苯亚甲基苯乙酮的性质苯亚甲基苯乙酮是一种无色液体,具有特殊的香味。
它可以溶于有机溶剂如醇和醚,但几乎不溶于水。
在常温下,苯亚甲基苯乙酮是稳定的,但在高温下会分解。
它是一种挥发性物质,具有一定的毒性。
4. 苯亚甲基苯乙酮的应用苯亚甲基苯乙酮在化学工业中有着广泛的应用。
它是合成药物的重要原料之一,可以用于制备抗菌药物、抗癌药物等。
此外,苯亚甲基苯乙酮还可以用作香料的成分,赋予香水和香精独特的香味。
除此之外,苯亚甲基苯乙酮还可以用于有机合成反应的催化剂,具有重要的工业价值。
5. 苯亚甲基苯乙酮的危害尽管苯亚甲基苯乙酮在化学工业中有广泛的应用,但它也存在一定的危害性。
苯亚甲基苯乙酮具有一定的毒性,对皮肤和眼睛有刺激作用。
长期接触或吸入苯亚甲基苯乙酮可能会对人体造成损害,包括对呼吸系统、中枢神经系统和肝脏的影响。
因此,在使用苯亚甲基苯乙酮时,需要注意安全使用,并采取相应的防护措施。
通过以上对苯亚甲基苯乙酮相对原子质量的描述,我们可以了解到它的分子结构、性质、应用和危害。
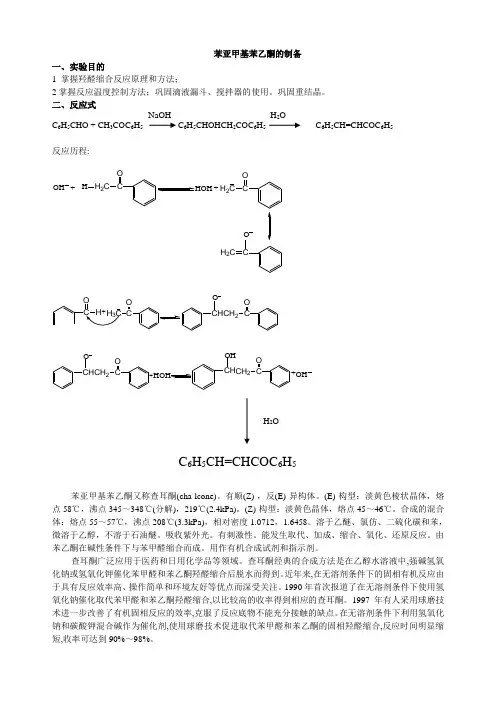
苯亚甲基苯乙酮的制备一、实验目的1 掌握羟醛缩合反应原理和方法;2掌握反应温度控制方法;巩固滴液漏斗、搅拌器的使用。
巩固重结晶。
二、反应式NaOH -H 2OC 6H 5CHO + CH 3COC 6H 5 C 6H 5CHOHCH 2COC 6H 5 C 6H 5CH=CHCOC 6H 5 反应历程:OH +CH 2C OH CH 2C O+CH 2C OCC OC OH CH CCH 2O O+CH CCH 2O O CH CCH 2O OH+OHC 6H 5CH=CHCOC 6H 5苯亚甲基苯乙酮又称查耳酮(cha-lcone)。
有顺(Z)-,反(E)-异构体。
(E)-构型:淡黄色棱状晶体,熔点58℃,沸点345~348℃(分解),219℃(2.4kPa)。
(Z)-构型:淡黄色晶体,熔点45~46℃。
合成的混合体:熔点55~57℃,沸点208℃(3.3kPa),相对密度1.0712,1.6458。
溶于乙醚、氯仿、二硫化碳和苯,微溶于乙醇,不溶于石油醚。
吸收紫外光。
有刺激性。
能发生取代、加成、缩合、氧化、还原反应。
由苯乙酮在碱性条件下与苯甲醛缩合而成。
用作有机合成试剂和指示剂。
查耳酮广泛应用于医药和日用化学品等领域。
查耳酮经典的合成方法是在乙醇水溶液中,强碱氢氧化钠或氢氧化钾催化苯甲醛和苯乙酮羟醛缩合后脱水而得到。
近年来,在无溶剂条件下的固相有机反应由于具有反应效率高、操作简单和环境友好等优点而深受关注。
1990年首次报道了在无溶剂条件下使用氢氧化钠催化取代苯甲醛和苯乙酮羟醛缩合,以比较高的收率得到相应的查耳酮。
1997年有人采用球磨技术进一步改善了有机固相反应的效率,克服了反应底物不能充分接触的缺点。
在无溶剂条件下利用氢氧化钠和碳酸钾混合碱作为催化剂,使用球磨技术促进取代苯甲醛和苯乙酮的固相羟醛缩合,反应时间明显缩短,收率可达到90%~98%。
-H 2O三、物理常数分子量状态熔点/℃沸点/℃比重溶解性苯乙酮120.15无色晶体,或淡黄色油状液体,有象山楂的香气。

实验名称:苯亚甲基苯乙酮的制备一、实验目的:1 掌握羟醛缩合反应原理和方法;2掌握反应温度控制方法;巩固滴液漏斗、搅拌器的使用。
巩固重结晶。
二、实验原理:强碱性条件下发生的羟醛缩合反应。
反应式如下:反应历程:苯亚甲基苯乙酮又称查耳酮(cha-lcone)。
有顺(Z)-,反(E)-异构体。
(E)-构型:淡黄色棱状晶体,熔点58℃,沸点345~348℃(分解),219℃(2.4kPa)。
(Z)-构型:淡黄色晶体,熔点45~46℃。
合成的混合体:熔点55~57℃,沸点208℃(3.3kPa),相对密度1.0712,1.6458。
溶于乙醚、氯仿、二硫化碳和苯,微溶于乙醇,不溶于石油醚。
吸收紫外光。
有刺激性。
能发生取代、加成、缩合、氧化、还原反应。
由苯乙酮在碱性条件下与苯甲醛缩合而成。
用作有机合成试剂和指示剂。
查耳酮广泛应用于医药和日用化学品等领域。
查耳酮经典的合成方法是在乙醇水溶液中,强碱氢氧化钠或氢氧化钾催化苯甲醛和苯乙酮羟醛缩合后脱水而得到。
近年来,在无溶剂条件下的固相有机反应由于具有反应效率高、操作简单和环境友好等优点而深受关注。
1990年首次报道了在无溶剂条件下使用氢氧化钠催化取代苯甲醛和苯乙酮羟醛缩合,以比较高的收率得到相应的查耳酮。
1997年有人采用球磨技术进一步改善了有机固相反应的效率,克服了反应底物不能充分接触的缺点。
在无溶剂条件下利用氢氧化钠和碳酸钾混合碱作为催化剂,使用球磨技术促进取代苯甲醛和苯乙酮的固相羟醛缩合,反应时间明显缩短,收率可达到90%~98%。
苯亚甲基苯乙酮是由苯甲醛与苯乙酮在10%氢氧化钠溶液催化下缩合而合成。
为了使反应顺利进行和控制苯甲醛的滴加速度,通常在装有搅拌器、温度计和滴液漏斗的三颈瓶中进行。
反应时间由滴加苯甲醛算起至加入晶种继续搅拌待反应瓶中有结晶止,需1.5~2.0h,产率67~72%。
三、物理常数试剂用量减半:苯乙酮3g,0.025mol;苯甲醛2.65g, 0.025mol ,理论产量:5.2g四、反应步骤在装有搅拌器、温度计和恒压漏斗的50 ml三口烧瓶中,加入12.5ml10%氢氧化钠溶液、7.5 ml 95%乙醇和3 ml苯乙酮。

超声辐射合成苯亚甲基苯乙酮的研究阿布力米提·阿布都卡德尔;孙亚栋;张永红;张增鹏【摘要】以乙醇为溶剂,苯甲醛和苯乙酮为原料,在无机碱NaOH为催化剂作用下通过超声辐射合成了苯亚甲基苯乙酮,产物经IR和1HNMR分析表征,并考察了原料配比、催化剂用量、超声辐射时间和功率等因素对产物收率的影响.实验结果表明,当苯甲醛与苯乙酮的的摩尔比为1:1,催化剂的用量为8.3 mL,超声波辐射功率为700W,超声波辐射40 min,苯亚甲基苯乙酮产率达92%.此合成方法与传统的合成方法相比,具有反应时间短、产率高、易纯化、物耗低及污染少等优点,体现了有机合成教学绿色化的改革目标.%Benzylidene acetophenone was synthesized with ethanol as solvent,benzaldehyde and acetophenone as raw material and inorganic alkali NaOH as catalyst under ultrasonic radiation.The products were characterized by IR and 1HNMR analysis.Meanwhile,the raw-material ratio,the amount of catalyst,ultrasonic irradiation time and other factors on the yield were examined as well.Experimental results show that when the molar ratio of benzaldehyde and acetophenone is 1:1,the amount of catalyst is 8.3 mL,ultrasonic radiation power is 700 W,for 40 min,benzylidene acetophenone was obtained in 92% yield within 40 min under ultrasonic pared to traditional synthetic methods this protocol has the advantages of short reaction time,high yield,easy purification,low material consumption and less pollution,etc.,which reflects the green organic synthesis teaching reform objectives.【期刊名称】《新疆大学学报(自然科学版)》【年(卷),期】2017(034)004【总页数】4页(P426-428,434)【关键词】苯亚甲基苯乙酮;超声波辐射;绿色合成【作者】阿布力米提·阿布都卡德尔;孙亚栋;张永红;张增鹏【作者单位】新疆大学化学化工学院,新疆乌鲁木齐830046;新疆大学化学化工学院,新疆乌鲁木齐830046;新疆大学化学化工学院,新疆乌鲁木齐830046;新疆大学化学化工学院,新疆乌鲁木齐830046【正文语种】中文【中图分类】Q939.97苯亚甲基苯乙酮又称查尔酮,具有多种药理作用和生物活性,广泛应用于医药和日用化学品等领域[1,2],苯亚甲基苯乙酮的合成实验是高等院校化学专业有机化学实验中必做的综合性实验.关于它的合成方法较多,主要有使用强碱或者强酸催化苯乙酮和苯甲醛的羟醛缩合,但是副反应较多,产率偏低[3].传统合成方法是以乙醇为反应溶剂,10%的氢氧化钠水溶液催化苯乙酮与苯甲醛发生羟醛缩合脱水而得,目前有机化学实验教材普遍采用该方法来合成苯亚甲基苯乙酮[4−7].在实验过程中,人们在如何更加简单高效的获得苯亚甲基苯乙酮方面做了很多的努力.如无溶剂条件下,发展了苯乙酮和苯甲醛在双组份固体碱氢氧化钠和碳酸钾催化下合成苯亚甲基苯乙酮的方法[8],固相条件下的机械振荡技术[9],还有功能化离子液体催化方法[10]等.人们也发展了微波辅助制备苯亚甲基苯乙酮的方法[11,12].20世纪80年代以来,随着声化学的发展,超声辐射(U.S.)在有机合成中的应用研究呈蓬勃发展之势,已广泛应用于氧化、还原、取代、缩合和水解等反应中,几乎涉及有机反应的各个领域[13−15].而且,近期也有文献报道使用超声技术[16,17]合成苯亚甲基苯乙酮.因此,我们也将超声波技术引入有机合成实验中,这样可以使有机反应速率比普通加热反应快数十倍甚至数万倍.既可以节约能源,缩短实验时间,又能提高反应产率.加之进行的是半微量反应实验,既减少了污染,也更符合当今“节能减排”和“绿色化学”的理念[18].合成路线见图1.图 1 超声辐射合成苯亚甲基苯乙酮1 实验部分主要仪器与试剂仪器:XH-2008D型智能温控低温超声波催化合成/萃取仪,超声波功率:1 500 W,频率:25 KHz,加热功率:300 W,制冷功率:450 W,北京祥鹄科技发展有限公司;CSF-3A型超声波清洗器,500 W,25 KHz,上海超声波仪器厂;B¨UCHI(M-560)型熔点仪;Bruker Equinox 55 FT-IR分光光度计(KBr压片);VARIAN INOVA-400型核磁共振仪.试剂:10%NaOH水溶液;95%乙醇;苯乙酮;新蒸苯甲醛;无水乙醇.2 实验步骤2.1 苯亚甲基苯乙酮的合成将10%NaOH水溶液6.3 mL,95%EtOH 7.5 mL,苯乙酮3 mL(3 g,25 mmol),依次加入50 mL锥形瓶中,冷却至室温,再加入新蒸苯甲醛2.5 mL(2.65 g,25 mmol).将反应瓶置于超声波催化合成仪或超声波清洗槽中,启动超声反应器.于25◦C∼30◦C反应至有结晶析出,反应需要30∼35 min,停止反应.2.2 苯亚甲基苯乙酮的分离与提纯反应混合液于冰浴中冷却,使其结晶完全.抽滤,用冷水洗涤(至滤液呈中性),然后用2.5 mL冰乙醇洗涤结晶,干燥,称量,计算收率.2.3 苯亚甲基苯乙酮的结构分析熔点:56◦C∼57◦C.1H NMR(400 MHz,CDCl3):δ 8.08-7.97(m,2H),7.81(d,J=15.7 Hz,1H),7.68-7.46(m,6H),7.45-7.36(m,3H).IR(KBr压片):3 053 cm−1和3 031 cm−1吸收峰是苯环C-H键的伸缩振动;1 663cm−1是羰基键C=O的伸缩振动;1 573 cm−1和1 607 cm−1吸收峰归属于苯环C=C键的面内伸缩振动;750 cm−1,749 cm−1和685 cm−1吸收峰是芳环单取代面外弯曲振动,说明有单取代苯存在;与标准图谱吸收峰的强度及位置一致,最终可以确定产物为苯亚甲基苯乙酮.3 结果与讨论3.1 超声辐射时间对苯亚甲基苯乙酮产率的影响量取10%NaOH水溶液6.3 mL,95%EtOH 7.5 mL,保持n(苯乙酮):n(苯甲醛)=1:1,反应温度25◦C∼30◦C等条件不变,改变超声辐射时间,以考察超声辐射时间对产品收率的影响,结果见图2.3.2 超声波强度对苯亚甲基苯乙酮产率的影响量取10%NaOH水溶液6.3 mL,95%EtOH 7.5 mL,保持n(苯乙酮):n(苯甲醛)=1:1,反应温度25◦C∼30◦C等条件不变,改变超声波强度,以考察超声波强度对产品收率的影响,结果见图3.可以看出,随着超声辐射功率的加强,产率收率有所增加.3.3 不同反应方式的对比从表1结果来看,超声波发生器促进的反应在40 min内能得到92%产率,而采用超声清洗器促进的方法在40 min内能得到88%产率.因此超声波促进的反应具有一定的优势,而且超声波辐射法降低了反应能耗,减少环境污染的目的,符合绿色化学的理念.3.4 反应物的摩尔比对产品收率的影响根据化学反应平衡原理,增大物质的量比有利于提高产品的收率,但会造成原料的浪费.本实验保持催化剂10%NaOH 6.3 mL,95%EtOH 7.5 mL,超声波辐射功率700 W,实验温度25◦C∼30◦C实验时间40 min等条件不变,改变苯甲醛的用量,考察苯乙酮与苯甲醛的摩尔比对产品收率的影响.结果见表2.结果显示,苯甲醛与苯乙酮的摩尔比为1:1得到最高的收率92%.图 2 超声辐射时间对苯亚甲基苯乙酮产率的影响图 3 超声波强度对苯亚甲基苯乙酮产率的影响表 1 不同反应方式对苯亚甲基苯乙酮产率的影响?3.5 催化剂用量的影响催化剂的用量对产品的收率有很大的影响.为考察催化剂用量对产品收率的影响,保持苯乙酮3 mL,苯甲醛2.5 mL,超声功率700 W,反应时间40 min,反应温度25◦C∼30◦C等条件不变,改变催化剂10%NaOH的用量,结果见表3.表 2 苯乙酮与苯甲醛的摩尔比对苯亚甲基苯乙酮产率的影响?表 3 催化剂用量对苯亚甲基苯乙酮产率的影响?由表3可知,随着催化剂用量的增加,产品收率显著提高,当催化剂用量为6.3 mL时,收率达到92%,再继续加大催化剂用量,产品收率并没有明显的升高.故选择催化剂用量6.3 mL为宜.4 结论1.本实验利用超声波辐射技术,以苯乙酮和苯甲醛为原料,10%氢氧化钠为催化剂合成了苯亚甲基苯乙酮,通过条件优化以高达92%收率获得了苯亚甲基苯乙酮.2.通过对超声波清洗器与超声波合成仪的对比,表明此方法具有催化剂价廉易得、催化效果好、合成路线短、反应条件温和、提纯操作简单,且超声波合成仪具有更为高效和符合绿色经济的优点.参考文献:[1]郑洪伟,牛新文,朱君,等.查尔酮类化合物生物活性研究进展[J].中国新药杂志,2007,16(18):1445-1449.[2]由业诚,张晓辉,郭明,等.微波辐射KF-Al2O3催化合成查尔酮的研究[J].化学研究与应用,2000,12(2):186-188.[3]郭宏雄,臧庶声,李文科,等.查耳酮的制备I[J].兰州医学院学报,1998,24(2):12213.[4]武汉大学化学与分子科学学院实验中心编.有机化学实验[M].武汉:武汉大学出版社,2004,241-242.[5]北京大学化学学院有机化学研究所编.有机化学实验:2版[M].北京:北京大学出版社,2002,168-169.[6]李兆陇,银金香,林天舒.有机化学实验[M].北京:清华大学出版社,2000,128-129.[7]李霁良.微型半微型有机化学实验[M].北京:高等教育出版社,2003,207-208.[8]胡晓允,周忠强,单自兴.苯亚甲基苯乙酮合成方法的改进[J].广州化工,2013,41(3):50-51.[9]王春山,吴浩浩,谭亚军,等.查尔酮及氮杂查尔酮的机械法合成[J].南通大学学报(自然科学版),2013,12(1):40-44.[10]胡晓允,韦丽艳,钟诗诗,等.功能化离子液体催化合成苯亚甲基苯乙酮[J].实验室科学,2015,18(3):48-50.[11]刘兴利,赵志刚,曾碧涛,等.微波干法合成查尔酮[J].化学研究与应用,2007,19(5):574-576.[12]张国喜,杨金凤,姬广军,等.微波辅助合成查尔酮衍生物的工艺[J].石河子大学学报(自然科学版),2011,29(6):785-788.[13]廖九中,杨慧文,潘育方.延胡索生物碱超声法提取工艺的研究[J].广东药学院学报,2012,28(2):153-155.[14]李记太,臧洪俊.超声波应用于有机合成方面的新进展[J].河北大学学报(自然科学版),2000,20(1):96-102.[15]赵新海,姬红,刘晨江.氨基磺酸铵:一种“一锅法”合成3,4-二氢嘧啶-2(1H)-(硫)酮的有效催化剂[J].新疆大学学报(自然科学版),2010,27(2):132-135. [16]黄丹,江国庆.超声技术在查尔酮合成中的应用研究[J].有机化学,2002,22(12):1057-1059.[17]贾兆海,陈馥衡,谢毓元.超声波在有机合成中的应用[J].化学进展,1998,10(1):63-73.[18]周先波,周赛春,王永红,等.在有机合成实验教学中超声波应用初探[J].实验科学与技术,2007,5(6):107-108.。


苯亚甲基丙酮合成方程式反应历程
苯亚甲基丙酮(也称为P2P)是一种合成毒品的中间体,其合成过程通常涉及到苯乙烯、甲酸和碘等原料,以下是其合成方程式反应历程:
1. 首先,将苯乙烯和甲酸放入反应器中,加入硫酸催化剂,在高温高压下进行反应,生成苯乙酸。
苯乙酸是一种无色液体,有刺激性气味,常用于合成香精和医药中间体。
C6H5CH=CH2 + HCOOH →C6H5CH2COOH
2. 然后,将苯乙酸加入另一个反应器中,加入碘和红磷催化剂,反应生成苯乙酮。
苯乙酮是一种无色液体,常用于合成树脂、涂料、橡胶和医药中间体等。
C6H5CH2COOH + I2 + H3PO4 →C6H5CH2COCH3 + CO2 + H2O
3. 最后,将苯乙酮和甲酸加入反应器中,加入氢氧化钠催化剂,反应生成苯亚甲基丙酮。
苯亚甲基丙酮是一种无色油状液体,是合成冰毒的重要中间体。
C6H5CH2COCH3 + HCOOH + NaOH →C9H10O + Na2CO3 + H2O
总的反应方程式为:
C6H5CH=CH2 + 2HCOOH + 2I2 + 2H3PO4 + 2NaOH →C9H10O + 2CO2 + 2Na2HPO4 + 2H2O
需要注意的是,苯亚甲基丙酮合成是一种非法活动,严格禁止从事。
本文仅介绍其化学反应历程,不鼓励任何违法行为。


超声辐射技术合成苯亚甲基苯乙酮
王振华;李记太;杨文智;孙汉文
【期刊名称】《实验室研究与探索》
【年(卷),期】2003(022)001
【摘要】超声辐射下,苯甲醛和苯乙酮在氢氧化钠催化下于25~30℃反应30~35 min,苯亚甲基苯乙酮的收率87%.是一个适合于本科生的声化学实验.
【总页数】2页(P50-50,52)
【作者】王振华;李记太;杨文智;孙汉文
【作者单位】河北大学,化学与环境科学学院,河北,保定,071002;河北大学,化学与环境科学学院,河北,保定,071002;河北大学,化学与环境科学学院,河北,保定,071002;河北大学,化学与环境科学学院,河北,保定,071002
【正文语种】中文
【中图分类】Q787
【相关文献】
1.苯亚甲基苯乙酮合成方法的改进 [J], 胡晓允;周忠强;单自兴
2.超声辐射合成苯亚甲基苯乙酮的研究 [J], 阿布力米提·阿布都卡德尔;孙亚栋;张永红;张增鹏
3.苯亚甲基苯乙酮-4-氯苯甲酰腙的合成、晶体结勾及荧光性质 [J], 王亮;刘娟;郑长征;任立娣
4.利用"思维激活法"培养学生的探究与创造兴趣的研究——以"制备苯亚甲基苯乙酮实验"为例 [J], 乔瑞;刘杰;魏影;刘鹏德;张淑萍
5.功能化离子液体催化合成苯亚甲基苯乙酮 [J], 胡晓允;韦丽艳;钟诗诗;陈玉;周忠强
因版权原因,仅展示原文概要,查看原文内容请购买。
苯亚甲基苯乙酮的制备
苯亚甲基苯乙酮是一种重要的有机化合物,可以用于制备各种有机化合物。
本文将介
绍苯亚甲基苯乙酮的制备方法。
苯亚甲基苯乙酮的化学式为C15H12O,分子量为208.26。
它是一种黄色的晶体,可溶
于乙醇和乙醚。
苯亚甲基苯乙酮可以通过苯甲醛和乙酸乙酯的缩合反应得到。
具体制备步骤如下:
1.将苯甲醛和乙酸乙酯按摩尔比1:1.1混合,并加入适量的醋酸催化剂。
2.在水浴中加热反应混合物,应控制温度在60℃左右。
3.反应进行2~3小时,此时观察到混合物已经变成黄色透明的凝胶状物质。
4.停止反应,将混合物降温至室温,放置冷却。
5.将冷却后得到的凝胶状物质用水洗涤至中性,然后用乙醚萃取。
6.将乙醚层过滤,蒸去乙醚,得到苯亚甲基苯乙酮的黄色晶体。
苯亚甲基苯乙酮在化学工业中有广泛的应用,例如可以用于制备染料、香精、药物等。
此外,苯亚甲基苯乙酮还可作为阳离子染料的染料原料,或者用于合成荧光染料。
总之,苯亚甲基苯乙酮的制备方法简单易行,且应用范围广泛。
在实际操作中应注意
反应条件的控制,以保证反应效果的最佳化。
苯亚甲基苯乙酮的制备实验报告苯亚甲基苯乙酮的制备实验报告引言:苯亚甲基苯乙酮,又称为P2P,是一种重要的有机化合物,广泛应用于医药、农药和染料等领域。
本实验旨在通过合成反应制备苯亚甲基苯乙酮,并对反应条件进行优化,以提高产率和纯度。
实验方法:1. 实验材料准备:a. 苯乙酮:用优质苯乙酮进行实验,确保原料的纯度。
b. 苯甲醛:选择高纯度的苯甲醛作为原料,以保证反应的可靠性。
c. 碱液:使用氢氧化钠(NaOH)溶液作为碱液,浓度为10%。
d. 氧化剂:选择过氧化氢(H2O2)作为氧化剂,浓度为30%。
e. 催化剂:采用氢氧化钠(NaOH)作为催化剂,在反应中起到加速反应速率的作用。
2. 实验步骤:a. 反应体系的配置:将苯乙酮、苯甲醛、碱液和催化剂按一定的摩尔比例加入反应瓶中,搅拌均匀。
b. 反应条件的控制:将反应瓶置于恒温槽中,控制反应温度在50℃左右,并在反应过程中不断搅拌。
c. 反应时间的控制:根据实验条件,控制反应时间为3小时,以确保反应充分进行。
d. 反应产物的提取:反应结束后,将反应混合物用醚进行提取,分离出有机相。
e. 产物的纯化:通过蒸馏或结晶等方法对有机相进行纯化,得到纯净的苯亚甲基苯乙酮。
实验结果与讨论:通过对反应条件的优化,我们得到了较高产率和纯度的苯亚甲基苯乙酮。
在本次实验中,我们选择了50℃的反应温度,这是由于在这个温度下,反应速率较快,同时产物的纯度也较高。
此外,我们还使用了10%的氢氧化钠溶液作为催化剂,其作用是加速反应速率,提高产物的收率。
实验中,我们还发现了一些问题。
首先,反应时间过长会导致产物的分解,从而降低产率。
因此,我们在实验中控制了反应时间为3小时,以确保反应的完全进行。
其次,苯乙酮和苯甲醛的摩尔比例也对产物的收率有一定影响。
在本次实验中,我们选择了适当的摩尔比例,以达到最佳的反应效果。
总结:通过本次实验,我们成功合成了苯亚甲基苯乙酮,并优化了反应条件,提高了产率和纯度。
课题二阿司匹林的合成(时间:45分钟)1.苯亚甲基苯乙酮俗称查尔酮,淡黄色棱状晶体,熔点58 ℃,沸点208 ℃(3.3 kPa)易溶于醚、氯仿和苯,微溶于醇。
制备原理如下:(1)制备过程中,需在搅拌下滴加苯甲醛,并控制滴加速度使反应温度维持在25~30 ℃,说明该反应是________(填“放热”或“吸热”)反应。
如温度过高时,则可以采取________________________措施。
(2)产品结晶前,可以加入几粒成品的查尔酮,其作用是____________________________________________________________。
(3)结晶完全后,需抽滤收集产物。
抽滤装置所包含的仪器除减压系统外还有______________、______________(填仪器名称)。
(4)获得的深色粗产品加入活性炭,以95%乙醇重结晶。
加入活性炭的作用是_________________________________________________________________________________________________________________________________。
解析(1)反应放热,需要控制滴液速度,且在搅拌散热下进行。
冰水可以降温,使反应速率减慢。
(2)提供晶种,可以加速结晶。
(3)抽滤装置中包含吸滤瓶、布氏漏斗。
(4)活性炭具有吸附性,从而可以脱色。
答案(1)放热冰水浴冷却(2)提供晶种,加速结晶(3)吸滤瓶布氏漏斗(4)吸附脱色2.草酸二乙酯可用于苯巴比妥等药物的中间体,实验室以草酸(HOOC—COOH)和乙醇为原料制备草酸二乙酯的实验步骤如下:步骤1:在如图所示装置中,加入无水草酸45 g,无水乙醇81 g,苯200 mL,浓硫酸10 mL,搅拌下加热6 870 ℃回流共沸脱水。
步骤2:待水基本蒸完后,分离出乙醇和苯。
步骤3:所得混合液冷却后依次用水、饱和碳酸氢钠溶液洗涤,再用无水硫酸钠干燥。
苯乙酮的制备研究苯乙酮是一种重要的化学原料,被广泛应用于医药、染料、香料、香精、树脂等领域。
其制备方法有多种,包括从苯乙烯、苯甲醛或苯乙酸等原料合成。
本文将探讨苯乙酮的制备研究,介绍不同方法的原理和优缺点,以期为相关领域的科研工作者提供参考。
一、苯乙酮的制备方法1. 从苯乙烯合成将苯乙烯和氧气在催化剂的存在下氧化反应,生成苯乙酮。
催化剂通常采用铜、铬、钴等金属氧化物,也可选择氧化硫酸亚铁等化合物。
该方法操作简便,但设备投资较大。
2. 从苯甲醛还原合成利用还原剂将苯甲醛还原得到苯乙醇,再经过氧化反应得到苯乙酮。
还原剂可选用金属钠、金属铝等。
该方法将苯甲醛作为原料,可利用多种合成途径制备苯乙酮。
首先将苯乙酸和氯化亚砜在氢氧化钠的存在下反应生成苯乙醛,然后再进行氧化反应制备苯乙酮。
该方法所需原料易得,操作简便,适合工业生产。
优点:原料易得,反应途径简单。
缺点:设备投资大,氧化反应选择催化剂需要谨慎,对环境要求高。
优点:利用多种还原剂可制备苯乙酮,适用性广。
缺点:苯甲醛原料价格较高,还原剂对环境有一定的影响。
3. 从苯乙酸酐羧化合成的优缺点优点:原料易得,操作简便,适合工业化生产。
缺点:反应条件要求严格,氯化亚砜等原料对人体有一定的毒性。
三、苯乙酮制备研究的发展趋势1. 利用生物技术随着生物技术的发展,利用酶、微生物等生物催化剂合成苯乙酮成为研究热点。
通过优化酶的反应条件和酶的特异性,可以提高合成效率,并减少对环境的污染。
2. 绿色合成方法在苯乙酮的合成过程中,绿色合成方法备受关注。
包括采用水为溶剂、利用可降解催化剂、减少废弃物产生等方法,致力于实现对环境友好的苯乙酮合成过程。
3. 新型催化剂研究新型催化剂对苯乙酮的合成具有重要作用,包括贵金属、过渡金属、离子液体等催化剂的研究。
这些催化剂不仅可以提高合成效率,还可以减少催化剂的使用量,降低成本。
苯亚甲基苯乙酮的制备
一、实验目的
1 掌握羟醛缩合反应原理和方法;
2掌握反应温度控制方法;巩固滴液漏斗、搅拌器的使用。
巩固重结晶。
二、反应式
NaOH -H 2O
C 6H 5CHO + CH 3COC 6H 5 C 6H 5CHOHCH 2COC 6H 5 C 6H 5CH=CHCOC 6H 5 反应历程:
OH +C
H 2C O
H C
H 2C O
+C
H 2C O
C
C O
C O
H CH C
CH 2
O O
+CH C
CH 2
O O CH C
CH 2
O OH
+OH
C 6H 5CH=CHCOC 6H 5
苯亚甲基苯乙酮又称查耳酮(cha-lcone)。
有顺(Z)-,反(E)-异构体。
(E)-构型:淡黄色棱状晶体,熔点58℃,沸点345~348℃(分解),219℃(2.4kPa)。
(Z)-构型:淡黄色晶体,熔点45~46℃。
合成的混合体:熔点55~57℃,沸点208℃(3.3kPa),相对密度1.0712,1.6458。
溶于乙醚、氯仿、二硫化碳和苯,微溶于乙醇,不溶于石油醚。
吸收紫外光。
有刺激性。
能发生取代、加成、缩合、氧化、还原反应。
由苯乙酮在碱性条件下与苯甲醛缩合而成。
用作有机合成试剂和指示剂。
查耳酮广泛应用于医药和日用化学品等领域。
查耳酮经典的合成方法是在乙醇水溶液中,强碱氢氧化钠或氢氧化钾催化苯甲醛和苯乙酮羟醛缩合后脱水而得到。
近年来,在无溶剂条件下的固相有机反应由于具有反应效率高、操作简单和环境友好等优点而深受关注。
1990年首次报道了在无溶剂条件下使用氢氧化钠催化取代苯甲醛和苯乙酮羟醛缩合,以比较高的收率得到相应的查耳酮。
1997年有人采用球磨技术进一步改善了有机固相反应的效率,克服了反应底物不能充分接触的缺点。
在无溶剂条件下利用氢氧化钠和碳酸钾混合碱作为催化剂,使用球磨技术促进取代苯甲醛和苯乙酮的固相羟醛缩合,反应时间明显缩短,收率可达到90%~98%。
-H 2O
三、物理常数
分子量状态熔点/℃沸点/℃比重溶解性
苯乙酮120.15
无色晶体,或淡黄色油状液
体,有象山楂的香气。
20.5 202.3 1.0281
乙醇,乙醚,
丙酮,苯,氯
仿
苯甲醛106.12
是无色或微黄色液体,具有
杏仁香味-26178 1.0415
乙醇,乙醚,
丙酮,苯,石
油醚
亚苄基
乙酰苯208 淡黄斜方或菱形晶体57~59 345-348 1.0712(62/4℃)
热乙醇
试剂用量减半:苯乙酮3g,0.025mol;苯甲醛2.65g, 0.025mol ,理论产量:5.2g
三、实验装置图
四、反应步骤
苯亚甲基苯乙酮是由苯甲醛与苯乙酮在10%氢氧化钠溶液催化下缩合而合成。
为了使反应顺利进行和控制苯甲醛的滴加速度,通常在装有搅拌器、温度计和滴液漏斗的三颈瓶中进行。
反应时间由滴加苯甲醛算起至加入晶种继续搅拌待反应瓶中有结晶止,需1.5~2.0h,产率67~72%。
在装有搅拌器、温度计和恒压漏斗的250ml三口烧瓶中,加入25ml10%氢氧化钠溶液、15ml乙醚和6ml苯乙酮。
搅拌下由恒压漏斗滴加5ml苯甲醛,控制滴加速度,保持反应温度在25~300C之间,必要时用冷水浴冷却。
滴加完毕后,继续保持此温度搅拌0.5h。
然后加入几粒苯亚甲基苯乙酮作为晶种,室温下继续搅拌1~1.5h,即有固体析出。
反应结束后将三口烧瓶置于冰水浴中冷却15~30min,使结晶完全。
抽滤收集产物,用水充分洗涤,至洗涤液对石蕊试纸显中性。
然后用少量冷乙醇(5~6ml)洗涤结晶,挤压抽干,得苯亚甲基苯乙酮粗品。
粗产物用95%乙醇重结晶(每克产物约需4~5ml溶剂),若溶液颜色较深可加少量活性炭脱色,得浅黄色片状结晶6~7g,熔点56~570C。
五、实验流程
六、注意要点
(1)苯甲醛须新蒸馏后使用。
(2)控制好反应温度,温度过低产物发粘,过高副反应多。
(3)产物熔点较低,重结晶加热时易呈熔融状,故须加乙醇作溶剂使呈均相。
七、思考题
1.为什么本实验的主要产物不是苯乙酮的自身缩合或苯甲醛的Cannizzaro反应?
答: 苯乙酮的自身缩合的空间位阻比较大;苯甲醛发生Cannizzaro反应须在更高浓度的碱(40%NaOH)中进行
2.本实验中如何避免副反应的发生?
答:先将苯乙酮与碱混合,产生碳负离子,控制低温,防止苯乙酮的自身缩合;采取控温滴加与搅拌,有利于发生交叉羟醛缩合而防止苯甲醛的岐化。
3.本实验中,苯甲醛与苯乙酮加成后为什么不稳定并会立即失水?
答:生成的反式烯烃稳定,或者说亚甲基氢受羰基和羟基的影响比较活泼,易于消除。