9 蛋白质及氨基酸的测定
- 格式:ppt
- 大小:1.49 MB
- 文档页数:44




第十章蛋白质和氨基酸的测定练习题一、填空题1、凯氏定氮法是通过对样品总氮量的测定换算出蛋白质的含量,这是因为。
答案:含氮是蛋白质区别于其它有机化合物的主要标志2.凯氏定氮法消化过程中H2SO4的作用是;CuSO4的主要作用是。
答案:使蛋白质分解,有机氮转化为氨;催化剂3.凯氏定氮法的主要操作步骤分为四个步骤;在消化步骤中,需加入少量辛醇并注意控制热源强度,目的是;在蒸馏步骤中,清洗仪器后从进样口先加入,然后将吸收液置于冷凝管下端并要求,再从进样口加入 20%NaOH至反应管内的溶液有黑色沉淀生成或变成深蓝色,然后通水蒸汽进行蒸馏;蒸馏完毕,首先应,再蒸1分钟后,再停火断气。
答案:消化、蒸馏、吸收、滴定;消泡;样品消化稀释液;冷凝管的下端插入液面下;将冷凝管下端提离液面清洗管口4、消化时还可加入、助氧化剂。
答案:过氧化氢;次氯酸钾5、消化加热应注意,含糖或脂肪多的样品应加入作消泡剂。
答案:辛醇或液体石蜡或硅油6、消化完毕时,溶液应呈颜色。
答案:蓝绿色7、用甲基红-溴甲酚绿混合指示剂,其在碱性溶液中呈色,在中性溶液中呈色,在酸性溶液中呈色。
答案:绿;灰;红8、凯氏定氮法用盐酸标准溶液滴定吸收液,溶液由变为色。
答案:蓝色;微红9、蛋白质分子中因含有两个以上的,与双缩脲结构相似,因此也有双缩脲反应。
答案:肽键10、双指示剂甲醛滴定法测氨基酸总量,所用的指示剂是剂。
此法适用于测定食品中氨基酸。
若样品颜色较深,可用处理或用方法测定。
答案:中性红指示剂和百里面酚酞指示剂;游离;活性碳;电位滴定法11、凯氏定氮法碱化蒸馏后,用作吸收液.。
答案:硼酸12、食品中氨基酸态氮含量的测定方法有和,该方法的作用原理是利用氨基酸的,甲醛的作用是。
答:电位滴定法;双指示剂甲醛滴定法;两性性质;固定氨基13、凯氏定氮法测定蛋白质步骤分为、、和。
答:湿法消化;碱化蒸馏;硼酸吸收;盐酸标定。
14、双指示剂甲醛滴定法测氨基酸总量,取等量的两份样品,在两份样品中分别加入指示剂和,用氢氧化钠标准溶液滴定至终点分别呈和颜色。


食品分析与检验蛋白质与氨基酸的测定蛋白质与氨基酸的测定在食品分析与检验领域中具有重要意义。
蛋白质是食品中重要的营养组分,而氨基酸是构成蛋白质的基本单元,对于评价食品的品质和安全性具有重要意义。
本文将介绍蛋白质与氨基酸的测定方法及其在食品分析与检验中的应用。
蛋白质的测定方法主要有几种:生物测定法、光谱法和色谱法。
其中,生物测定法主要是通过测定食品中的氮元素含量来间接测定蛋白质含量。
常用的方法有凯氏氮法、造浆法和改良Kjeldahl法等。
光谱法主要是通过根据蛋白质的特征光吸收谱测定其含量。
常用的方法有紫外-可见光谱法、荧光光谱法和红外光谱法等。
色谱法是通过分离和检测蛋白质的各种成分来测定其含量。
常用的方法有凝胶过滤层析法、液相色谱法和气相色谱法等。
氨基酸是构成蛋白质的基本单元,对于评价蛋白质的营养价值和品质具有重要作用。
氨基酸的测定方法主要有色谱法和生物传感器方法。
其中,色谱法是目前最主要的氨基酸定量方法,其主要包括高效液相色谱法和气相色谱法。
高效液相色谱法常用于氨基酸的定性和定量分析,具有灵敏度高、选择性好和分析速度快的特点;气相色谱法通常用于氨基酸的定性分析,具有高分离能力和分析速度快的优势。
生物传感器方法是一种新兴的氨基酸测定方法,通过利用生物传感器对氨基酸的选择性响应来测定其含量。
生物传感器方法具有灵敏度高、反应快和操作简便等特点。
在食品分析与检验中,蛋白质与氨基酸的测定具有广泛的应用。
首先,蛋白质含量是评价食品营养价值的重要指标之一、通过测定食品中蛋白质的含量,可以评估其蛋白质营养价值和食品质量。
其次,氨基酸是判定食品蛋白质种类和品质的重要指标。
通过测定食品中各种氨基酸的含量,可以评价蛋白质的品质和营养价值。
此外,蛋白质与氨基酸的测定还可以用于食品的伪标问题的检验,如检验食品中是否含有非法添加的蛋白质或氨基酸衍生物。
综上所述,蛋白质与氨基酸的测定在食品分析与检验中具有重要意义。
通过选择合适的测定方法,可以准确、快速地测定食品中的蛋白质含量和氨基酸组成,从而评价食品的品质、安全性和营养价值。

测定食品中的蛋白质---2013.3.25组员:***实验目的:(1)会测定食品中粗蛋白的含量。
(2)明确常见的食品蛋白质含量,以及测定原理。
实验原理:将被检样品加入浓硫酸,以硫酸铜,硫酸钾为催化剂共同加热消化食品中蛋白质分解为氨,并与硫酸结合成硫酸铵,通过碱化蒸馏,使氨分离出来,用硼酸吸收形成硼酸按后,再用盐酸标准溶液滴定,根据消耗的标准盐酸的体积,通过换算系数,可测定食品中蛋白质的含量。
实验仪器:凯氏烧瓶、可调式电炉、定氮蒸馏装置试剂:①硫酸铜CuSO4.5H2O ②硫酸钾③硫酸(密度为1.8149g/L)④40g/L 硼酸溶液⑤混合试剂;1g/L甲基红乙醇溶液与1g/L亚甲基蓝乙醇溶液,用时按2:1的比例混合。
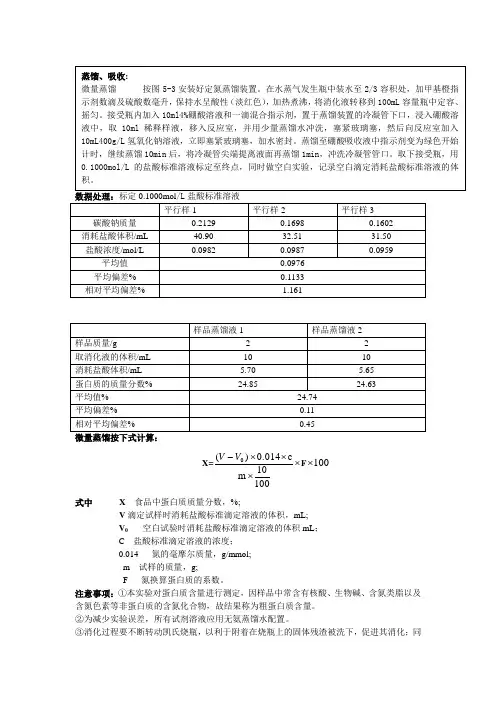
实验步骤:数据处理:标定0.1000mol /L 盐酸标准溶液微量蒸馏按下式计算:X=⨯⨯⨯⨯-10010m c0.014)(0V V F 100⨯式中 X 食品中蛋白质质量分数,%;V 滴定试样时消耗盐酸标准滴定溶液的体积,mL;V 0 空白试验时消耗盐酸标准滴定溶液的体积mL ;C 盐酸标准滴定溶液的浓度; 0.014 氮的毫摩尔质量,g/mmol; m 试样的质量,g;F 氮换算蛋白质的系数。
注意事项:①本实验对蛋白质含量进行测定,因样品中常含有核酸、生物碱、含氮类脂以及含氮色素等非蛋白质的含氮化合物,故结果称为粗蛋白质含量。
②为减少实验误差,所有试剂溶液应用无氨蒸馏水配置。
③消化过程要不断转动凯氏烧瓶,以利于附着在烧瓶上的固体残渣被洗下,促进其消化;同时为防止造成氮损失,不要用强火,应保持缓和沸腾。
④样品中含脂肪或糖较多,消化过程中易产生大量泡沫,为防止泡沫外溢,在消化开始时用小火加热,并时时摇动,并可以加入少量辛醇、液体石蜡或硅油消泡剂,并控制热源强度。
⑤一般消化至呈透明后,继续消化30min即可,但对于含有特别难以氨化的氮化合物的样品,如含赖氨酸、组氨酸、色氨酸、酪氨酸或脯氨酸等时,呈较深绿色。


实验9 蛋白质及氨基酸的颜色反应一、目的和要求1、了解蛋白质和某些氨基酸的特殊颜色反应及其原理2、掌握几种常用鉴定蛋白质和氨基酸的方法二、试剂1.鸡蛋清。
2.蛋白质溶液:将鸡蛋清用蒸馏水稀释10~20倍,3层纱布过滤,滤液冷藏备用。
3.10% NaOH溶液;20% NaOH。
4.浓硝酸(比重1.42);浓盐酸;浓硫酸(分析纯);冰醋酸(一般含有乙醛酸杂质,故可用冰醋酸代替乙醛酸)。
5.1% CuSO4溶液。
6.10% Pb(Ac)2溶液(醋酸铅溶液)。
7.醋酸铅试纸:将滤纸条浸入10% 醋酸铅溶液中,湿透后取出,100℃烘干即可。
8.0.5% 甘氨酸溶液。
9.0.3% 色氨酸溶液。
10.0.3% 酪氨酸溶液。
11.0.3% 精氨酸。
12.0.3% 组氨酸溶液。
13.0.1% 茚三酮水溶液。
14.0.1% 茚三酮-乙醇溶液(称取0.1g茚三酮,溶于100mL 95% 乙醇。
临用前配制)。
15.头发;指甲屑。
16.0.5% 苯酚溶液。
17.1% α-萘酚乙醇溶液,临用时配制。
18.NaBrO溶液:2克溴溶于100ml 5% NaOH中,置棕色瓶中,可在暗处保存两周。
19.偶氮试剂:溶液A:5克亚硝酸钠溶于1000ml水中。
溶液B:5克对氨基苯磺酸溶于1000ml水中,溶解后再加入5ml浓硫酸。
A、B溶液分别保存在密闭瓶中,用时以等体积混合。
三、实验内容对蛋白质及氨基酸的双缩脲反应、茚三酮反应、黄色反应、坂口反应、乙醛酸反应、偶氮反应、醋酸铅反应等进行定性确定。
(一)双缩脲反应1、实验原理当尿素加热到180℃左右时,两个分子的尿素缩合可放出一个分子氨后形成双缩脲,双缩脲在碱性溶液中与铜离子结合生成复杂的红色配合物,此呈色反应称为双缩脲反应。
由于蛋白质分子中含有多个肽键,其结构与双缩脲相似,故能呈此反应,而形成紫红色或蓝紫色的配合物。
此反应常用作蛋白质的定性或定量的测定。
2、操作取一支试管,加入蛋白质溶液约1ml 和10% NaOH 溶液2ml ,摇匀,再加1% CuSO 4溶液两滴,随加随摇。

习题九、食品中蛋白质的测定一、填空题1.凯氏定氮法是通过对样品总氮量的测定换算出蛋白质的含量,这是因为。
2.凯氏定氮法消化过程中浓H2SO4的作用是 ;CuSO4的作用是。
3.凯氏定氮法测定蛋白质含量时,在消化步骤中,有时需加入少量辛醇并注意控制热源强度,目的是 ;在蒸馏步骤中,清洗仪器后,然后将吸收液置于冷凝管下端并要求 ,然后从加样口加入 再加入10mL40%NaOH至反应管内的溶液有黑色沉淀生成或变成深蓝色,然后通水蒸汽进行蒸馏;蒸馏完毕,首先应,再停火断气。
4.氨基酸态氮反映的是样品中 的总量。
5.凯氏定氮法测定蛋白质含量过程中,样品经消化进行蒸馏之前加入NaOH的目的是 ,这是溶液的颜色会变为 ,是因为 ,如果颜色没有发生变化,应该 。
6.氨基酸态氮测定时,加入甲醛的作用是 。
7.凯氏定氮法共分四个步骤 、 、 、 。
8.消化加热应注意,含糖或脂肪多的样品应加入 作消泡剂。
9.消化完毕时,溶液应呈 颜色。
10.凯氏定氮法测定蛋白质含量时,滴定用甲基红-溴甲酚绿混合指示剂,其在碱性溶液中呈 色,在酸性溶液中呈 色。
11.凯氏定氮法加入K2SO4的目的是 。
12.构成蛋白质的基本物质是 。
蛋白质区别于其他有机化合物的主要标志是。
13.凯氏定氮法碱化蒸馏后,用 吸收液。
二、判断题1.凯氏定氮法测定蛋白质时,加碱蒸馏前应将冷凝管的下端先没入硼酸吸收液中;蒸馏完毕,直接切断热源即可。
( )2.凯氏定氮法测得的蛋白质含量是样品中粗蛋白质的含量。
( )3.用复合电极测定溶液的pH时,必须首先进行定位校正。
( )4.某实验员在滴定分析中用最小刻度为0.1mL,标称容量为25mL的滴定管进行滴定,最后记录结果为16.4mL。
( )三、名词解释粗蛋白含量 蛋白质系数四、问答题1.凯氏定氮法测定蛋白质的原理及操作步骤如何?加入的各种试剂起什么作用?操作过程中有哪些注意事项?2.蛋白质蒸馏装置的水蒸气发生器中的水为什么要用硫酸调成酸性?3.凯氏定氮法测定蛋白质含量的测定结果为什么要乘以蛋白质系数?五、综合题现测定某试样中蛋白质的含量。
蛋白质与氨基酸的测定
蛋白质测定可以采用以下方法:
1. 比色法:常用的比色剂有布鲁姆甘蓝G、伯胺蓝、硫酸铜-法明斯试剂等。
比色法的原理是蛋白质与比色剂形成复合物,复合物的颜色与蛋白质的含量成正比。
2. 生物学方法:通过测定蛋白质在生物体中所起的生物学作用,如酶活性、免疫反应等来定量测定蛋白质的含量。
3. 尿素-二元酸法:通过加入细胞膜清洗液中的尿素和二元酸,并利用这两种化合物对蛋白质的溶解性,然后根据其溶解度定量测定蛋白质的含量。
氨基酸的测定可以采用以下方法:
1. 比色法:在酸性条件下,氨基酸与2,4-二硝基苯肼、2,4-二硝基苯胺等发生磺酰化反应,形成淡棕色的产物,比色法根据产物的吸光度来定量测定氨基酸的含量。
2. 二级结构破坏法:通过加热和高浓度酸的处理,使蛋白质的二级结构破坏,进而测定其中的氨基酸含量。
3. 比重法:在油水分离流程中,用比重法分离出有机相,然后加入酸性溶液,
氨基酸与酸反应,形成有颜色的产物,根据产物的吸光度来定量测定氨基酸的含量。