食品中蛋白质和氨基酸的测定(精)
- 格式:ppt
- 大小:123.00 KB
- 文档页数:51

食物中氨基酸的测定方法测定食物中的胱氨酸使用过甲酸氧化-氨基酸自动分析仪法,测定色氨酸使用荧光分光光度法,测定其它氨基酸使用氨基酸自动分析仪法。
一、氨基酸自动分析仪法1.原理食物蛋白质经盐酸水解成为游离氨基酸,经氨基酸分析仪的离子交换柱分离后,与茚三酮溶液产生颜色反应,再通过分光光度计比色测定氨基酸含量。
一份水解液可同时测定天冬,苏,丝,谷,脯,甘,丙,缬,蛋,异亮,亮,酪,苯丙,组,赖和精氨酸等16种氨基酸,其最低检出限为10pmol。
2.适用范围GB/T14965-1994食物中氨基酸的测定方法。
本法适用于食物中的16种氨基酸的测定。
其最低检出限为10pmol。
本方法不适用于蛋白质含量低的水果、蔬菜、饮料和淀粉类食物的测定3.仪器和设备3.1真空泵3.2恒温干燥箱3.3水解管:耐压螺盖玻璃管或硬质玻璃管,体积20~30ml。
用去离子水冲洗干净并烘干。
3.4真空干燥器(温度可调节)3.5氨基酸自动分析仪。
4.试剂全部试剂除注明外均为分析纯,实验用水为去离子水。
4.1浓盐酸:优级纯4.26mol/L盐酸:浓盐酸与水1:1混合而成。
4.3苯酚:需重蒸馏。
4.4混合氨基酸标准液(仪器制造公司出售):0.0025mol/L4.5缓冲液:4.5.1 pH2.2的柠檬酸钠缓冲液:称取19.6g柠檬酸钠(Na3C6H5O7.2H2O)和16.5ml浓盐酸加水稀释到1000ml,用浓盐酸或50%的氢氧化钠溶液调节pH至2.24.5.2 pH3.3的柠檬酸钠缓冲液:称取19.6g柠檬酸钠和12ml浓盐酸加水稀释到1000ml,用浓盐酸或50%的氢氧化钠溶液调节至pH至3.3。
4.5.3 pH4.0的柠檬酸钠缓冲液:称取19.6g柠檬酸钠和9ml浓盐酸加水稀释到1000ml,用浓盐酸或50%的氢氧化钠溶液调节pH至4.0。
4.5.4 pH6.4的柠檬酸钠缓冲液:称取19.6g柠檬酸钠和46.8g氯化钠(优级纯)加水稀释到1000ml,用浓盐酸或50%的氢氧化钠溶液调节pH至6.4。


习题九、食品中蛋白质的测定 答案一、填空题1.新鲜食品中的含氮化合物大都以蛋白质为主体。
2.脱水和氧化;催化剂、指示消化反应的完成、蒸馏时碱性反应的指示剂。
3.防止消化时产生的泡沫溢出瓶外;冷凝管尖端插入液面之下,样品消化液,将冷凝管尖端提离液面。
4.游离氨基酸。
5.使消化液呈碱性,便于氨游离出来,深蓝色或产生黑色沉淀,反应生成氢氧化铜,增加氢氧化钠的用量。
6.与氨基结合使氨基酸的碱性消失。
7.消化、蒸馏、吸收、滴定。
8.少量辛醇或液体石蜡或硅油。
9.澄清透明的蓝绿色。
10.蓝绿色、暗红色。
11.提高溶液沸点。
12.氨基酸,含氮。
13.硼酸。
二、判断题1.× 2.√ 3.√ 4.×三、名词解释1.粗蛋白含量:新鲜食品中含氮化合物大都以蛋白质为主体,凯氏定氮法是通过测出样品中的总含氮量再乘以相应的蛋白质系数而求出蛋白质的含量的方法。
由于样品中含有少量非蛋白质含氮化合物,如核酸、生物碱、含氮类脂、卟啉以及含氮色素等非蛋白质的含氮化合物,所以结果为粗蛋白含量。
2.蛋白质系数:每份氮素相当于的蛋白质的份数。
一般蛋白质含氮为16%,所以1份氮素相当于6.25份蛋白质,此数值(6.25)称为蛋白质系数。
不同种类食品的蛋白质系数不同。
四、问答题1.凯氏定氮法测定蛋白质的原理及操作步骤如何?加入的各种试剂起什么作用?操作过程中有哪些注意事项?原理:样品、浓硫酸和催化剂一同加热消化,使蛋白质分解,其中碳和氢被氧化为二氧化碳和水逸出,而样品中的有机氮转化为氨,并与硫酸结合成硫酸铵。
然后加碱蒸馏,使氨逸出,用硼酸溶液吸收后,再以标准盐酸溶液滴定。
根据消耗的标准盐酸液的体积可计算蛋白质的含量。
测定步骤:样品的消化、蒸留、吸收和滴定。
试剂及作用:硫酸铜催化剂和指示剂;硫酸钾提高沸点(4000C);浓硫酸消化;氢氧化钠溶液蒸留出氨气;硼酸溶液吸收氨气;盐酸标准溶液标定硼酸氨;溴甲酚绿-甲基红指示剂。
注意事项:所用试剂需用无氨蒸馏水配;消化初期先小火防泡沫溢出;蒸馏装置要密封,冷凝管要插入吸收瓶液液面之下;蒸馏结束一定要先撤吸收瓶再关电炉。



食品中氨基酸总量的测定实验报告一、实验目的本实验旨在测定食品中氨基酸的总量,了解食品中蛋白质的组成和营养价值,为食品质量控制和营养评估提供依据。
二、实验原理氨基酸是含有氨基和羧基的有机化合物,它们在一定条件下与某些试剂反应可以产生特定的颜色或荧光,通过比色或荧光检测可以定量测定氨基酸的含量。
本实验采用茚三酮显色法测定食品中氨基酸的总量。
茚三酮在弱酸性溶液中与氨基酸反应,生成蓝紫色化合物,其颜色的深浅与氨基酸的含量成正比。
在一定波长下测定溶液的吸光度,通过与标准曲线对比,可以计算出样品中氨基酸的总量。
三、实验材料与设备1、实验材料标准氨基酸溶液(已知浓度)待测食品样品(如肉类、豆类、谷物等)茚三酮试剂缓冲溶液(pH 值 50)乙醇蒸馏水2、实验设备分光光度计分析天平容量瓶(100 mL、50 mL、25 mL 等)移液管(1 mL、2 mL、5 mL 等)具塞刻度试管(25 mL)水浴锅离心机四、实验步骤1、标准曲线的绘制分别吸取 000 mL、020 mL、040 mL、060 mL、080 mL、100 mL 标准氨基酸溶液于 25 mL 具塞刻度试管中,用蒸馏水补足至 100 mL。
向各试管中加入 100 mL 缓冲溶液(pH 值 50)和 100 mL 茚三酮试剂,摇匀。
将试管置于沸水浴中加热 15 min,取出后立即用冷水冷却至室温。
向各试管中加入 500 mL 60%乙醇,摇匀。
使用分光光度计,在 570 nm 波长下,以蒸馏水为空白,测定各溶液的吸光度。
以氨基酸的含量(μg)为横坐标,吸光度为纵坐标,绘制标准曲线。
2、样品处理称取适量待测食品样品,精确至 0001 g,放入研钵中研碎。
将研碎的样品转移至离心管中,加入适量蒸馏水,在沸水浴中加热30 min,以提取氨基酸。
冷却后,离心(3000 rpm,10 min),取上清液备用。
3、样品测定吸取 100 mL 样品上清液于 25 mL 具塞刻度试管中,按照标准曲线绘制的步骤进行操作,测定样品溶液的吸光度。


图1 蛋白质含量的标准曲线图2.2 蜂蜜样品中蛋白质的含量蜂蜜各样品中的蛋白质含量,见表1。
1 六个蜂蜜样品中的蛋白质含量表/(g/100 g)相对标准偏差/%5平均值0.0430.0460.044±0.002 5.4240.0540.0510.054±0.004 6.4470.3880.3900.391±0.0030.6660.3740.3780.376±0.0030.6940.2220.2250.221±0.003 1.2570.3060.3020.302±0.0030.948以氨基酸含量为横坐标,吸光度值为纵坐标,绘制标准曲线,如图2所示。
曲线回归方程为:y=0.001 5x,R2=0.999 1XIANDAISHIPIN109现代食品/图2 氨基酸含量的标准曲线图表2 六个蜂蜜样品中的氨基酸含量表氨基酸含量12310.030 40.030 60.030 620.032 20.03160.032 430.048 00.04830.048 740.048 30.04810.047 750.055 10.05470.055 260.054 90.05510.055 93 结语从测定结果可知,考马斯亮蓝法和茚三酮显色法分别测定蜂蜜样品中的蛋白质和氨基酸含量,方法的精密度较高。
蜂蜜样品中蛋白质和氨基酸的含量有一定的差别[5]。
作为出口蜂蜜品种,龙眼蜜和荔枝蜜中的蛋白质含量相对较高,两个冬蜜样品中的含量稍低,但氨基酸的含量则相反。
野菊花蜜和山野百花蜜中的蛋白质及氨基酸的含量都极低。
参考文献:让.国家《蜂蜜》标准解读[J].蜜蜂春种一粒粟,秋成万颗子现代食品XIANDAISHIPIN。

食品中氨基酸总量的测定实验报告氨基酸含量的测定氨基酸含量的测定标准曲线绘制准确吸取200ug/ml的氨基酸标准溶液0.0,0.6,0.8,1.0,1.2,1.5,2.0ml,分别置于25ml容量瓶或比色管中,各加水补充至溶剂为4.0ml,然后加入茚三酮和磷酸缓冲溶液各1ml,混合均匀,于水浴上加热15min,取出迅速冷至室温,再摇匀,加水至标线25ml,摇匀。
静置15min后,在570nm波长下,以试剂空白为参比液夨订其余各溶液的吸光度A。
以氨基酸的微克数为横坐标,吸光度A为纵坐标,绘制标准曲线。
样品的测定:将虾研磨冷却过滤后稀释10倍,吸取澄清的样品溶液1.5ml,平行三次,按标准曲线制作步骤,在相同条件下测定吸光度A值,用测得的A值在标准曲线上即可查得氨基酸的微克数。
公式:氨基酸总量(ug/100g)=(c/m*1000)*100*10式中c是指从标准曲线上查得的氨基酸的ug数;M是指测定的样品溶液相当于样品的质量g;PH计酸度计测量ph的方法:(1)拿下笔帽(2)按on/off键,机器显示运作(3)将ph计放入待测液中(4)轻轻晃动ph计,保证内气泡逸出,使之于溶液充分接触,勿碰撞杯壁(5)ph计会立即显示数值,将笔置入待测液待数值稳定,30秒内将显示正确数值,(特:ph计数值上下浮动或不稳定是正常现象) (6)按hold键锁定数值,可在待测溶液外记录读取,继续按hold 键解除锁定(7)按on/off键关闭ph计(8)轻甩PH计测试笔上多于的水,用蒸馏水或脱离子水冲洗,盖上笔帽测量温度方法在测试模式下,温度数值与ph数值同步显示在液晶面板上,但在校准模式下不显示,数值默认为摄氏温度。
(一)挥发性盐基氮(TVB-N)的测定半微量定氮法(1)原理:蛋白质在酶和细菌的作用下分解后产生碱性含氮物质,有氨、伯胺、仲胺等,此类物质具有挥发性,可在碱性溶液中被蒸馏出来,用标准酸滴定,计算含量。
(2)试剂①氧化镁混悬液(10g/L)称取1.0g氧化镁,加100ml水,振摇成混悬液。
测定食品中的蛋白质---2013.3.25组员:***实验目的:(1)会测定食品中粗蛋白的含量。
(2)明确常见的食品蛋白质含量,以及测定原理。
实验原理:将被检样品加入浓硫酸,以硫酸铜,硫酸钾为催化剂共同加热消化食品中蛋白质分解为氨,并与硫酸结合成硫酸铵,通过碱化蒸馏,使氨分离出来,用硼酸吸收形成硼酸按后,再用盐酸标准溶液滴定,根据消耗的标准盐酸的体积,通过换算系数,可测定食品中蛋白质的含量。
实验仪器:凯氏烧瓶、可调式电炉、定氮蒸馏装置试剂:①硫酸铜CuSO4.5H2O ②硫酸钾③硫酸(密度为1.8149g/L)④40g/L 硼酸溶液⑤混合试剂;1g/L甲基红乙醇溶液与1g/L亚甲基蓝乙醇溶液,用时按2:1的比例混合。
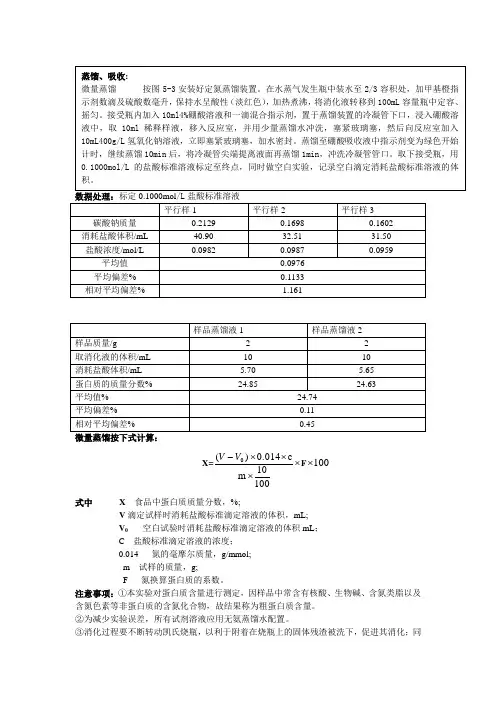
实验步骤:数据处理:标定0.1000mol /L 盐酸标准溶液微量蒸馏按下式计算:X=⨯⨯⨯⨯-10010m c0.014)(0V V F 100⨯式中 X 食品中蛋白质质量分数,%;V 滴定试样时消耗盐酸标准滴定溶液的体积,mL;V 0 空白试验时消耗盐酸标准滴定溶液的体积mL ;C 盐酸标准滴定溶液的浓度; 0.014 氮的毫摩尔质量,g/mmol; m 试样的质量,g;F 氮换算蛋白质的系数。
注意事项:①本实验对蛋白质含量进行测定,因样品中常含有核酸、生物碱、含氮类脂以及含氮色素等非蛋白质的含氮化合物,故结果称为粗蛋白质含量。
②为减少实验误差,所有试剂溶液应用无氨蒸馏水配置。
③消化过程要不断转动凯氏烧瓶,以利于附着在烧瓶上的固体残渣被洗下,促进其消化;同时为防止造成氮损失,不要用强火,应保持缓和沸腾。
④样品中含脂肪或糖较多,消化过程中易产生大量泡沫,为防止泡沫外溢,在消化开始时用小火加热,并时时摇动,并可以加入少量辛醇、液体石蜡或硅油消泡剂,并控制热源强度。
⑤一般消化至呈透明后,继续消化30min即可,但对于含有特别难以氨化的氮化合物的样品,如含赖氨酸、组氨酸、色氨酸、酪氨酸或脯氨酸等时,呈较深绿色。

实验九食品中氨基酸含量的测定――茚三酮比色法1、目的通过实验,掌握茚三酮比色法测定氨基酸的方法。
2、原理凡含有自由氨基的化合物,如蛋白质、多肽、氨基酸的溶液与水合茚三酮共热时,能产生紫色化合物,可用比色法进行测定。
氨基酸与茚三酮的反应分两个步骤。
第一步是氨基酸被氧化形成CO2、NH3和醛、茚三酮被还原成还原型茚三酮;第二步是所形成的还原型茚三酮与另一个茚三酮分子和NH3缩合生成有色物质。
3、实验材料与仪器3.1材料大豆、奶粉、火腿肠等(1) 0.2mol/L柠檬酸缓冲液,pH5.0(2) 80%乙醇(3) 10mmol/L KCN:称取0.1638gKCN溶于蒸馏水中,稀释至250ml备用(注意:KCN剧毒!)(4) KCN-乙二醇甲醚-茚三酮溶液:称取1.25g重结晶茚三酮溶于25ml经重蒸馏的乙二醇甲醚中使成5%溶液。
将2.5ml10mmol/L KCN溶液用乙二醇甲醚溶液稀释至125ml充分混合。
然后将125mlKCN—乙二醇甲醚溶与25ml茚三酮-乙二醇甲醚溶液相混合,置试剂瓶待用,正常情况下应为浅黄色。
(5 )标准氨基酸溶液:称取亮氨酸20mg溶于10ml蒸馏水中,则得浓度为200μg/ml的母液。
上述所有试剂必须放在草酸保护的干燥器中,以免被空气中的NH3所污染。
(6) 乙二醇甲醚(CH3OCH2CH2OH, methyl cellusolve)的处理:将5g硫酸亚铁加在500g乙二醇甲醚中,振摇1─2小时。
过滤除去硫酸亚铁(若滤液混浊没有关系),再在蒸馏瓶中蒸馏,收集沸点121─125℃部分,此时应为透明无色液体。
KCN-乙二醇甲醚-茚三酮溶液配制后必须隔夜才能应用。
配制后1星期内稳定,若超过1星期则灵敏度降低,不宜作定量。
(7) 茚三酮重结晶:即使AR级的茚三酮,由于保管不当,常带微红色,配成溶液后也带红色,影响比色测定,故需重结晶一次方可应用。
5g茚三酮溶于15ml热蒸馏水中,加入0.25g活性炭,轻轻摇动,若溶液太稠不易操作,可酌量加水5─10ml,30分钟后用滤纸过滤,滤液放冰箱中过液,次晨即见微黄色结晶出现,过滤,再以1ml冷水洗涤结晶,置于干燥器中干燥,最后装入棕色试剂瓶中保存。
习题九、食品中蛋白质的测定一、填空题1.凯氏定氮法是通过对样品总氮量的测定换算出蛋白质的含量,这是因为。
2.凯氏定氮法消化过程中浓H2SO4的作用是 ;CuSO4的作用是。
3.凯氏定氮法测定蛋白质含量时,在消化步骤中,有时需加入少量辛醇并注意控制热源强度,目的是 ;在蒸馏步骤中,清洗仪器后,然后将吸收液置于冷凝管下端并要求 ,然后从加样口加入 再加入10mL40%NaOH至反应管内的溶液有黑色沉淀生成或变成深蓝色,然后通水蒸汽进行蒸馏;蒸馏完毕,首先应,再停火断气。
4.氨基酸态氮反映的是样品中 的总量。
5.凯氏定氮法测定蛋白质含量过程中,样品经消化进行蒸馏之前加入NaOH的目的是 ,这是溶液的颜色会变为 ,是因为 ,如果颜色没有发生变化,应该 。
6.氨基酸态氮测定时,加入甲醛的作用是 。
7.凯氏定氮法共分四个步骤 、 、 、 。
8.消化加热应注意,含糖或脂肪多的样品应加入 作消泡剂。
9.消化完毕时,溶液应呈 颜色。
10.凯氏定氮法测定蛋白质含量时,滴定用甲基红-溴甲酚绿混合指示剂,其在碱性溶液中呈 色,在酸性溶液中呈 色。
11.凯氏定氮法加入K2SO4的目的是 。
12.构成蛋白质的基本物质是 。
蛋白质区别于其他有机化合物的主要标志是。
13.凯氏定氮法碱化蒸馏后,用 吸收液。
二、判断题1.凯氏定氮法测定蛋白质时,加碱蒸馏前应将冷凝管的下端先没入硼酸吸收液中;蒸馏完毕,直接切断热源即可。
( )2.凯氏定氮法测得的蛋白质含量是样品中粗蛋白质的含量。
( )3.用复合电极测定溶液的pH时,必须首先进行定位校正。
( )4.某实验员在滴定分析中用最小刻度为0.1mL,标称容量为25mL的滴定管进行滴定,最后记录结果为16.4mL。
( )三、名词解释粗蛋白含量 蛋白质系数四、问答题1.凯氏定氮法测定蛋白质的原理及操作步骤如何?加入的各种试剂起什么作用?操作过程中有哪些注意事项?2.蛋白质蒸馏装置的水蒸气发生器中的水为什么要用硫酸调成酸性?3.凯氏定氮法测定蛋白质含量的测定结果为什么要乘以蛋白质系数?五、综合题现测定某试样中蛋白质的含量。
第十章 蛋白质和氨基酸的测定第一节 概述蛋白质是生命的物质基础,是构成生物体细胞组织的重要成分,是生物体发育及修补组织的原料。
一切有生命的活体都含有不同类型的蛋白质。
人体内的酸、碱及水分平衡,遗传信息的传递,物质代谢及转运都与蛋白质有关。
人及动物只能从食物中得到蛋白质及其分解产物,来构成自身的蛋白质,故蛋白质是人体重要的营养物质,也是食品中重要的营养成分。
蛋白质在食品中含量的变化范围很宽。
动物来源和豆类食品是优良的蛋白质资源。
部分种类食品的蛋白质含量见表10-1表10-1 部分食品的蛋白质含量蛋白质是复杂的含氮有机化合物,摩尔质量大,大部分高达数万~数百万,分子的长轴则长达1nm ~100nm ,它们由20种氨基酸通过酰胺键以一定的方式结合起来,并具有一定的空间结构,所含的主要化学元素为C 、H 、O 、N ,在某些蛋白质中还含有微量的P 、Cu 、Fe 、I 等元素,但含氮则是蛋白质区别于其它有机化合物的主要标志。
不同的蛋白质其氨基酸构成比例及方式不同,故各种不同的蛋白质其含氮量也不同。
一般蛋白质含氮量为16%,即1份氮相当于6.25份蛋白质,此数值(6.25)称为蛋白质系食 品 种 类 蛋白质的质量分数(以湿基计)/% 食 品 种 类 蛋白质的质量分数(以湿基计)/%谷类和面食大米(糙米、长粒、生) 7.9大米(白米、长粒、生、强化) 7.1小麦粉(整粒) 13.7玉米粉(整粒、黄色) 6.9意大利面条(干、强化) 12.8玉米淀粉 0.3乳制品牛乳(全脂、液体) 3.3牛乳(脱脂、干) 36.2切达干酪 24.9酸奶(普通的、低脂) 5.3水果和蔬菜苹果(生、带皮) 0.2芦笋(生) 2.3草莓(生) 0.6莴苣(冰、生) 1.0土豆(整粒、肉和皮) 2.1 豆类 大豆(成熟的种子、生) 36.5 豆(腰子状、所有品种、 23.6 成熟的种子、生) 豆腐(生、坚硬) 15.6 豆腐(生、普通) 8.1 肉、家禽、鱼 牛肉(颈肉、烤前腿) 18.5 牛肉(腌制、干牛肉) 29.1 鸡(可供煎炸的鸡胸肉、 23.1 生) 火腿(切片、普通的) 17.6 鸡蛋(生、全蛋) 12.5 鱼(太平洋鳕鱼、生) 17.9 鱼(金枪鱼、白色、罐 26.5 装、油浸、滴干的固体)数。
食物蛋白质氨基酸评分实验(查表计算法)(编写人: 南方医科大学公共卫生与热带医学学院甘露) (一)实验目的1. 掌握食物蛋白质氨基酸评分的计算方法;2. 通过对膳食中不同食物的蛋白质进行氨基酸评分,评价膳食中蛋白质的营养价值,并提出膳食改进建议。
(二)实验原理1. 氨基酸模式和限制氨基酸氨基酸模式(amino acid pattern):指某种蛋白质中各种必需氨基酸的构成比例。
计算方法为将该种食物蛋白质中的色氨酸含量定为1,分别计算其他必需氨基酸的相应比值,这一系列的比值就是该种蛋白质的氨基酸模式。
优质蛋白质(High Quality Protein):当食物蛋白质的氨基酸模式与人体蛋白质氨基酸模式相近时,必需氨基酸被机体利用的程度也越高,食物蛋白质的营养价值也相对越高。
这种蛋白质也被称为优质蛋白质,如动物性蛋白质中蛋、奶、肉、鱼等以及大豆蛋白,均属于优质蛋白。
参考蛋白(reference protein):鸡蛋蛋白质与人体蛋白质氨基酸模式最为接近,在实验中常以它作为参考蛋白。
限制氨基酸(limiting amino acid,LAA):食物蛋白质中一种或几种必需氨基酸相对含量较低,导致其它的必需氨基酸在体内不能被充分利用而浪费,造成其蛋白质营养价值降低,这些含量相对较低的必需氨基酸为限制氨基酸。
其中含量最低的为第一限制氨基酸,余者以此类推。
2. 氨基酸评分(Amino Acid Score,AAS):是用被测食物蛋白质的必需氨基酸与推荐的理想模式或参考蛋白的氨基酸模式进行比较,计算出比值,比值最低者为第一限制氨基酸。
即为该食物蛋白质的氨基酸评分。
3. 蛋白质的互补作用:将不同的食物适当混合,这些食物蛋白质之间可以取长补短,使其必需氨基酸的构成更加接近人体氨基酸需要量模式,从而提高蛋白质在体内的利用率,此为蛋白质互补作用。
食物蛋白质互补作用原则:生物学种属越远越好,搭配种类越多越好,同时食用最好。