苏州大学 分析化学 课程试卷与答案12
- 格式:doc
- 大小:145.00 KB
- 文档页数:11

苏州大学分析化学课程(7)卷参考答案共页院系化学化工学院专业一.选择题1. (2119) (3)2. (2214) (4)3. (0216) (1)4. (0305) (1)5. (3016) (1)6. (1564) (3)7. (4514) (1)8. (1348) (4)9. (1101) (4) 10. (1705) (3) 11. (1698) (4) 12. (1187) (3) 13. (1124) (2) 14. (1138) (2) 15. (1060) (2)16. (1051) (3) 17. (1467) (2) 18.(1453)(4)二.填空题1.(0340 2分)1.8⨯10-4,2.4⨯10-8(10-3.75,10-7.62)2.(2720 2分)[ML] + [ML2]+[M(OH)]+[M(OH)2]+[M][MY] +[ML] + [ML2]+[M(OH)]+[M(OH)2]+[M]3.(2471 2分)雾化器预混合室和燃烧头4.(3110 2分)2lgT05.(2004 2分)更高6.(2010 2分)0.17.(2387 2分)氢火焰离子化检测器三. 计算题1.(2357 5分)设缓冲溶液中[A -]=x (mol/L ),则4.60=4.30+lg 0.5)25.0*100(0.5100-+x 解得x=[A -]=0.38 (mol/L)原缓冲溶液的pH 为pH=4.30+ lg (0.38/0.25)=4.482.(2933 5分)∵(cV )S 2O 32- =6(cV )K 2Cr2O 7 =- 6⨯(490.3/294.2)⨯(25.00/100.00)∴c (Na 2S 2O 3)=- [6⨯(490.3/294.2)⨯(25.00/100.00)]/25.00 =0.1000(mol/L )3.(3093 5分)4.(3345 5分)5.(3049 5分)四.问答题1.(4399 5分)(1)伸缩振动强(2)反对称伸缩振动强(3)基频峰强因红外吸收峰强度与偶极矩变化大小及振动形式有关。

苏州大学分析化学课程试卷(5)卷共8页考试形式闭卷年月日院系年级专业学号姓名成绩一.选择题(共36分)1.(本题2分)以下物质必须采用间接法配制标准溶液的是——————-—( )(1)K2Cr207 (2)Na2S203 (3)Zn (4)H2C204·2H202.(本题2分)关于总体平均值的概念不正确的理解是—————―――――( )(1) 随机变量有向某个中心值集中的趋势(2) 无限多次测定的平均值即为总体平均值μ(3) 总体平均值就是真值(4) 标准正态分布的μ=03.(本题2分)若醋酸的p K a=4.74,则其有效数字位数为———一——――—( )(1) 一位 (2) 二位 (3) 三位 (4) 四位4.(本题2分)中性水溶液是指————————————————――—( ) (1) pH = 7 (2) [H+]=[OH-](3) pH + pOH = 14 (4) pOH = 75.(本题2分)对0x-Red电对,25˚C时条件电位(E˚’)等于----------------( )(1) E˚ + 0.059/nlg a Ox/a Red(2) E˚ + 0.059/nlg c Ox/c Red(3) E˚ + 0.059/nlg γOx⋅a Ox/γRed⋅a Red(4) E˚ + 0.059/nlg γOx⋅a Red/γRed⋅a Ox6. (本题2分)在下面四个电磁辐射区域中,能量最大者是--------------------( )(1) X射线区(2) 红外区(3) 无线电波区(4) 可见光区7.(本题2分)发射光谱分析中,具有低干扰、高精度、高灵敏度和宽线性范围的激发光源是-------------------------------------------------------( )(1) 直流电弧(2) 低压交流电弧(3) 电火花(4) 高频电感耦合等离子体8.(本题)在原子吸收分光光度计中,目前常用的光源是----------------( )(1) 火焰(2)空心阴极灯(3)氙灯(4) 交流电弧9(本题2分)采用调制的空心阴极灯主要是为了-------------------------( ) (1) 延长灯寿命(2)克服火焰中的干扰谱线(3)防止光源谱线变宽(4) 扣除背景吸收10.(本题2分)原子化器的主要作用是-------------------------------- ( )(1) 将样品中待测元素转化为基态原子(2) 将样品中待测元素转化为激发态原子(3) 将样品中待测元素转化为中性分子(4) 将样品中待测元素转化为离子11.(本题2分)以下四种气体不吸收红外光的是――――――――――――()(1) H20(2) CO2(3) HCl(4) N212.(本题2分)试比较同一周期内下列情况的伸缩振动(不考虑费米共振与生成氢键)产生的红外吸收峰强度最大的是―――――――――――――――()(1)C-H(2)N-H(3)O-H(4)F-H13.(本题2分)在下面四个结构式中,哪个画有圈的质子有最大的屏蔽常数σ------------------------------------------------------()(1) (2)R C CH3(H)H CH3C CH3(H)H(3) (4)CH3C CH3(H)CH3H C H(H)H14.(本题2分)利用选择性系数可以估计干扰离子带来的误差,若K i,j = 0.05,干扰离子的浓度为0.1 mol/L,被测离子的浓度为0.2mol/L,其百分误差为(i、j均为一价离子)-------------------------------------------------( )(1) 2.5(2) 5(3) 10(4) 2015.(本题2分)分析挥发性宽沸程样品时,采用下列哪种方法---------------- ( )(1) 离子交换色谱法(2) 空间排阻色谱法(3) 梯度洗脱液相色谱法(4)程序升温气相色谱法16.(本题2分)分配系数是指在一定温度、压力下,组分在气-液两相间达到分配平衡时--------------------------------------------------------( )(1) 组分配在液相中的质量与分配在气相中的质量之比(2) 组分在液相中与组分在流动相中的浓度比(3) 气相所占据的体积与液相所占据的体积比(4) 组分在气相中的停留时间与组分在液相中的停留时间之比17.(本题2分)组分与固定液组分分子之间的作用力主要有-----------------( )(1) 静电力和诱导力(2) 色散力(3)氢键力(4) (1),(2),(3)18.(本题2分)在气相色谱法中,适于用氢火焰离子化检测器分析的组分是----( )(1) CS2(2) CO2(3) CH4(4) NH3二.填空题(共14分)1.(本题2分)丙二酸的p K a1=3.04,p K a2 =4.37,其共轭碱的K b1 = ,K b 2 = .2.(本题2分)对于某金属离子M与EDTA的络合物MY,其1g K'(MY)先随溶液pH增大而增大, 这是由于,而后又减小;这是由于。

苏州大学分析化学课程试卷(9)卷共8页一.选择题 (共36分)1.下面哪种说法不符合正态分布的特点————————————( 4 )(1) 大误差出现的概率小,小误差出现的概率大(2) 绝对值相同,正负号不同的误差出现的概率相等(3) 误差为零的测量值出现的概率最大(4) 各种数值的误差随机出现2.按四舍六入五成双规则将下列数据修约为四位有效数字(0.1058)的是( 3 ) (1) 0.10574 (2) 0.105749 (3) 0.10585 (4) 0.1058513.已知H3PO4的p K a1 = 2.12,p K a2 = 7.20,p K a3 = 12.36。
今有—磷酸盐溶液的pH=4.66,则其主要存在形式是——————————————( 2 )(1) HPO42-(2) H2PO4-(3) HPO42-+ H2P04-(4) H2PO4-+H3PO44.强酸滴定弱碱,以下指示剂不适用的是——―――――――( 3 )(1) 甲基橙(2 ) 甲基红(2) 酚酞(4) 溴酚蓝(p T=4.0 )5.由图所示说明比移值R f是指哪两段距离之比------------------( 2 )(1) AC (2) AB (3) AB (4) BCAB AC BC AB溶剂前沿斑点起始6.常用的紫外区的波长范围是------------------------------( 1 )(1) 200~360nm (2)360~800nm (3) 100~200nm (4) 103 nm7.用发射光谱进行定性分析时,作为谱线波长的比较标尺的元素是( 3 )(1) 钠(2) 碳(3) 铁(4) 硅8.原子吸收光谱分析过程中,被测元素的原子质量愈小,温度愈高,则谱线的热变宽将是――――――――――――――――――――――――( 1 )(1)愈严重(2)愈不严重(3)基本不变(4)不变9.在红外光谱分析中,用KBr作为样品池,这是因为―――――――( 3 )(1)KBr晶体在4000-400cm-1范围内不会散射红外光(2)KBr在4000-400cm-1范围内有良好的红外光吸收特性(3)KBr在4000-400cm-1范围内无红外光吸收(4)在4000-400cm-1范围内,KBr对红外无反射10.在下列化合物中,核磁共振波谱,OH基团的质子化学位移δ值最大的是(不考虑氢键影响)--------------------------------------( 2 )(1)R-OH (2)R-COOH (3)OH(4)Cl11.H H H⎪⎪⎪⋅ C ⋅ B ⋅ A丙烷H—C—C—C—H ,1H-NMR谱其各组峰面积之比(由高场至低场)是( 1 )⎪⎪⎪H H H(1) 3:1 (2) 2:3:3 (3) 3:2:3 (4)3:3:212.下列说法中,正确的是--------------------------( 4 ) 氟电极的电位(1) 随试液中氟离子浓度的增高向正方向变化(2) 随试液中氟离子活度的增高向正方向变化(3) 与试液中氢氧根离子的浓度无关(4) 上述三种说法都不对13.对于一对较难分离的组分现分离不理想,为了提高它们的色谱分离效率, 最好采用的措施为--------------------------------------------( 2 )(1) 改变载气速度(2) 改变固定液(3) 改变载体(4) 改变载气性质14.在以下因素中,属热力学因素的是-------------------------( 1 )(1) 分配系数(2) 扩散速度(3) 柱长(4) 理论塔板数15 .在气—液色谱分析中,组分与固定相间的相互作用主要表现为下述哪种过程?―――――――――――――――――――――――――( 2 )(1) 吸附—脱附(2) 溶解—挥发(3) 离子交换(4) 空间排阻16.下列检测器分析甜菜萃取液中痕量的含氯农药宜采用―――( 3 )(1) 热导检测器(2) 氢火焰离子化检测器(3) 电子捕获检测器(4) 碱火焰离子化检测器17.在液相色谱中,梯度洗脱最宜于分离――――――――――――( 4 )(1) 几何异构体(2) 沸点相近,官能团相同的试样(3) 沸点相差大的试样(4) 分配比变化范围宽的试样18.原子吸收光度法中的背景干扰表现为下述哪种形式?―――――( 3 )(1)火焰中被测元素发射的谱线(2)火焰中干扰元素发射的谱线(3)光源产生的非共振线(4)火焰中产生的分子吸收二.填空题(共14分)1. 0.1mol/L NaCl溶液的质子平衡式是 [H+] = [OH-] 。

结构 。
GB 计算与评价。
几次平行测定结果札I 互,偏差 《分析化学》课程试卷(3)参考答案 13・ 滴定,化学计量点,滴定终点,滴定误差/终点误差。
14. 1.00 ; 2.87 。
15.[A C I/CHAC 或 &/(©+["]) , 5心=\叽 16. P K HIQ , pK H m±l o 指小•剂的变色范囤应处于或部分处于化学计量点附近 的pH 突跃范|韦|内,且指示剂的颜色变化应便于观察。
17.cKa^lO'8 o K al /K a2^105 o 18.两性物质,A 严,A1O 2- o 19.EDTA , 乙二胺四乙酸 , Na 2H 2Y > 2H 2O ; 1 o 20.言接滴定法、返滴定法、置换滴定法、间接滴定法,言接滴定法。
21. 身指示剂、 变色指示剂,E]/应落在化学计量点附近的电位突跃范围 内,且尽量与E SD 接近 。
22.标定;酸。
棕色 。
23.共同离了效应、酸效应、络合效应、盐效应。
24.摩尔法、佛尔哈徳法、法扬司法。
A 在有机相总浓度 斑点中心到原点的距离°(。
加) 25. A 在两相总浓度% ° ; 溶剂前沿到原点的距离。
、填空题(1・6小题每空1分,其余每空0.5分,共35分)12. 测定结果与真实值,误差。
cir =^xl 00% = -^°l% X 100% = 0.05%0.02(%)二、选择填空题(共13分,请把选项的序号填在括号内)1(2 分). ①(B ); ②(D ); ③(D ); @(A); ⑤(D); (6)( C); ©( A)o2(2 分). (B 、 D ),(C )o3(2 分). (A ), (D ),(B 、 C )o 4(1 分). (A )°5(1 分). (B )o6(1 分). (D ); (B )。



大学分析化学课程试卷(6)卷共8页考试形式闭卷年月日院系年级专业学号成绩一.选择题(共36分)1.(本题2分)下列各项定义中不正确的是—————————————-—()(1) 绝对误差是测定值与真值之差(2)相对误差是绝对误差在真值中所占的百分比(3) 偏差是指测定值与平均值之差(4)总体平均值就是真值2.(本题2分)下列各数中,有效数字位数为四位的是—————————()(1) w(CaO)=25.30% (2) [H+]=0.0235mol/L(3)pH=10.46 (4) 4200 kg3.(本题2分)在下列各酸碱组分中,属于共轭酸碱对的是—---------------()(1) HCN―NaCN (2) H3P04—Na2HP04(3) +NH3CH2COOH—NH2CH2COO– (4) H30+—OH–4.(本题2分)浓度为c (mol/L)的NaCl水溶液的质子平衡式是——————( )(1) [Na+]+[C1―]= c (2) c = [Na+]+ICl―](3) [H+]=[OH–] (4) [H+] +[Na+]= [0H―]+ICl―]5.(本题2分)指出下列哪一个反应的滴定曲线在化学计量点前后是对称的——( )(1) 2Fe3++Sn2+=Sn4++2Fe2+(2) MnO4―+5Fe2++8H+=Mn2++5Fe3++4H20(3) Ce4++Fe2+=Ce3++Fe3+(4) I2+2S2O32-=2I―+S4062-6.(本题2分)在下面五个电磁辐射区域中,波长最短的是---------------( )(1) X射线区(2) 红外区(3) 无线电波区(4) 可见光区7.(本题2分)下面几种常用的激发光源中,分析的线性围最大的是-----( )(1) 直流电弧(2) 交流电弧(3) 电火花(4)高频电感耦合等离子体8.(本题2分)在原子吸收分光光度计中,目前常用的光源是-------------- ( )(1) 火焰(2) 空心阴极灯(3) 氙灯(4) 交流电弧9.(本题2分)在原子吸收分析中,如灯中有连续背景发射,宜采用-------- ( )(1) 减小狭缝(2) 用纯度较高的单元素灯(3) 另选测定波长(4)用化学方法分离10.(本题2分)在紫外光谱中,λmax最大的化合物是---------------------( )11.(本题2分)下列化合物中,同时有n→π*,π→π*,σ→σ*跃迁的化合物是----( )(1) 一氯甲烷(2) 丙酮(3) 1,3-丁二烯(4)甲醇12.(本题2分)CO2的如下振动中,何种属于非红外活性振动?------------()←→→←→↑↑↷↷(1)O = C = O (2) O = C = O (3) O=C=O (4) O=C=O↓13.(本题2分)在CH3CH2Cl 分子中何种质子σ值大?―――――――――――()(1)CH3-中的(2)CH2-中的(3)所有的(4)离Cl原子最近的14.(本题2分)钾离子选择电极的选择性系数为K K+,Mg2+=1.8⨯10-6,当用该电极测浓度为1.0⨯10-5mol/L K+,浓度为1.0⨯10-2mol/L Mg2+溶液时,由Mg2+引起的K+测定误差为-------------------------------------------------( )(1) 0.00018%(2) 134%(3) 1.8%(4)3.6%15.(本题2分)欲使分配比减小,采用的方法是-------------------------( )(1) 减小流动相速度(2) 增加固定相量(3) 增加柱温(4)增加柱长16.(本题2分)下列诸式中哪一个式子不能用来表示相对保留值γ2,1 ---------( )(1) t’R(2) / t’R(1)(2) v’R(2) / v’R(1)(3) k’R(2) / k’R(1)(4) t R(2) / t R(1)17.(本题2分)速率理论常用于-------------------------------------- ( )(1) 塔板数计算(2) 塔板高度计算(3) 色谱流出曲线形状的解释(4)解释色谱流出曲线的宽度与哪些因素有关18.(本题2分)在液相色谱中,空间排阻色谱的分离机理是根据被测组分在多孔凝胶中对孔的---------------------------------------------------- ( )(1) 渗透或被孔的排斥不同而分离的(2) 离子交换或亲合能力不同而分离的(3) 吸附或被孔的解吸不同而分离的(4)毛细扩散或被孔溶解不同而分离的二.填空题(共14分)1.(本题2分)H3PO4的p K a1 =2.12;p K a2 =7.20,p K a3 =12.36,则P043-的 p K b1=,p K b2 =, p K b3 =。

《分析化学》课程期末考试试卷一.单选题。
每题1分,共20分。
1、根据“四舍六入五留双”的修约原则,下列哪项是错误的() [单选题] *A、保留五位有效数字:7.28355→7.2836B、保留四位有效数字:17.4551→17.45(正确答案)C、保留三位有效数字:2.005→2.00D、保留四位有效数字:14.446→14.45E、保留四位有效数字:15.0250→15.022、下列哪种情况应采用返滴定法() [单选题] *A、用AgNO3标准溶液测定NaCl试样含量B、用HCl标准溶液测定Na2CO3试样含量C、用EDTA标准溶液测定Al3+试样含量(正确答案)D、用Na2S2O3标准溶液测定K2Cr2O7试样含量E、用EDTA标准溶液测定骨钙3、下列各项所造成的误差那一项属于系统误差() [单选题] *A、滴定管的读数15.05ml记为15.50mlB、滴定时温度有变化C、称重时天平的平衡点有变动D、用1:10的HCl代替1:1的HCl(正确答案)E、滴定过程中有溶液溅出4、下列滴定分析法的特点哪一项是错误的() [单选题] *A、操作简便、快速B、应用范围广C、准确度高D、可测痕迹量组分(正确答案)E、相对误差可达到0.1%5、强碱滴定强酸时,浓度均增大10倍,则滴定突跃范围将() [单选题] *A、增大0.5个pH单位(正确答案)B、增大1个pH单位C、增大1.5个pH单位D、增大2个pH单位E、不变6、将pH=1和pH=14的两种强电解质溶液按等体积混合,混合溶液pH为() [单选题] *A、1B、7C、7.5D、13E、13.65(正确答案)7、配制HClO4-冰醋酸溶液要加入计算量的醋酐,其目的是() [单选题] *A、增大样品溶解能力B、增大样品的酸碱性C、除去HClO4冰醋酸中的水分(正确答案)D、增大突跃范围使终点敏锐E、增强溶剂的区分(均化)效应8、在EDTA标准溶液的标定过程中采用的缓冲溶液是() [单选题] *A、醋酸-醋酸盐缓冲溶液B、磷酸-磷酸盐缓冲溶液C、硼酸-硼酸盐缓冲溶液D、枸橼酸-枸橼酸钠缓冲溶液E、氨-氯化铵缓冲溶液(正确答案)9、EDTA在什么酸度下主要以Y4-的形式存在() [单选题] *A、pH<2.0B、pH=2.7-6.2C、pH=2.0-2.7D、pH=6.2-10.2E、pH>10.2(正确答案)10、标定Na2S2O3标准溶液,常用下列何种基准物质() [单选题] *A、重铬酸钾(正确答案)B、铬酸钾C、草酸D、碳酸钠E、高锰酸钾11、引起酸差的溶液,其pH() [单选题] *A、pH<1(正确答案)B、pH>1C、pH>9D、pH<9E、pH<212、能级跃迁所需能量最小的是() [单选题] *A、σ→σ*B、σ→π*C、π→π*D、n→σ*E、n→π*(正确答案)13、激发光、荧光、磷光三者的波长关系正确的是() [单选题] *A、λ激发光>λ荧光>λ磷光B、λ激发光<λ荧光<λ磷光(正确答案)C、λ激发光=λ荧光=λ磷光D、λ激发光>λ磷光>λ荧光E、λ磷光>λ激发光>λ荧光14、在一般的质谱图上出现非整数质核比的峰,它可能是() [单选题] *A、分子离子峰B、碎片离子峰C、亚稳离子峰(正确答案)D、同位素峰E、同位素峰或碎片离子峰15、红外光谱上的特征区的波数范围是() [单选题] *A、4000~1300cm-1(正确答案)B、3000~1300cm-1C、2000~1300cm-1D、1375~720cm-1E、1300~400cm-116、在CH3CH2CH3 的高分辨NMR谱上,CH2质子的吸收峰分裂为() [单选题] *A、三重峰B、四重峰C、六重峰D、七重峰(正确答案)E、八重峰17、某化合物的质谱图中,检测出分子离子峰的质荷比m/z为115,化合物含有() [单选题] *A.偶数个氮原子B、奇数个氮原子(正确答案)C.任意数目的氮原子D.没有氮原子E、都不对18、对称峰的拖尾因子符合要求的范围是() [单选题] *A、0.85~1.15B、0.90~1.10C、0.95~1.05(正确答案)D、0.99~1.01E、0.2~0.819、用气相色谱法进行定量时,要求混合物中每一个组分都出峰的是() [单选题] *A、外标法B、内标法C、内标对比法D、归一化法(正确答案)E、外标一点法20、高效液相色谱法的定性指标是() [单选题] *A、峰面积B、保留时间(正确答案)C、半高峰宽D、峰高E、标准偏差二、判断题(每题2分,共30分)1、定量分析中,系统误差影响测定结果的精密度,偶然误差影响测定结果的准确度。

苏州大学分析化学课程试卷(8)卷一.选择题(共36分)1.在定量分析中,精密度与准确度之间的关系是————————( 3 )(1)精密度高,准确度必然高(2)准确度高,精密度也就高(3)精密度是保证准确度的前提(4)准确度是保证精密度的前提2.以下标准溶液可以用直接法配制的是——————————-—( 3 )(1) KMnO4 (2) NaOH (3) K2Cr2O7 (4)FeSO43.可以减小随机误差的方法是———————————————( 3 )(1) 对仪器进行校准(2) 做空白实验(3) 增加平行测定次数(4) 做对照试验4.浓度为c (mol/L)的NaCl水溶液的电荷平衡式是———————( 4 )(1) [H+] = [OH-] (2 ) [Na+]=[Cl-]= c(3)[Na+]+[Cl-]= c (4) [H+] +[H+] =[OH-]+[Cl-]5.以下溶液稀释10倍时pH改变最小的是——————————( 1 )(1) 0.1 mol/L NH4Ac (2) 0.1 mol/L NaAc(3)0.1 mol/L HAc (4) 0.1mol/L HCl6.用洗涤的方法能有效地提高沉淀纯度的是—――――――――( 2 )(1) 混晶共沉淀(2) 吸附共沉淀(3)包藏共沉淀(4) 后沉淀7.电子能级差愈小,跃迁时发射光子的――――――――――――( 2 )(1)能量越大(2)波长越长(3)波数越大(4)频率越高8.由原子无规则的热运动所产生的谱线变宽称为――――――――( 4 )(1)自然变宽(2)斯塔克变宽(3)劳伦茨变宽(4)多普勒变宽9.原子吸收光谱是――――――――――――――――――――( 4 )(1)分子的振动、转动能级跃迁时对光的选择吸收产生的(2)基态原子吸收了特征辐射跃迁到激发态后又回到基态时所产生的(3)分子的电子吸收特征辐射后跃迁到激发态所产生的(4)基态原子吸收特征辐射后跃迁到激发态所产生的10.红外光谱仪光源使用――――――――――――――――――( 2 )(1)空心阴极灯(2)能斯特灯(3)氘灯(4)碘钨灯11.某一个自旋核,产生核磁共振现象时,吸收电磁辐射的频率大小取决于------------( 4 )(1)样品的纯度(2)在自然界的丰度(3) 样品的存在状态(4) 外磁场强度大小12.离子选择电极的电位选择性系数可用于----------------------------------( 3 )(1) 估计电极的检测限(2) 估计共存离子的干扰程度(3) 校正方法误差(4) 计算电极的响应斜率13.根据范弟姆特方程式,在高流速情况下,影响柱效的因素主要是( 1 )(1) 传质阻力(2) 纵向扩散(3) 涡流扩散(4) 柱弯曲因子14.对于具有宽沸程组分的样品,为了保证分离度和缩短分析时间,色谱柱柱温的升温速度应采用――――――――――――――――――――( 3 )(1) 快速升温(2) 慢速升温(3) 程序升温(4)控制在某一固定温度15.测定有机溶剂中的微量水,下列四种检测器宜采用―――――( 1 )(1) 热导检测器(2) 氢火焰离子化检测器(3) 电子捕获检测器(4) 碱火焰离子化检测器16.塔板理论不能用于―――――――――――――――――――( 4 )(1) 塔板数计算(2)塔板高度计算(3)解释色谱流出曲线的形状(4)解释色谱流出曲线的宽度与哪些因素有关17.在化合物3,3—二甲基己烷的质谱图中,下列离子峰强度最大者为( 3 )(1) m/e 29 (2) m/e 57 (3) m/e 71 (4) m/e 8518.在醇类化合物中,O-H伸缩振动频率随溶液浓度的增加,向低波数方向位移的原因是――――――――――――――――――――――――( 2 )(1)溶液极性变大(2)形成分子间氢键随之加强(3)诱导效应随之变大(4)易产生振动偶合二.填空题 (共14分)1. HPO42-是 PO43-的共轭酸,是 H2PO4-的共轭碱,其水溶液的质子条件式是 [H+] +2[H3PO4]+[H2PO4-]=[OH-]+[PO43-] 2. 如下络合滴定反应中 M + Y = MY⎪ H+H i Y(i=1-6)[Y’]= [Y’] =[Y]+∑[H i Y] ,__ c(Y)=[Y’]+[MY] 。

苏州大学分析化学课程试卷( 2 )卷一.选择题 (共36分)1.下列物质中属于两性物质的有———————―――――――—( 3 )(1) H2C03(2) 氨基乙酸盐酸盐(3) 氨基乙酸(4) 氨基乙酸钠2.实验室中一般都是进行少数的平行测定,则其平均值的置信区间为―――――――――――――――――――――――――――( 4 )3.在磷酸盐溶液中,HP042-浓度最大时的pH是————――――( 1 ) (已知H3P04的离解常数p K a1 = 2.12,p K a2 = 7.20,p K a3 = 12.36)(1) 4.66 (2) 7.20 (3) 9.78 (4) 12.364.指出下列叙述中错误的结论———————————―――—( 4 )(1) 络合剂的酸效应使络合物的稳定性降低(2) 金属离子的水解效应使络合物的稳定性降低(3) 辅助络合效应使络合物的稳定性降低(4) 各种副反应均使络合物的稳定性降低5.下列表述中,最能说明偶然误差小的是――――――――――( 1 )(1)高精密度(2)与已知含量的试样多次分析结果的平均值一致(3)标准偏差大(4)仔细校正所用砝码和容量器皿等6.电子能级间隔越小,跃迁时吸收光子的――――――――――( 2 )(1)能量越大(2) 波长越长(3) 波数越大(4) 频率越高7.原子吸收分析对光源进行调制,主要是为了消除――――――( 2 )(1) 光源透射光的干扰(2) 原子化器火焰的干扰(3) 背景干扰(4) 物理干扰8.在原子吸收分析中,过大的灯电流除了产生光谱干扰外,还使发射共振线的谱线轮廓变宽.这种变宽属于――――――――――――――( 4 )(1) 自然变宽(2) 压力变宽(3) 场致变宽(4) 多普勒变宽(热变宽)9.甲烷分子振动自由度是――――――――――――――( 3 )(1) 5 (2) 6 (3) 9 (4) 1010.试比较同一周期内下列情况的伸缩振动(不考虑费米共振与生成氢键)产生的红外吸收峰强度最大的是――――――――――――――――( 4 )(1) C-H (2) N-H (3) O-H (4) F-H11.将11H放在外磁场中时,核自旋轴的取向数目为――――――( 2 )(1) 1 (2) 2 (3) 3 (4)512.氟化镧单晶膜氟离子选择电极的膜电位的产生是由于――――( 2 )(1) 氟离子在晶体膜表面氧化而传递电子(2) 氟离子进入晶体膜表面的晶格缺陷而形成双电层结构{3} 氟离子穿透晶体膜而使膜内外氟离子产生浓度差而形成双电层结构(4) 氟离子在晶体膜表面进行离子交换和扩散而形成双电层结构13.一般气相色谱法适用于―――――――――――――――――( 3 )(1) 任何气体的测定(2) 任何有机和无机化合物的分离、测定(3) 无腐蚀性气体与在气化温度下可以气化的液体的分离与测定(4) 任何无腐蚀性气体与易挥发的液体、固体的分离与鉴定14. 气相色谱中,用静电力、诱导力、色散力、氢键作用力四种力来说明――――――( 3 )(1) 被测分子间的作用力(2) 被测分子与流动相分子间的作用力(3) 被测分子与固定液分子间的作用力(4) 流动相分子与固定液分子间的作用力15.应用GC法来检测啤酒中微量硫化物的含量,宜选用那种检测器―――――――( 4 )(1)热导池检测器(2) 氢火焰离子化检测器(3) 电子捕获检测器(4) 火焰光度检测器16.利用气相色谱来测定某有机混合物,已知各组分在色谱条件下均可出峰,那么定量分析各组分含量时应采用―――――――――――――( 3 )(1) 外标法(2) 内标法(3) 归一化法(4) 工作曲线法17.在液相色谱中,某组分的保留值大小实际反映了哪些部分的分子间作用力――-( 3 )(1) 组分与流动相(2) 组分与固定相(3) 组分与流动相和固定相(4) 组分与组分18.在进行发射光谱定性和半定量分析时,――――――――――-( 1 )(1) 固定暗盒而移动哈特曼光栏(2) 固定哈特曼光栏而移动暗盒(3) 暗盒和光栏均要移动(4) 暗盒和光栏均不移动二.填空题:(共14分)1.用强碱滴定弱酸,当酸的浓度一定时,酸愈强(K a值愈大),它的共轭碱愈弱,滴定反应的完全程度愈高,突跃范围也愈大。
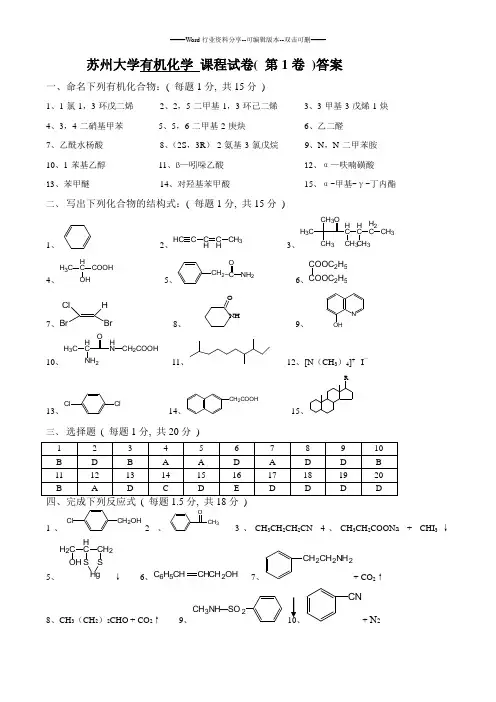
苏州大学有机化学 课程试卷( 第1卷 )答案一、命名下列有机化合物:( 每题1分, 共15分 )1、1-氯-1,3-环戊二烯2、2,5-二甲基-1,3-环己二烯3、3-甲基-3-戊烯-1-炔4、3,4-二硝基甲苯5、5,6-二甲基-2-庚炔6、乙二醛7、乙酰水杨酸8、(2S ,3R )-2-氨基-3-氯戊烷 9、N ,N-二甲苯胺10、1-苯基乙醇 11、ß—吲哚乙酸12、α—呋喃磺酸13、苯甲醚14、对羟基苯甲酸 15、α-甲基-γ-丁内酯二、 写出下列化合物的结构式:( 每题1分, 共15分 )1、 2、HC C C H C H CH 33、H 3CCH 3CH 3H C H C CH 3CH 3H 2C CH 3O4、H 3C HC COOHOH5、C O NH 2CH 2 6、COOC 2H 5COOC 2H 57、ClBrH Br8、9、NOH10、H 3C H CNH 2OHN CH 2COOH11、 12、[N (CH 3)4]+ I—13、Cl Cl14、CH 2COOH15、R三、 选择题 ( 每题1分, 共20分 )1、ClCH 2OH2 、OCH 33、CH 3CH 2CH 2CN4、CH 3CH 2COONa + CHI 3↓5、H 2C HC CH 2S SHg OH ↓ 6、CH CH 2OH C 6H 5CH7、CH 2CH 2NH 2+ CO 2↑8、CH 3(CH 2)2CHO + CO 2↑ 9、CH 3NH —SO 210、CN+ N 211、O COONa+OCH2OH12、COOHCOOH五、共12分)1、丙醛↓丙酮(—)(—)(—)褪色2、苯丙氨酸黄色(—)色氨酸HNO3 黄色紫色(—)3、乙醚溶解(不分层)乙烷分层乙醇↑4、(—)褪色丙烷(—)(—)丙烯褪色丙炔↓六、( )1、(共6分:推断2分⨯ 2,结构式2分)推导: 无还原性,不成脎,无变旋光,不成苷-----------无半缩醛羟基麦芽糖酶水解-------------------------------------α-苷键结构式:2、( 共6分:结构式1分⨯ 3,反应式1分⨯ 3 )结构式:A:C H2C H2CH3CH(C H3)2或B:CH3CH2CH3C:CH3CH3CH3反应式:CH2CH2CH3CH(CH3)2或(A)CH2CH2CH3CH(CH3)2NO2CH2CH2CH3CH(CH3)2NO2NO2NO2+或或CH3CH2CH3(B)NO2NO2+CH3CH2CH3CH3CH2CH3,CH3CH3(C)32( 注: A只答一个的扣0.5分)3、(共8分:结构式1分⨯4, 反应式1分⨯4 )浓H2SO4KMnO4Br2水HOOCCHO,H2SO4或浓HNO3浓H2SO4浓HNO3浓H2SO4结构式:A 、HOCH 2CONHCH (CH 3)COOHB 、HOCH 2COOHC 、CH 3CH (NH 2)COOHD 、CH 3CH (OH )COOH反应式:HOCH 2CONHCH (CH 3)COOHH 2COH N CH 3OO(可写可不写)(A)HOCH 2COOH + CH 3CH(NH 2)COOH(B) (C)HOCH 2COOH (B)HOOC —COOHCH 3CH (NH 2)COOH (C) CH 3CH (OH )COOH (D) + N 2↑CH 3CH (OH )COOH (D)CH 2COCOOH苏州大学有机化学 课程试卷 ( 第2卷 )答案四、命名下列有机化合物:( 每题1分, 共15分 )1、3,4,4-三甲基-2-乙基-1-戊烯2、α-萘酚3、苯甲醚4、4-乙基-2-环己烯酮5、丁烯二酸酐6、丙二酸二乙酯7、R-2-氨基丁酸8、E-3-甲基-2-戊烯 9、N-苯基苯甲酰胺10、对氨基苯磺酰胺 11、6-氨基嘌呤 12、D-葡萄糖13、叔丁基醇14、4-苯基-3-丁烯醛 15、苯丙氨酸二、写出下列化合物的结构式:( 每题1分, 共15分 )1、2、CH 2Br3、C HC CHCH 3HC4、 OH5、CHOOH 3C 6、H CH 3BrC 2H 57、CH 3HH 3CBr8、OO9、A B C D 1234567891011121314161715R10、H 2C HC SH COOHNH 211、H 2C CNH 2NH O HC CH 2PhCOOH12、ON(CH 3)2H13、C C OO O14 15、OBr3H +H 2O /H +[O] HNO 2 [O]四、完成下列反应式 ( 除注明外, 每题1.5分, 共18分 )1、CH 2OHCl2、H 2CCH 3OH 3C 3、COOH COOH4、CH 3CH 2CH 2CN5、H 3C H 2C C O CH 3+ CO 2 + H 2O6、CHCH 2OH C 6H 5CH7、OHSO 3Na8、CH 3CH 2—CH=CH —COOH9、H 2C CH 2Br Br (),H 2C CH 2CN CN (1.5分),H 2C CH 2C C O OOH OH(1.5分), H 2C CH 2C C O OO(1.5分)五、鉴别题( 每题3分, 共12分 )1、葡萄糖(—) ↓ 褪色果糖 (—) ↓ 甲基葡萄糖苷 (—) (—)淀粉 蓝色 2 、 苯胺 ↓乙酰苯胺 (—) 苯酚 显色3、 CH 2=CHCH 2Cl 褪色 AgNO 3 ↓(CH 3)2CHCH=CHCH 3 褪色 (—) (CH 3)2CHCH(CH 3)2 (—)4、甲乙胺 C 6H 5-SO 2Cl ↓ NaOH 不溶 乙二胺 ↓ 解溶 三乙胺 (—)六、推证结构式 (共20分 )1、( 共7分: 结构式 1分 ⨯3, 反应式 1分 ⨯4 )结构式: Ⅰ:CH 3CH 2COOH , Ⅱ:O OH CH 2CH 3 Ⅲ:O OH 3CCH 3反应式:CH 3CH 2COOH (Ⅰ)+ NaHCO 3 CH 3CH 2COONa + CO 2↑ + H 2OO O HCH 2CH 3HCOOH + C 2(Ⅱ) 3 ↓ + HCOONaO OH 3C CH 3 CH 3COONa + CH 3OH(Ⅲ)2、( 共7分: 结构式 1分 ⨯3, 反应式 1分 ⨯4 )结构式: A :CH 3CHCH 2CHCH 3NH 2CH 3B :CH 3CHCH 2CHCH 3OHCH 3C :CH 3CH=CHCHCH 3CH 3反应式:OH - H 2O H 2O OH -Br 2 Br 2水 AgNO 3 NH 3·H 20 I 2CH 3CHCH 2CHCH 3NH 2CH 3N 2 +CH 3CHCH 2CHCH 3OHCH 3(A)(B)3CHCH 2CHCH 3OHCH 3(B)I 2 / NaOHCH 3CH=CHCHCH 3CH 3(C)CHI 3+NaOOCCH 2CHCH 3CH 3CH 3CH=CHCHCH 3CH 34+(C)CH 3COOH +(CH 3)2CHCOOH3、(共6分: 结构式 1.5分 ⨯2, 反应式 1分 ⨯3 )结构式: A :H 3C H 2C C CH B :C H C HH 2CCH 2反应式:H 3C H 2C C CHH 3C H 2CC CAg ↓ (A )[O]H 3C H 2C COOH + CO 2↑ + H 2OC H CHH 2C CH 2CO 2 ↑+ HOOC —COOH + H 2O(B )苏州大学有机化学 课程试卷 ( 第 3卷) 答案一、命名下列化合物 (每题1分, 共15分)1、3-氯环戊烯2、甲基异丙基醚3、3-环戊烯-1-醇4、4-甲基-2-环己烯酮5、2-甲基-3-苯基丙烯酸6、甲酸乙酯7、R-2-氯丁烷8、E-1-氯-1,2-二溴乙烯 9、对羟基偶氮苯10、β-吡啶甲酰胺 11、 α-D-吡喃葡萄糖12、甘丙肽13、2-甲基-5-硝基-1,4-苯二酚 14、碘化三乙基苯铵 15、乙丙酐二、写出下列化合物的结构式 (每题1分, 共15分)1、S2、H 2C C 2H 5C O 3、OO H 2C4、H 2CCOOCH 3COOC 2H 55、AgNO 3 NH 3·H 2O[O]O OO6、Br H COOHH BrCH 37、HCH 38、NH 2BrBrBr 9、OCOOH 10、OH11、HOCH 2CHCOOHNH 212、NHO13、CH 3ONH 3CH 3C 14、OH CHO CH 2OH H15、N OHH三、选择题 (每题1分, 共20分)四、完成下列反应 ( 除注明外每题1.5分, 共18分)1、F 3C H 2C CH 2Br2、COOH3、CH 2Br(CHBr 2,CBr 3)4、CH 3CH 2COONa + CHI 3 ↓5、CH 3CH=N —NH 26、CH 3CH 2CH=CHCOOH7、CH 3(CH 2)2CHO + CO 2 ↑8、C 6H 5CH 2CH 2CH 2CH 39、COONaCH 2OH10、N NHOCH 311、H 2N C O HN C ONH 212、2H 5五、鉴别题 (每题3分, 共12分)1、 丙醛 ↓ 丙酮 (—) ↓ 异丁醇(—) (—)2、 果糖 ↓ Br 2水 (—)↓ 褪色 蔗糖 (—) 淀粉 蓝色3、 C 6H 6 (—) (—)C 6H 5CH 3 (—) 褪色C CCH 3CH 3 褪色+AgNO3 NH 3·H 20 NaOH I 2 NH 3·H 20 AgNO 3 KMnO4 H + Br 24、 苄基氯↓氯苯 (—) 继续 加热 (—) 4-氯环己烯 (—) ↓六、推证结构 (共20分)1、( 共7分, 结构式 1分⨯2 +2分 , 反应式 1分 ⨯4 ) 结构式: A :NH 2B :N 2+Cl -C :N N OH(2分)反应式:NH 2HCl NH 3+Cl -N 2+Cl -(A ) 0-5℃ (B )OH,N NOH(C )2、( 共7分, 结构式 1分 ⨯4, 反应式 1分 ⨯3 )结构式: A :CH 3CH 2CH 2Br B :CH 3CH=CH 2 C :CH 3COOH D :CH 3CHBrCH 3 反应式: CH 3CH 2CH 2Br CH 3CH=CH 2 CH 3COOH + CO 2 + H 2O(A)(B) (C)CH 3CHBrCH 3 (D)3、( 共6分, 结构式 1分 ⨯6 )结构式: A :CH 3CH(NH 2)CH 2COOH B :CH 3CH(OH)CH 2COOHC :CH 3 CO CH 2COOHD :CH 3 C(OH)=CHCOOHE :COOH HHH 3CF : H COOH H H 3C(注:若E 和F 互换也算正确)苏州大学有机化学课程试卷( 第4卷) 答案一、命名下列有机化合物 (每题1分,共15分)1、4,5,8,9-四甲基-3-乙基-2-癸烯-6-炔2、3,4-二硝基甲苯3、 4-甲基-3-乙基苯酚4、γ-丁内酯5、四氢呋喃(1,4-环氧丁烷)6、 4-甲基-2-环己烯酮7、(2R ,3S )-二羟丁二酸8、 E-3-甲基-2-戊烯 9、对甲基苯磺酰胺AgNO 3 HNO 2OH —KOH 醇 HBr [O]10、α-D-甲基葡萄糖苷 11、半胱氨酸(β-巯基-α-氨基丙酸) 12、1,2-环氧戊烷13、3-苯基-2-丙烯醇14、草酰乙酸(α-酮丁二酸) 15、对苯醌二、写出下列化合物的结构式(每题1分,共15分)1、 Cl2、H 2C C H H 2C C CH3、OHNO 2NO 2O 2N4、Ph H 2C C OC 2H 55、N COOH6、OOO7、 CH 2OHOCH 2OH 8、HC C NH 2H 3C O NHCH 2COOH9、C OO H 2C10、C O NCH 3CH 311、COOHCOOHHH OHCl12、CH 3HH 3CBr13、H 2C O HCO H 2C OOO OR 3R 2R 114、H 3CH NSH15、OHOH三、选择题 (每题1分,共20分)四、完成下列反应 (每题1.5分,共18分)1、H 3CH 2COCH 32、C(CH 3)3COOHCOOH3、 CH 3CH 2COCH 3 + CO 2↑ + H 2O4、(CH 3)3C —Cl5、CH 2CH 2NH 26、CH 3CH 2COONa + CHI 3 ↓7、 O(若答OCOOH扣0.5分)8、COOHOCOCH 39、N NOHCH 3 10、COOHCOOH11、 OHHOH 2C12、H 3C C HCH 3C CH 3CH 3Br五、鉴别题 (每题3分,共12分)1、 酪氨酸 黄色 (—)色氨酸 黄色紫色 丙氨酸 (—)2、 丙酸 ↑丙醛 (—) ↓ 丙酮 (—) (—) I 2 ↓ 丙醇 NaOH (—)3、 2-甲基丁烷3-甲基-1-丁炔 ↓3-甲基-1-丁烯 (—) 4、OH(—) 显色CH 2OH(—)CH 2COOH↑六、推结构题 (共20分)1、(共7分: 结构式 1分 ⨯3, 反应式 1分 ⨯4 )结构式:(Ⅰ):CH(CH 3)2OHH 3C(Ⅱ):CH(CH 3)2OH 3C(Ⅲ):H 3CHC C(CH 3)2反应式:CH(CH 3)2OHH 3CCH(CH 3)2OH 3CCHI 3↓ + NaOOCCH(CH 3)2(Ⅰ) (Ⅱ)△ 浓H 2SO 4HNO 3 浓H 2SO 4 HOC-COOH NH 3∙H 2O AgNO 3 NaHCO 3 + NaHCO 3 AgNO 3 NH 3·H 20 [O]I 2NaOHH 3CHCC(CH 3)2 (Ⅲ)HC C(CH 3)2H 3C Br Br2、(共7分: 结构式 2分 ⨯2, 反应式 1.5分 ⨯2 )结构式: A :CHO COOHH HOOH H B :CHOCOOHOH HOH H反应式:CHO COOH H HOOH HCOOH COOH H HOOH HCHO COOH OH HOH HCOOHCOOH OH HOH H(A) (B)3、(共6分: 结构式 1.5分 ⨯2, 反应式 1.5分 ⨯2 )结构式: A : CH=CH 2C 2H 5(Cl) HCl (H) B :C 2H 5HC C 2H 5Cl反应式:CH=CH 2C 2H 5(Cl) HCl (H)(A,具旋光性) CO 2↑+ H 2O + HOOCCHClC 2H 5C 2H 5CHClC 2H 5 (B,无旋光性)苏州大学有机化学课程试卷( 第 5卷)答案一、命名下列有机化合物 ( 每题1分, 共15分 )1、4-乙基环己基醇2、3-苯基-3-氯丙烯3、E-乙醛肟4、β-甲基萘5、二苯甲酮6、丙二酸二乙酯7、R-2-氯丁烷8、对氨基苯磺酰胺 9、β-吲哚乙酸10、苦味酸(2,4,6-三硝基苯酚)11、四碘吡咯12、水合三氯乙醛13、4-甲基-2-戊烯醛14、二甲亚砜 15、2 -甲氨基丁烷二、写出下列化合物的结构式 ( 每题1分, 共15分 )HNO 3 [O][H]Br 2水HNO 31、H C H 2C C CH H 2C2、H 2C HC OH SH CH 2SH 3、CH CH 3H 3COH 3CO4、COOC 2H 5COOC 2H 5 5、CH 3CH 3HCCH6、HOCH 3H C 2H 57、NHO8、C 2H 5O C(CH 3)3 9、H 2C CH 2Br10、HC CHCHO11、H 2NOH NNH 2O12、OCOOH13、HCC H 2C C CH 14、HCHOCH 2OH OH15、CH 3CH(NH 2)CONHCH 2COOH三、选择题 ( 每题1分, 共20分 )1 2 3 4 5 6 7 8 9 10 A D D D A D E D C A 11 12 13 14 15 16 17 18 19 20 DBCCEEEECD四、完成下列反应式 ( 除注明外每题1.5分, 共18分 )1、COCH 32、C C l 3(若答CH 2Cl CHCl 2,也对)3、CH 3CH 2COONa + CHI 3↓4、(1分) ,CH 3CH=CHCHO (0.5分)5、COO6、HCCHBr Br ,HC CHCN CN ,HCCHC C O O ,HCCHC C OOOH OH (各1.5分)7、CH 3CH 2COCH 3 + CO 2↑ 8、N HBr BrBr Br9、CH 3CH 2NH 2 + CO 2↑五、鉴别题 ( 每题3分, 共12分 )1、 甘氨酸 (—)酪氨酸 HNO 3 黄色 FeCl 3 显色 苯丙氨酸 黄色 色氨酸 黄色 紫色HOC-COOH 浓 H 2SO 42、 甲酸 ↓乙酸 (—)丙二酸 ↑3、 苯 (—) (—)甲苯 (—) 褪色 苯酚 显色(或白色沉淀) ↓ 4、 丙胺丙酰胺 ↑ 尿素 ↑ 紫色1、( 共7分, 结构式C 为 1分, 其余 1.5分 ⨯4 ) 结构式:A :CH 2CH 2COCH 2COOHB :CH 2CH 2COCH 3C :CH 2CH 2CSO 3NaOHCH 3↓ ( 1分 )D :CH 2CH 2C CH 3N OHE :CH 2CH 2COONa2、(共8分: 结构式 2分 ⨯2, 反应式2分 ⨯2 )结构式: A : CH=CH 2C 2H 5(Cl) HCl (H) B :C 2H 5HC C 2H 5Cl反应式:CH=CH 2C 2H 5(Cl) HCl (H) (A,具旋光性) CO 2↑+ H 2O + HOOCCHClC 2H 5C 2H 5CHClC 2H 5 (B,无旋光性)3、 (共5分: 结构式 2分, 反应式1分, 过程 1分 ⨯2 )结构式: OCH 2OH反应式:KMnO 4 /H + △ [O][H]OCH 2OHOHCH 2OH(水杨苷) (β-D-葡萄糖) (水杨醇) 推导过程:水杨苷与FeCl 3不发生显色反应无酚-OH用苦杏仁酶水解时得到D-(+)-葡萄糖和水杨醇 为 β-型苷键苏州大学有机化学课程试卷( 第 6卷)答案一、命名下列有机化合物 ( 每题1分, 共15分 )1、2,5-二甲基-1,3-环己二烯2、β-萘磺酸3、5,6-二甲基-1-庚炔4、3-氯-1,2-丙二醇5、2,3-二甲基丁二酸6、α-酮戊二酸(草酰丙酸)7、反-1,4-环己二醇8、R-2-氨基丁酸 9、E-3-甲基-2-戊烯10、3-甲基-4-苯基-2-戊酮 11、ß-吡啶甲酰胺12、三乙胺13、甲基异丙基醚14、丙二酸甲乙酯 15、苯甲酰氯二、写出下列化合物的结构式 ( 每题1分, 共15分 )1、(CH 3)3CBr2、H 2C H C H 2C HC CH 3、CH 2CHCH2OH SHSH4、CHCOOHOHCH 3 5、C 2H 5CH 3H 3CH6、HC(CH 3)37、H 2NOH NONH 28、OCHO9、10、O O OO OOR 1R 2R 311、NH 2CH 2CONHCHCOOH CH 2Ph12、NH 3+Cl -13、CH 3CHCHCHCOOH CH 314OOCH 3H 3C15、SO 2H 2N NH 2H 2O + 苦杏仁酶四、完成下列反应式( 每题1.5分, 共18分)1、CH3COCH32、CH3CHBrCH33、COOH C(CH3)34、COONa,CH2OH5、CH3CH2OHCOOHCH6、BrNH2CH3Br7、CN+ N28、NNO29、COOHCH2OH10、CH3CH2CH2COOH 1112、HO(CH2)3COONa五、鉴别题( 每题3分, 共12分)1、丙酸↑(—)丙二酸↑↑丙醇2、甲酸↓↑甲醛↓(—)甲醇(—)3、丙甘肽(—)(—)甘酪肽(—)显色谷胱甘肽紫色4、乙胺溶二乙胺不溶三乙胺(—)1、( 共8分,结构式2分⨯2 , 反应式1分⨯4 )结构式: A:HCH3CH3CCH2CH2CCH3OB:CH3COCH2CH2COOH反应式: AgNO3NH3·H20△NaOH / CuSO4NaHCO3(A)HCH3CH3CCH2CH2CCH3O+ Br2HCH3CH3CCH2CH2CCH3OBrBr(A )HCH3CH3CCH2CH2CCH3O+NHNH2HCH3CH3CCH2CH2CCH3NHN(A)HCH3CH3CCH2CH2CCH3OCH3COCH3 + HOOC—CH2CH2COCH3(B)I2/ NaOHCHI3 ↓+ NaOOCCH2CH2COONa2、( 共6分,结构式1分⨯6 )结构式:A:CH3CH(NH2)CH2COOH B:CH3CH(OH)CH2COOH C:CH3 CO CH2COOH D:CH 3 C(OH)=CHCOOHE:COOHHHH3C F:HCOOHHH3C(注:若E和F互换也算正确)3、(共6分:推断2分⨯ 2,结构式2分)推断: 无还原性,不成脎,无变旋光,不成苷-----------无半缩醛羟基麦芽糖酶水解-------------------------------------α-苷键结构式:苏州大学有机化学课程试卷( 第7卷) 答案一、命名下列化合物(每题1分,共15分)1、3-氯环戊烯2、3-甲基-3-戊烯-1-炔3、β-萘磺酸4、甲基异丙基醚5、2-甲基-1,4-萘醌6、丁烯二酸酐7、2,3-二甲基丁二酸8、R-2-氨基丁酸9、E-3-甲基-2-戊烯10、氢氧化三甲基乙基铵11、对氨基苯磺酰胺(磺胺)12、β-吲哚乙酸[O]或13、对二氯苯 14、苄醇 15、丁内酰胺二、写出下列化合物的结构式(每题1分, 共15分 )1、CH 2Br2、H 2C H C H 2C C CH3、CHOOH 3C4、OO H 2C5、H 3C HC OHCOOH6、OO OO OO R 1R 2R 37、BrCH 3H C 2H 58、CH 3HH 3CBr9、OOO10、H 2NNH 2NH11、CHOCH 2OH12、H 3CNH 2OHN CH 2COOH13、 14、N (CH 3)3 15、 OHH 3CH 3C三、选择题(每题1分, 共20分 )四、完成下列反应(每题1.5分, 共18分 )1、ClCH 2OH2、COOH3、NO 2Cl4、(CH 3)3C —Cl5、OH CN6、COONa+CH 2OH7、OH+ N 2↑8、N 2+Cl -9、NH+Cl -10、H 2NH 2CCOOH SSCH 2NH 2HOOC11、CH 2CH 2NH 212、CH 3CH 2CHO +CO 2五、鉴别题(每题3分, 共12分 )1、 葡萄糖(—)褪色I 2Br 2水果糖(—) (—)淀粉 兰色2、 乙醚Na(—) 乙醇 (—) ↑ 乙酸 ↑3、 丙甘肽 (—) (—)苯丙氨酸 (—) 黄色 谷胱甘肽 紫色 4、 (—) 甲苯 褪色 2-丁炔褪色)1、(共9分, 结构式 1.5 分 ⨯4, 反应式 1分 ⨯3 )结构式: A :CH 3CH 2CH 2Br B :CH 3CH=CH 2 C :CH 3COOH D :CH 3CHBrCH 3反应式:CH 3CH 2CH 2Br CH 3CH=CH 2 CH 3COOH + CO 2 + H 2O(A)(B) (C)CH 3CHBrCH 3(D)2、(共6分, A,B 的结构式 1 分 ⨯2, A 的顺反异构 1分 ⨯2, B 的对映体 1 分 ⨯2 )A,B 的结构式: A :CH 3COOH CH 3CHB :CH 3CH 2CH CH 3COOHA 的顺反异构: CCCH 3CH 3COOH H(顺) ,CCCH 3CH 3COOH H(反)B 的对映体:3H 25 ( R ) , CH HH 25 ( S ) 3、(共5分, 结构式 2 分, 反应式 1分 ⨯3 )三肽结构式: H 3CNH 2OH N H 2COHN CH 2COOH反应式:H 3CNH 2OH N H 2COHN CH 2COOHH 3CNH 2COOH + 2 NH 2CH 2COOHH 3CNH 2OH N H 2COHN CH 2COOHH 3COHOH N H 2COHN CH 2COOHNaHCO 3 浓HNO 3, (黄蛋白反应) KOH 醇 HBr [O] 水解 HNO 2水解H3COH COOH+ 2 NH2CH2COOH苏州大学有机化学课程试卷(第8卷)答案一、命名下列有机化合物:(每题1分, 共15分)1、3-丙基-1-己烯2、异丙苯3、α-萘酚4、苯甲醚5、2,5-二甲基-1,4-苯醌6、丁烯二酸酐7、β-甲基-γ-丁内酯8、E-1-氯-1,2-二溴乙烯9、(2R,3S)-二羟丁二酸10、N,N-二甲基苯胺11、6-氨基嘌呤12、α-D-甲基吡喃葡萄糖苷13、丝氨酸(α-氨基-β-羟基丙酸)14、4-苯基-2-丁烯醇15、4-溴-1-丁烯二、写出下列化合物的结构式:(每题1分, 共15分)1、NO2NO22、CH2Br3、CHC CHCH3HC4、H3CHCOHH2CHC CCH3CH35、CH2CHCH2OH SHSH6、PhH2COC2H57、CH3C2H5H3CH8、HC2H5HOCH39、N(CH3)4+I-10、O COOH11、R1234567891011121314161715A BC D12、CHNOHCCH2PhCOOHNH2CH213、CH3COOCH(CH3)214、HCO—N(CH3)215、CHO CH2OH1、CH3COCH3 + CH3COOH2、CH3CH=C(CH3)23、CH3CH2COONa + CHI3↓4、C CHCH 3CH 3CH 3CH 2 5、H 2C HC OH CH 2S Hg S6、O H 3COO7、CH 2NHCCH 3O8、H 2NOH NONH 29、NN O 210、2 CH 3COONa + H 2O 11、COOHCH 2OH12、CH 2CH 2NH 2+ CO 2↑五、鉴别题 (分 1、 丙醛丙酮↓ 或 丙酸 ↑2、 甲基葡萄糖苷 (—)葡萄糖 ↓ Br 2 / H 2O 褪色 果糖 ↓ (—)3、CH 2CH CH 2Cl Cl(一(一(-)CH 2=CHCH 2CHCH 2ClCH 34、 甲胺 SO 2Cl↓ 溶 二甲胺 ↓ 不溶 三甲胺(—)六、推证结构式 ( 共20分 )1、(共9分: 结构式 1分 ⨯3, 反应式 1.5分 ⨯4 )结构式: (Ⅰ):CH(CH 3)2OHH 3C(Ⅱ):CH(CH 3)2OH 3C(Ⅲ):H 3CHC C(CH 3)2反应式:CH(CH 3)2OHH 3C CH(CH 3)2O H 3C CHI 3↓ + NaOOCCH(CH 3)2(Ⅰ) (Ⅱ)浓H SO 4 , H 3CHCC(CH 3)2(Ⅲ) H C C(CH 3)2H 3C Br Br2、(共6分: 结构式 1.5分 ⨯2, 反应式 1分 ⨯3 )结构式: A :H 3C H 2C C CH B :C H C HH 2CCH 2反应式:NaOH ↓ (—) AgNO 3 NH 3·H 2O [O] I 2 NaOH Br 2水 AgNO 3H 3C H 2C C CHH 3C H 2C C CAg ↓ (A )[O]H 3C H 2C COOH + CO 2↑ + H 2OC H CHH 2C CH 2CO 2 ↑+ HOOC —COOH + H 2O(B )3、(共5分, 结构式 2 分, 反应式 1分 ⨯3 )三肽结构式: H 3CNH 2OH N H 2COHN CH 2COOH反应式:H 3CNH 2OH N H 2COHN CH 2COOHH 3CNH 2COOH + 2 NH 2CH 2COOHH 3CNH 2OH N H 2COHN CH 2COOHH 3COHO H N H 2COHN CH 2COOHH 3COHCOOH+ 2 NH 2CH 2COOH苏州大学有机化学课程试卷 ( 第9卷) 答案五、命名下列有机化合物:(每题1分, 共15分 )1、3 –丙基-1-己烯2、4-乙基环己醇3、邻溴甲苯4、3-氯-1,2-丙二醇5、苯甲醚6、2,5-二甲基对苯醌7、二苯甲酮8、乙酰水杨酸 9、反-1,4-环己基二醇10、(2R,3S)-二羟丁二酸 11、β-甲基吡啶12、D-葡萄糖13、Z-3-甲基-2-溴戊酸14、二甲亚砜 15、3-溴丁酰溴二、写出下列化合物的结构式:(每题1分, 共15分 )NH 3·H 2O[O]水解 HNO 2水解1、 AgCCAg2、NO 2NO 23、(CH 3)2C CH 24、335、2O 226、CHOH 3CO7、O OO 8、COOH COOHOH OH HH9、[N (C 2H 5)4]+I -10、CHNOH11、 C (CH 3)4 12、NCH 2COOH13、CH 2CHCOOHNH 214、HOCOOCH 215、CH 3CN1、CHCH 2SNa HONa O2、CH 3COCH 3 + CH 3COOH3、NO 24、CH 3CH 2CCH 3CH 3Br5、(CH 3)3C-Cl6、OHBrBrBr7、NNOCOOH8、O9、OOCOOH()若答扣0.5分 10、NO 2CH 3Cl11、COONa+ CHI 312、COOHCOOH五、鉴别题 (分)1 、苯酚显色苯甲醇 (—)Na ↑苯甲醚 (—) (—) 2、尿素 ↑ 紫色 乙二胺 ↑ (—) 二乙胺3、酪氨酸 黄色 显色 苯丙氨酸 黄色 (—) 丙氨酸 (—)4、乙酰丙酮 褪色 丙酮 (—) I 2 / NaOH ↓ 丙醇 (—) (—)六、推证结构式 ( 共20分 )1、( 共5分: 结构式 1分 ⨯3, 反应式 0.5分 ⨯4 )结构式: Ⅰ:CH 3CH 2COOH , Ⅱ:O OH CH 2CH 3 Ⅲ:O OH 3CCH 3反应式:CH 3CH 2COOH (Ⅰ)+ NaHCO 3 CH 3CH 2COONa + CO 2↑ + H 2OO O HCH 2CH 3HCOOH + C 2(Ⅱ) 3 ↓ + HCOONaO OH 3C CH 3 CH 3COONa + CH 3OH(Ⅲ)2、( 共9分: 结构式 1.5分 ⨯3, 反应式 1.5分 ⨯3 ) 结构式: (Ⅰ):COOHHO(Ⅱ):COOHH 3CCOO(Ⅲ):COOCH 3HO反应式:COOHHOCOONaHO (Ⅲ)(Ⅰ)硝化 (CH 3CO)2OFeCl 3 Br 2 水 ① 155-160℃② NaOH / CuSO 4 HNO 3 NaCO 3 CH 3OHCOOCH 3HOOH - H 2O H 2O OH -COOCH 3HOO 2NCOOHH 3CCOO(只有一种一硝基衍生物) (Ⅱ) 3、( 共6分, 结构式 1分 6 )结构式: A :CH 3CH(NH 2)CH 2COOH B :CH 3CH(OH)CH 2COOHC :CH 3 CO CH 2COOHD :CH 3 C(OH)=CHCOOHE :COOH HHH 3CF : H COOH H H 3C(注:若E 和F 互换也算正确)苏州大学有机化学课程试卷(第10卷)答案一、命名下列有机化合物:(每题1分, 共15分)1、4-甲基-1-戊炔2、2,4,6-三硝基甲苯3、2-甲基-3-巯基戊烷4、对羟基苯甲醛5、乙二醇6、邻苯醌7、1,1-二甲氧基乙烷8、对溴苯甲酰溴9、E-苯甲醛肟 10、S-2-氨基丙酸 11、氯化重氮苯 12、戊内酰胺 13、β-萘甲酸 14、二苯甲酮 15、甘丙肽二、写出下列化合物的结构:(每题1分, 共15分)1、H 3CCH 3CH 3CH 3 2、OHOCH 33、H 2C H C CH ClCH 3 4、OO5、C OCH 2CH 36、COOHCOOH7、OO O8、COOH H Br BrHCOOH 9、HC H 3C COOHOH10、H 2N C NHNH 2 11、OCH 2OHOH OHOH OH12、H COOH H 2NCH 2Ph13、HON N14、H 3C H C OH H C OH H C HC CH 315、CH 3COOCOCH 2CH 3四、完成反应:(每题1.5分, 共18分)1、H 3C C CH 3O2、H 3CC COOH O3、HC CNNHPh NNHPhCH 2OH4、CH 3COONa+C 2H 5OH 5、CH 3COOH+N 2↑+H 2O6、N=NOH7、BrBrBr+ N 2 ↑ 8、CH 2=CH —CH=CHCH 3 9、COONa+ CHI 3↓10、O11, HOOCCH 3 + CO 2 ↑ 12,CH=CHCH 3五、鉴别题 (每题3分, 共12分)1、 谷胱甘肽丙甘肽 ↓(一) 酪氨酸 黄色 显色 黄色 (—) 2、 苯胺 苯酚 ↑ 甲苯 3、 甲酸↓乙酸 (—) (—) ↑ (—) ↑ ↓ 4、 丙醛 ↓丙酮 (—) ↓ 丙醇 (—)六、推证结构 ( 共20分 )1、 ( 共7分, 结构式 1分 ⨯3, 反应式 1分 ⨯4 ) 结构式: A:NH 2H 3CB:H 3CN 2+Cl - C:H 3CNNOH反应式:NaOH I 2 在加热后的体系中加入AgNO 3(NH 3·H 2O ) NaOH CuSO 4△ AgNO 3, NH 3·H 2ONHH 3CH 3CN 2+-HO CH 3(A) (B)(C)2、 (共6分: 结构式 2分, 过程 2分 ⨯2 )结构式: OCH 2OH推导过程:水杨苷与FeCl 3不发生显色反应 无酚-OH用苦杏仁酶水解时得到D-(+)-葡萄糖和水杨醇 为 β-型苷键 3、 ( 共7分, 结构式 2分 ⨯2, 反应式 1分 ⨯3 )结构式: A :C 2H 5OHC 2H 5 B :C 2H 5OC 2H 5反应式:C 2H 5OHC 2H 5 + NaC 2H 5ONaC 2H 5 + H 2↑(A)C 2H 5OHC 2H 5C 2H 5OC 2H 5(A) (B)C 2H 5OC 2H 5 +H NH 2N H NNC C 2H 5C 2H 5(B)苏州大学有机化学 课程试卷 ( 第11卷 )答案一、命名下列有机化合物:(每题1分,共15分)1、2—甲基—1,3—丁二烯2、1—苯基—2—溴乙烷3、5—氯—2—萘酚4、苯乙醛5、1,2—环己二甲酸6、N —甲基苯甲酰胺7、 R-2,3-二羟丙醛 (R-甘油醛)8、N,N-二甲基乙酰胺9、α,α’-二甲基呋喃 (2,5-二甲基呋喃) 10、α-D-葡萄糖(直立氧环式) 11、苯丙氨酸12、Z-苯甲醛肟 13、邻苯二甲酸酐14、α-酮戊二酸 (草酰丙酸) 15、胆胺(乙醇胺, 氨基乙醇)[O]H 2OHNO 3二、写出下列化合物的结构式:(每题1分,共15分)1、HCH2CCH3CH32、OH3、CH2CHCH2SH SHOH4、OO CH3H3C5、COOHOCH36、HCH3BrC2H57、NHCOOH8、H2NONH29、N HBr10、3H211、NH3+Cl-O2N12、CF2=CF213、OOCH3H3C14、NHO15、H2CCOOHCOOC2H5四、完成下列反应式(每题1.5分,共18分)1、CH3CHCH3OSO3H,CH3CHCH3OH+H2SO42、CN3、NHCOCH3Br4、COONa+CHI3↓5、OO6、CH3CH2CH2CH37、OOClClClCl或OOClCl8、OOO9、OCOONa+OCH2OH10、CH3COCH3或(CH3COCH3)11、312、OHCH3CHCOOH+ N2↑五、鉴别题(每题3分,共12分)1 、苯胺(—)↓Br2水N-乙基苯胺 FeCl3(—)(—)苄醇(—)(—) ↑对-甲基苯酚 显色2、苯甲酸 ↑ 苯甲醛 (—) AgNO 3 ↓ 对甲苯酚 显色 NH 3•H 2O 苯甲醇 (—) (—)3、褪色乙醚 KMnO 4 (—)溶丙烯 褪色 H + 戊烷 (—) 不溶 4、↓ 褪色 果糖 ↓ (—) 蔗糖 淀粉显色六、推证结构式(共20分)1、( 共8分, 结构式2分⨯3, 反应式1分⨯2 ) 结构式: A :CH 3CH 2CH 2Br B :CH 3CH=CH 2 C :CH 3CHBrCH 3 反应式:CH 3CH 2CH 2Br CH 3CH=CH 2 CH 3CHBrCH 3(A ) (B ) (C )2、( 共6分:×4 )A :H 3CCH 3ONH 2 B 、H 3CCH 3OOHC :H 3CCH 3CH 2OHD 、H 3CCH 3CH 23、( 共6分, 结构式1分⨯3, 反应式1分⨯3 )结构式: A :C 2H 5H 3C B 、C :(同一物质)COOHCOOHNO 2反应式:KOH /醇 HBrC 2H5H 3C CH 3C 2H 5NO 2CH 3C 2H 5NO 2(A )COOHCOOH NO 2COOHCOOH NO 2(B ) (C )(B ,C 为同一物质)苏州大学有机化学课程试卷 ( 第 12卷)答案六、命名下列有机化合物:( 每题1分, 共15分 )1、对溴甲苯2、3-乙基-3-丁烯-2-醇3、1-甲氧基乙醇4、丙烯酰氯5、苯乙酮6、R-1-苯基丙醇7、叔丁基环己烷(优势构象)8、Z-偶氮苯 9、溴化二甲基二乙基铵10、2-环己烯醇 11、对氨基苯甲酸乙酯12、5-硝基-2-呋喃甲醛13、α-萘乙酸14、酪氨酸 15、油酸(9-十八碳烯酸)二、写出下列化合物的结构式:( 每题1分, 共15分 )1、CH 3CHCH 2CH 2CH 3CH 32、3、OHNO 2O 2N24、OO5、Cl3BrCl6、Cl COCH 3HPh7、HCOOC 3H 78、S OOCH 3H 3CO O 9、COOH HOOC10、2NH 2H 3H 3 11、 PhHC=CH —CHO 12、OBrBrHNO 3H 2SO 4,△ ++[O]13、CHO CH 2OH CHOCH 2OH14、N(CH 3)2C 2H 5C 2H 515、CH 2CHCOOHHONH 2四、完成下列反应式 ( 每题1.5分, 共18分 )1、Cl 3CCH 2—CH 2Cl ;2、CH 2CHCH 2CH 2BrBr3、CH 3COCH 34、OCl5、OOO OH 3CCH 36、O7、CHH CCH 2CH 38、CH OCH 3OCH 3H 3C 9、BrNHCOCH 310、CHCOONa OHHO 11、OH12OCOONa+OCH 2OH五、鉴别题分 )1 、(—) (—)(—) (—) 褪色↓ 显色 2、(—)显色↓ (—) 3、脯氨酸 苯丙氨酸 (—) 色氨酸 紫色 4、5~10分钟后分层 立即分层 甘油1、( 共5分, 结构式 1分 ⨯3, 反应式 1分 ⨯2 )HOOC-CHO/ H 2SO 4 AgNO 3 NH 3•H 2O KMnO 4 H +结构式:A:CH3C2H5H3CC2H5B:CH3COC2H5C:OHH3CH3COHC2H5C2H5反应式:OH H3CC2H5OHCH3C2H5CH32H5H3CC2H5(C)(A)2、(共7分,结构式1分⨯3,反应式1分⨯4)结构式:A:OBr CH2CH3B:OHBr CH2CH3C:HCBr CHCH3反应式:OBr CH2CH3+NO2O2NNH2NHNO2O2NNNHBrCH2CH3(A)OHBr CH2CH3HCBr CHCH3(B)(C)COOHBr+ CH3COOH 3、(共8分,结构式2分⨯4 )结构式:A:CHCH3H3CH3COHB、H3CCH3H3C COKMnO4H+ (B)KMnO4冷,OH—[H]浓H2SO4△[O]2 CH3COC2H5C :CHI 3 ↓D : CHCH 3H 3CH 3C苏州大学有机化学 课程试卷 (第13卷 )答案一、 命名下列有机化合物:(每题1分, 共15分)1、4-甲基-3-戊烯-1-炔2、对氯苄基氯3、均三溴苯 (1,3,5-三溴苯)4、邻羟基苯甲醛5、乙醛肟6、1,4—萘醌7、2-甲基-3-甲氧基丁烷8、邻苯二甲酸酐 9、(2S ,3S )-2-羟基-3-氯丁二酸10、氯化重氮苯11、3-甲基-2-丁烯酰胺 12、 2,5-二甲基呋喃13、β-甲基-γ-丁内酯 14、 2,2,4-三甲基-3-庚酮 15、β-D-甲基吡喃葡萄糖苷二、写出下列化合物的结构式:(每题1分, 共15分)1、H 2CSH NH 2COOH2、CH 2OHOCH 2OH 3、O O4、N H H 3C5、2H 26、NH 3+Cl -7、O HN8、Br I HCl9、CH 3HH10、CH 2BrCCH 3O11、COOHCOOC 2H 512、CH 3CH=CHCH 2OH13、H 3C NH 2CONHCH 2COOH 14、OO OO OOR 1R 2R 315、COOH OHH 2N四、完成下列反应式 ( 除注明外,每题1.5分, 共18分 )1、Cl 3CCH 2CH 2Br2、BrSO 3H+BrSO 3H3、CHI 3↓+HCOONa4、C H 3COCH 35、CH(CH 3)2(若写成CH 2CH 2CH 3扣0.5分)6、 CH 3COCH 2COOH (1.5分) CH 3COCH 3+CO 2 (1.5分)7、CH3COCH3 (1.5分)C HO CNCH 3H 3C (1.5分) OHCOOH CH 3H 3C(1.5分)8、 CH 3OO9、OO O五、鉴别题 (每题3分, 共12分)1 、↓ (—) ↑,生成CH 3COOH ↑,生成HCOOH ↓ 2、 乙醛↓丙酮↓ 丙醇 乙酰乙酸乙酯3、 苯胺 ↓N,N-(—) (—)N -甲基苯胺(—)SO 2Cl↓ 不溶苄胺(—) ↓ 溶 4、 酪氨酸 (—)色氨酸 紫色 赖氨酸六、推证结构式 ( 共20分 )1、 (共6分: 结构式2分×1, 反应式2分 × 2 )结构式: A :CH 2(NH 2)CONHCH (CH 3)COOH反应式:H 2N H 2COH NCH 3COOHHO H 2COH NCH 3COOH(A )HO H 2COOH + H 2NCH 3COOHNaOH HOOCCHO H 2SO 4 HNO 2 H 2O/ H +2、( 共8分:结构式2分× 3, 反应式0.5分× 4 )结构式:A:H2COHH2COClB:H2COHH2C COOHC:CH2=CH—COOH反应式:H2COH H2C COCl H2COHH2C COOH(C)(A)(B)Br BrCOOHCO2 + H2O + HOOC-COOH (注:若写成“α-羟基丙酰氯”等扣1-2分)3、( 共6分:结构式2分×3 )结构式:A:OHCOOHCH3H3CB:ClCOOHCH3H3CC:COOHCOOHCH3H3C苏州大学有机化学课程试卷( 第14卷) 答案七、命名下列有机化合物:(每题1分,共15分)1、2-甲基-4-甲氧基苯甲醇2、E-2-甲基-3-溴-3-己烯3、1-环己基乙醇4、2-丁炔5、乙酰丙酮6、R-乳酸,(R-2-羟基丙酸)7、甲酸苄酯8、甲基异丙基醚9、2-羟基-4-甲氧基苯甲醛10、N-甲基-β–吡啶甲酰胺11、1-苯基-2-溴-2-丁烯12、对羟基偶氮苯13、赖氨酸,(2,6-二氨基己酸)14、2-戊烯酸15、9-溴菲二、写出下列化合物的结构式:(每题1分,共15分)132、OHNO2O2NNO23、HOH4、NH3CH3COH5、COOHH OHHHOCOOH6、H3CClH2COClKMnO4/H+Br2水H2O CH2=CH—COOH7、SO 2NH 2HN8、NCOOH9、NHOO10、COOH NH 2CH 3H 11、 HOOCCOCH 2COOH 12、(CH 3)2CHCH 2NH 213、H COOHHCOOH14、CH 3CH 2CH 2CHCH 2CHOHBr15、四、完成下列反应式 ( 除注明外每题1.5分,共18分 )1、CH 32、CH 3COONa +(CH 3)2CCOONa3、(CH 3)3CCl ,C(CH 3)3CH 3,C(CH 3)3COOH(各1.5分 ) 4、ClO 2N5、CH 2Br6、CHO7、CH 3CH=CHCH 38、O9+ H 2O10、OH CN OOH 3C五、鉴别题 ( 每题3分,共12分 )1 、甲酸(—) ↓乙酸 (—) (—) 丙二酸 ↑ 2、乙醛 ↓葡萄糖甘氨酸 ↑ 3、(—) 丙炔 褪色 ↓ 乙醇 褪色 (—) (—)乙烯褪色 (—) 褪色4、乙酰乙酸乙酯 显色 NaHCO 3 (—) 水杨酸 显色 ↑FeCl 3 Br 2水 AgNO 3 NH 3•H 2O AgNO 3 NH 3•H 2O乳酸(—)六、推证结构式 (共20分 )1、( 共8分, 结构式 2分 ⨯3, 反应式1分 ⨯2 )结构式 : A :SOCH 3B :SCH 3NOH C :SCOONa反应式:SCOONaSOCH 33(C ) (A ) (B )2、( 共5分, 结构式 1分 ⨯5 )结构式: A :CH 3COCH 2CH 2COOH B :CH 3CH(OH)CH 2CH 2COOH C :CH 3CHBrCH 2COOH D :CH 3CHBrCH 2CH 2COONa E :CH 3CHCNCH 2CH 2COONa 3、 ( 共7分, 结构式 1分 ⨯3 ,推导 1分 ⨯4 )结构式: A :CH(CH 3)2B :C : CH OHH 3CCH 3推导: 无还原性 形成的是糖苷(即无半缩醛-OH ) 苦杏仁酶水解 β-苷键B 被溴水[O]成D-G 酸 糖部分应为D-葡萄糖C 有碘仿反应 C 应为异丙醇苏州大学有机化学课程试卷 ( 第 15卷) 答案八、命名下列有机化合物:( 每题1分, 共15分 )1、3,4,4-三甲基-2-乙基-1-戊烯2、α-萘酚3、苯甲醚4、4-甲基-2-环己烯酮5、二苯甲酮6、丁烯二酸酐7、丙二酸二乙酯8、R-2-氨基丁酸 9、E-3-甲基-2-戊烯10、N-苯基苯甲酰胺 (苯甲酰苯胺) 11、对氨基苯磺酰胺 12、四碘吡咯13、丙烯醛14、D-葡萄糖 15、色氨酸 (或α-氨基-β-(3-吲哚基)丙酸)I 2/NaOH。
苏州大学分析化学课程试卷(17)卷共9页考试形式闭卷年月日院系年级专业学号姓名成绩一.选择题(共36分)1.(本题2分)以下关于偶然误差的叙述正确的是-------------------------------------- ( )(1) 大小误差出现的概率相等(2) 正负误差出现的概率相等(3) 正误差出现的概率大于负误差(4) 负误差出现的概率大于正误差2.(本题2分)下列算式的结果应以几位有效数字报出----------------------------------( )0.1010 (25.00 24.80)/1.0000(1) 五位(2 ) 四位(3) 三位(4) 二位3.(本题2分)测定(NH4)2SO4中的氮时,不能用NaOH标准溶液直接滴定,这是因为-------------------------------------------------------------------------------------( )(1) NH3的K b太小(2) (NH4)2SO4不是酸(3) NH4+的K a太小(4) (NH4)2SO4中含游离H2SO44.(本题2分)下列滴定(浓度均为0.1 mol/L)中可行的是--------------------------------( )已知p K a (HA)=4.85,p K a (HB)=9.3,p K b (NOH)=8.70,p K b (ROH)=3.80(1) HCl滴定A-(2) NaOH滴定R+(3) HCl滴定NOH (4) HCl滴定B-5.(本题2分)叙述Na2H2Y溶液以Y4-形式存在的分布系数(δY4-)时,说法正确的是--------------------------------------------------------------------------------------( ) (1) δY 4- 随酸度的增大而增大 (2) δY 4- 随pH 值的增大而减小 (3) δY 4- 随pH 值的增大而增大 (4) δY 4- 与pH 值的大小无关6.(本题2分)可以消除原子吸收法中的物理干扰的方法是-------------------------------( ) (1) 加入释放剂 (2) 加入保护剂 (3) 扣除背景 (4) 采用标准加入法7. (本题2分)指出下列哪种是紫外—可见分光光度计常用的光源----------------------( ) (1) 硅碳棒 (2) 激光器 (3) 空心阴极灯 (4) 卤钨灯8.(本题2分)红外光谱仪光源使用----------------------------------------------------------( ) (1) 空心阴极灯 (2) 能斯特灯 (3) 氘灯 (4) 碘钨灯9.(本题2分)羰基化合物中,c 伸缩振动频率最高者为------------------------------------( )R C ORR COFR COClR COBr (1)(2)(3)(4)10.(本题2分)在下列化合物中,用字母标出的4种质子的化学位移值(δ)从大到小的顺序是--------------------------------------------------------------------------------( )CC H2O(1) d c b a (2) a b c d(3) d b c a (4) a d b c11.(本题2分)原子发射光谱是由下列哪种跃迁产生的?----------------------------()(1)辐射能使气态原子外层电子产生跃迁(2)辐射能使气态原子内层电子产生跃迁(3)电热能使气态原子内层电子产生跃迁(4)电热能使气态原子外层电子产生跃迁12.(本题2分)离子选择电极的电位选择性系数可用于----------------------------------( )(1) 估计电极的检测限(2) 估计共存离子的干扰程度(3) 校正方法误差(4) 计算电极的响应斜率13.(本题2分)对色谱柱的分离效率最有影响的是-----------------------------------------( )(1) 柱温(2) 载气的种类(3) 柱压(4) 固定液膜厚度14.(本题2分)非极性的色谱柱,用于分离非极性组分时,分之间作用力主要是----( )(1) 库仑力(2) 诱导力(3) 色散力(4) 化学键15.(本题2分)气相色谱中,用静电力、诱导力、色散力、氢键作用力四种力来说明( )(1) 被测分子间的作用力(2) 被测分子与流动相分子间的作用力(3) 被测分子与固定液分子间的作用力(4) 流动相分子与固定液分子间的作用力16.(本题2分)在气相色谱中,适于用氢火焰离子化检测器分析的组分是------------( )(1) 二硫化碳(2) 二氧化碳(3) 甲烷(4) 氨气17.(本题2分)3,3-二甲基戊烷H3CH2C C CH2CH3CH3CH3452163受到电子流轰击后,最容易断裂的键位是----------------------------- ( )(1) 1和4(2) 2和3(3) 5和6(4)( 2)和(3)18. (本题2分)可以说明原子荧光光谱与原子发射光谱在产生原理上具有共同点的是--------------------------------------------------------------------------------()(1) 辐射能使气态基态原子外层电子产生跃迁(2) 辐射能使原子内层电子产生跃迁(3) 能量使气态原子外层电子产生跃迁(4) 电,热能使气态原子外层电子产生发射光谱二. 填空题:(共14分)1.(本题2分)写出计算以下溶液[H+ ]或[OH-]的公式0.10 mol/L 三乙醇胺(pK b= 6.24) __________________________________0.10 mol/L邻苯二甲酸氢钾(p K a1=2.95,p K a2=5.41) ____________________0.10 mol/L H2C2O4 (p K a1=1.22,p K a2= 4.19) __________________________2.(本题2分)含有Ca , Mg的样品溶解后,加不含CO32-的NaOH 使溶液的pH为13,则分别以________ ____、_______________ 形态存在,使两者得到分离。
苏州大学_分析化学(一下)期中考试_试卷(__卷)共7页学院__材料与化学化工_ 专业_化学类及师范专业_ 成绩______ 年级__08_ 学号_________ 姓名_________ 日期__2010年5月一、选择题( 共15题30分)1. 2 分(1412)应用GC法来检测啤酒中微量硫化物的含量, 宜选用的检测器为( )(1) 热导池检测器(2) 氢火焰离子化检测器(3) 电子捕获检测器(4) 火焰光度检测器2. 2 分(1064)根据范弟姆特方程式,在高流速情况下,影响柱效的因素主要是( )(1) 传质阻力(2) 纵向扩散(3) 涡流扩散(4) 柱弯曲因子3. 2 分(1442)在液相色谱中, 下列哪种检测器不能用于梯度洗脱?( )(1) 电化学检测器(2) 荧光检测器(3) 示差折光检测器(4) 紫外吸收检测器4. 2 分(1177)在色谱分析中通常可通过下列何种方式来提高理论塔板数?( )(1) 加长色谱柱(2) 在高流速区操作(3) 增大色谱柱的直径(4) 进样量增加5. 2 分(1711)分配系数是指在一定温度、压力下, 组分在气-液两相间达到分配平衡时, ()(1) 组分分配在液相中的质量与分配在气相中的质量之比(2) 组分在液相中与组分在流动相中的浓度比(3) 气相所占据的体积与液相所占据的体积比(4) 组分在气相中的停留时间与组分在液相中的停留时间之比6. 2 分(1465)对于具有宽沸程组分的试样, 为了保证分离度和缩短分析时间, 色谱柱柱温的升温速度应采用( )(1) 快速升温(2) 慢速升温(3) 程序升温(4) 控制在某一固定温度7. 2 分(1426)气相色谱中, 用静电力、诱导力、色散力、氢键作用力四种力来说明( )(1) 被测分子间的作用力(2) 被测分子与流动相分子间的作用力(3) 被测分子与固定液分子间的作用力(4) 流动相分子与固定液分子间的作用力8. 2 分(1457)在气-固色谱分析中, 色谱柱内装入的固定相为( )(1) 一般固体物质(2) 载体(3) 载体+固定液(4) 固体吸附剂9. 2 分(1460)在气相色谱分析中, 相邻两组分的分离度与下述哪些参数有关?()(1) 保留指数(2) 相邻两组分保留值之差(3) 相邻两组分峰底宽之和(4) (2)和(3)10. 2 分(1439)在液相色谱中, 为了获得较高柱效能, 常用的色谱柱是( )(1) 直形填充柱(2) 毛细管柱(3) U形柱(4) 螺旋形柱11. 2 分(1558)在下面四个电磁辐射区域中, 能量最大者是( )(1) X射线区(2 ) 红外区(3) 无线电波区(4) 可见光区12. 2 分(1567)下面几种常用激发光源中, 分析灵敏度最高的是( )(1) 直流电弧(2) 交流电弧(3) 电火花(4) 高频电感耦合等离子体13. 2 分(1235)在下列激发光源中,何种光源要求试样制成溶液?( )(1) 火焰(2) 交流电弧(3) 激光微探针(4) 辉光放电14. 2 分(1375)可以说明原子荧光光谱与原子发射光谱在产生原理上具有共同点的是( )(1) 辐射能使气态基态原子外层电子产生跃迁(2) 辐射能使原子内层电子产生跃迁(3) 能量使气态原子外层电子产生发射光谱(4) 电、热能使气态原子外层电子产生发射光谱15. 2 分(1360)为了消除火焰原子化器中待测元素的发光干扰, 应采取的措施是( )(1) 直流放大(2) 交流放大(3) 扣除背景(4) 数字显示二、填空题( 共5题10分)1. 2 分(2817)超临界流体色谱法是以_______________为流动相的色谱法, 其流动相的性质是_______________________________________。
苏州大学分析化学课程试卷(12)卷共8页考试形式闭卷年月日院系年级专业学号姓名成绩一.选择题(共36分)1..(本题2分)下列有关偶然误差的论述中不正确的是---------------------------------------()(1) 偶然误差具有随机性(2) 偶然误差具有单向性(3) 偶然误差在分析中是无法避免的(4)偶然误差是由一些不确定的偶然因素造成的2.(本题2分)下列数据中有效数字为四位的是----------------------------------------------()(1) 0.056 (2) 35.070 (3)pH=4.008 (4)0.70003. (本题2分)影响平衡常数的因素是--------------------------------------------------------( )(1) 反应物和产物的浓度(2) 溶液的酸度(3) 温度(4) 催化剂4.(本题2分)已知EDTA的各级离解常数分别为10-0.9、10-1.6,10-2.0、10-2.67、10-6.16和10-10.26,在pH=2.67—6.16的溶液中,EDTA最主要的存在形式----------------( )(1) H3Y- (2) H2Y2-(3)HY3-(4) Y4-5.(本题2分)用纸上色层上行法分离物质A和B时,已知A组分的比移值R f(A)=0.45,B 组分的比移值R f(B)=0.63。
欲使分离后,A、B两组分的斑点中心之间的距离为2.0cm,那么色层用的滤纸条的长度(cm)至少应为-------------------------()(1) 9 (2) 10(3) 11 (4) 156.(本题2分)频率υ=10 15Hz属于下列哪一种光谱区-----------------------------------( ) (已知:光速c=3.0 1010cm/s)(1) 红外区(2) 可见区(3) 紫外区(4) 微波区7.(本题2分)几种常用光源中,产生自吸现象最小的是---------------------------------( )(1) 交流电弧(2) 等离子体光源(3) 直流电弧(4) 火花光源8.(本题2分)为了消除火焰原子化器中待测元素的发光干扰,应采取的措施是( )(1) 直流放大(2) 交流放大(3) 扣除背景(4) 数字显示9.(本题2分)荧光分析是基于测量---------------------------------------------------------- ( ) (1)辐射的吸收(2) 辐射的发射(3) 辐射的散射(4) 辐射的折射10.(本题2分)用比色法测定邻菲罗啉一亚铁配合物时,配合物的吸收曲线,如图1所示,今有a、b、c、d滤光片可供选用,它们的透光曲线如图2所示,你认为应选的滤光片为---------------------------------------------------------------------- ( ) 图1 图2邻菲罗啉-亚铁吸收曲线滤光片的透光曲线(a,b,c,d,e为滤光片)11.(本题2分)助色团对谱带的影响是使-------------------------------------------------------( )(1) 波长变长(2) 波长变短(3) 波长不变(4) 谱带蓝移12.(本题2分)并不是所有的分子振动形式其相应的红外谱带都能被观察到,这是因为------------------------------------------------------------------------------------( )(1) 分子既有振动运动,又有转动运动,太复杂(2) 分子中有些振动能量是简并的(3) 因为分子中有C、H、0以外的原子存在(4) 分子某些振动能量相互抵消了13.(本题2分)化合物Cl-CH2-Cl1 H-NMR谱图上为-----------------------------------( )(1) 1个单峰(2) 1个三重峰(3) 2个二重峰(4) 2个三重峰14.(本题2分)玻璃电极在使用前一定要在水中浸泡几小时,目的在于---------------( )(1) 清洗电极(2) 活化电极(3) 校正电极(4) 除去沾污的杂质15(本题2分)在气相色谱分析中,用于定量分析的参数是--------------------------------( )(1) 保留时间(2) 保留体积(3) 半峰宽(4) 峰面积16.(本题2分)在气相色谱分析中,要使分配比增加,可以采取------------------------( )(1) 增加柱长(2) 减小流动相速度(3)降低柱温(4 ) 增加柱温17.(本题2分)在气—固色谱分析中,色谱柱内装入的固定相为------------------------( )(1) 一般固体物质(2) 载体(3) 载体+固定掖(4) 固体吸附剂18.(本题2分)应用GC方法来测定痕量硝基化合物,宜选用那种检测器------------( )(1) 热导池检测器(2) 氢火焰离子化检测器(3)电子捕获检测器(4) 火焰光度检测器二. 填空题(共14分)1.(本题2分)0.1mol/L Na2CO3溶液中,有关Na+的物料平衡式是__________________________________。
有关CO32-的物料平衡式是_______________________________________________________。
2.(本题2分)下列现象各是什么反应(填A,B,C,D)(1) MnO4- 滴定Fe2+时,C1-的氧化被加快__________(2) MnO4-滴定C2042-时,速度由慢到快____________(3) Ag+存在时,Mn2+氧化成MnO4- _______________(4) PbSO4沉淀随H2S04浓度增大溶解度增加(A) 催化反应(B) 自动催化反应(C) 副反应(D) 诱导反应3.(本题2分)分子对红外辐射产生吸收要满足的条件是(1)_______________________________________________(2)_______________________________________________4.(本题2分)核磁共振波谱法,是由于样品在强磁场作用下,用适宜频率的电磁辐射照射,使_______________________________________________________吸收能量,发生能级跃迁而产生的。
5.(本题2分)Br-离子选择电极有C1-离子干扰时,选择系数可写作:_____________。
6.(本题2分)色谱法按两相状态可分为____________________(它包括__ __________和________ ___ )及__________ _____(它包括________________和__________________ )。
7.(本题2分)红外光区在可见光区和微波光区之间,习惯上又将其分为三个区:,和,其中的应用最广。
三. 计算题(共25分)1.(本题5分)某实验室经常测定铁矿中含铁量,若固定称取试样为0.5000g,欲使消耗K2Cr2O7溶液的体积为Fe2O3 含量的一半,则应配制多大浓度的K2Cr2O7?( Mr(Fe2O3)=159.7)2.(本题5分)计算以0.20mol /L Ba(OH)2 溶液滴定0.10mol/L HCOOH溶液至化学计量点时,溶液的pH值为多少? (HCOOH的Ka=2.0 10-4)3. (本题5分)某化合物的最大吸收波长λmax=280nm,光线通过该化合物的 1.0⨯10-5 mol/L溶液时,透过率为50%(用2cm吸收池),求该化合物在280nm处的摩尔吸收系数。
4.(本题5分)有一样品含甲酸、乙酸、丙酸及不少水、苯等物质,称取此样品1.055g,以环己酮作内标,称取0.1907g 环己酮,加到样品中,混合均匀后,吸取此试液3μL 进样,得到色谱图。
从色谱图上测得的各组分峰面积及已知的S’值如下:甲酸乙酸环己酮丙酸峰面积 14.8 72.6 133 42.4相对响应值S’ 0.261 0.562 1.00 0.938求:甲酸、乙酸、丙酸的含量。
5.(本题5分)向pH=5.0的20.00 mL0.0200 mol•L-1 Zn2+溶液中加入20.04 mL0.200 mol•L-1 EDTA溶液后,游离的[Y]和[Zn2+]各为多少?(pH=5.0时, lgαY(H)=6.45 lgKZnY=16.50)四.问答题(共25分)1.(本题5分)指出下列化合物的紫外吸收波长,按由长波到短波吸收波长排列.CH3(1) (2) (3) (4)2.(本题5分)在液相色谱中,范氏方程中哪一项对柱效能的影响可以忽略不计? 为什么?3.(本题5分)气相色谱仪的基本设备包括哪几部分?各有什么作用?4.(本题5分)何谓助色团与生色团?试举例说明。
5.(本题5分)下列是一些乙烯CH 2= CH 2的正常振动模式。
试指出它们在红外光谱上,哪些是红外活性的?哪些是非红外活性的?C CH HH伸缩CCH HH(2)C-H 伸缩CCH HHH(3) C-H 摇摆C C H H HH(4)CH 2扭曲C CH HH(5)C=C 伸缩CCH HH(6)C-H 剪式苏州大学分析化学课程(12)卷参考答案共页院系化学化工学院专业一.选择题1.(0207)(2)2. (2264)(4)3. (0315)(3)4. (0329)(2)5.(1248)(3)6. (1103)(3)7. (1003)(2)8. (1360)(2)9.(1353)(2)10. (1019)(b)11. (1232)(1)12. (1088)(2)13.(1674)(1)14. (1255)(2)15. (1462)(4)16. (1215)(3)17.(1457)(4)18. (1411)(3)二.填空题1.(0358 2分)[Na+]=0.2[CO32-]+[HCO3-]+[H2CO3]=0.12.(0968 2 分)1. D2. B3. A4. C3.(2051 2分)(1)选择吸收能量(量子化能级能量差)(2)分子中相邻两原子具有不同的电子云密度(能产生偶极矩变化)4.(2496 2分)具有磁性的原子核5.(2088 2分)K Potj i,,K PotClBr--,6.(2374 2分)气相色谱,气液色谱,气固色谱,液相色谱,液液色谱,液固色谱7.远红外光区,中红外光区,近红外光区,中红外光区三.计算题1.(2163 5分)按x = (3 x c x x/2 x 159.7)/(0.5000 x 1000) x 100解得c=0.02087 mol/L2. (0538 5分)滴定反应Ba(OH)2 +2HCOOH = Ba(HCOO)2 + 2H2O设HCOOH溶液的体积为V (mL),根据反应的计量关系滴定至计量点时,Ba(OH)2溶液消耗的体积为V/4(mL),HCOO-的浓度为[HCOO-]计= (0.100 x V)/(V + V/4)= 0.08(mol/L)已知HCOOH Ka=2.0 x 10-4,HCOO- Kb = 5.0 x 10-11[OH-]计= 0800*0.5-= 2.0 x 10-6(mol/L)10*.011pOH计= 5.70 pH计= 8.303.(3096 5分)∵A = ε b c ,而A = - lg T %∴ε = (- lg T %/ b c)= - lg 0.5 %/(1.0 x 10-5 x 2)ε = 1.5 x 1044.(3356 5分)w(甲酸)=[(14.8/0.261)/(133/1.00)] x(0.1907/1.055)=0.077w(乙酸)=[(72.6/0.562)/(133/1.00)] x(0.1907/1.055)=0.176w(丙酸)=[(42.4/0.938)/(133/1.00)] x(0.1907/1.055)=0.0615.(3130 5分)[Y’]=[ (20.04-20.00)⨯0.0200]/(20.04+20.00) ≈ 2⨯10-5 mol.L-1 = 10-4.70 mol.L-1∵pH=5时lgαY(H) = 6.45∴[Y] =[Y’]/αY(H) =2⨯10-5/106.45=7.1⨯10-12mol.L-1=10-11.15lgK’ZnY = lgKZnY -lgαY(H)=16.50-6.45=10.05∴[Zn2+]= [ZnY]/ ([Y’] K’ZnY)=(0.02/2)/(10-4.70⨯1010.05)= 10-7.35= 4.5⨯10-8 mol•L-1或者∴[Zn2+]= [ZnY]/ ([Y] KZnY)=(0.02/2)/(10-11.15⨯1016.50)= 10-7.35= 4.5⨯10-8 mol•.L-1四.问答题1.(4439 5分)(3)>(4)>(1)>(2)2.(4072 5分)由于组分在液相中的扩散系数比在气相中的扩散系数小4~5个数量级。