1绪论 有机化合物的概述
- 格式:pptx
- 大小:629.65 KB
- 文档页数:12

第一节有机化合物和有机化学有机化学是化学的一个分支,它是研究有机化合物的来源、制备、结构、性能、应用以及有关理论和方法学的科学。
有机化合物的主要特征是含有碳原子,即都是含碳化合物,因此有机化学就是研究碳化合物的化学。
但少数碳的氧化物(如二氧化碳、碳酸盐等)和氰化合物(如氢氰酸、硫氰酸等),仍归属无机化合物范畴。
一、有机化学的发展有机化学作为一门科学是在十九世纪产生的,但有机化合物在生活中和生产中的应用由来已久。
最初是从天然产物中提取有效成分。
例如:从植物中提取染料、药物、香料等。
在十八世纪末,已经得到了许多纯粹的化合物如酒石酸、柠檬酸、乳酸、尿素等。
这些化合物有许多共同性质,但与当时从矿物来源得到的化合物相比,则有明显的区别。
在十九世纪初曾认为这些化合物是在生命力的作用下生成的,有别于从无生命中的矿物中得到的化合物。
因此叫做有机化合物,后者叫做无机物。
有机化合物早期的定义是“来自有生命机体的物质内”简称“有机物”。
这是因为,在化学发展的前期,无机物被大量合成,而有机物只能从动植物体获得。
如1769年从葡萄汁中取得纯的酒石酸;1773年从尿中取得尿素;1780年从酸奶中取得乳酸;1805年从鸦片中取得吗啡等。
因此,人们认为有机物是与生命现象密切相关的,是生物体内一种特殊的、神秘的“生命力”作用下产生的,只能从生物体内得到,不能人工合成。
这就是瑞典化学权威Berzelius为代表的“生命力”学说的观点。
由于人们认识局限性和对权威的迷信,“生命力”学说统治化学界达半个世纪之久,严重阻碍了有机化学的发展。
1828年德国化学家韦勒(F.W hler)将氰酸铵的水溶液加热得到了尿素:氰酸铵可以从无机物NH4Cl和氰酸钾(或银)反应生成。
此后,许多化学家也在实验室用简单的无机物做为原料,成功地合成了许多其他有机物。
如1845年colbe合成了醋酸;1854年Berthelot合成了油脂类物质等。
在大量的科学事实面前,化学家摒弃了“生命力”学说,加强了有机化合物的人工合成实践,促进了这门科学的发展。




1第1章 绪 论1.1 基本要求● 掌握有机化合物与有机化学的定义、有机化合物的特点。
● 掌握有机化合物结构特点,熟悉共价键的性质及其意义。
根据有机化合物的价键特征分析分子间作用力,进一步理解有机化合物特点。
● 掌握共价键的断裂方式与有机反应类型、有机反应中间体。
1.2 基本知识点1. 有机化合物及其特点 有机化合物是指含碳的化合物或碳、氢化合物及其衍生物。
组成有机化合物的主要元素包括C ,H ,O ,N ,S ,P ,X (卤素)。
仅由碳、氢两种元素组成的有机物称为烃,若还含有其他官能团,则称为烃的衍生物。
有机化学是研究有机物的组成、结构、性质及其相互转化的一门学科。
与无机物相比,有机物具有以下特点:多数有机物易燃烧;熔点低;化学反应速率慢,副反应多;难溶于水,易溶于有机溶剂。
有机物的以上特点都是由其结构特征所决定的。
2. 经典结构理论 组成分子的若干原子在分子内是按一定的顺序和结合方式连接着的,这种排列和结合方式称为结构。
19世纪中叶,由凯库勒(A.Kekul é)、库柏尔(A.Couper )、布特列洛夫(A.M.Buteleroff )、范特荷夫(J.H.van't Hoff )、勒贝尔(J.A.Le Bel )等提出的经典结构理论要点如下:(1)有机化合物中的碳元素总是四价的,其他元素都有各自的氧化值,如氢一价、氧二价、氮三价、卤素一价;(2)碳原子间可以彼此以单键、双键或叁键结合。
例如: (3)饱和碳原子具有正四面体结构:(4)分子结构决定分子性质,性质反映结构。
根据上述要点,就可以依分子式写出化合物的可能结构。
经典结构理论反映了原子间的结合方式及组成,但无法说明为什么要以一定比例结合。
3. 原子轨道 原子轨道是波函数Ψ的图像。
Ψ是描写原子核外电子运动状态的数学函数式,可以粗略地把Ψ看作是在x,y,z 三维空间里能找到电子的一个区域。
原子轨道有s ,p ,d ,f ,g 等不同类型。

大一有机化学绪论知识点1.有机化合物的分类:有机化合物是含有碳元素的化合物,按照功能基团可以分为醇、醚、醛、酮、羧酸、酯等。
2.有机化学键:有机化合物中的化学键可以分为共价键和极性键。
共价键是由共用电子对形成的,常见的有单键、双键和三键。
极性键则是由于电负性差异而产生的偏向性。
3.共轭体系:共轭体系是指一个或多个单键和一个或多个共轭双键相互交替排列而形成的一组π键的结构。
共轭体系具有较小的能量差异,因此比较稳定。
4.异构体:异构体是指分子式相同但结构不同的化合物。
包括构造异构体、空间异构体和立体异构体。
构造异构体是指化合物的分子结构不同,如链异构体和环异构体。
空间异构体是指化合物的空间取向不同,如顺反异构体。
立体异构体是指化合物分子中具有手性中心,存在手性异构体。
5.有机反应的基本原理:有机反应是有机化合物发生变化的过程。
常见的有机反应包括加成反应、消除反应、取代反应和重排反应。
加成反应是指两个分子结合而形成一个新的分子,消除反应是指一个分子分解为两个分子,取代反应是指一个原子或基团被另一个原子或基团取代,重排反应是指分子内原子或基团的位置发生变化。
6.极性和溶解性:极性是指分子中正负电荷分布的不均匀性。
极性分子通常具有较强的溶解性,而非极性分子溶解性较差。
极性溶剂通常可以溶解极性物质,非极性溶剂可以溶解非极性物质。
7.共沉淀和分配:共沉淀是指两种或更多种物质在溶液中发生反应而形成沉淀。
分配是指两个相互不相溶的液体中的物质在两相之间分配的过程。
分配系数是用来描述分配过程的指标。
8.杂环化合物:杂环化合物是指含有不同原子的环状化合物。
常见的杂环化合物包括含氧杂环、含氮杂环、含硫杂环等。
杂环化合物具有较强的化学活性和生物活性。
9.光学活性和手性:光学活性是指一些化合物对旋光的作用。
手性是指分子不具有镜面对称性,分为左旋体和右旋体。
手性分子与手性反应物之间发生反应时会产生对映异构体。
10.环加成反应和开链加成反应:环加成反应是指在环状化合物中发生加成反应,如环状醇的开环加成反应。


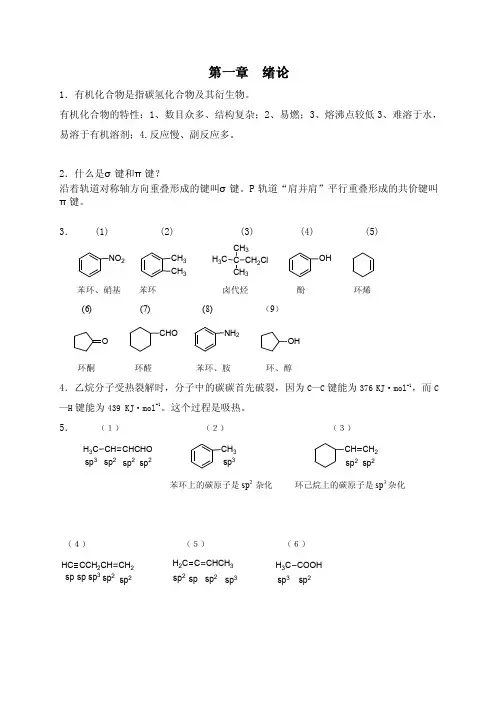
第一章绪论1.有机化合物是指碳氢化合物及其衍生物。
有机化合物的特性:1、数目众多、结构复杂;2、易燃;3、熔沸点较低3、难溶于水,易溶于有机溶剂;4.反应慢、副反应多。
2.什么是σ键和π键?沿着轨道对称轴方向重叠形成的键叫σ键。
P轨道“肩并肩”平行重叠形成的共价键叫π键。
3. (1) (2) (3) (4) (5)NO2CH3CH3H3C CCH3CH3CH2Cl OH苯环、硝基苯环卤代烃酚环烯(6) (7) (8) (9)O CHO NH2OH环酮环醛苯环、胺环、醇4.乙烷分子受热裂解时,分子中的碳碳首先破裂,因为C—C键能为376 KJ²mol-1,而C —H键能为439 KJ²mol-1。
这个过程是吸热。
5.(1)(2)(3)H3C CH CHCHO sp3sp2sp2sp2CH3sp3CH CH2sp2sp2苯环上的碳原子是sp2 杂化环己烷上的碳原子是sp3杂化(4)(5)(6)HC CCH2CH CH2sp3sp sp sp2sp2H2C C CHCH3sp2sp sp2sp3H3C COOHsp3sp2第二章烷烃1.解:(1)CH 3CH 2CHCH 2CH 2CH 2CH 3CH 2CH 3(2)CH 3CCH 2CHCH 3CH 3CH 3CH 3(3)CH 3CH 2CH 2CHCHCH 2CH 2CH 3CH 3CH 2CH 3(4)CH 3CH 2CCHCHCH 2CH 2CH 3CH 2CH 3CH(CH 3)2H 3CCH 2CH 2CH 32.解:(1) 2,3-二甲基辛烷(2) 2,7-二甲基-4-乙基壬烷 (3) 3,6-二甲基壬烷 3.解:(1)C CH 3CH 3H 3C CH 3(2) CH 3CHCH 2CH 3CH 3(3)CH 3CH 2CH 2CH 2CH 34.解:(1)CH 3CH 2CH 2CH 2CH(CH 3)2,(CH 3)2CHCH 2CH(CH 3)2,CH 3CH 2CHCHCH 3CH 3CH 3,H 3C C HC CH 3H 3C H 3CCH 3(2)CH 3CH 2CH 2CHCH 3CH 3,CH 3CH 2CHCH 2CH 3CH 3(3)H3C CHC CH3 H3CH3CCH35.解:(1)CH2CH2CH3,CH2CH2CH3(正戊烷绕C1-C2σ键旋转产生的交叉式和重叠式构象)(2)C2H5H3C,C2H5CH3,C2H5CH3,C2H5CH3(正戊烷绕C2-C3σ键旋转产生的全重叠式、邻位交叉式、部分重叠式、对位交叉式构象)(3)CH3C2H5,CH3C2H5(异戊烷绕C1-C2σ键旋转产生的交叉式和重叠式构象)(4)H3C CH3CH3H3C CH3CH3H3C CH3H3CH3C CH3CH3(异戊烷绕C2-C3σ键旋转产生的全重叠式、邻位交叉式、部分重叠式、对位交叉式构象)(5)CH(CH3)2CH(CH3)2(异戊烷绕C3-C4σ键旋转产生的交叉式和重叠式构象)(6)H3C CH3H3CCH3CH3H3C(新戊烷绕C1-C2σ键旋转产生的交叉式和重叠式构象)6.解:(3)>(2)>(4)>(1)7.解:1°H =12;2°H =0;3°H =08.解:FF FF9.解:CH310.解:链引发:Cl2hvCl²+Cl²链增长:Cl²+CH3CH3CH3CH2²+HClCl2+CH3CH2²Cl²+CH3CH2Cl链终止:Cl²+Cl²2Cl²+CH3CH2²3CH2ClCH3CH2²+CH3CH2CH3CH2CH2CH3(辽宁医学院赵延清)第三章烯烃炔烃二烯烃1. (1)4–甲基–1–己烯 (2)3–甲基–1–丁炔 (3)4–甲基–1,3–戊二烯(4)2,7–二甲基–2,7–壬二烯 (5)3–乙基–4–己烯–1–炔(6)5–甲基–1,3–环己二烯 (7)( Z )–3–甲基 –3–庚烯 (8)顺,反–2,4–庚二烯(或(2Z,4E )–2,4–庚二烯) 2.CH 3C H CCH(CH 3)2HH 3CH C3)CH 2CH 3CH 3CCl Br C CH 2CH 2CH 3HCl HC C C(CH 3)2CH 2CH 2CH 3CH CHH 2C C 2H 5C CH(1)(2)(3)(4)(5)(6)3.(1)(2)(3)(4)(5)(6)(7)(8)CH 3CH 3CH 2CH 2COOH + CO 2CH 3CCH 2CH 2CH 3CH 3BrCH 2ClCH 2CF 3CH 3CH CH 3SO 3HCH 3CH CH 3OH COOC 2H 5COOC 2H 5CH 3CH 2CH 2CH 2BrCH 3CH 2CHCCH 3OCuCCCH 34.答案不唯一,只要方法可行都可以。
第1章绪论一、有机化学和有机化合物人类对有机化合物(organic compound)的认识,最初主要基于实用的目的。
例如,用谷物酿酒和食醋;从植物中提取染料、香料和药物等。
到18世纪末,已经得到了一系列纯粹的化合物,例如酒石酸、柠檬酸、乳酸、苹果酸等。
这些从动植物来源得到的化合物具有许多共同的性质,但与当时从矿物来源得到的化合物相比,则有明显的区别。
由于受到生产力水平的限制,在18世纪末到19世纪初,曾认为这些化合物是由动植物有机体内的“生命力”影响而形成的,故有别于从没有生命的矿物中得到的化合物。
将前者称为有机化合物,后者称为无机化合物。
“生命力”学说曾一度阻碍了有机化学的发展,尤其是减缓了有机合成的前进步伐。
给予“生命力”学说的第一次沉重打击是1928年德国年轻的化学家乌勒(Friedrich Wöhler,1802~1882)首次从无机化合物氰酸铵合成了有机化合物尿素,这也是有机合成的开端。
NH4OCN-→NH2CONH2氰酸铵尿素尿素的人工合成,突破了无机化合物与有机化合物之间的绝对界限,不仅动摇了“生命力”学说的基础,开创了有机合成的道路,而且启迪了人们的哲学思想,有助于生命科学的发展。
德国化学家拜尔(Adolf von Beyer,1835~1917)与他人合作,1870年首次合成了靛蓝。
由于他对靛蓝及其衍生物的深入研究而荣获1905年诺贝尔化学奖。
与此同时,人们又合成了大量的有机化合物。
至此,“生命力”学说彻底破产了。
此后,人们还合成了成千上万种与日常生活密切相关的染料、药品、香料、炸药等有机物。
在一个“老的自然界”旁,再放上一个远远超过它的“新的自然界”。
这也是为什么要将有机化学(organic chemistry)单独作为一个化学分支的原因之一。
因此,有机化学是直到18世纪末才开始发展起来的一门科学。
在19世纪初期,由于测定物质组成的方法的建立和发展,在测定许多有机化合物的组成时发现,它们都含有碳,是碳的化合物。