吸收光谱法同时检测食品中的苯甲酸钠与山梨酸钾_李秋萍
- 格式:pdf
- 大小:457.94 KB
- 文档页数:6

摘 要苯甲酸是目前食品中较为理想的防腐剂。
少量食用,并无生命危险。
但如果大量食用,会导致中毒,甚至危及生命。
所以,确定食品中苯甲酸的含量并严格控制食用量是十分必要的。
本文采用紫外分光光度法对食品中苯甲酸含量进行了研究。
苯甲酸的特征峰在224nm处。
为选择最佳的UV-VIS分析条件,对饱和氯化钠溶液加入量、1:1HCl加入量、振荡和静置时间进行了研究。
正交实验结果表明,最佳的分析条件为,用10ml饱和氯化钠溶液、8ml:1HCl萃取含有苯甲酸的溶液,振荡3min 后静置2min,测其吸光度。
分别配制不同浓度的苯甲酸标准溶液,在224nm处测吸光度绘制A-C标准曲线。
同时测定回收率为93.8%-109.5%、RSD为0.6%、最小检出限为0.005mg/ml。
最后对样品中苯甲酸含量进行了测定。
结果表明,此方法灵敏、快速、准确。
关键词:苯甲酸,测定,紫外分光光度法AbstractBenzoic acid is the ideal food preservative. A small amount of it in food has no danger, but a large amount of it in food will lead poisoning and even life threatening . Therefore, determining the content of benzoic acid in food consumption and a strict control is necessary. A Ultraviolet Spectrophotometric determination of the food additive of benzoic acid has been studied. The maximum absorption of benzoic acid is 224nm. The best conditions for UV-VIS analysis :the quantity of saturated NaCl solution is 10ml, 1:1HCl is 8ml,shaking and standing time are 3min and 2min, and then measure the absorbance. We prepare with different concentrations of benzoic acid standard solution and measure absorbance for drawing A-C standard curve. The result shows that the recovery is 93.8%-109.5%,RSD is0.6%, the detection limit is 0.005 mg/ml. This method for determination of benzoic acid in sample is sensitive, rapid and accurate.Key words: benzoic acid, determine, Ultraviolet Spectrophotometric目 录第一章 前言 (1)1.1 苯甲酸含量的研究意义 (1)1.2 选题背景 (1)1.3 文献综述 (2)1.4 研究的基本内容,拟解决的主要问题 (8)第二章 实验材料与方法 (9)2.1 实验药品及仪器 (9)2.2 实验方法 (11)第三章 实验结果与讨论 (15)3.1 λmax选择 (15)3.2 饱和NaCl溶液加入量 (15)3.31:1HCl加入量 (16)3.4 振荡时间 (18)3.5 静置时间 (19)3.6 最佳实验条件选择(正交实验) (20)3.7 工作曲线绘制 (20)3.8 回收率测定 (22)3.9RSD测定 (22)3.10 共存离子干扰实验 (23)3.11 样品测定 (28)3.12 讨论 (29)第四章 结论与展望 (30)4.1 结论 (30)4.2 对进一步研究的展望 (30)参考文献 (31)致 谢 (33)声 明 (34)第一章 前 言1.1 苯甲酸含量的研究意义社会的发展,人们生活节奏的加快,促使食品工业特别是方便食品、半成品迅速发展。
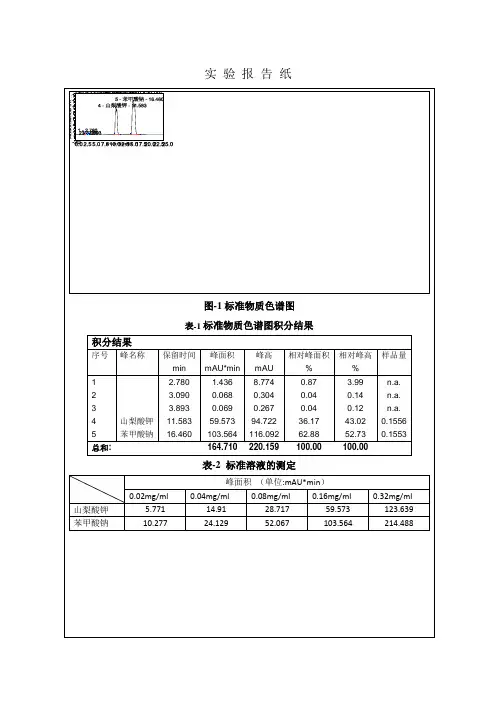
图-1标准物质色谱图表-1标准物质色谱图积分结果积分结果序号峰名称保留时间峰面积峰高相对峰面积相对峰高样品量min mAU*min mAU % %1 2.780 1.436 8.774 0.87 3.99 n.a.2 3.090 0.068 0.304 0.04 0.14 n.a.3 3.893 0.069 0.267 0.04 0.12 n.a.4 山梨酸钾11.583 59.573 94.722 36.17 43.02 0.15565 苯甲酸钠16.460 103.564 116.092 62.88 52.73 0.1553总和: 164.710 220.159 100.00 100.00表-2 标准溶液的测定峰面积(单位:mAU*min)0.02mg/ml 0.04mg/ml 0.08mg/ml 0.16mg/ml 0.32mg/ml 山梨酸钾 5.771 14.91 28.717 59.573 123.639 苯甲酸钠10.277 24.129 52.067 103.564 214.488山梨酸钾图-3 待测物质色谱图表-4 待测物质积分结果分析积分结果序号峰名称保留时间峰面积峰高相对峰面积相对峰高样品量min mAU*min mAU % %1 1.683 2.843 3.058 4.00 0.57 n.a.2 2.243 5.267 93.777 7.41 17.38 n.a.3 2.290 14.124 174.078 19.88 32.27 n.a.4 2.360 13.416 115.601 18.89 21.43 n.a.5 2.630 1.363 17.059 1.92 3.16 n.a.6 2.697 0.562 11.160 0.79 2.07 n.a.7 2.830 0.243 3.887 0.34 0.72 n.a.8 2.933 1.076 10.714 1.51 1.99 n.a.9 2.980 0.959 9.079 1.35 1.68 n.a. 10 3.467 2.141 5.633 3.01 1.04 n.a. 11 3.980 0.660 4.566 0.93 0.85 n.a. 12 4.0674.6204.666 6.50 0.86 n.a. 13 山梨酸钾 11.397 11.04838.135 15.55 7.07 0.0289 14 11.640 12.716 48.085 17.90 8.91 n.a. n.a.苯甲酸钠n.a. n.a.n.a.n.a.n.a.n.a. 总和:71.037 539.499 100.00 100.00待测物质的积分结果中,保留时间为11.397min 有检测信号,与标准物质的积分结果进行对比,此处为山梨酸钾的检测信号,说明待测物质中含有山梨酸钾。


饮料中防腐剂苯甲酸钠和山梨酸钾的同时测定
陈海春;余萍;王颖;赵洪岩
【期刊名称】《沈阳理工大学学报》
【年(卷),期】2002(021)002
【摘要】利用苯甲酸钠和山梨酸钾的紫外吸收光谱差异,采用多元线性回归紫外吸光光度法同时测定饮料中苯甲酸钠和山梨酸钾.该方法加和性好,准确度高,经F检验表明回归方程有实际意义.对实际样品进行测定并做加标回收实验表明,苯甲酸钠和山梨酸钾的平均回收率分别为103.0%和102.2%.
【总页数】3页(P98-100)
【作者】陈海春;余萍;王颖;赵洪岩
【作者单位】沈阳工业学院,化工分院,辽宁,沈阳,110045;沈阳工业学院,化工分院,辽宁,沈阳,110045;沈阳工业学院,化工分院,辽宁,沈阳,110045;沈阳工业学院,化工分院,辽宁,沈阳,110045
【正文语种】中文
【中图分类】O657.32
【相关文献】
1.两种吸收光度法同时测定果味饮料中苯甲酸钠和山梨酸钾含量的比较研究 [J], 汪显阳;冯伟;胡岩岩;刘贤香
2.紫外分光光度法同时测定饮料中山梨酸钾和苯甲酸钠 [J], 桑宏庆;蔡华珍;王大勇
3.同时测定碳酸饮料中苯甲酸钠、山梨酸钾和安赛蜜的高效液相色谱法 [J], 郭友珍;王志宏
4.偏最小二乘法-紫外光度法同时测定防腐剂尼泊金乙酯钠、山梨酸钾和苯甲酸钠[J], 叶姗
5.液相色谱同时测定饮料中苯甲酸钠山梨酸钾和糖精钠的方法研究 [J], 王爱军因版权原因,仅展示原文概要,查看原文内容请购买。


高效液相色谱法同时检测食品中脱氢乙酸、山梨酸、苯甲酸、糖精钠的含量【摘要】:由于生活水平的提高,人们越来越注重食品的安全性。
本文选用紫外检测器,反向C18柱,以甲醇醋酸铵水溶液(0.02mol/L)(5:95比例)为流动相,同时检测食品中脱氢乙酸、山梨酸、苯甲酸和糖精钠的含量,提高了试验的效率可执行性。
尤其是脱氢乙酸,在230nm波长下检验,降低了检出限,提高了痕量元素检测精确度。
【关键词】:食品添加剂;高效液相色谱法;食品卫生检验食品添加剂即为使食品的质量、色、香、味得到改善,延长存放的时间等需求下使用的合成或自然化学物质。
现阶段许多生产商家在饮品、酱制品、发酵豆制品中加入的甜味素一般是糖精钠、安赛蜜(AK糖)等。
使用的防腐剂通常是苯甲酸、山梨酸、脱氢乙酸。
但过度摄入这些添加剂对人体健康有一定的危害[1~2]。
目前,我国的《食品添加剂使用标准》(GB2760—2014)中对这些添加剂的应用范畴和最大允许使用量都有明确的规定[3~4]。
为了更好地测量和提高效率,在有关参考文献的基础上,本次研究选择高效液相色谱法同时检测了食品中脱氢乙酸、山梨酸、苯甲酸、糖精钠添加剂的含量,现报告如下:1 材料和方法1.1 关键仪器和实验试剂液相色谱仪:Waters 1525,装有紫外检测器;离心机:10 000r/min,TGL-16A离心机,长沙普通仪器有限公司;工业甲醇:色谱纯,tedia公司;乙酸铵:优级纯,广州试剂厂;碳酸氢钠:优级纯,Comio实验试剂;紫外线可见光度计:TU-1810,北京谱仪通用性仪器有限公司1.0mg/mL脱氢乙酸标液:精确称量0.100g脱氢乙酸标准物质,添加5mL碳酸氢钠(20g/L),微热状态下溶解,转移到100mL容量瓶中,放水滴定剂至100mL,作为储备液,在4摄氏度的环境下保存。
1.0mg/mL山梨酸标液:精确称量0.100g山梨酸标准物质,添加5mL碳酸氢钠(20g/L),加温溶解,转移到100mL容量瓶中,放水滴定剂至100mL,作为贮备溶液。

苯甲酸钠、山梨酸及山梨酸钾的测定—气相色谱法一、实训内容适用于测定酱油、果子汁等食品的苯甲酸钠、山梨酸及山梨酸钾的含量。
通过酸化处理从样品中提取苯甲酸钠、山梨酸及山梨酸钾,气相色谱法测定,绘制标准曲线,计算样品含量。
二、实训目的、要求①理解气相色谱法的原理,能熟练操作气相色谱仪。
②能熟练处理样品。
三、实训原理样品酸化后,用乙醚提取山梨酸,用氢火焰离子化检测器的气相色谱仪进行分离测定,与标准系列比较定量。
四、仪器和用具气相色谱仪:Agilent 7890气象色谱仪,配有氢火焰离子化检测器。
五、试剂①乙醚:不含过氧化物。
②石油醚:沸程30~600 ℃③盐酸。
④无水硫酸钠。
⑤盐酸(1+1):取100 mL盐酸,加水稀释至200 mL。
⑥氯化钠酸性溶液(40 g/L):向氯化钠溶液(40 g/L)中加少量盐酸(1+1)酸化。
⑦山梨酸标准溶液:准确称取山梨酸(0.1g左右)g,置于100 mL容量瓶中,用石油醚-乙醚(3+1)混合溶剂溶解后并稀释至刻度。
此溶液相当于(1m g/mL左右)山梨酸。
⑧山梨酸标准使用液:吸取适量的山梨酸标准溶液,以石油醚-乙醚(3+1)混合溶剂稀释至每毫升相当于0.5150 mg、0.2575mg、0.1288 mg、0.06438 mg、0.03219 mg山梨酸。
⑨苯甲酸钠标准溶液:准确称取苯甲酸钠(0.1g左右)g,置于100 mL容量瓶中,用石油醚-乙醚(3+1)混合溶剂溶解后并稀释至刻度。
此溶液相当于(1m g/mL左右)苯甲酸钠。
⑩苯甲酸钠标准使用液:吸取适量的苯甲酸钠标准溶液,以石油醚-乙醚(3+1)混合溶剂稀释至每毫升相当于0.5245 mg、0.2623mg、0.1311 mg、0.06556mg、0.0375 0mg苯甲酸钠。
六、操作步骤1. 样品提取(可口可乐、“6个柠檬”)称取(10g左右)g可口可乐和(10g左右)g6个柠檬事先混合均匀的样品,分别置于50mL带塞锥形瓶中,加0.5mL盐酸(1+1)酸化,用15mL、10mL乙醚提取2次,每次振摇1min,将上层乙醚提取液吸入另一个25mL带塞锥形瓶中。



HPLC法测定番茄果脯中的安赛蜜、苯甲酸、糖精钠和山梨酸肖丽恒;吕任一;李萍【摘要】对液相色谱法测定番茄果脯中安赛蜜、苯甲酸、糖精钠、山梨酸进行了方法优化,对色谱条件进行了调整,采用ODS-C18型(250mm×4.6mm,5μm)色谱柱,流动相甲醇-0.02 mol/L乙酸铵(体积比15:85),流速为1.0mL/min,采用紫外检测器,检测波长为230 nm.方法测定结果的相对标准偏差小于2%(n=5),平均回收率安赛蜜、苯甲酸、糖精钠、山梨酸均大于90%,该法满足实验要求.【期刊名称】《楚雄师范学院学报》【年(卷),期】2013(028)003【总页数】4页(P35-38)【关键词】高效液相色谱法;番茄果脯;安赛蜜;苯甲酸;糖精钠;山梨酸【作者】肖丽恒;吕任一;李萍【作者单位】楚雄州质量技术监督综合检测中心,云南楚雄675000;楚雄州质量技术监督综合检测中心,云南楚雄675000;楚雄州质量技术监督综合检测中心,云南楚雄675000【正文语种】中文【中图分类】R155.5随着人民生活水平提高及食品工业快速发展,休闲食品的种类不断增加。
番茄是一种营养丰富的食物,可进行深加工制成果脯而有利于保存。
为了增加番茄果脯的保存时间及口感,厂家常在番茄果脯中添加过量的防腐剂和甜味剂。
苯甲酸及其钠盐、山梨酸及其钾盐由于对微生物有很好的抑制作用而且价格便宜,是比较常用的防腐剂。
安赛蜜、糖精钠的甜度是蔗糖的很多倍,相对于蔗糖来说,甜度高、用量少,成本低,成为番茄果脯制作中普遍使用的甜味剂,但安赛蜜、糖精钠过量摄入会对人体产生危害。
防腐剂和甜味剂的测定方法主要有紫外光度法、色谱法[1]。
其中,高效液相色谱法在按国标推荐的色谱条件应用时,色谱分离的时间太长[2,6],不利于常规的实验室快速检测分析。
别外,国标检测方法在测定苯甲酸、山梨酸和糖精钠的高效液相色谱法中,检测样品只是液体的样品,而对其它样品的处理方法没有提及[2]。

食品中苯甲酸和山梨酸的检测摘要:近年来食品安全卫生已成为社会、政府关注的焦点之一。
食品安全已越来越引起广大消费者的密切关注和担忧。
目前我国每年食物中毒报告例数约2万人,但据专家估计实际数量要比这个数字大10倍左右。
食品安全问题不仅涉及广大消费者的健康,还涉及相关企业的经济效益和市场空间,关系到整个食品行业的发展。
苯甲酸可与人体内的氨基乙酸结合生成马尿酸而随尿液排出体外。
如过量摄入苯甲酸和苯甲酸钠,将会影响肝脏酶对脂肪酸的作用,其次苯甲酸钠中过量的钠对人体血压、心脏、肾功能也会产生影响。
特别是对心脏、肝、肾功能弱的人群而言,苯甲酸和苯甲酸钠的摄食是不适合的嘲。
另外还会出现代谢性酸中毒、惊厥和气喘等病症。
在体外测定中还可以测到一些弱断裂剂的放射性。
苯甲酸及其钠盐因为有叠加中毒现象的报道,在使用上有争议,虽仍为各国允许使用,但应用范围愈来愈窄。
日本的进口食品中就限制使用,甚至部分禁止使用,日本已停止生产。
但因价值低廉,在中国仍作为主要防腐剂使用。
山梨酸具有较低的毒性,是迄今为止国际公认的最好的防腐剂,已经成为了西方发达国家的主流防腐剂。
但事实上,现在已经报道了许多案例(荨麻疹和假过敏)说明人体中对过多的山梨酸所带来的危害。
由于山梨酸和苯甲酸在食品中的广泛使用,所以在此讨论苯甲酸和山梨酸的检测以技术及以及各种检测技术的利弊。
1防腐剂的检测在食品工业中,作为防腐剂,不能影响人体正常的生理功能,一般说来,在正常规定的使用范围内使用食品防腐剂对人体没有毒害或毒性极小。
因此,食品防腐剂的定性与定量的检测在食品安全性方面是非常重要的。
目前,测定防腐剂的方法主要有:薄层色谱法、高效液相色谱法、毛细管电泳法、气相气谱法等1.1苯甲酸和山梨酸各种检测方法1.1.1高效薄层色谱法和高效液相色谱法M.Thomassin等人曾经采用高效薄层色谱法和高效液相色谱法对尼泊金酯类作过检测,实验发现高效薄层色谱法的相对标准偏差要大于高效液相色谱法,但是高效薄层色谱法对于尼泊金酯类的定量就更为快速。
离子色谱法同时测定食品中的三种甜味剂和两种防腐剂摘要:本文使用IonPac AS17-C低疏水性阴离子交换色谱柱分离,两阶等浓度淋洗液洗脱,电导方法检测,研究了食品中三种甜味剂(山梨酸钾、苯甲酸钠和甜蜜素)和两种防腐剂(安赛蜜和糖精钠)的同时分析方法。
不同种类的食品经过直接稀释或水提后,样品溶液通过前处理柱去除有机物质。
该方法分析速度快,灵敏度高,结果准确可靠,适用于多种食品中上述甜味剂和防腐剂的测定。
关键词:甜味剂;防腐剂;离子色谱;食品质量分析一.前言食品中人工合成添加剂的使用情况,关系到食品的安全,是食品卫生监测的重要内容[1,2]。
为了使食品质量监督工作能够及时有效的开展,迫切需要准确灵敏的方法同时测定多种添加剂[3]。
本文研究的三种甜味剂(甜蜜素、安赛蜜、糖精钠)和两种防腐剂(山梨酸钾、苯甲酸钠),均有国标测定方法,但测定条件不同。
可以使用液相色谱法进行同时测定,但甜蜜素的灵敏度低[4]。
中国色谱网由于这五种物质分子中都带有易电离的阴离子基团,可通过阴离子交换分离,电导检测器检测[5],因此离子色谱作为合适的测定方法得到很快发展。
目前采用的离子色谱同时分析方法多采用梯度淋洗,以获得较好的分离度[6]。
本文采用一种新型阴离子交换色谱柱,通过淋洗条件优化,使用两阶等浓度氢氧化钾淋洗液洗脱,使待测离子和样品基体峰获得了更好的分离效果,在多种食品测定中获得了成功的应用。
1、实验部分1.1仪器与试剂仪器:ICS-3000型离子色谱仪(Dionex,美国)试剂和样品:甜蜜素(99.5%,Dr. Ehrenstorfer公司,德国);安赛蜜(99.5%,Dr. Ehrenstorfer 公司,德国);糖精钠(99.0%,Dr. Ehrenstorfer公司,德国);山梨酸钾(99.0%,Acros公司,美国);苯甲酸钠(分析纯,国药集团);氢氧化钠(50%,Acros公司,美国);甲醇(色谱纯,百灵威公司);超纯水(Millipore,电阻率为18.2MΩ/cm);前处理净化柱;0.22μm 尼龙滤膜;市售食品。
食品安全国家标准食品中苯甲酸、山梨酸和糖精钠的测定1 范围本标准规定了食品中苯甲酸、山梨酸和糖精钠含量的测定方法。
本标准第一法适用于食品中苯甲酸、山梨酸和糖精钠的测定;第二法适用于酱油、水果汁、果酱中苯甲酸、山梨酸的测定。
第一法液相色谱法2原理样品经处理后,用液相色谱分离,紫外检测器检测,外标法定量。
3试剂和材料注:除非另有说明,本方法所用试剂均为分析纯,水为GB/T 6682规定的一级水。
3.1 试剂3.1.1氨水(NH3•H2O)。
3.1.2氢氧化钠(NaOH)。
3.1.3硫酸(H2SO4)。
3.1.4亚铁氰化钾(K4Fe(CN)6•3H2O)。
3.1.5乙酸锌(Zn(CH3COO)2•2H2O)。
3.1.6氯化钠(NaCl)。
3.1.7酒石酸(C4H6O6)。
3.1.8硅酮树脂。
3.1.9磷酸二氢钠(NaH2PO4•12H2O)。
3.1.10磷酸二氢钾(KH2PO4)。
3.1.11中性氧化铝。
3.1.12甲醇(CH3OH):色谱纯。
3.1.13乙酸铵(CH3COONH4)。
3.2 试剂配制3.2.1 氨水(1+1):氨水与水等体积混合,经微孔滤膜过滤后备用。
3.2.2 氢氧化钠溶液(4 g/L):称取4 g氢氧化钠,溶于水并稀释至1000 mL。
3.2.3硫酸溶液(0.5 mol/L):移取30 mL浓硫酸(约70%)边搅拌边慢慢加入至500 mL水中,冷却至室温后,转移至1000 mL容量瓶中,用水定容至刻度。
3.2.4亚铁氰化钾溶液(92 g/L):称取106 g亚铁氰化钾加水至1000 mL。
3.2.5 乙酸锌溶液(183 g/L):称取220 g乙酸锌溶于少量水中,加入30 mL冰乙酸,加水稀释至1000 mL。
3.2.6 酒石酸溶液(15%):称取15 g酒石酸,用水定容100 mL。
3.2.7的磷酸盐缓冲液(pH 7.2):分别称取16.72 g磷酸二氢钠和2.72 g磷酸二氢钾,用水溶解后定容至1000 mL,经微孔滤膜过滤后备用。