JXHL0900401_棕榈酸帕利哌酮注射液进口标准
- 格式:doc
- 大小:169.00 KB
- 文档页数:6

98中国处方药 第19卷 第4期·疗效评价·脑血管病杂志,2019,17(11):1726-1729.[10]高建华.丹红注射液治疗脑卒中恢复期48例临床观察[J].山西医药杂志,2017,46(13):1603-1604.[11]李新燕,周霖,李维辰.活血化瘀类中成药联合丁苯酞注射液治疗急性脑梗死疗效与安全性的系统评价[J].中国医院用药评价与分析,2019,19(6):724-728.[12]王守章,胡旻雷,饶容丽.丁苯酞注射液联合依达拉奉对老年急性脑梗死患者神经功能及血清hs-CRP、NSE水平的影响[J].中国现代医学杂志,2019,29(19):63-67.[13]郑迪,周骏宇,王亮.丁苯酞对实验性脑梗死小鼠神经功能改善、脑保护及促进血管新生的作用[J].中国药师,2019,22(11):2003-2007.[14]王晓荣,乌云高娃,赵福全,等.丁基苯酞通过激活PI3K/Akt/GSK-3β信号通路及其在局部脑缺血损伤脑梗死中的神经保护作用[J].实用医学杂志,2019,35(19):2998-3003.[15]张海萍,袁梅,彭慧.艾地苯醌联合丁苯酞对老年血管性痴呆患者氧化应激损伤和MMSE评分、ADL-R评分的影响[J].中国老年学杂志,2019,39(15):3625-3628.[16]夏东晖,张静,张新杰,等.艾地苯醌联合依达拉奉治疗急性脑梗死临床研究[J].中国药业,2019,28(23):66-69.[17]高玲,唐红.艾地苯醌抑制氧化应激所致皮层神经细胞凋亡的机制[J].中国老年学杂志,2018,38(4):899-901.[18]金钱倩,经屏,张玲.丁苯肽联合艾地苯醌对血管性痴呆患者丘脑葡萄糖代谢与血管内皮细胞功能的影响[J].医学临床研究,2018,35(6):1198-1200.精神分裂症是指以明显的阳性症状、阴性症状、精神运动性障碍及现实检验能力严重受损为特征的一组精神障碍,其病因、临床表现、治疗反应及病程因人而有所不同[1]。

甲苯磺酸艾多沙班进口标准甲苯磺酸艾多沙班(苯巴比妥)是一种重要的中枢神经系统抑制药,常用于治疗癫痫、焦虑和睡眠障碍等疾病。
进口的药品必须符合国家的标准和要求,以确保药品的质量和安全性。
在本文中,我们将深入探讨甲苯磺酸艾多沙班的进口标准,包括其相关的内容、要求和意义。
一、甲苯磺酸艾多沙班的进口标准概述1.进口标准的定义进口标准是指作为进口商品合法性、安全性和质量的评价依据,是国家对进口商品质量的要求和规定。
对于药品来说,进口标准是保障患者用药安全的重要保障。
2.甲苯磺酸艾多沙班的进口标准意义甲苯磺酸艾多沙班作为一种用于治疗严重疾病的药物,其进口标准的意义不言而喻。
严格的进口标准可以保证药品的质量、疗效和安全性,有效地保障患者的用药需求。
3.甲苯磺酸艾多沙班的进口标准内容和要求甲苯磺酸艾多沙班的进口标准内容和要求涉及药品的生产、贮存、运输、质量控制等方方面面,其中包括原料药的质量标准、成品药的质量标准、包装标准、标签标识要求等。
二、甲苯磺酸艾多沙班进口标准的评估1.甲苯磺酸艾多沙班进口标准的深度评估对于甲苯磺酸艾多沙班的进口标准,需要进行深度评估,包括对进口标准的内涵和要求进行详细了解和分析。
还需要了解国际上相关的进口标准,以及不同国家对于这一药品的标准差异,这样才能更全面地评估进口标准的深度。
2.甲苯磺酸艾多沙班进口标准的广度评估除了深度评估,还需要对甲苯磺酸艾多沙班的进口标准进行广度评估,这包括了解不同国家和地区对于这一药品的进口标准要求情况,以及了解国际上对于这一领域的最新发展和要求,从而更好地把握进口标准的整体情况。
三、甲苯磺酸艾多沙班进口标准的撰写1.甲苯磺酸艾多沙班进口标准的关键内容在撰写甲苯磺酸艾多沙班进口标准的文章中,需要重点提及其关键内容,包括对原料药的质量标准、成品药的质量标准、包装标准、标签标识要求等方面进行详细的阐述和分析。
2.甲苯磺酸艾多沙班进口标准的总结和回顾在文章的总结和回顾部分,需要对甲苯磺酸艾多沙班进口标准的要点进行回顾,强调其重要性和必要性,同时也可以对未来的发展和趋势进行展望,为读者提供更加全面、深刻和灵活的理解。

帕利哌酮缓释片(芮达)的说明书如今社会压力大,人们忙于应付各种工作需求,相对来说,人的神经功能就承受着巨大的压力。
长期处于这种压力状态下很容易让人的神经功能出现问题,神经功能紊乱就是其中一种比较常见的疾病。
目前对于神经功能疾病的治疗,服用帕利哌酮缓释片(芮达)能有起到很好的治愈效果,并且任何副作用。
【药品名称】通用名称:帕利哌酮缓释片商品名称:帕利哌酮缓释片(芮达)英文名称:Paliperidone Extended-Release Tablets拼音全码:PaLiZuoTongHuanShiPian(ruiDa)【主要成份】帕利哌酮。
【性状】本品为浅褐色薄膜衣片。
【适应症/功能主治】适用于精神分裂症急性期的治疗。
【规格型号】6mg*7s【用法用量】本品推荐剂量为6mg,一日一次,早上服用,超始剂量不需要进行滴定。
虽然没有系统性地确立6mg以上剂量是否具有其他益处,但一般的趋势是较高剂量具有较大的疗效。
但必须权衡,因为不良反应随剂量增加也会相应增多。
因此,甘些患者可能从最高12mg/天的较高剂量中获益,而某些患者服用3mg/天的较低剂量已经足够。
仅在经过临床评价后方可将剂量增加到6mg/天以上,而且间隔时间通常应大于5天。
当提示需要增加剂量时,堆荐采用每次3mg/天的增量增加,推荐的最大剂量是12mg/天。
【不良反应】1.会增高痴呆相关性精神病老年患者的死亡率;2.脑血管不良反应,包括中风,痴呆相关性粗神症老年患者;3.抗精神病药恶性综合征;4.QT间期延长;5.迟发性运动障碍;6.高血糖和糖尿病;7.高催乳素血症;8.胃肠梗阻的可能性;9.体位性低血压和晕厥;10.可能的认知和运动功能障碍;11.癫痫;12.吞咽困难;13.自杀; 14.阴茎异常勃性; 15.血栓性血小板减速少性紫癜;16.体温调节功能破坏; 17.止吐作用; 18.帕金森症或存在路易氏小体性痴呆患者的敏感性增高; 19.影响代谢或血液动力学反应的疾病或病症。


核准日期:哌柏西利胶囊说明书请仔细阅读说明书并在医师指导下使用【药品名称】通用名称:哌柏西利胶囊商品名称:爱博新® / IBRANCE®英文名称:Palbociclib Capsules汉语拼音:Paiboxili Jiaonang【成份】本品主要成份为哌柏西利其化学名称为:6-乙酰基-8-环戊基-5-甲基-2-[[5-(1-哌嗪基)-2-吡啶基]氨基]吡啶[2,3-d]嘧啶-7(8H)-酮化学结构式:分子式:C24H29N7O2分子量:447.53辅料名称:微晶纤维素、单水乳糖、羧甲基淀粉钠、胶态二氧化硅、硬脂酸镁【性状】本品为胶囊剂,内容物为类白色至黄色粉末。
【适应症】本品适用于激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的局部晚期或转移性乳腺癌,应与芳香化酶抑制剂联合使用作为绝经后女性患者的初始内分泌治疗。
【规格】(1) 75 mg; (2) 100 mg; (3) 125 mg【用法用量】应由具抗癌药物使用经验的医生开始并监督本品治疗。
推荐剂量哌柏西利的推荐剂量为125 mg,每天一次,连续服用21 天,之后停药7 天(3/1 给药方案),28 天为一个治疗周期。
治疗应当持续进行,除非患者不再有临床获益或出现不可接受的毒性。
当与来曲唑联用时,来曲唑的推荐剂量为 2.5 mg,口服,每天一次,在整个28 天治疗周期连续服药。
具体请参见来曲唑批准的说明书。
给药方法口服。
应与食物同服,最好随餐服药以确保哌柏西利暴露量一致(见【药代动力学】)。
哌柏西利不得与葡萄柚或葡萄柚汁同服(见【药物相互作用】)。
哌柏西利胶囊应整粒吞服(吞服前不得咀嚼、压碎或打开胶囊)。
如果胶囊出现破损、裂纹或其他不完整的情况,则不得服用。
应鼓励患者在每天大约相同的时间服药。
如果患者呕吐或者漏服,当天不得补服。
应照常进行下次服药。
剂量调整建议根据个体安全性和耐受性调整哌柏西利的剂量。
出现某些不良反应时可能需要暂时中断/延迟给药和/或减低剂量,或永久停药来进行控制,请参照表1、2 和 3 中提供的方案进行剂量调整(见【注意事项】和【不良反应】)。

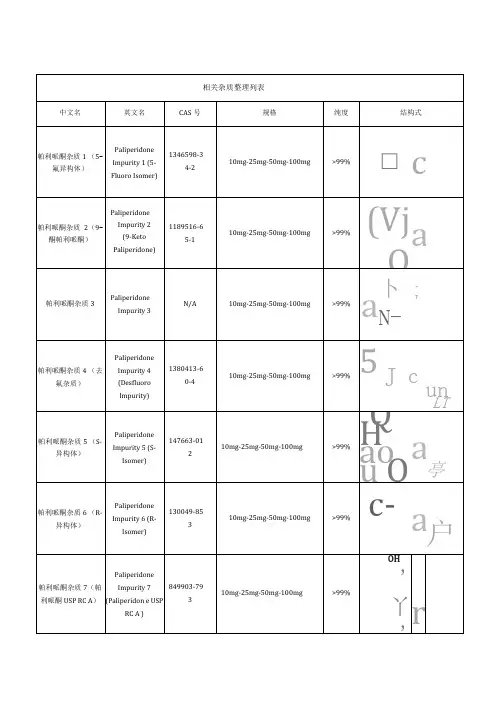
棕榈酸帕利哌酮质量标准?
答:棕榈酸帕利哌酮(Paliperidone Palmitate)是一种用于治疗精神分裂症的药物,其质量标准通常包括以下方面:
1.外观:药物应为白色至类白色的粉末或结晶性粉末。
2.鉴别:药物应通过特定的化学或物理方法进行鉴别,以确保其为棕榈酸帕利哌酮。
3.溶出度:药物在规定条件下应能够溶出,并符合规定的限度。
4.含量测定:药物中棕榈酸帕利哌酮的含量应通过适当的方法进行测定,并符合规定的含量范围。
5.杂质检查:药物中的杂质应符合规定,不得超过规定的限度。
6.微生物限度:药物中的微生物污染应符合规定,不得超过规定的限度。
此外,对于棕榈酸帕利哌酮的制剂,如注射液,还需要符合以下质量标准:
1.溶液的澄清度和颜色:注射液应为澄清无色或几乎无色的液体。
2.pH值:注射液的pH值应在规定的范围内。
3.渗透压摩尔浓度:对于注射用无菌粉末,其渗透压摩尔浓度应符合规定。
4.无菌:注射液应无菌。
5.细菌内毒素:注射液中的细菌内毒素应符合规定。
6.其他:注射液还应符合装量、可见异物等其他相关的质量标准。

紫杉醇注射液进口药品注册标准下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!本店铺为大家提供各种类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you! In addition, this shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts, other materials and so on, want to know different data formats and writing methods, please pay attention!紫杉醇注射液是一种常用的抗癌药物,被广泛用于治疗各种类型的癌症,如乳腺癌、卵巢癌、非小细胞肺癌等。

棕桐酸帕利哌酮注射液(善思达)中文说明书警示语增加患有痴呆相关精神病的老年患者的死亡率与安慰剂相比,使用非典型抗精神病药治疗患有痴呆相关精神病的老年患者时,死亡的风险会增加。
对在患有痴呆相关精神病的老年患者中进行的17项安慰剂对照临床试验(平均众数治疗时间为10周)的分析发现,药物治疗组患者死亡的危险性为安慰剂对照组的1.6-1.7倍。
在一项10周对照临床试验中,药物治疗组的死亡率为4.5%,安慰剂对照组为2.6%o虽然死亡原因各异,但是大多数死于心血管病(如心衰、猝死)或感染(如肺炎)。
研究显示,与非典型抗精神病药物相似,采用传统抗精神病药物治疗可能增加死亡率。
观察研究中死亡率的增加归因于抗精神病药物还是患者本身的某些特性造成的,目前尚不清楚。
本品未被批准用于治疗痴呆相关的精神病患者(参见【注意事项】)。
【通用名称】棕桐酸帕利哌酮注射液【商品名称】善思达®InvegaSustenna【英文名称】Pa1iperidonePa1mitateInjection【汉语拼音】Zong1vsuanPa1ipaitongZhusheye【成份】主要成份:棕相酸帕利哌酮化学名称:(±)-3-[2-[4-(6-氟-1,2-苯并异嘿嗖-3■基)-I-哌名]乙基]-6,7,8,9-四氢-2-甲基-4-氧-4H-口比咤[1,2-a]嗜咤-9-基棕桐酸酯化学结构式:分子式:C39H57FN4O4分子量:664.89辅料:聚山梨醇20、聚乙二醇4000、枸檬酸、无水磷酸氢二钠、磷酸二氢钠一水合物、氢氧化钠和注射用水。
【性状】本品为白色至灰白色的混悬液。
【适应症】本品用于精神分裂症急性期和维持期的治疗。
【规格】(1)0.75m1:75mg(2)1.0m1:IOOmg(3)1.5m1:150mg(按帕利哌酮计)【用法用量】给药方式每次注射都必须由专业医护人员操作。
只要产品和包装容器许可,注射制剂在使用前都应目视检查有无异物和变色。

芮达(帕利哌酮缓释片)说明书【芮达商品名】芮达【芮达通用名】帕利哌酮缓释片【芮达英文名】pailperidoneextended-releasetablets【芮达汉语拼音】PaiLiPaiTongHuanShiPian【芮达成份】帕利哌酮【芮达分子式】C23H27FN4O3【芮达分子量】426.49【芮达性状】帕利哌酮为白色薄膜衣片,或浅褐色薄膜衣片,或粉红色薄膜衣片【芮达适应症】帕利哌酮缓解释片适用于精神分裂症急性期的治疗【芮达用法用量】帕利哌酮推举剂量为6mg, 一日一次,早上服用,超始剂量不需要进行滴定。
虽然没有系统性地确立6mg以上剂量是否具有其他好处,但一般的趋势是较高剂量具有较大的疗效。
但必需权衡,由于不良反应随剂量增加也会相应增多。
因此,某些患者可能从12mg∕天的较高剂量中获益,而某些患者服用3mg∕天的较低剂量已经足够。
仅在经过临床评价后方可将剂量增加到6mg∕天以上,而且间隔时间通常应大于5天。
当提示需要增加剂量时,推举采纳每次3mg∕天的增量增加,推举的剂量是12mg∕天。
【芮达药理毒理】帕利哌酮是利陪酮的主要代谢产物。
与其他抗精神分裂症药物一样,帕利哌酮的作用机制尚不清晰,但目前认为是通过对中枢多巴胺2 (D2)受体和5・羟色胺2 (5HT2A)受体拮抗联合介导的。
帕利哌酮也是。
1和。
2肾上腺素能受体以及H1组胺受体的拮抗剂,这可能是该药物某些其他作用的缘由。
帕利哌酮与胆碱能毒蕈碱受体或B 1-和P 2-肾上腺受体无亲和力。
在体外,(+)-和(-)-帕利哌酮对映体的药理学作用是相像的。
【芮达遗传毒理】帕利哌酮Ames试验、小鼠淋巴瘤试验、大鼠微核试验结果均为阴性。
【芮达生殖毒性】1.在一项生育力试验中,经口赐予帕利哌酮,剂量高达2.5mg∕kg∕天时,雌性大鼠生殖力未见影响。
但是在该剂量下,着床前与着床后丢失率增加,活胎数稍微降低,也可见稍微的母体毒性。
在剂量为0.63mg∕kg时这些剂量未受影响,该剂量按mg∕平方米推算,相当于人推举剂量的一半。
棕榈酸帕利哌酮注射液治疗急性精神分裂症的疗效及安全性研究目的探讨棕榈酸帕利哌酮注射液治疗急性精神分裂症的疗效及安全性。
方法对42例急性精神分裂症患者使用棕榈酸帕利哌酮注射液(75~150mg)。
在治疗前及治疗后第1、2、4、8w末分别评定阳性与阴性症状量表(PANSS),用副反应量表(TESS)评定不良反应,并进行前后对比分析。
结果有40例患者完成8w的临床研究,临床治愈率33%,有效率80%;在第1w末PANSS总分及各分量表评分均较基线明显降低(阴性症状分P<0.05,其余均P<0.01);治疗中无严重不良反应。
结论棕榈酸帕利哌酮注射液对急性精神分裂症效果良好,起效快,且具有良好的安全性和耐受性。
标签:棕榈酸帕利哌酮;精神分裂症抗精神病药物长效针剂的出现,为患者及其照料者简化了治疗过程,并且提高了患者的依从性[1,2]。
棕榈酸帕利哌酮是一种已被批准用于成人精神分裂症治疗的长效注射液,是首个每月注射1次的非典型长效针剂,在首次肌注后的第1d,帕利哌酮即释放入血循环中,并持续释放126d,达峰时间平均为13d[3],其使用方法可以使药物快速达到治疗浓度,控制精神分裂症急性期患者的病情[4]。
本研究应用棕榈酸帕利哌酮治疗急性精神分裂症,以探讨其疗效及安全性。
1资料与方法1.1一般资料为我院2013年1月~8月的住院患者。
纳入标准:①年龄在18~60岁;②符合国际疾病分类(ICD-10)精神分裂症诊断标准;③受试者处于精神分裂症急性发作阶段,基线期的PANSS总分≥70分;④所有受试者均经其本人或法定监护人签署了知情同意书。
1.2排除标准①筛选前3个月使用了长效注射类抗精神病药或氯氮平;②既往规范使用利培酮、帕利哌酮治疗无效或不能耐受者;③足量足疗程应用两种以上抗精神病药治疗效果不佳者;④有重大或不稳定的躯体疾病,包括目前存在有临床意义的实验室检查异常(血、尿常规及血生化);⑤有酒精、物质滥用或依赖者;⑥曾经或目前存在迟发性运动障碍症状的患者;⑦曾有抗精神病药所致恶性综合征病史的患者;⑧存在暴力或者自伤行为或倾向者;⑨妊娠或哺乳期的女性;⑩代谢或其他因素可能影响帕利哌酮活性的患者。
帕利哌酮对急性期精神分裂症患者机体泌乳素水平以及社会功能的影响发表时间:2017-04-25T15:15:37.983Z 来源:《心理医生》2017年3期作者:朱颖之[导读] 并且药物安全性优于利培酮,但作为长效针剂运用于急性期精神分裂症患者临床治疗中,还需要大样本、多中心研究加以证实。
(江苏省常州市德安医院江苏常州 213000)【摘要】目的:探讨帕利哌酮治疗急性期精神分裂症对患者机体泌乳素(PRL)水平以及社会功能的影响。
方法:选择在我院住院治疗精神分裂症患者60例,随机分为利培酮治疗组与帕利哌酮治疗组各30例,两组持续治疗4个月后比较患者血浆中PRL水平、社会功能、治疗效果与药物不良反应等情况。
结果:治疗4个月后,帕利哌酮治疗组患者PRL水平明显低于利培酮治疗组(P<0.01),而PSP量表评分显著高于利培酮治疗组(P<0.01);治疗4个月后,帕利哌酮治疗组患者药物不良反应评估量表分明显低于对照组(P<0.05)。
结论:帕利哌酮治疗急性期精神分裂症,能有效改善患者的疾病症状,提高社会功能,并且药物安全性优于利培酮。
【关键词】精神分裂症;帕利哌酮;社会功能【中图分类号】R749 【文献标识码】A 【文章编号】1007-8231(2017)03-0132-02利培酮是我国临床常用的治疗效果确切的抗精神病药物,但随着药物研究不断深入,发现使用利培酮可出现高泌乳素血症、体重升高等诸多不良反应,对患者的用药依从性产生不良影响,也不利患者恢复社会功能。
注射用帕利哌酮是一种新型抗精神病药物,临床证实其具有疗效佳、用药依从性高等优点[1]。
本次研究是探讨帕利哌酮对急性期精神分裂症患者机体泌乳素水平以及社会功能恢复的影响。
报道如下。
1.资料与方法1.1 一般资料选择我院在2015年1月至2016年10月期间收治的住院精神分裂症患者60例为研究对象,均符合我国CCMD-3中的诊断标准,年龄在18~65周岁之间。
【化学结构式】
【适应症】适用于敏感菌所致的各种感染如肺炎及其他下呼吸道感染、尿路感染、胆道感染、皮肤软组织感染、败血症、腹膜炎、盆腔
感染等,后两者宜与抗厌氧菌药联合应用。
【规格】按C25H27N9O8S2计算 (1) 0.5g (2)0.75g (3)1.0g (4)1.5g (5)2.
0g (6) 3.0g
【用法用量】可供肌内注射、静脉注射或静脉滴注。
成人常用量:一般感染,一次1~2g,每12小时1次;严重感染,一次2~3g,每8小时1次。
接受血液透析者,透析后应
补给1次剂量。
成人一日剂量不超过9g,但在免疫缺陷病人有
严重感染时,剂量可加大至每日12g。
小儿常用量:每日50~200mg/ kg,分2~3次静脉滴注。
制备肌内注射液,每1g药物加灭菌注射用水2.8ml及2%利多卡因注射液1ml,其浓
度为250mg/ml。
静脉徐缓注射者,每1g药物加葡萄糖氯化钠
注射液40ml溶解;供静脉滴注者,取1~2g头孢哌酮溶解于1
00~200ml葡萄糖氯化钠注射液或其他稀释液中,最后药物浓
度为2~25mg/ml。
每1g头孢哌酮的钠含量为1.5mmol(34m
g)。
【不良反应】1.皮疹较为多见,达2.3%或以上。
2.少数病人尚可发生腹泻、腹痛、嗜酸粒细胞增多,轻度中性。
棕榈酸帕利哌酮结构式概述说明1. 引言1.1 概述棕榈酸帕利哌酮(Paliperidone palmitate)是一种常用的抗精神病药物,属于非典型抗精神病药(atypical antipsychotic)。
作为一种长效注射剂,它能够提供持久而稳定的治疗效果,减轻患者每日服药的负担。
由于其强大的治疗效果和方便的使用方式,棕榈酸帕利哌酮在临床上得到广泛应用。
1.2 文章结构本文将分为四个主要部分进行介绍。
首先,在引言部分将对棕榈酸帕利哌酮进行总体概述并阐明文章的目的。
然后,在"2. 棕榈酸帕利哌酮结构式"部分,我们会详细地探讨其定义、特点以及分子结构解析,并介绍其化学性质和各种用途。
接着,在"3. 正文"部分,我们将回顾棕榈酸帕利哌酮的历史与发现背景,并深入探讨其合成方法与工艺流程,以及生物活性和医药应用研究。
最后,在"4. 结论"部分,我们将总结主要的研究发现和成果,并展望未来的研究方向和建议。
1.3 目的本文旨在全面介绍棕榈酸帕利哌酮的结构式以及其相关内容。
通过对棕榈酸帕利哌酮的分析和探讨,我们希望读者能够更好地了解这一药物的定义、特点、化学性质等方面信息,并加深对其历史背景、合成方法、生物活性以及医药应用研究等方面内容的理解。
最终,我们也希望通过本文所提供的内容,为今后关于棕榈酸帕利哌酮的研究和进一步发展提供一定的参考依据。
2. 棕榈酸帕利哌酮结构式2.1 定义与特点棕榈酸帕利哌酮(Paliperidone palmitate)是一种药物,属于抗精神病类药物。
它是帕利哌酮的植物脂肪酸衍生物,通过与棕榈酸发生酯化反应制得。
棕榈酸帕利哌酮具有改善精神症状和控制兴奋状态的作用。
2.2 分子结构解析在棕榈酸帕利哌酮的分子中,帕利哌酮部分与普通的帕利哌酮相同,而其巯基(thiol group)则与棕榈酸发生化学反应形成脂肪酰基链(palmitoyl chain)。
棕榈酸帕利哌酮注射液治疗老年精神分裂症的有效性及安全性分析顾培;仇玉莹;靳秀;毛富强【摘要】目的:探讨棕榈酸帕利哌酮注射液治疗老年精神分裂症患者的疗效、耐受性、安全性及社会功能的恢复.方法:将天津市安定医院2014年8月-2016年3月老年科收治的80例老年精神分裂症患者随机分为研究组和对照组,每组40例患者.研究组用棕榈酸帕利哌酮注射液治疗,第1日注射75 mg,第8日注射75 mg,此后每隔1个月左右注射50~75 mg;对照组用利培酮片剂治疗,第1日口服0.5 mg,在2周内逐步增量至最佳给药剂量,最大给药剂量不超过2 mg/d,疗程24周.治疗前及治疗后4、8、16和24周采用阳性和阴性症状量表(PANSS)、依从性评定量表(MARS)、副反应量表(TESS)来评估疗效及安全性,用个人和社会功能量表(PSP)来评估社会功能.结果:72例患者完成24周临床治疗,有8例患者脱落.①两组PANSS 评分在治疗第4、8、16和24周时均低于基线水平,差异均有统计学意义(P均<0.01);两组间同一时点PANSS评分比较,差异均无统计学意义(P均>0.05).②研究组MARS评分在治疗第4、8、16和24周均高于基线水平,差异均有统计学意义(P均<0.01);对照组MARS评分在治疗第4、8周均有显著统计学意义(P均<0.05);两组间除基线外同一时点MARS评分比较,差异均有统计学意义(P均<0.01).③研究组同一治疗时点PSP评分均高于对照组,且差异均有统计学意义(P均<0.01);对照组PSP评分在治疗第4、8、16和24周均高于基线水平,差异有统计学意义(P 均<0.05);两组间除基线外同一时点PSP评分均高于对照组,差异均有统计学意义(P 均<0.05).④两组患者均无严重不良反应发生,组间不良反应发生率比较差异无统计学意义(P均>0.05).结论:老年精神分裂症患者采用棕榈酸帕利哌酮注射液治疗疗效与利培酮片剂相当,但服药依从性好,社会功能明显恢复,无明显不良反应.【期刊名称】《天津药学》【年(卷),期】2017(029)003【总页数】4页(P42-45)【关键词】棕榈酸帕利哌酮注射液;老年精神分裂症;疗效;安全性;社会功能【作者】顾培;仇玉莹;靳秀;毛富强【作者单位】天津市安定医院,天津 300222;天津医科大学 300070;天津市安定医院,天津 300222;天津医科大学 300070;天津医科大学 300070【正文语种】中文【中图分类】R971+.41精神分裂症的治疗目标随着精神医学的发展而不断变化,已由原来的单一注重疗效,逐渐发展成为更强调患者服药的安全性、耐受性及社会功能的恢复。
国家食品药品监督管理局
进口药品注册标准
标准号:JX20100263
棕榈酸帕利哌酮注射液
Zonglvsuan Palipaitong Zhusheye
Paliperidone Palmitate Injection
本品含棕榈酸帕利哌酮按帕利哌酮(C23H27FN4O4)计算,应为标示量90.0%~110.0%。
【性状】本品为白色至灰白色的混悬液。
【鉴别】(1)取本品1支,摇匀,取1滴至溴化钾片的表面。
照红外分光光度法(中国药典2010年版二部附录IV C)测定,其红外光吸收图谱在3200-2600cm-1,1800-1500cm-1和1200-750cm-1范围内应与对照品的红外光吸收图谱一致。
(2)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
【检查】重混悬性与抽针试验取本品3支,在10秒钟内振摇30次,振摇幅度约为25cm,振摇后溶液应均匀,不得检出可见异物或团块物。
用23号针头(蓝色针座)的注射器抽取,应顺利通过,不得阻塞。
pH值应为6.5~7.5(中国药典2010年版二部附录VI H)。
粒度分布取本品1支,加水稀释至250ml(1.5ml规格稀释至500ml),混匀后测试。
应用Malvern Mastersizer 2000 激光粒度仪,红光检测,泵速为1250转/分,颗粒折射率为1.56,颗粒吸收率为0.01,遮光度在6.8%-7.2%之间稳定1分钟后测试,测试时间为30秒。
d(0.1)应为0.3-0.6μm,d(0.5)应为0.9-1.4μm,d(0.9)应为2.0-4.4μm。
有关物质照含量测定项下的色谱条件,精密量取含量测定项下供试品溶液和对照品溶液各10μl注入液相色谱仪,记录色谱图。
供试品溶液色谱图中如有杂质峰,加校对因子校正后,按外标法以对照品溶液中主峰面积计算各杂质的含量,单个杂质峰面积不得过0.2%,各杂质的总和不得过0.4%。
单个杂质含量计算公式如下:
式中G 为注射液的密度,1.037g/ml
q s为供试品称样量,g
P r为对照品纯度
F r为棕榈酸帕利哌酮与帕利哌酮的换算因子1.56
RRF为校正因子,杂质R130696为0.933(相对保留时间为0.70),其他杂质均为1.0 r i为供试品溶液中单个杂质色谱峰的峰面积
Q th为标示含量,100mg/ml
r r为对照品溶液色谱图中主峰的峰面积
q r为对照品溶液中对照品的称样量,mg
释放度取本品,照溶出度测定法(美国药典32版<711> 第二法),以0.489%聚山梨醇酯20的0.001mol/L盐酸溶液900ml为释放介质,介质温度为25 ︒C±0.5︒C,转速为每分钟50 转,依法操作,向每个溶出杯中加入相当于0.5ml±0.025ml的均匀混悬液样品【加样方式:取本品足够支数,摇匀,预先混合,量取0.5ml±0.025ml,置样品杯(规格为高14mm,内径14mm,壁厚1mm)中,精密称定,使样品杯悬于释放介质正上方,接近溶出杯的边沿,在桨转动时将样品投入;或将预先混合注射液约0.5ml±0.025ml,置1ml规格的带针头注射器内,精密称定,当桨转动时,将上述混悬液加入每个溶出杯中,精密称定带有针头的空注射器】。
经1.5分钟、20分钟和45分钟时,分别取释放介质4.5ml,立即用0.2μm孔径的滤膜滤过,弃去初滤液至少3ml,取续滤液1.5ml作为供试品溶液;另取棕榈酸帕利哌酮对照品33.8mg,精密称定,置50ml 量瓶中,加四氢呋喃5ml,振摇溶解,用二甲基甲酰胺稀释至刻度,精密量取10ml,置50ml 量瓶中,用二甲基甲酰胺稀释至刻度,摇匀,作为对照品溶液。
精密量取对照品溶液10ml置于50ml量瓶中,用二甲基甲酰胺稀释至刻度,摇匀,作为20%对照品溶液。
照含量均匀度项下的色谱条件,精密量取上述三种溶液20μl,按外标法以峰面积,分别计算出每杯中帕利哌酮在不同时间的释放量,本品每杯在1.5分钟,20分钟和45分钟的释放量应分别相应为不得过标示量的20%,48%-75%和72%-93%,均应符合规定。
(试验过程中不需要在操作容器中补充释放介质,计算公式中不需要对释放介质的体积进行校正。
)
含量均匀度取本品1支,摇匀,取22号针头(灰色针座)安装在注射器上,将内容物转移置50ml(0.25ml规格)或100ml(0.5ml规格)或150ml(0.75ml规格)或200ml(1.0ml 规格)或300ml(1.5ml规格)量瓶中,加适量稀释溶液【四氢呋喃-二甲基甲酰胺(5:95)】振摇溶解,加稀释溶液稀释至刻度,摇匀,作为供试品溶液;另取棕榈酸帕利哌酮对照品约78mg,精密称定,置100ml量瓶中,加5ml四氢呋喃,振摇溶解,用二甲基甲酰胺稀释至刻度,摇匀,作为对照品溶液。
照高效液相色谱法测定,以十八烷基硅烷键合硅胶为填充剂,以流动相A (0.01mol/L醋酸铵溶液1000ml中加入1ml甲酸)-流动相B(取700ml乙腈,加入300ml异丙醇,加入1ml甲酸)(25:75)为流动相,流速为1.2ml/min,检测波长为275nm,柱温为35 C。
取对照品溶液进样5针,帕利哌酮峰面积的相对标准偏差不得过2.0%。
精密量取上述两种溶液10 μl,按外标法以峰面积,分别计算出每支注射液中帕利哌酮的含量,应符合规定(美国药典32版<905>)。
每支注射液中帕利哌酮的含量计算公式如下:
式中P r为对照品纯度
F r为棕榈酸帕利哌酮与帕利哌酮的换算因子1.56
r m为供试品溶液色谱图中主峰的峰面积
r r为对照品溶液色谱图中主峰的峰面积
q r为对照品称样量,mg
q s注射液的包装规格,ml
V m为供试品溶液的稀释体积,ml
Q th为标示含量,100mg/ml
不溶性微粒取本品10支,摇匀,取内容物加空白试剂【冰醋酸-水(1:2)】385ml,振摇溶解,超声脱气后测定,测定结果用空白溶液进行校正,依法检查(中国药典2010年版二部附录IX C),应符合规定。
细菌内毒素取本品,依法检查(中国药典2010版二部附录XI E),每1mg棕榈酸帕利哌酮中含内毒素的量应小于2EU。
无菌取本品,用薄膜过滤法处理,滤过,以0.9%无菌氯化钠溶液为冲洗液,每膜约冲洗100ml(50ml/次,冲洗2次),以金黄色葡萄球菌为阳性对照菌,依法检查(中国药典2010版
二版附录XI H),应符合规定。
其他应符合注射剂项下有关的各项规定(中国药典2010年版二部附录I B)。
【含量测定】照高效液相色谱法(中国药典2010年版二部附录I B)。
色谱条件与系统适用性试验用十八烷基硅烷键合硅胶为填充剂(YMC Pro C18, ,
150mm ⨯ 3.0mm,5μm或效能相当色谱柱);流动相A:0.01mol/L醋酸铵溶液,流动相B:甲醇-乙腈(20:80);按下表进行梯度洗脱;检测波长为280nm;柱温为35 °C;进样器温度为10°C;流速为0.6ml/min。
系统适用性试验溶液记录的色谱图中,杂质R206474(相对保留时间为0.63)和R130696峰(相对保留时间为0.70)的分离度不小于2.0;取对照品溶液连续进样5针,帕利哌酮峰面积的相对标准差不得过2.0%。
定量限溶液记录的色谱图中,帕利哌酮峰的响应因子与对照品溶液中主峰的响应因子比应为0.7-1.3。
(系统适用性试验溶液的典型色谱图如附图所示)
系统适用性试验溶液的制备取棕榈酸帕利哌酮定性对照品约40mg,精密称定,置50ml 量瓶中,加5ml四氢呋喃,振摇溶解,用二甲基甲酰胺稀释至刻度,摇匀,即得。
定量限溶液的制备精密量取对照品溶液5ml,置100ml量瓶中,加稀释溶液【四氢呋喃-二甲基甲酰胺(5:95)】稀释至刻度,摇匀,精密量取1ml,置100ml量瓶中,加稀释溶剂稀释至刻度,摇匀,即得。
对照品溶液的制备取棕榈酸帕利哌酮对照品约80mg,精密称定,置100ml量瓶中,加5ml四氢呋喃,振摇溶解,用二甲基甲酰胺稀释至刻度,摇匀,即得。
供试品溶液的制备取本品5支,摇匀,将内容物置具塞试管中,摇匀,精密称取适量(相当于帕利哌酮100mg),置200ml量瓶中,加50ml稀释溶剂,振摇至完全溶解,加稀释溶剂稀释至刻度,摇匀。
测定法取供试品溶液与对照品溶液各10 μl分别注入液相色谱仪,记录色谱图,按外标法以峰面积计算供试品中帕利哌酮的含量(棕榈酸帕利哌酮与帕利哌酮的换算因子为1.56)。
含量计算公式如下:
式中G为注射液的密度,1.037gml
q s 为供试品称样量,g
P r 为对照品纯度
F r 为棕榈酸帕利哌酮与帕利哌酮的换算因子为1.56
r m为供试品溶液色谱图中主峰的峰面积
r r为对照品溶液色谱图中主峰的峰面积
Q th为标示含量,100mg/ml
q r为对照品溶液中对照品的称样量,mg
【类别】精神分裂症治疗药物
【规格】(1)0.25ml:25mg,(2)0.5ml:50mg ,(3)0.75ml:75mg,(4)1.0ml:100mg,(5)1.5ml:150mg(按帕利哌酮计)
【贮藏】30°C下常温保存。
请勿冷冻保存。
【有效期】24个月
【生产国家及生产厂】Belgium(比利时)Janssen Pharmaceutica N.V.
【复核单位】中国药品生物制品检定所。