第二章 原子结构和晶体的结合力
- 格式:pptx
- 大小:5.38 MB
- 文档页数:39


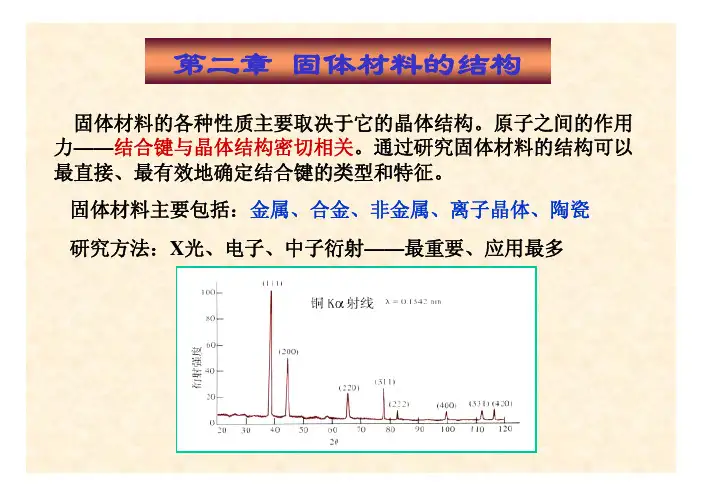
第二章固体材料的结构固体材料的各种性质主要取决于它的晶体结构。
原子之间的作用结合键与晶体结构密切相关。
通过研究固体材料的结构可以最直接、最有效地确定结合键的类型和特征。
固体材料主要包括:金属、合金、非金属、离子晶体、陶瓷研究方法:X光、电子、中子衍射——最重要、应用最多§2-1 结合键结合键——原子结合成分子或固体的结合键决定了物质的物理、化学、力学性质。
一切原子之间的结合力都起源于原子核与电子间的静电交互作用(库仑力)。
不同的结合键代表了实现结构)的不同方式。
一、离子键典型的金属与典型的非金属元素就是通过离子键而化合的。
从而形成离子化合物或离子晶体由共价键方向性特点决定了的SiO2四面体晶体结构极性共价键非极性共价键五、氢键含有氢的分子都是通过极性共价键结合,极性分子之间结合成晶体时,通过氢键结合。
例如:H 2O ,HF ,NH 3等固态冰液态水§2-2 金属原子间的结合能一、原子作用模型固态金属相邻二个原子之间存在两种相互作用:a) 相互吸引——自由电子吸引金属正离子,长程力;b) 相互排斥——金属正离子之间的相互排斥,短程力。
平衡时这二个力相互抵消,原子受力为0,原子处于能量最低状态。
此时原子间的距离为r0。
§2-3 合金相结构基本概念♦合金——由两种或两种以上的金属或金属非金属元素通过化学键结合而组成的具有金属特性的材料。
♦组元、元——组成合金的元素。
♦相——具有相同的成分或连续变化、结构和性能的区域。
♦组织——合金发生转变(反应)的结果,可以包含若干个不同的相,一般只有一到二个相。
♦合金成分表示法:(1) 重量(质量)百分数A-B二元合金为例m B——元素B的重量(质量m A——元素A的重量(质量合金中的相分为:固溶体,化合物两大类。
固溶体金属晶体(溶剂)中溶入了其它元素(溶质)后,就称为固溶体。
一、固溶体的分类:♦按溶质原子在溶剂中的位置分为:置换固溶体,间隙固溶体♦按溶解度分为:有限固溶体,无限固溶体♦按溶质原子在溶剂中的分布规律分为:有序固溶体,无序固溶体置换固溶体:溶质原子置换了溶剂点阵中部分溶剂原子。





第2章晶体的结合思考题1.是否有与库仑力无关的晶体结合类型?[解答]共价结合中, 电子虽然不能脱离电负性大的原子, 但靠近的两个电负性大的原子可以各出一个电子, 形成电子共享的形式, 即这一对电子的主要活动范围处于两个原子之间, 通过库仑力, 把两个原子连接起来. 离子晶体中, 正离子与负离子的吸引力就是库仑力. 金属结合中, 原子实依靠原子实与电子云间的库仑力紧紧地吸引着. 分子结合中, 是电偶极矩把原本分离的原子结合成了晶体. 电偶极矩的作用力实际就是库仑力. 氢键结合中, 氢先与电负性大的原子形成共价结合后, 氢核与负电中心不在重合, 迫使它通过库仑力再与另一个电负性大的原子结合. 可见, 所有晶体结合类型都与库仑力有关.2.如何理解库仑力是原子结合的动力?[解答]晶体结合中, 原子间的排斥力是短程力, 在原子吸引靠近的过程中, 把原本分离的原子拉近的动力只能是长程力, 这个长程吸引力就是库仑力. 所以, 库仑力是原子结合的动力.3.晶体的结合能, 晶体的内能, 原子间的相互作用势能有何区别?[解答]自由粒子结合成晶体过程中释放出的能量, 或者把晶体拆散成一个个自由粒子所需要的能量, 称为晶体的结合能.原子的动能与原子间的相互作用势能之和为晶体的内能.在0K时, 原子还存在零点振动能. 但零点振动能与原子间的相互作用势能的绝对值相比小得多. 所以, 在0K时原子间的相互作用势能的绝对值近似等于晶体的结合能.4.原子间的排斥作用取决于什么原因?[解答]相邻的原子靠得很近, 以至于它们内层闭合壳层的电子云发生重叠时, 相邻的原子间便产生巨大排斥力. 也就是说, 原子间的排斥作用来自相邻原子内层闭合壳层电子云的重叠.5.原子间的排斥作用和吸引作用有何关系? 起主导的范围是什么?[解答]在原子由分散无规的中性原子结合成规则排列的晶体过程中, 吸引力起到了主要作用. 在吸引力的作用下, 原子间的距离缩小到一定程度, 原子间才出现排斥力. 当排斥力与吸引力相等时, 晶体达到稳定结合状态. 可见, 晶体要达到稳定结合状态, 吸引力与排斥力缺一不可. 设此时相邻原子间的距离为0r, 当相邻原子间的距离r>0r时, 吸引力起主导作用; 当相邻原子间的距离r<0r时, 排斥力起主导作用.6.共价结合为什么有“饱和性”和“方向性”?[解答]设N为一个原子的价电子数目, 对于IV A、V A、VI A、VII A族元素,价电子壳层一共有8个量子态, 最多能接纳(8- N)个电子, 形成(8- N)个共价键. 这就是共价结合的“饱和性”.共价键的形成只在特定的方向上, 这些方向是配对电子波函数的对称轴方向, 在这个方向上交迭的电子云密度最大. 这就是共价结合的 “方向性”.7. 共价结合, 两原子电子云交迭产生吸引, 而原子靠近时, 电子云交迭会产生巨大的排斥力, 如何解释?[解答]共价结合, 形成共价键的配对电子, 它们的自旋方向相反, 这两个电子的电子云交迭使得体系的能量降低, 结构稳定. 但当原子靠得很近时, 原子内部满壳层电子的电子云交迭, 量子态相同的电子产生巨大的排斥力, 使得系统的能量急剧增大. 8.试解释一个中性原子吸收一个电子一定要放出能量的现象.[解答]当一个中性原子吸收一个电子变成负离子, 这个电子能稳定的进入原子的壳层中, 这个电子与原子核的库仑吸引能的绝对值一定大于它与其它电子的排斥能. 但这个电子与原子核的库仑吸引能是一负值. 也就是说, 当中性原子吸收一个电子变成负离子后, 这个离子的能量要低于中性原子原子的能量. 因此, 一个中性原子吸收一个电子一定要放出能量. 9.如何理解电负性可用电离能加亲和能来表征?[解答]使原子失去一个电子所需要的能量称为原子的电离能, 电离能的大小可用来度量原子对价电子的束缚强弱. 一个中性原子获得一个电子成为负离子所释放出来的能量称为电子亲和能. 放出来的能量越多, 这个负离子的能量越低, 说明中性原子与这个电子的结合越稳定. 也就是说, 亲和能的大小也可用来度量原子对电子的束缚强弱. 原子的电负性大小是原子吸引电子的能力大小的度量. 用电离能加亲和能来表征原子的电负性是符合电负性的定义的.10.为什么许多金属为密积结构?[解答]金属结合中, 受到最小能量原理的约束, 要求原子实与共有电子电子云间的库仑能要尽可能的低(绝对值尽可能的大). 原子实越紧凑, 原子实与共有电子电子云靠得就越紧密, 库仑能就越低. 所以, 许多金属的结构为密积结构. 11.何为杂化轨道?[解答]为了解释金刚石中碳原子具有4个等同的共价键, 1931年泡林(Pauling)和斯莱特(Slater)提出了杂化轨道理论. 碳原子有4个价电子, 它们分别对应s 2ϕ、xp 2ϕ、yp 2ϕ、zp 2ϕ量子态, 在构成共价键时, 它们组成了4个新的量子态).(21),(21),(21),(2122221222212222122221z y x z y x z y x z y x p p p s p p p s p p p s p p p s ϕϕϕϕψϕϕϕϕψϕϕϕϕψϕϕϕϕψ+−−=−+−=−−+=+++=,4个电子分别占据1ψ、2ψ、3ψ、4ψ新轨道, 在四面体顶角方向(参见图1.18)形成4个共价键.12.你认为固体的弹性强弱主要由排斥作用决定呢, 还是吸引作用决定?[解答]如上图所示, 0r 附近的力曲线越陡, 当施加一定外力, 固体的形变就越小. 0r 附近力曲线的斜率决定了固体的弹性性质. 而0r 附近力曲线的斜率主要取决于排斥力. 因此, 固体的弹性强弱主要由排斥作用决定. 13.固体呈现宏观弹性的微观本质是什么?[解答]固体受到外力作用时发生形变, 外力撤消后形变消失的性质称为固体的弹性. 设无外力时相邻原子间的距离为0r , 当相邻原子间的距离r >0r 时, 吸引力起主导作用; 当相邻原子间的距离r <0r 时, 排斥力起主导作用. 当固体受挤压时, r <0r , 原子间的排斥力抗击着这一形变. 当固体受拉伸时, r >0r , 原子间的吸引力抗击着这一形变. 因此, 固体呈现宏观弹性的微观本质是原子间存在着相互作用力, 这种作用力既包含着吸引力, 又包含着排斥力.14.你是如何理解弹性的, 当施加一定力, 形变大的弹性强呢, 还是形变小的强?[解答]对于弹性形变, 相邻原子间的距离在0r 附近变化. 令r r r ∆+=0, 则有).1(),1()1()(0000000r rnr r r rmr r rr r r r n n m m m m m ∆∆∆∆−≈−≈+=+=−−−−−−−因为0/r r ∆是相对形变, 弹性力学称为应变, 并计作S , 所以原子间的作用力.)(000000S r Bn r Am r BnS r AmS r B r A r B r A f n m n m n m n m −=−++−=+−=再令c r Bnr Am nm =−00, cS f =.可见, 当施加一定力, 形变S 大的固体c 小, 形变S 小的固体c 大. 固体的弹性是固体的属性, 它与外力和形变无关. 弹性常数c 是固体的属性, 它的大小可作为固体弹性强弱的度量. 因此, 当施加一定力, 形变大的弹性弱, 形变小的强. 从这种意义上说, 金刚石的弹性最强.15.拉伸一长棒, 任一横截面上的应力是什么方向? 压缩时, 又是什么方向?[解答]如上图所示, 在长棒中取一横截面, 长棒被拉伸时, 从截面的右边看, 应力向右, 但从截面的左边看, 应力向左. 压缩时, 如下图所示, 应力方向与拉伸时正相反. 可见, 应16.固体中某一面积元两边的应力有何关系?[解答以上题为例, 在长棒中平行于横截面取一很薄的体积元, 拉伸时体积元两边受的应力如图所示.压缩时体积元两边受的应力如下图所示.当体积元无限薄, 体积元将变成面积元. 从以上两图可以看出, 面积元两边的应力大小相等方向相反.17.沿某立方晶体一晶轴取一细长棒做拉伸实验, 忽略宽度和厚度的形变, 由此能否测出弹性劲度常数11c ?[解答]立方晶体c b a , ,轴是等价的, 设长棒方向为x (a , 或b , 或c )轴方向, 做拉伸实验时若忽略宽度和厚度的形变, 则只有应力1T 应变1S 不为0, 其它应力应变分量都为0. 由(2.55)可得 1111S c T =. 设长棒的横截面积为A , 长度为L , 拉伸力为F , 伸长量为L ∆, 则有: L L S A F T / ,/11∆==. 于是, L A FL c ∆/11=.18.若把上题等价成弹簧的形变, 弹簧受的力kx F −=, k 与11c 有何关系?[解答]上题中长棒受的力L c L AF ∆11=,长棒的伸长量L ∆即是弹簧的伸长量x . 因此,.11c L A k =可见, 弹簧的弹性系数k 与弹性劲度常数的量纲是不同的.19.固体中的应力与理想流体中的压强有何关系?[解答]固体受挤压时, 固体中的正应力321 , ,T T T 与理想流体中的压强是等价的, 但654 , ,T T T 不同于理想流体中的压强概念. 因为压强的作用力与所考虑截面垂直, 而654 , ,T T T 与所考虑截面平行. 也就是说, 理想流体中不存在与所考虑截面平行的作用力.这是因为理想流体分子间的距离比固体原子间距大得多, 流层与流层分子间不存在切向作用力.20.固体中的弹性波与理想流体中的传播的波有何差异? 为什么?[解答]理想流体中只能传播纵波. 固体中不仅能传播纵波, 还能传播切变波. 这是因为理想流体分子间距离大, 分子间不存在切向作用力, 只存在纵向作用力;而固体原子间距离小, 原子间不仅存在纵向作用力, 还存在切向作用力.。


目录第二章晶体的结合题目(共90道题) (2)一、名词解释(共12道题) (2)二、简答题:(共33道题) (3)三、作图题(共2道题) (12)四、证明题(共8道题) (13)五、计算题(共35道题) (22)第二章晶体的结合题目(共90道题)一、名词解释(共12道题)1.晶体的结合能答:一块晶体处于稳定状态时,它的总能量(动能和势能)比组成此晶体的N个原子在自由状态时的总能量低,两者之差就是晶体的结合能。
2.电离能答:一个中性原子失去一个电子所需要的能量。
3.电子的亲和能答:指一中性原子获得一个电子成为负离子时所放出的能量。
4.电负性答:描述化合物分子中组成原子吸引电子倾向强弱的物理量。
5.离子键答:两个电负性相差很大的元素结合形成晶体时,电负性小的原子失去电子形成正离子,电负性大的得到电子形成负离子,这种靠正、负离子之间库仑吸引的结合成为离子键。
6.共价键答:量子力学表明,当两个原子各自给出的两个电子方向相反时,能使系统总能量下降,从而使两个原子结合在一起,由此形成的原子键合称为共价键(原子晶体靠此种键相互结合)。
7.范德瓦尔斯键答:分子晶体的粒子间偶极矩相互作用以及瞬时偶极矩相互诱生作用称为范德瓦耳斯力。
8.氢键答:氢原子处于两个电负性很强的原子(如氟、氧、氮、氯等)之间时,可同时受两个原子的吸引而与它们结合,这种结合作用称为氢键。
9.金属键答:在金属中,组成金属的原子的价电子已脱离母原子而成为自由电子,自由电子为整个晶体共有,而剩下的离子实就好像沉浸在自由电子的海洋中。
自由电子与离子实间的互相吸引作用具有负的势能,使势能降低形成稳定结构。
这种公有化的价电子(自由电子)与离子实间的互作用称为金属键。
10.葛生力答:葛生力是极性分子的永久偶极矩间的静电相互作用。
11.德拜力答:德拜力是非极性分子被极性分子电场极化而产生的诱导偶极矩间的相互作用。
12.伦敦力答:伦敦力:非极性分子的瞬时偶极矩间的相互作用。
固体材料是由大量的原子(或离子)组成约1 mol / cm 3原子(或离子)结合成晶体时,外层电子作重新分布,外层电子的不同分布产生了不同类型的结合力.Na Cl +=NaCl 离子键共价键金属键结合力类型决定了晶体的微观结构乃至宏观物理性质.本章主要介绍不同结合类型中原子间相互作用与晶体内能、晶体的微观结构和宏观物理性质之间的联系.共价键结合(金刚石)--原子间束缚非常强,导电性差金属键结合(金属Cu )--对电子束缚较弱,良导体——原子的电子分布核外电子的分布遵从泡利不相容原理、能量最低原理和洪特规则.能量最低原理电子在原子核外排布时,要尽可能使电子的能量最低1s、2s、2p、3s、3p、4s、3d、4p、4d……泡利不相容原理每一轨道中只能客纳自旋相反的两个电子.洪特规则电子在原子核外排布时,将尽可能分占不同的轨道,且自旋平行——原子的电子分布_----电离能_----电离能_----电离能_----电子亲和能_----原子电负性_----原子电负性2.Pauling鲍林提出的电负性计算方法(较通用):_----原子电负性•横向•电离能•亲和能•电负性按结合力的性质和特点,晶体可分为5种类型:离子晶体(离子结合)共价晶体(共价结合)金属晶体(金属结合)氢键晶体(氢键结合)如何理解各种晶体呢?离子晶体:正离子与负离子的吸引力就是库仑力.共价结合:靠近的两个电负性大的原子各出一个电子形成电子共享的形式.金属结合:原子实依靠原子实与电子云间的库仑力紧紧地吸引着.氢键结合:氢先与电负性大的原子形成共价结合后, 氢核与负电中心不在重合, 迫使它通过库仑力再与另一个电负性大的原子结合.分子结合:电偶极矩把原本分离的原子结合成了晶体. 电偶极矩的作用力实际就是库仑力.可见, 所有晶体结合类型都与库仑力有关.原子间相互作用势能----结合力的共性吸引力排斥力库仑引力库仑斥力泡利原理引起(1)吸引力和排斥力都是原子间距离r 的函数.注:(2)吸引力是长程力,排斥力短程力.(3)当r =r 0时, 原子间合力为零, 原子处于平衡.类比于弹簧振子()()⎟⎠⎞⎜⎝⎛−−=−=++11n m r nB r mA dr r du r f 为什么排斥力是短程力?()()()B A r u r u r u +−=+=()()⎜⎛−−=−=nB mA r du r f设晶体中第i个原子与第j个原子之间的相互作用势能u(r)为ij()()∑∑∑==NNNr u r u U 1晶体的结合能:()()∑=N r u Nr u晶格常数由于晶格具有周期性,设临近两原子间距R,则晶体体积可写成体弹性模量单位压强引起的体积的相对变化率。
第二章 晶体的结合组成晶体的原子能够保持中性稳定的周期性排列,说明原子之间有着强烈的相互作用力。
晶体粒子之间的相互作用力包括两种类型:吸引力和排斥力。
当原子受到压缩时,这种作用表现为斥力;当晶体受到拉伸时,这种作用表现为引力。
当斥力和引力平衡时,晶体保持一定的体积和外形。
因此,晶体结构取决于组成晶体的原子的性质及相互作用。
从能量的观点来看,一块晶体处于稳定状态时,它的总能量0E (原子的动能和相互作用势能的总和)比组成这晶体的原子处于自由状态时的总能量N E 低。
两者之差被定义为晶体的结合能W :即0N W E E =-。
结合能就是把晶体分离成自由原子所需要的能量。
对于晶体中原子相互作用的研究,实际上是量子力学的多粒子问题。
由于问题的复杂性,只能采取多种近似的方法进行处理。
本章首先介绍晶体结合类型的物理本质,然后利用经典理论重点讨论离子晶体和分子晶体的结合能。
§2-1晶体的结合类型与原子电负性对原子结合成晶体起主要作用的是各原子的最外层的电子。
按原子间相互作用的性质,可把晶体分为离子晶体、共价晶体、金属晶体、分子晶体和氢键晶体等等。
2.1.1晶体的结合类型 1.离子晶体离子晶体是由正、负离子所组成,依赖离子之间的静电相互作用结合成晶体。
最典型的离子晶体是碱金属元素和卤族元素之间形成的化合物,它们的晶体结构也比较简单,分别属于NaCl 或CsCl 两种典型结构。
在NaCl 晶体中,Na +和Cl -离子相间排列,每一种离子都是以异性离子为最近邻,总的库仑作用的效果是吸引的。
同时,由于Na +和Cl -离子都具有满电子壳层结构,当两个离子相互接近电子云发生重叠时,除静电相互作用外,由于泡利不相容原理,它们之间将产生很强的排斥作用,晶体正是依靠库仑吸引和排斥相平衡结合成稳定的结构。
由于离子具有满壳层电子结构,其电荷分布近似于球对称,所以离子键是没有方向性的,是晶格配位数较高的结构。
这种离子键是相当强的,其结合能的数量级约为800kJ/mol ,离子间的吸引能的数量级约为几eV ,因此一般离子晶体的熔点较高,硬度较大。