第十届Chemy化学奥林匹克竞赛联赛
- 格式:pdf
- 大小:552.75 KB
- 文档页数:6

Advances in Education教育进展, 2023, 13(10), 8119-8134Published Online October 2023 in Hans. https:///journal/aehttps:///10.12677/ae.2023.13101259中国化学奥林匹克竞赛中关于亲核取代反应的试题分析张琴1,2,杨大成11西南大学化学化工学院,重庆2重庆市璧山中学校,重庆收稿日期:2023年9月23日;录用日期:2023年10月23日;发布日期:2023年10月30日摘要中国化学奥林匹克竞赛(以下简称化学竞赛)是中国化学会为普通高中生举办的竞赛活动,化学竞赛促进了中国化学教育。
本研究采用统计法、分类归纳法对近年化学竞赛中关于亲核取代的试题进行整理,发现:亲核取代知识虽有单独出题,但多数融入其他考题之中;题目的情境不仅来源于大学教材,也取材于期刊论文中的科技前沿知识。
亲核取代反应几乎是每年的必考内容,考查比例逐年增高,考查难度逐年增大。
笔者建议教师在日常教学中不仅要要求学生掌握坚实的知识基础,规范书写,还要鼓励广泛阅读期刊杂志。
关键词中国化学奥林匹克竞赛,有机化学,亲核取代反应,试题分析Analysis and Research on “NucleophilicSubstitution Reaction” Test Questions inChinese Chemistry Olympiad ExaminationQin Zhang1,2, Dacheng Yang11School of Chemistry and Chemical Engineering, Southwest University, Chongqing2Chongqing Bishan Middle School, ChongqingReceived: Sep. 23rd, 2023; accepted: Oct. 23rd, 2023; published: Oct. 30th, 2023AbstractThe Chinese Chemistry Olympiad (hereinafter referred to as the chemistry competition) is a com-petition organized by Chinese Chemical Society for ordinary high school students. The Chemistry张琴,杨大成Olympiad has promoted chemistry education in China. Statistics and classified induction were used to sort out the examination questions about nucleophilic substitution reaction. It was found that most of the nucleophilic substitution knowledge was integrated into other examination ques-tions, and there were also separate questions. The knowledge background of the examination ques-tions is not only derived from university textbooks, but also from scientific and technological fron-tier knowledge in journal articles. The nucleophilic substitution reaction was almost an annual compulsory examination. The proportion of examination questions increased and the difficulty of examination enhanced year by year. It is suggested that competition teachers should not only re-quire students to master solid basic knowledge and standardize their writing, but also encourage them to read periodicals widely.KeywordsChinese Chemistry Olympiad, Organic Chemistry, Nucleophilic Substitution Reaction, QuestionAnalysisCopyright © 2023 by author(s) and Hans Publishers Inc.This work is licensed under the Creative Commons Attribution International License (CC BY 4.0)./licenses/by/4.0/1. 引言中国化学奥林匹克竞赛(以下简称“化学竞赛”)是中国化学会为普通高中生举行的竞赛活动,起始于1984年,并于1987年选拔出优秀学生参与国际奥林匹克竞赛,是中国高中学生的一场盛大的化学“全运会”。

第一届Chemy化学奥林匹克竞赛联赛答案(2016年8月28日9:00 ~ 12:00)·竞赛时间3小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
·试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
·姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
·允许使用非编程计算器以及直尺等文具。
第1题(8分)1-1 将明矾置于河水中搅拌,生成载带着悬浮物的氢氧化铝,然后沉降,使水澄清。
但若用蒸馏水代替河水,便不会发生以上现象,请解释该过程的原因,并写出生成氢氧化铝的方程1-2 在氯化汞溶液中逐滴加入碘化钾溶液,生成橘红色沉淀,继续滴加,发现沉淀溶解,写1-3 在含有四氨合铜离子的溶液中加入硫酸,溶液的颜色由绛蓝色变为蓝色,写出总反应方第2题(8分)有一个经验规则可以用于估算基元反应的活化能:BE是反应中断掉的键的键能之和。
①反应中没有键的断裂的反应;②自由基与分子的放热反应;③反应中键不完全断裂(如协同反应)的反应。
④反应中键完全断裂的反应。
根据上述经验规则,估算氢气与氯气反应中各步基元反应的活化能,并与实验值比较。
Cl2 = 2Cl·E a1 = 242.8 kJ·mol-1Cl· + H2 = HCl + H·E a2= 25.1 kJ·mol-1H· + Cl2 = HCl + Cl·E a3= 12.6 kJ·mol-1-1;BE(H-H) = 436 kJ·mol-1;BE(H-Cl) = 431 kJ·mol-1第3题(8分)3-1 Cr2,Mo2与W2分子中存在着六重键,金属的ns轨道与(n-1)d轨道参与成键。

第五届Chemy化学奥林匹克竞赛联赛试题答案第五届Chemy化学奥林匹克竞赛联赛试题答案(2021年8月27日 9:00 ~ 12:00)题号满分得分评卷人 1 13 2 11 3 13 4 10 5 11 6 8 7 9 8 14 9 11 总分 100 ・竞赛时间3小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
・试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
・姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
・允许使用非编程计算器以及直尺等文具。
H He 相对原子质量 1.008 4.003 Li Be B C N O F Ne 6.941 9.012 10.81 12.01 14.01 16.00 19.00 20.18 Na Mg Al Si P S ClAr 22.99 24.31 26.98 28.09 30.97 32.07 35.45 39.95 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 39.10 40.08 44.96 47.88 50.94 52.00 54.94 55.85 58.93 58.69 63.55 65.41 69.72 72.61 74.92 78.96 79.90 83.80 Rb Sr Y Zr Nb Mo Tc RuRh Pd Ag Cd In Sn Sb Te I Xe 85.47 87.62 88.91 91.22 92.91 95.94 [98] 101.1 102.9 106.4 107.9 112.4 114.8 118.7 121.8 127.6 126.9 131.3 Cs Ba La-Hf Ta WRe Os Ir Pt Au Hg Tl Pb Bi Po At Rn 132.9 137.3 Lu 178.5 180.9 183.8 186.2190.2 192.2 195.1 197.0 200.6 204.4 207.2 209.0 [210] [210] [222] Fr Ra Ac-Rf Db Sg Bh Hs Mt Ds Rg Cn Uut Uuq Uup Uuh Uus Uuo [223] [226] La LaCe Th Pr Pa Nd U Pm Np Sm Pu Eu Am Gd Cm Tb Bk Dy Cf Ho Es Er Fm Tm Md YbNo Lu Lr Ac第1题(13分)1-1 氢化锂铝是有机反应常用的还原剂,过量的氢化锂铝常使用叔丁醇淬灭,写出淬灭过程的反应方程式。
第十届Chemy化学奥林匹克竞赛联赛答案(2018年10月3日18:00 ~ 22:00)·竞赛时间4小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
·试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
·姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
·允许使用非编程计算器以及直尺等文具。
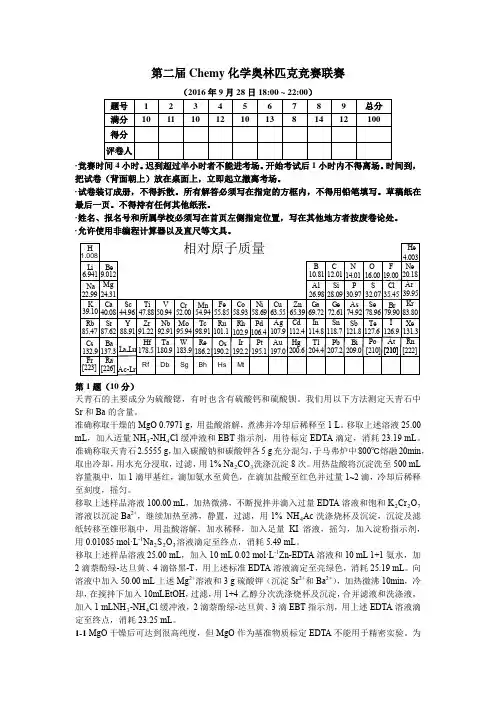
第1题(13分)多齿配体HTPPNOL(如右图所示)与铜形成的配合物可以用于模拟双核含铜酶的活性中心。
在形成的所有配合物中,只由Cu2+与来自TPPNOL-的原子构成的环均为五元环。
1-1 在乙酸钠溶液中HTPPNOL与Cu2+反应生成双核配合物[Cu2(TPPNOL)(CH3COO)]2+。
这个配离子中,Cu2+有两种配位数,其中一个为五配位(三角双锥构型),配合物结构中包含一个六元环。
(3分)1-1-2 将该配离子的盐溶于水,则溶液中仅存在两个Cu配位数一致的双核配合物,且其中两种主要配离子物种的浓度关系随pH关系如下图所示。
画出A和B的结构并指出pK a(A)。
已知C中没有六元环。
画出该配离子的结构。
2位构型相同,且仍保留了Cu2+-HTPPNOL配合物骨架的结构特点。
D中存在三个氧原子的化学环境与配位数均各不相同的碳酸根配体,不存在O-H键,且配离子整体存在对称中心。
(2分)1-4测量配合物的结构最重要的是获得其晶体结构数据,这往往需要选取合适的溶液体系,减小配离子在溶液中的溶解度并得到质量较好的晶体。
若需要测量D的晶体结构,试根据上述信息提出一条策略并作出简要解释。
第2题(10分)为纪念门捷列夫发现元素周期律150周年,国际纯粹和应用化学联合会将2019年设为“国际化学元素周期表年”。
门捷列夫预言了多种当时未知的元素,M即为其中之一。

中国奥林匹克化学赛决赛中国奥林匹克化学赛(Chinese National Chemistry Olympiad,简称CNChO)是中国最高水平的化学竞赛之一。
该赛事旨在选拔并培养具有较高化学素养和创新能力的中学生,以提高他们的科学素养和培养其对化学科学的热爱。
中国奥林匹克化学赛决赛是整个比赛过程中的最重要环节,本文将对本次决赛进行详细介绍。
1. 决赛概述中国奥林匹克化学赛决赛是在全国范围内选拔出的优秀参赛选手参加的一场竞赛。
该决赛旨在通过复杂、富有挑战性的化学题目考察学生的知识水平、实验技能和解题能力。
决赛通常在两到三天内进行,参赛选手在规定的时间内完成笔试和实验环节。
2. 决赛内容中国奥林匹克化学赛决赛包含两个主要环节:笔试和实验。
2.1 笔试决赛的笔试环节是对学生化学知识掌握程度的综合考核。
该环节的试题通常包括选择题、填空题、简答题和计算题。
这些试题涵盖了化学的各个领域,包括有机化学、无机化学、物理化学等。
选手需要在规定时间内完成试题,并提供详细的解答过程。
2.2 实验决赛的实验环节是对学生实验操作技能和解题能力的考察。
在实验环节中,参赛选手需要根据规定的实验操作步骤进行实验,并记录实验数据。
实验内容通常包括化学合成、反应机理解析、物质鉴定等。
选手需要准确、独立地完成实验,并提供实验结果和分析。
3. 参赛要求3.1 选拔赛参与中国奥林匹克化学赛决赛需要首先通过区域选拔赛的选拔。
全国各省市在不同时间进行选拔赛,选拔赛的试题通常较为简单,主要考察学生的化学基础知识。
3.2 决赛资格选拔赛中表现优秀的学生将获得参加中国奥林匹克化学赛决赛的资格。
具体资格标准会根据各个省市的考试情况而有所不同。
3.3 参赛要求参赛选手需要具备较扎实的化学理论知识和实验操作技能,具备较高的解题能力和创新思维。
选手需要遵守比赛规则,积极参与相关培训和训练。
4. 奖励与评选中国奥林匹克化学赛决赛中,优胜选手将有机会获得各种奖励与荣誉,包括但不限于以下几种:•冠军:获得中国奥林匹克化学赛的冠军将获得奖杯、证书和丰厚的奖金。

2024 化学奥林匹克竞赛试题一、试题有一化学反应 A + B → C,在一定温度下,当A 的浓度为0.5mol/L,B 的浓度为1mol/L 时,反应速率为0.2mol/(L·s)。
若将 A 的浓度增大到1mol/L,B 的浓度不变,此时反应速率变为多少?解析根据反应速率方程v = k[A]^m[B]^n,设该反应中 A 的反应级数为m,B 的反应级数为n。
1. 首先求反应级数:-当 A 的浓度为0.5mol/L,B 的浓度为1mol/L 时,反应速率v1 = 0.2mol/(L·s),可得方程①:0.2 = k×0.5^m×1^n。
-当A 的浓度增大到1mol/L,B 的浓度不变时,设此时反应速率为v2,可得方程①:v2 = k×1^m×1^n。
-用方程①除以方程①可得:v2/0.2 = (k×1^m×1^n)/(k×0.5^m×1^n),化简得v2/0.2 = 2^m。
-由于只改变了A 的浓度,B 的浓度不变,且反应速率变为原来的倍数只与A 的浓度变化有关,所以可以通过设特殊值来确定m 的值。
-假设m = 1,则v2/0.2 = 2,解得v2 = 0.4mol/(L·s)。
-假设m = 2,则v2/0.2 = 4,解得v2 = 0.8mol/(L·s)。
-假设m = 3,则v2/0.2 = 8,解得v2 = 1.6mol/(L·s)等,依次类推,可通过给出的选项来确定m 的值,进而确定反应速率v2。
二、试题已知在25①时,水的离子积常数Kw = 1×10^(-14)。
在该温度下,某溶液的pH = 3,求该溶液中氢氧根离子的浓度。
解析1. 因为pH = -lg[H①],已知pH = 3,则[H①]=1×10^(-3)mol/L。
2. 又因为在任何水溶液中,Kw = [H①][OH①]。

2023中国化学奥林匹克竞赛获奖名单2023年中国化学奥林匹克竞赛是一场备受关注的盛会,来自全国各地的优秀学生们齐聚一堂,展示自己的才华和知识。
经过激烈的角逐,最终有一批优秀的学生获得了奖项,下面是2023年中国化学奥林匹克竞赛的获奖名单。
金奖获得者:1.李明:来自北京市的李明在竞赛中展现出了卓越的化学知识和解题能力,他的答卷得到了评委的高度认可,因此获得了金奖。
2.王小红:来自上海市的王小红在竞赛中展现出了出色的化学实验技巧和分析能力,她的实验报告令评委刮目相看,因此获得了金奖。
3.张明阳:来自广州市的张明阳在竞赛中表现出了卓越的逻辑思维和问题解决能力,他的答卷让评委眼前一亮,因此获得了金奖。
银奖获得者:1.李晓琳:来自成都市的李晓琳在竞赛中展现出了扎实的化学基础和分析能力,她的理论推导令评委赞叹不已,因此获得了银奖。
2.王小明:来自深圳市的王小明在竞赛中展现出了丰富的化学知识和实验技能,他的实验操作规范得到了评委的肯定,因此获得了银奖。
3.张亚飞:来自武汉市的张亚飞在竞赛中展现出了灵活的思维和创新意识,他的解题方法让评委刮目相看,因此获得了银奖。
铜奖获得者:1.王小芳:来自天津市的王小芳在竞赛中展现出了良好的化学基础和实验技巧,她的实验报告得到了评委的认可,因此获得了铜奖。
2.李阳:来自重庆市的李阳在竞赛中表现出了良好的逻辑思维和问题解决能力,他的答卷让评委眼前一亮,因此获得了铜奖。
3.张小云:来自南京市的张小云在竞赛中展现出了积极的学习态度和实验精神,她的实验操作规范得到了评委的赞赏,因此获得了铜奖。
以上是2023年中国化学奥林匹克竞赛的部分获奖名单,这些学生都展现出了在化学领域的卓越才华和潜力,他们的成绩和努力将为中国的科学事业做出重要贡献。
希望这些获奖学生能够继续努力学习,为将来的科学研究和发展做出更大的贡献。

中国化学奥林匹克竞赛历届获奖名单中国化学奥林匹克竞赛历届获奖名单序中国化学奥林匹克竞赛(China Chemistry Olympiad,简称CCO)作为国内高中学生最高水平的化学竞赛活动,旨在通过选拔优秀的化学学生,培养和推广化学知识、实验技能以及创新思维。
自1998年首届竞赛举办以来,CCO已经在国内外享有极高的声誉,并每年吸引着来自全国各地的优秀学子参与。
一、CCO的起源和发展CCO起源于1998年,是中国化学会、中国科学院研究生院等单位共同主办的化学竞赛。
早期,CCO主要参考国际化学奥林匹克竞赛(International Chemistry Olympiad,简称ICO)的题型和难度,并且设置了国内初赛和复赛等环节。
经过多年的发展,CCO逐渐形成了自己独特的赛事风格,更加注重培养学生的实际能力和创新思维。
二、CCO获奖名单回顾1. 第1届中国化学奥林匹克竞赛(1998年)在第1届CCO中,共有1000余名学生参赛,经过激烈角逐,最终产生了一等奖10名、二等奖20名、三等奖30名的获奖选手。
他们在竞赛中展现出了扎实的化学基础和卓越的解题能力,为CCO未来的发展奠定了基础。
2. 第10届中国化学奥林匹克竞赛(2007年)在第10届CCO中,参赛人数已经超过了4000人。
此次竞赛中,通过初赛、复赛和集训等环节,最终有10位选手获得一等奖,20位选手获得二等奖,30位选手获得三等奖。
2012年和2013年,正在读大学的这10位一等奖选手分别组队参加了国际化学奥林匹克竞赛,为中国赢得了多个金牌和荣誉。
3. 第20届中国化学奥林匹克竞赛(2017年)随着CCO的不断发展,竞赛规模也逐渐扩大。
在第20届CCO中,参赛选手超过了2万人,其中经过层层选拔,最终有10名选手获得一等奖,20名选手获得二等奖,30名选手获得三等奖。
此次竞赛不仅彰显了中国化学竞赛的影响力和水平,也为中国培养了一大批优秀的化学学子。

第三届C h e m y化学奥林匹克竞赛联赛试题(2017年1月7日9:00~12:00)·竞赛时间3小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
·试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
·姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
·允许使用非编程计算器以及直尺等文具。
第1题(10分)将(NH4)2NiF4在氨气流中加热至360-410°C得到一种黑灰色的粉末A。
经鉴定:A中仅含X和Y两种元素,是一种六方晶体,X原子做六方最密堆积,Y原子有序地填入部分的八面体空隙中,结构类同于ε-Fe3N;A的主要化学性质如下:(1)在氢气中温度155°C或在氮气中450°C分解;(2)不与氢氧化钠溶液反应;(3)与盐酸反应放出气体。
1-1写出A的化学式。
1-2写出A与盐酸反应的方程式。
1-3指出X原子的配位数,指出Y原子填充八面体空隙的填隙率。
1-4晶体A的a=462.2pm,c=430.6pm,Z=2,计算此晶体的密度。
1-5将晶体A中的X换为钠,此时形成的晶体B为立方晶体,但Y原子的配位数不变。
试画出此晶体B的一个正当晶胞。
第2题(8分)原子单位制中的能量单位能量是Hartree/particle(以Hartree-Fock方法的提出者之一D.Hartree命名,简写为Ha),1Ha就是一个基态氢原子势能的绝对值,也是一个基态氢原子能量绝对值的2倍。
2-1氢原子能量的表达式为E n=-m e e4/(8n2ε02h2),其中ε0=8.8542×10-12F/m,通过计算完成下列单位换算式:1Ha=_____eV=_____J=_____kJ·mol-1=_____kcal·mol-12-2以Ha为单位表示:(1)氢原子的电离能I1;(2)基态氢原子电子的动能E k。

Chemy化学竞赛联赛试题合集第一辑(第一届~第八届)参考答案Chemy化学竞赛团队两周年献礼2018年5月本版试题合集仅用于非商业用途交流使用,婉拒商业机构等盈利组织未经授权的转载行为。
版权归全体试题作者共有,侵权必究。
第一届Chemy化学奥林匹克竞赛联赛答案(2016年7月24日19:00 ~ 21:00)·竞赛时间3小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
·试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
·姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
·允许使用非编程计算器以及直尺等文具。
第1题(8分)1-1 将明矾置于河水中搅拌,生成载带着悬浮物的氢氧化铝,然后沉降,使水澄清。
但若用蒸馏水代替河水,便不会发生以上现象,请解释该过程的原因,并写出生成氢氧化铝的方程式。
程式。
出化学反应方程式。
第2题(8分)有一个经验规则可以用于估算基元反应的活化能。
①反应中没有键的断裂的反应;②自由基与分子的放热反应;③反应中键不完全断裂(如协同反应)的反应。
④反应中键完全断裂的反应。
遵循上述情况时,分别通过对应下表中计算方法计算活化能:BE是反应中断掉的键的键能之和。
根据上述经验规则及所提供的键能信息,估算氢气与氯气反应中各步基元反应的活化能,并与所给出的实验值比较。
Cl2 = 2Cl·E a1 = 242.8 kJ·mol-1Cl· + H2 = HCl + H·E a2= 25.1 kJ·mol-1H· + Cl2 = HCl + Cl·E a3= 12.6 kJ·mol-1-1-1-1第3题(8分)3-1 Cr2,Mo2与W2分子中存在着六重键,金属的ns轨道与(n-1)d轨道参与成键。
第六届Chemy化学奥林匹克竞赛联赛试题答案第六届Chemy化学奥林匹克竞赛联赛试题答案·竞赛时间3⼩时。
迟到超过半⼩时者不能进考场。
开始考试后1⼩时内不得离场。
时间到,把试卷(背⾯朝上)放在桌⾯上,⽴即起⽴撤离考场。
·试卷装订成册,不得拆散。
所有解答必须写在指定的⽅框内,不得⽤铅笔填写。
草稿纸在最后⼀页。
不得持有任何其他纸张。
·姓名、报名号和所属学校必须写在⾸页左侧指定位置,写在其他地⽅者按废卷论处。
第1题(8分)⾃从上世纪Re2Cl82-的结构确定后,含有类似结构的配离⼦引起了⼈们的兴趣。
现有⼀种羰基配合物X,已知X中含氧36.4%,且中⼼元素Z存在于某种固氮酶中。
将X在冰⼄酸中回流,待反应完全后得到了化合物A,A的理论摩尔电导率为0,所得A的物质的量是参与反应的X的物质的量的⼀半。
A在浓盐酸中与氯化钾反应得到含⾦属元素55.1%的化合物B,经实验测得B 与A中含有相同的化学键且⽣成B的物质的量与反应的A的物质的量相等。
第2题(11分)2-1硫化汞不溶于浓盐酸(12.0 mol·L-1),可溶于浓硝酸(16.0 mol·L-1),易溶于王⽔(浓硝酸与浓盐酸以体积⽐1:3配制⽽成),写出溶解反应的化学⽅程式并通过计算说明硫化汞在平衡时[Cl-] = 1.5 mol·L-1,计算混合物中硝酸和盐酸的浓度。
已知:HgS的溶度积K sp = 1.6 × 10-52,H2S的电离常数p K a1,2 = 7.05, 12.92。
φ (NO3-,H+/NO) = 0.957 V,φ (S/H2S) = 0.142 V。
HgCl42-的稳定常数lgβ4 = 15.08。
第3题(15分)第六周期元素X在同族元素中拥有最⼤的电负性,且存在负氧化态的化合物。
X的单质为化学性质稳定的⾦属,不溶于硫酸、盐酸,但溶于盐酸与硝酸按⼀定⽐例混合的溶液,形成带有⼀个负电荷的配合物离⼦XA n-,其中X原⼦为4配位。
历届化学奥赛名次历届化学奥赛名次是指国际高中生化学奥林匹克竞赛的历届获奖名次。
自1968年该比赛首次举行以来,越来越多的国家和地区参与其中,每年都有来自世界各地的优秀学生参加。
以下是历届化学奥赛的部分获奖名次:1968年(首届):美国第一,英国第二,捷克斯洛伐克第三1970年:美国第一,加拿大第二,英国第三1972年:美国第一,瑞典第二,英国第三1974年:美国第一,瑞典第二,英国第三1976年:美国第一,苏联第二,瑞典第三1978年:美国第一,捷克斯洛伐克第二,波兰第三1980年:美国第一,苏联第二,瑞士第三1982年:美国第一,捷克斯洛伐克第二,苏联第三1984年:美国第一,中国香港第二,捷克斯洛伐克第三1986年:美国第一,苏联第二,捷克斯洛伐克第三1988年:美国第一,苏联第二,捷克斯洛伐克第三1990年:美国第一,中国香港第二,捷克斯洛伐克第三1992年:美国第一,中国香港第二,捷克斯洛伐克第三1994年:美国第一,中国香港第二,中国大陆第三1996年:美国第一,中国大陆第二,日本第三1998年:美国第一,中国香港第二,中国大陆第三2000年:美国第一,中国大陆第二,中国香港第三2002年:美国第一,中国香港第二,中国大陆第三2004年:美国第一,中国大陆第二,俄罗斯第三2006年:美国第一,韩国第二,中国大陆第三2008年:美国第一,中国大陆第二,日本第三2010年:美国第一,中国大陆第二,中国香港第三2012年:美国第一,中国大陆第二,俄罗斯第三2014年:美国第一,中国大陆第二,新加坡第三2016年:美国第一,中国大陆第二,俄罗斯第三2018年:美国第一,中国大陆第二,俄罗斯第三2020年因新冠疫情暂停。
以上是历届化学奥赛的部分获奖名次,其中美国的表现一直稳定居于第一位,中国大陆在近年来也一直表现优异,获得多次第二名的好成绩。
国际化学奥林匹克竞赛历届成绩
国际化学奥林匹克竞赛是一项旨在选拔和表彰国际间优秀化学学生的赛事。
以下是历届竞赛中的成绩:
第1届国际化学奥林匹克竞赛于1968年举行,地点为捷克斯洛伐克的布拉迪斯拉发。
当时有18个国家参与,来自罗马尼亚、匈牙利和苏联的选手获得了前三名。
从第2届开始,该竞赛每年举办。
历届竞赛中,苏联、德国、美国、瑞士等国常常获得优异成绩,并且多次荣获前三名。
在2000年以后的竞赛中,中国化学学生的成绩有显著提高。
中国队在多个年份中荣获前三名,并且在部分年份中取得了冠军。
自2006年开始,国际化学奥林匹克竞赛分为两个阶段:理论考试和实验考试。
这一改革增强了竞赛的科学性和实践性,也为学生提供了更全面的考核方式。
过去的几年中,韩国、日本、俄罗斯等国家的学生表现出色,并且在竞赛中取得了多个奖项。
总体来说,国际化学奥林匹克竞赛是一个展示化学学生才华和创造力的重要平台,为全世界的化学领域培养了许多杰出的人才。
第十届全国大学生化工设计竞赛(丙烷脱氢制丙烯)一、概述戊烯是一种重要的有机化工原料,其用量仅次于乙烯,除用于生产聚戊烯外,还是生产戊烯腈,丁醇、辛醇、环氧戊烷、异戊醇、戊苯、戊烯酸、羰基醇及壬基酚等产品的主要原料。
随着聚戊烯等衍生物需求的迅猛增长,对戊烯的需求量也逐年递增。
预计2050年世界戊烯的需求量约为8600万吨,其增长率将超过乙烯一倍。
预计2050年世界戊烯的产量约为7730万吨,其中59%来自蒸汽裂解装置生产乙烯的副产品,33%来自炼油厂催化裂化装置生产汽柴油的副产品,3%由戊烷脱氢产生,5%由其他方法得到。
产量与戊烯需求量相比,存在着约870万吨的产量缺口。
蒸汽裂解装置的主要产品是乙烯,戊烯是副产品。
不同原料得到的产品分布差别很大,以石脑油为原料生产乙烯,每生产5吨乙烯,副产0.5-0.6吨戊烯;以乙烷为原料,生产5吨乙烯,仅副产0.05~0.06吨戊烯。
但今后的发展趋势是,石脑油的用量将从目前占裂解原料的50%以上降低到50%以下,乙烷用量将由目前的近30%上升到30%以上,这意味着从蒸汽裂解装置得到戊烯的产量将减少,戊烯的短缺量将进一步扩大。
因此,由其他来源生产戊烯就变得日益重要,这些来源主要包括采用戊烷脱氢,催化裂化装置升级,烯烃裂解和烯烃易位技术等。
戊烷催化脱氢制戊烯比烃类蒸气裂解能产生更多的戊烯,当用蒸气裂解生产戊烯时,戊烯收率最多只有33%,而用催化脱氢法生产戊烯,总收率可达75%~86%,用唯一原料生产唯一产品,催化脱氢的设备投资比烃类蒸气裂解低33%,并且采用催化脱氢的方法,能有效地利用液化石油气资源使之转变为有用的烯烃。
二、戊烯增产技术进展进入新世纪以来,世界石化原料和石化产品需求仍将持续增长,据2002年召开的第57届世界石油大会预测,5998~2050年间,乙烯需求将由8000万吨增加到52000万吨,戊烯将由5500万吨增加到8200万吨,丁烯-5将由80万吨增加到550万吨,α-烯烃将由500万吨增加到220万吨,苯将由2700万吨增加到5000万吨,对二甲苯将由5500万吨增加到3000万吨。
第九届Chemy化学奥林匹克竞赛联赛答案·竞赛时间3小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
·试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
·姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
第1题(12分)写出下列反应的方程式:溶液后,用硫酸酸化。
1-6Sn(II)水解产生一种具有特殊结构的水合氧化物。
该氧化物晶体中存在具有高对称性的第2题(10分)2-1已知K sp(AgCN) = 1.2 × 10-16,K稳(Ag(CN)2-) = 1.3 × 1023。
现有2.0 L 0.10 mol·L-1的AgNO3溶液,向其中加入NaCN固体,忽略CN-水解,计算:(1)当AgCN沉淀一半时,除氢离子、2-2现有一电池Ag(s)|Ag(CN)2(0.01 mol·L),CN(0.1 mol·L)||Ag(1 mol·L)|Ag(s)。
判断电池的正负极,计算该原电池的电动势。
第3题(11分)向CoCl2和NH4Cl的混合溶液中加入少量活性炭,混以浓氨水并滴加过氧化氢,然后加热溶液,待充分反应后,加入浓盐酸并冷却,析出一种橙黄色晶体X。
实验证实,X是钴(III)的六配位单核配合物。
将0.1000 g X溶于水,加入适量10% NaOH溶液并充分加热,然后加入0.5 g KI并酸化,用0.01525 mol·L-1 Na2S2O3溶液滴定,消耗24.52 mL。
3-4在不同气氛下X的分解情况有所不同。
将X在1 atm的氮气中加热至370°C,得到的差热曲线有两个吸热峰,分别位于280°C和341°C附近;而在3 atm的氨气中加热至370°C却只得到一个位于300°C附近的吸收峰。
第十届Chemy化学奥林匹克竞赛联赛(2018年10月3日18:00 ~ 22:00)·竞赛时间3小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
·试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
·姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
·允许使用非编程计算器以及直尺等文具。
第1题(13分)多齿配体HTPPNOL(如右图所示)与铜形成的配合物可以用于模拟双核含铜酶的活性中心。
在形成的所有配合物中,只由Cu2+与来自TPPNOL-的原子构成的环均为五元环。
1-1 在乙酸钠溶液中HTPPNOL与Cu2+反应生成双核配合物[Cu2(TPPNOL)(CH3COO)]2+。
这个配离子中,Cu2+有两种配位数,其中一个为五配位(三角双锥构型),配合物结构中包含一个六元环。
1-1-1画出该配合物的结构。
1-1-2 将该配离子的盐溶于水,则溶液中仅存在两个Cu2+配位数一致的双核配合物,且其中两种主要配离子物种的浓度关系随pH关系如下图所示。
画出A和B的结构并指出pK a(A)。
1-2 在无其他配体的碱性溶液中Cu2+-HTPPNOL体系里存在与B结构类似的双核配离子C,已知C中没有六元环。
画出该配离子的结构。
1-3 向C的溶液中通入CO2,则得到二价四核配离子D,该配合物中所有Cu2+配位数和配位构型相同,且仍保留了Cu2+-HTPPNOL配合物骨架的结构特点。
D中存在三个氧原子的化学环境与配位数均各不相同的碳酸根配体,不存在O-H键,且配离子整体存在对称中心。
1-3-1画出D的结构。
1-3-2写出由C反应生成D的化学方程式。
1-4测量配合物的结构最重要的是获得其晶体结构数据,这往往需要选取合适的溶液体系,减小配离子在溶液中的溶解度并得到质量较好的晶体。
若需要测量D的晶体结构,试根据上述信息提出一条策略并作出简要解释。
第2题(10分)为纪念门捷列夫发现元素周期律150周年,国际纯粹和应用化学联合会将2019年设为“国际化学元素周期表年”。
门捷列夫预言了多种当时未知的元素,M即为其中之一。
M是一种银白色金属,质软,能溶于浓硫酸、硝酸、盐酸和稀碱溶液。
M与氧气加热到250°C 反应,可得到淡黄色固体A,A经SOCl2处理可得到亮黄色固体B,B也可由M与黄绿色气体C直接加热反应得到;若将B与单质气体D加热至200°C反应,则转化为红色固体E;将M直接溶于稀盐酸,也可得到E的溶液;但若将镀有M的镁片溶于稀盐酸,可以制得少量二元化合物F;F在常温下为液体,不稳定,其水溶液显酸性;F能与金属钾反应,生成具有反萤石结构的淡灰色固体G,并放出单质气体D。
2-1写出M的元素符号和电子组态。
2-2写出A ~ G的化学式。
2-3写出镀有M的镁片溶于稀盐酸,得到F的化学反应方程式。
2-4实际上,M溶于盐酸所得到的E溶液并不能长期稳定存在,而是会逐渐转化为含B的溶液。
请简述这一转化是如何发生的。
第3题(12分)上世纪50年代,美国联合碳化物公司(UCC)的Milton等人在铝硅酸盐凝胶中加入碱金属氢氧化物,合成了一系列具有三维结构的沸石,A型沸石就是其中一种。
A型沸石中Al原子和Si原子数目相同。
右图是A型沸石结构的一部分,其中多面体的每一个顶点均代表一个T原子(T为Al或Si),每一条边代表一个氧桥。
该结构可看做是由由6个正方形和8个正六边形围成的β笼,通过立方体笼(γ笼)与相邻的β笼相连而形成的三维结构,结构间隙中有钠离子和水分子。
A型沸石经加热可彻底脱水,但其三维骨架结构仍能维持不变。
3-1 写出该晶体中α笼、β笼和γ笼的数目比。
3-2写出A型沸石脱水后的化学式。
若钠离子仅填充在α笼中,则平均一个α笼中有几个钠离子?3-3设相邻β笼中心之间的距离为1230 pm,估算A型沸石脱水后的密度。
3-4关于该晶体中Al原子和Si原子的位置,人们曾提出过多种可能的模型:A:Al和Si统计分布;B:Al和Si有序分布,不同种[TO4]多面体之间相连接,但同种[TO4]多面体之间互相不连接;C:Al和Si有序分布,β笼由同种[TO4]多面体之间相连接构成,β笼间不同种[TO4]多面体之间相连接;D:Al和Si有序分布,β笼由不同种[TO4]多面体之间相连接构成,β笼间同种[TO4]多面体之间相连接;3-4-1分别指出A ~ D四种晶体各属于十四种布拉维点阵中的哪一种?3-4-2脱水的A型沸石的29Si-NMR谱在-89.6 ppm出现一个尖锐的单峰(对比:霞石(Na,K)AlSiO4和石英中硅的化学位移分别为-84.8 ppm和-107.0 ppm)。
据此,能否定上述A ~ D中的哪些结构?3-5人们提出了一种A型沸石中Al和Si分布的新的晶体结构模型。
该晶体结构属立方晶系,其中[TO4]四面体所连接的其他四面体的种类和数目与A型沸石中相同。
若单看1个β笼,则其呈现C3i对称性(具有C3轴和i),含12个铝原子和12个硅原子。
3-5-1分别用黑球和白球代表铝和硅,在右图中补全一个β笼的结构,标出C3轴。
3-5-2该晶体中,β笼之间如何连接?简述判断理由。
3-6与其他具有相同硅铝比的沸石相比,A型沸石呈现更差的酸耐受性。
X型和Y型沸石在酸洗(pH ~ 3)后仍然能稳定存在,但A型沸石在pH < 6的条件下即会被破坏。
产生这一差别的可能原因是什么?第4题(8分)有机萃取剂HA能将水溶液中的Ce3+以Ce(A)x(HA)y的形式萃取至有机相。
HA在水中几乎不溶解,而在有机相中仅以H2A2的二聚体形式存在。
为测定该铈配合物在有机相的具体形式,进行如下实验:将示踪量144Ce3+溶于水,并用少量硝酸酸化,制成含144Ce3+的水相;移取上述水相及含HA的有机相各2.50 mL于室温下充分混合萃取,待平衡后,取水相和有机相各1.00 mL,测定其放射性强度之比;另取一份平衡后的水相,测定其pH值。
当H2A2的初始浓度c0(H2A2) = 0.240 mol·L-1时,测得平衡时有机相与水相放射性强度比为2929:416,水相[H+] = 3.4 × 10-2 mol/L;当c0(H2A2) = 0.120 mol·L-1时,测得平衡时有机相与水相放射性强度比为1542:1682,水相[H+] = 3.4 × 10-2 mol·L-1。
请通过计算和推理确定x和y的值,并计算萃取反应的平衡常数(不考虑Ce3+的水解及Ce3+与NO3-的络合)。
第5题(17分)近日,研究者提出了一种从空气中直接收集二氧化碳的工艺,工艺可表示为如下图的两个循环过程:5-1-1写出四个容器中发生反应的化学方程式。
5-1-2研究者在以下场景中模拟第一个循环过程:常温常压下将10 m3的新鲜空气(CO2体积分数为0.06%)缓缓通入1升吸收液(含有1 mol KOH和0.5 mol K2CO3)中,然后将吸收液加入反应器回收循环重新利用。
假设CO2视为理想气体,吸收后空气中CO2体积分数降为0.02%。
5-1-2-1计算298.2 K下反应器中离子反应的标准平衡常数KꝊ和吸收后溶液的组成。
5-1-2-2通过计算说明能否使回收后的溶液与原吸收液相同?如果能,请计算所需Ca(OH)2的质量;如果不能,请计算KOH的最大回收率。
5-1-3熟化过程会剧烈放热,这部分热量可以被用在工艺的哪一步中?简要说明理由。
5-2-1富集得到的CO2可以作为锂离子电池的工作气体,请分别写出锂-空气电池和锂-二氧化碳电池放电时的电极反应式。
5-2-2近日研究者开发了一种新型的硼、氮共掺杂的多孔石墨烯材料作为锂-二氧化碳电池的正极催化剂,得到具有长循环寿命的锂-二氧化碳二次电池,请简要说明这种材料起到的作用。
第6题(11分)正常而言,化学反应的反应速率都随温度升高而上升。
然而偌大的自然界总是存在着例外的情况,比如我们熟知的一氧化氮被氧气氧化为二氧化氮的反应,其反应速率随温度上升而降低。
其反应机理一般用下图表示:6-1根据稳态近似推导一氧化氮被氧气氧化为二氧化氮的反应速率方程。
6-2若上述反应历程中第一步为快平衡,第二步反应为决速步,根据平衡态近似推导出反应速率方程。
6-3通过平衡态近似推导出的方程可由稳态近似推出的方程通过近似而得来,写出何种条件下能够进行此种近似。
6-4判断k1/k2随温度的变化情况。
6-5 简要解释为何上述反应会出现反应速率随温度上升而降低的情况,并判断该反应的表观活化能是正值还是负值。
第7题(7分)7-1 在19世纪,曾有科学家试图使用铝作为还原剂在苯溶剂中进行Wurtz偶联反应:但该反应反而得到了大量的氯化氢,产物中碳的含量也明显超过理论值。
据此推测,体系中实际上发生了什么反应,得到了什么有机产物?7-2 通过以下反应得到了产物A(C7H8O2)。
将A于CCl4溶液中加热至70°C,A经历中间体B而部分转化为其同分异构体C。
A、B、C三者在平衡时的比例为29:42:29。
请据此画出A、B、C的结构简式。
7-3 通过以下反应得到了含三个六元环的化合物:已知X的化学式为C15H13NO2,红外光谱显示X在1668 cm-1和1692 cm-1附近出现吸收峰。
请画出X和Y的结构简式。
第8题(11分)有机锂试剂在有机化学中占有极其重要的地位,比如LTMP、LHMDS、secBuLi、nBuLi均为常用的有机强碱,在官能团转换里有着重要应用。
如下图所示反应中:8-1 已知A ~ D均为离子型化合物,画出A ~ F的结构简式。
有机炔醇锂也是常用的有机锂试剂之一,如下图反应中,用预先制备的丙炔醇锂与另一底物合成天然产物(±)-curcumin E:8-2写形成该产物过程中两个关键电中性中间体及所有产物。
第9题(11分)串联反应,也称多米诺(Domino)反应,即多步合成反应结合在一种合成操作中完成,无需额外的试剂或反应条件变化;中间体无需分离,随后转化为能量较低的物种。
多米诺反应在有机全合成中有重要应用:9-1(+)-18-Keto-pseudoyohimbane的手性合成过程中经历了多米诺反应。
画出反应过程中经历的三个关键中间体的结构简式。
9-2生物碱(-)-Gilbertine的全合成以一步正离子多米诺反应收尾。
首先,在吲哚环系的参与下,叔碳离子被稳定,接着发生[1,7]-H迁移反应生成第一个关键中间体;而后反应过程中经历三元环中间体生成产物。