卤素单质及化合物的颜色培训资料
- 格式:docx
- 大小:6.37 KB
- 文档页数:1


卤素单质水溶液的颜色和有机溶剂的颜色随着化学知识的普及和深入,我们对于化学元素的性质和特点有了越来越多的了解。
其中,卤素单质作为化学元素中的一种,其水溶液和有机溶剂中的颜色表现引起了我们的广泛关注。
在本文中,将深入探讨卤素单质在水溶液和有机溶剂中的颜色表现,带领读者全面了解这一化学现象。
1. 氯素单质水溶液的颜色首先让我们来探讨氯素单质在水溶液中的颜色表现。
一般情况下,氯素单质溶解于水中会生成氯离子,而氯离子在水中呈现淡黄绿色的颜色。
这种颜色对于氯素单质在水溶液中的特征有着重要的指示作用,也是我们在实验室中常见的化学现象之一。
2. 氟素单质水溶液的颜色我们来探讨氟素单质在水溶液中的颜色表现。
与氯素单质不同,氟素单质在水中溶解后并不会显现出明显的颜色。
这是由于氟离子在水中呈现无色的特点所决定的。
在实验操作中,我们往往需要通过其他检测方法来确认氟素单质在水溶液中的存在。
3. 溴素单质有机溶剂的颜色除了在水溶液中的颜色表现,我们还需要了解溴素单质在有机溶剂中的颜色变化。
一般情况下,溴素单质在有机溶剂中会呈现出深红色或红棕色的颜色。
这种颜色的呈现是由于溴素单质分子间的相互作用导致的,也是我们在化学实验中常见的观察结果之一。
4. 碘素单质有机溶剂的颜色让我们来探讨碘素单质在有机溶剂中的颜色表现。
一般来说,碘素单质在有机溶剂中会呈现出紫色或紫黑色的颜色。
这种颜色的呈现也是由于碘素单质分子间的相互作用所导致的,同时也是我们在化学实验中观察到的有机溶剂中的颜色现象之一。
从以上对于卤素单质在水溶液和有机溶剂中的颜色表现的探讨中,我们可以看到不同卤素单质在不同溶剂中呈现出的独特颜色,这为我们对于这一化学现象的理解提供了重要的参考。
对于这一现象的深入探讨也有助于我们在实验操作中准确把握颜色指示的特点,从而更好地完成化学实验。
个人观点和理解作为化学领域的一部分,我对于卤素单质在水溶液和有机溶剂中的颜色表现十分感兴趣。
这一化学现象不仅反映了卤素单质分子间的相互作用特点,也为化学实验操作提供了重要的参考依据。


卤素(VII A族)元素卤族元素简称卤素,包含F、Cl、Br、I、At等元素。
At和F因性质特殊通卤素的性质○1卤素能溶于水,易溶于有机溶剂(酒精、苯、四氯化碳、丙酮等)。
此性质常用作萃取。
○2与氢气反应F2+H2(冷暗处反应,爆炸)Cl2+H(光照混合的气体发生爆炸(光爆反应);点燃则安静的燃烧,呈苍白色火焰,瓶口有白色酸雾。
)Br2+H(反应较慢)I2+H2(反应慢,反应产物不稳定,易分解)反应产物HX为无色刺激气体,极易溶于水,生成氢卤酸。
酸性:HI>HBr>HCl,此三者皆为强酸,HF为弱酸。
○3单质氧化性F2>Cl2>Br2>I2○4离子还原性F-<Cl-<Br-<I-○5卤素和水发生反应:2F2+2H2O=4HF+O2+H2HCl+HClOCl+2H2BrI2与水不反应○6氧化性较强的卤素单质能将溶液中的氧化性较弱的卤素离子置换成单质,例如:Cl2+2KI=2KCl+I2(通常用湿润的淀粉碘化钾试纸检验氯气)○7卤化银均为不溶物AgCl 白色AgBr 浅黄色AgI黄色卤素由上至下电子层数不断增多,原子核吸引电子能力减弱(尽管质子数不断增多,但电子野增加使质子对最外层电子吸引能力减弱。
)氯气Cl2①大多数金属单质能直接于Cl2化合,并且金属氧化为高价的氯化物。
2Na+Cl(白烟)Cu+Cl2(棕黄色的烟)2Fe+3Cl3(棕褐色的烟)②与非金属化合2P+3Cl3(l)2P+5Cl5(S)H2+Cl2+H2③与水反应Cl④与碱反应Cl2+2NaOH2O3Cl23+3H2O⑤与氨气反应:3Cl2+8NH3=N2+6NH4Cl,其中OR部分:3Cl2+2NH3=N2+6HCl⑥与还原性盐:6FeBr2+3Cl2(少量)=2FeCl3+4FeBr32FeBr2+3Cl2(足量)=2FeCl3+2Br2Na2S+Cl2=2NaCl+S↓⑦氧化具有还原性的化合物⑧与CH4反应与CH2=CH2反应⑨关于Cl的含氧酸1.HClO4(高氯酸):是最强的无机酸2.HClO(次氯酸):Cl2与H2O反应生成HClO与HCl,其中HClO具有强氧化性,可以用来杀菌消毒、漂白。

卤素单质及化合物的颜色
1.卤族元素它们自身的颜色
F2,淡黄绿色气体,没有水溶液,因为与水迅速反应,2F2+2H2O=4HF+O2。
Cl2,黄绿色气体,氯水淡黄绿色,因为在水中的溶解度不大。
Br2,深红棕色液体,蒸气红棕色,溴在水中溶解度不大,所以溴水橙色,溴在有机溶剂中的溶解度较大,所以溴的苯溶液、溴的CCl4溶液都是橙红色。
I2,紫黑色固体,蒸气紫红色,碘在水中的溶解度很小,所以碘水棕黄色,碘在有机溶剂中的溶解度较大,所以碘的苯溶液、碘的CCl4溶液都是紫红色,但碘的酒精溶液是棕黄色的。
【注】溶液的颜色与浓稀有关,浓溶液颜色深,稀溶液颜色浅,如饱和溴水为红棕色,而很稀的溴水则为浅黄色。
2.常见化合物的颜色
它们的离子都是无色的,所以它们的化合物多数是无色,或白色固体。
AgF是可溶于水的,无色溶液,AgCl是白色沉淀,AgBr是淡黄色沉淀,AgI是黄色沉淀。
3.他们之间鉴别的方法
Cl-、Br-、I-的鉴别可以用AgNO3溶液,根据产生的沉淀的颜色不同进行鉴别,白色沉淀Cl-,淡黄色沉淀Br-,黄色沉淀I-。
1 / 11 / 1。

卤素单质性质提纲【知识要点板书设计】一.卤素的原子结构及其单质的物理性质1.原子结构2.单质的递变规律色状熔沸点密度水溶性氟 F +9 2 7 浅气小小大氯 Cl+17 2 8 7 气溴 Br+35 2 8 18 7 液碘 I+53 2 8 18 18 7 深固高大小3.溴和碘单质的溶解性(1)萃取:利用溶质在互不相溶的溶剂里溶解度的不同,用一种溶剂把溶质从它与另一溶剂所组成的溶液里提取出来的方法。
(2)萃取的条件:①萃取剂与原溶液不发生反应②萃取剂与原溶剂互不相溶③萃取剂比原溶剂的溶解能力强注意:酒精不能做萃取剂(3)溴和碘在不同溶剂中所生成溶液(由稀到浓)的颜色变化溶剂溶质水苯汽油四氯化碳Br2 黄橙(橙黄)橙橙红橙橙红橙橙红I2深黄褐(橙红)淡紫紫红淡紫紫红紫深紫密比水轻比水轻比水重度二.卤素单质(X2)的化学性质(1) + 金属金属氯化物氧化性1.相似性(2) + H2 HX(3) + H2O HX + HXO(4) + OH- X- + XO-既有氧化性又有还原性(F2除外)(1) + 金属氧化性:F2 > Cl2 > Br2 > I2 (还原性:I- > Br- > Cl- > F-)2.递变性+ H2稳定性:HF > HCl > HBr > HI(2)置换能力: Cl2 > Br2 > I2 (F2除外) (X2 + 2Y-= 2X- + Y2)3.特性(1)F2:是最活泼的非金属单质(只有正价、无正价 ) (2)I2:遇淀粉变蓝色三.卤素的几种化合物1.AgCl、 AgBr和AgI NaCl制取:NaBr + AgNO3NaI 光照特性:见光分解 2AgBr == 2Ag + Br2用途:AgBr做感光剂、AgI人工降雨2.Cl-、Br-、I-的鉴别方法Cl-白色沉淀Br- + AgNO3 + HNO3浅黄色沉淀I-黄色沉淀。

卤素复习提纲一、卤素单质:1、物理性质:卤素单质F2Cl2Br2I2常温下的色态蒸气的颜色易溶于有机溶剂(苯、汽油、CCl4)水溶液的颜色熔沸点密度(1)碘的升华:。
用于。
如氯化钠中含有单质碘。
易升华的物质有:碘、干冰、萘等,属变化。
(2)试剂的存放:①氯水:瓶,不能用橡皮塞。
②液溴:瓶,不能用橡皮塞。
③固态碘:瓶。
④AgNO3溶液:瓶。
(3)萃取①萃取剂的选择应注意两点①萃取剂难溶于水,分层。
②溶质在萃取剂中的溶解性于在水中的溶解性。
②萃取分液操作:a检查分液漏斗是否漏水(瓶塞、活塞)b加入溶液和萃取剂c把分液漏斗倒转用力振荡(萃取)d分液漏斗放在铁架台上静置。
原因:使混合液分层。
e打开玻璃塞或使塞上的凹槽或小孔对准漏斗口上的小孔。
原因:使分液漏斗内外空气相通,保证漏斗中的液体能顺利流下来。
f分液操作。
应注意:①漏斗下口紧挨着烧杯壁;②不要使上层的液体流下来。
g上层液体要从分液漏斗的上口倒出。
2、结构与性质的关系:(1)F Cl Br I At的增多的增大氧化性(非金属性)(2)F-Cl-Br-I-At-的增多的增大离子的还原性依次(一)与金属反应(显氧化性):(1)代表:写出Cl2与Cu、Na、Fe的反应式,有何种颜色的烟,加水后溶液的颜色。
点燃(2)F2、Cl2、Br2与金属反应生成高价盐:例:2Fe+3Br22FeBr3(3)I2与金属反应生成低价盐:例:Fe+I2=FeI2(二)与非金属反应(显氧化性):(1)代表:写出H2、P与Cl2反应的方程式(注明条件),有何现象。
(2)H2与F2、Cl2、Br2、I2反应的条件(3)HF HCl HBr HI HAt形成条件:由易到难气态氢化物的稳定性:(原因:)还原性:逐渐(见卤素离子的还原性)水溶液(氢卤酸)的酸性:逐渐(HF为弱酸,其它均为强酸)(三)与水的反应(歧化反应):(1)代表:①氯水中的反应式②新制氯水中存在大量氯气分子⇒新制氯水呈浅黄绿色;新制氯水中存在H+、HClO⇒滴入石蕊试液,溶液先变红色,然后再褪为无色。
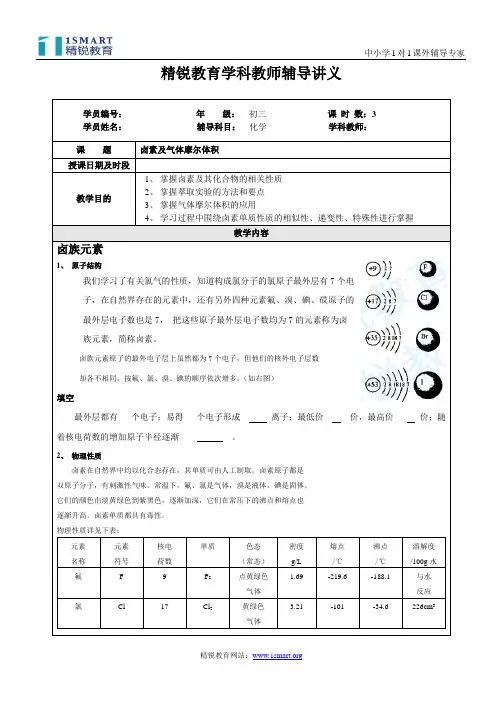
精锐教育学科教师辅导讲义学员编号:年级:初三课时数:3 学员姓名:辅导科目:化学学科教师:课题卤素及气体摩尔体积授课日期及时段教学目的1、掌握卤素及其化合物的相关性质2、掌握萃取实验的方法和要点3、掌握气体摩尔体积的应用4、学习过程中围绕卤素单质性质的相似性、递变性、特殊性进行掌握教学内容卤族元素1、原子结构我们学习了有关氯气的性质,知道构成氯分子的氯原子最外层有7个电子,在自然界存在的元素中,还有另外四种元素氟、溴、碘、砹原子的最外层电子数也是7,把这些原子最外层电子数均为7的元素称为卤族元素,简称卤素。
卤族元素原子的最外电子层上虽然都为7个电子,但他们的核外电子层数却各不相同,按氟、氯、溴、碘的顺序依次增多。
(如右图)填空最外层都有___个电子;易得___个电子形成__ _离子;最低价__ __价,最高价___ _价;随着核电荷数的增加原子半径逐渐____ __。
2、物理性质卤素在自然界中均以化合态存在,其单质可由人工制取。
卤素原子都是双原子分子,有刺激性气味。
常温下,氟、氯是气体,溴是液体,碘是固体。
它们的颜色由淡黄绿色到紫黑色,逐渐加深,它们在常压下的沸点和熔点也逐渐升高。
卤素单质都具有毒性。
物理性质详见下表:元素名称元素符号核电荷数单质色态(常态)密度g/L熔点/℃沸点/℃溶解度/100g水氟 F 9 F2点黄绿色气体1.69 -219.6 -188.1 与水反应氯Cl 17 Cl2黄绿色气体3.21 -101 -34.6 226cm3溴Br35Br 2深红棕色 液体3.12 -7.2 58.784.16g碘I53I 2紫黑色 固体4.93 113.5 184.4 0.029g3、 化学性质氟、氯、溴、碘最外层电子层上都有7个电子,容易获得一个电子而形成稳定结构,因此它们的化学性质具有很大的相似性。
随着核电荷数的增加以及电子层数的增多,卤素原子的的电子能力逐渐减弱,活泼性(氧化性)也随之减弱;另一方面,对卤素阴离子来说,随着核电荷数的增加,离子失电子能力(还原性)逐渐增强。


第17章卤素17-1卤素单质17-2卤化氢和氢卤酸17-3卤化物与拟卤素17-4卤素的含氧化合物卤素(VIIA族):氟F,氯Cl,溴Br,碘I,砹At 。
它们都易形成盐,统称为卤素。
价电子构型:n s2n p5氧化态:除氟外(–1),其余均可呈现–1,0,+1,+3,+5,+7卤素的存在形式:氟:萤石CaF 2,冰晶石Na 3AlF 6,氟磷灰石Ca 5F(PO 4)3 ;氯:以NaCl 的形式存在于海水、盐湖、盐井中,矿物中以KCl 、光卤石KCl ·MgCl 2 ·6H 2O ;溴:以溴化物的形式存在于海水和地壳中;碘:碘在海水中存在的更少,主要被海藻所吸收。
通常以碘化物形式存在,南美洲智利硝石含有少许的碘酸钠。
砹:放射性元素,仅以微量而短暂地存在于镭、锕和钍的蜕变产物中。
17 -1卤素单质17 -1 -1物理性质F2Cl2 Br2 I2聚集状态g g l s分子间力小大解离能先上升再下降b.p./℃–188 –34 59 185 m.p. /℃–220 –102 –7 114颜色浅黄黄绿红蓝黑随着原子序数的增加,这种轨道之间的能量差逐渐减少,所需要外界提供的能量随之减少,即所吸收的光的波长逐渐增加,透过或反射的光的波长也呈现规律性变化。
卤素单质在水中的溶解度F2 氧化能力极强,与水剧烈反应。
Cl2在水中溶解度较小。
Br2在水中溶解度是卤素单质中最大的一个,100 g 水中可溶解3.58 g 溴。
I2 在水中的溶解度最小,但在CCl4中的溶解度很大。
I2 在KI 或其他碘化物溶液中溶解度变大,而且随I-浓度增大而增大。
I-+ I2 = I3-17 -1 -2化学性质F 2 Cl 2 Br 2 I 2X 2 氧化性:强弱X –还原性:弱强E ( X 2 / X –)/V :2.87 1.36 1.07 0.54结论:氧化性最强的是F 2,还原性最强的是I –。
卤素单质是强氧化剂,其中F 2 的氧化性最强,随原子序数增大,氧化能力逐渐变弱。

卤素单质的颜色
氟气为浅黄绿色气体,与水剧烈反应得到氢氟酸和氧气,在三种有机溶剂中可认为是黄绿色。
氯气为黄绿色气体,氯水为浅黄绿色,在有机溶剂中可认为是黄绿色。
溴为深红棕色液体,溴水为橙色,在有机溶剂中为橙红色。
碘为紫黑色固体,碘水为黄褐色,在有机溶剂中为紫红色。
卤族元素
卤族元素指周期系ⅦA族元素。
包括氟(F)、氯(Cl)、溴(Br)、碘(I)、砹(At)、石田(Ts),简称卤素。
它们在自然界都以典型的盐类存在,是成盐元素。
卤族元素的单质都是双原子分子,它们的物理性质的改变都是很有规律的,随着分子量的增大,卤素分子间的色散力逐渐增强,颜色变深,它们的熔点、沸点、密度、原子体积也依次递增。
卤素都有氧化性,氟单质的氧化性最强。
卤族元素和金属元素构成大量无机盐,此外,在有机合成等领域也发挥着重要的作用。
卤素之间可以形成卤素互化物,它们有的性质类似卤素单质。
精品文档
1. 卤族元素它们自身的颜色
F2,淡黄绿色气体,没有水溶液,因为与水迅速反应,2F2+2H2O=4HF+O2
CI2,黄绿色气体,氯水淡黄绿色,因为在水中的溶解度不大。
Br2,深红棕色液体,蒸气红棕色,溴在水中溶解度不大,所以溴水橙色,溴在有机溶剂中的溶解度较大,所以溴的苯溶液、溴的CCI4溶液都是橙红色。
I2 ,紫黑色固体,蒸气紫红色,碘在水中的溶解度很小,所以碘水棕黄色,碘在有机溶剂中的溶解度较大,所以碘的苯溶液、碘的CCI4溶液都是紫红色,但碘的酒精溶液是棕黄色的。
【注】溶液的颜色与浓稀有关,浓溶液颜色深,稀溶液颜色浅,如饱和溴水为红棕色,而很稀的溴水则为浅黄色。
2. 常见化合物的颜色
它们的离子都是无色的,所以它们的化合物多数是无色,或白色固体。
AgF是可溶于水的,无色溶液,AgCI是白色沉淀,AgBr是淡黄色沉淀,AgI是黄色沉淀。
3. 他们之间鉴别的方法
Cl-、Br-、I-的鉴别可以用AgNO3溶液,根据产生的沉淀的颜色不同进行鉴别, 白色沉淀CI-,淡黄色沉淀Br-,黄色沉淀I- 0
精品文档。