苯乙酮的制备
- 格式:doc
- 大小:187.50 KB
- 文档页数:4

苯乙酮的制备研究苯乙酮,也被称为乙苯酮,是一种有机化合物,化学式为C8H8O。
它是一种常用的有机合成中间体,广泛应用于医药、香料以及化妆品等领域。
本文将介绍苯乙酮的制备方法研究。
目前,苯乙酮的制备方法主要有四种:烯丙基化、芳香亲核取代、还原反应和酸解反应。
1. 烯丙基化法:烯丙基化法通过烯丙基基团与苯基团的偶联反应来制备苯乙酮。
一种常用的烯丙基化试剂是苯乙炔,它和很多齐聚试剂(如醇、醛、酮等)反应可以得到苯乙酮。
苯乙炔可以与酮类反应,生成相应的苯乙酮。
2. 芳香亲核取代法:芳香亲核取代法通过芳香化合物与酸、酰基化合物或酰化试剂反应制备苯乙酮。
常用的亲核试剂有醇、胺和硫氢化物等。
芳香亲核取代法的一个优点是可以采用氢氧化钠或碳酸钠等碱性条件作为催化剂,从而使得反应条件温和。
3. 还原反应法:还原反应法通过将酮化合物还原为相应的醇,然后进一步氧化为醛或酮,从而制备苯乙酮。
常用的还原剂有金属氢化物(如锂铝氢化物)、酸性溶液(如硫酸和亚硫酸)等。
4. 酸解反应法:酸解反应法通过酸催化将醇酮类化合物加水分解得到苯乙酮。
乙醇醇酮可以经过酸解反应得到苯乙酮。
酸解反应法的优点是操作简单,但副反应较多,需要选择适当的酸和反应条件,以提高产率。
还有很多其他的方法也可以用于苯乙酮的制备,如金属催化的氨基还原反应、过渡金属催化的C-H键取代反应等。
这些方法相对较新,需要更多的研究来完善优化。
苯乙酮的制备方法多种多样,可以根据需要选择适合的方法进行实验研究。
在制备苯乙酮的过程中,需要考虑反应的选择性、产率、操作简便性等因素,以达到高效、高产的目的。
未来的研究还可以通过改进催化剂、溶剂以及反应条件等方面,进一步提高制备苯乙酮的效率和选择性。

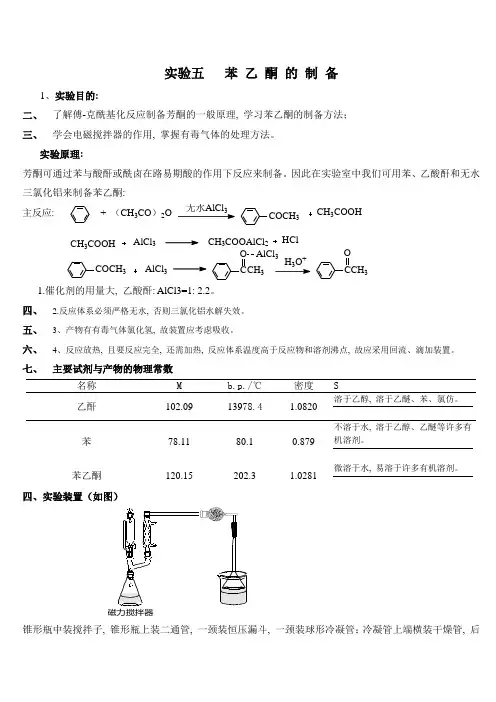
实验五 苯 乙 酮 的 制 备1、实验目的:二、 了解傅-克酰基化反应制备芳酮的一般原理, 学习苯乙酮的制备方法; 三、 学会电磁搅拌器的作用, 掌握有毒气体的处理方法。
实验原理:芳酮可通过苯与酸酐或酰卤在路易期酸的作用下反应来制备。
因此在实验室中我们可用苯、乙酸酐和无水三氯化铝来制备苯乙酮:主反应: + (CH 3CO )2O3COCH 3CH 3COOHCOCH 3AlCl 3CH 3COOAlCl 2HClAlCl 3CH 3COOHCCH 3O AlCl 3H O +CCH 3O1.催化剂的用量大, 乙酸酐: AlCl3=1:2.2。
四、 2.反应体系必须严格无水, 否则三氯化铝水解失效。
五、 3、产物有有毒气体氯化氢, 故装置应考虑吸收。
六、 4、反应放热, 且要反应完全, 还需加热, 反应体系温度高于反应物和溶剂沸点, 故应采用回流、滴加装置。
七、 主要试剂与产物的物理常数名称 M b.p./℃ 密度 S乙酐 102.09 13978.4 1.0820 溶于乙醇, 溶于乙醚、苯、氯仿。
苯 78.11 80.1 0.879 不溶于水, 溶于乙醇、乙醚等许多有机溶剂。
苯乙酮120.15202.31.0281微溶于水, 易溶于许多有机溶剂。
四、实验装置(如图)锥形瓶中装搅拌子, 锥形瓶上装二通管, 一颈装恒压漏斗, 一颈装球形冷凝管;冷凝管上端横装干燥管, 后装长颈漏斗, 用碱液吸收。
五、操作步骤向装有恒压滴液漏斗、电磁加热搅拌器和回流冷凝管(上端通过一氯化钙干燥管与氯化氢气体吸收装置相连)的50 mL三颈(或二颈)烧瓶中迅速加入研细的6.0g无水三氯化铝和8.0mL无水苯。
在电磁搅拌下自滴液漏斗慢慢滴加2 mL乙酐(加2 mL苯稀释), 开始少加几滴, 待反应发生后再继续滴加, 切勿使反应过于激烈, 滴加速度以烧瓶稍热为宜。
加完后(约需10~15min), 待反应速度稍缓和后, 水浴加热回流, 直到不再有氯化氢气体逸出为止。

实验六苯乙酮的制备一、实验目的1.掌握傅瑞德尔-克拉夫茨酰基化反应;2.学习电动搅拌器的安装、使用以及减压蒸馏操作方法。
二、实验原理傅瑞德尔-克拉夫茨反应是指芳香烃在无水三氯化铝等催化剂存在下,同卤代烃、酰氯或酸酐作用,在苯环上发生亲电取代反应而引入烷基或酰基的反应。
(CH3CO)2O CH3COOH 无水AlClCH3O三、主要仪器和试剂1.仪器:电动搅拌器、电热套、三口瓶、球形冷凝管、分液漏斗、温度计、园底烧瓶、氯化钙干燥管;2.试剂:苯35g、无水三氯化铝20g、乙酸酐6.5g 、浓硫酸、浓盐酸、5%氢氧化钠溶液。
四、实验仪器及装置图五、实验操作流程搭建装置填料回流1小时冰水浴冷却加盐酸苯萃取洗涤,无水硫酸镁干燥常压蒸馏140度停热稍冷减压蒸馏,收集92~96度六、实验操作步骤现象、解释1、干燥仪器,及保证药品的无水。
2、20g无水三氯化铝和30ml苯,在滴液漏斗中加6ml乙酸酐和10ml苯的混合物;搅拌下缓慢滴加,反应开始,放出氯化氢气体,三氯化铝溶解,体系升温,控制温度,加料时间约20min。
3、加完乙酸酐关闭滴液漏斗旋塞,用电热套加热保持缓缓回流1h。
4、回流后,将三口瓶用冰水浴冷却至5~10℃,不断搅拌下滴加80ml20%盐酸至固体溶解。
分液漏斗分出苯层,水层用30ml苯分两次萃取。
用20ml氢氧化钠溶液洗涤,再用水洗涤。
分出苯层,用无水硫酸镁干燥。
5、将含苯的粗产物放入100ml圆底烧瓶,加沸石,蒸出苯,温度升到140℃左右,停止加热。
收集116~120℃/8.00kPa的馏分。
七、产率的计算,n D 20=1.5372。
纯苯乙酮,无色油状液体,熔点20℃,沸点202℃,d204=1.026。

苯乙酮的制备实验报告
目录
1. 实验目的
1.1 原料准备
1.2 实验步骤
1.2.1 反应体系
1.2.2 反应条件
1.2.3 操作步骤
1.2.4 产物提取
1.3 实验结果分析
实验目的
本实验旨在通过苯乙酮的制备实验,让学生掌握重要的有机合成技术,提高其对化学反应机理的理解能力。
原料准备
- 苯
- 乙酰氯
- NaOH
- 水
- 氯仿
实验步骤
反应体系
在反应釜中,加入适量苯和乙酰氯,同时控制好反应温度。
反应条件
控制反应的温度在适宜范围内,观察反应进程,及时调整反应条件。
操作步骤
1. 将苯加入反应釜中;
2. 加入适量的乙酰氯;
3. 控制反应温度并搅拌均匀反应体系;
4. 加入NaOH溶液进行中和反应;
5. 分离产物层并进行提取。
产物提取
通过对反应产物进行适当的提取步骤,得到苯乙酮等目标产物。
实验结果分析
通过对实验过程、反应条件和产物的分析,总结实验结果,对实验过
程中的问题进行讨论,并提出改进措施,以提高实验的准确性和效率。


苯⼄酮的制备【实验⽬的】1、学习利⽤Friedel—Crafts酰基化反应制备芳⾹酮的原理和⽅法。
2、学习⽆⽔操作。
【实验原理】Friedel—Crafts酰基化反应是制备芳⾹酮的最重要和最常⽤的⽅法之⼀,可⽤FeCl3,SnCl4,BF3,ZnCl3,AlCl3等Lewis 酸作催化剂,催化性能以⽆⽔AlCl3和⽆⽔AlBr3为最佳。
本实验采⽤⽆⽔AlCl3作催化剂,⽤苯和⼄酐反应制苯⼄酮。
反应⽅程式为:+(CH3CO)2O⽆⽔AlCl3COCH3+CH3COOH【实验装置】图1 图2【仪器和药品】1、仪器:25mL三颈烧瓶、恒压滴液漏⽃、25mL圆底烧瓶、直形冷凝管、接液管、三⾓烧瓶、铁圈、⼩烧杯、分液漏⽃、漏⽃、⼲燥管、电炉、。
2、药品:⽆⽔苯、⼄酐、⽆⽔AlCl3、浓盐酸、碎冰、10%的氢氧化钠溶液、⽔、⽆⽔氯化钙、⽆⽔硫酸镁。
【实验步骤】(上)6.5.0g(0.048moL)⽆⽔AlCl3 加⼊25mL三颈烧瓶中,8mL(约7g,0.09moL)⽆⽔苯如图1所⽰,⼲燥管中装⽆⽔氯化钙。
2mL(约2.15g,0.02moL)⼄酐(从滴液漏⽃缓慢加⼊)⾄⽆氯化氢⽓体逸出停⽌实验。
⼩磁⼦、沸⽯【实验步骤】(下)往装有反应混合物的三颈瓶中倒⼊9mL浓盐酸和18mL冰⽔的混合物(在通风橱中进⾏),将反应混合物倒⼊分液漏⽃中(若三颈瓶中有固体不溶物,加适量浓盐酸溶解)。
分液混合物分液上层:有机层下层:⽔层加⼊2×4mL苯分液有机层合并有机层依次⽤8mL10%的氢氧化钠溶液、8mL⽔洗涤,⽤⽆⽔硫酸镁⼲燥。
然后在⽔浴上蒸馏回收苯。
【实验注意事项】1、本实验要求⽆⽔系统,实验过程中应尽量避免体系敞⼝在空⽓中。
2、滴加⼄酐时应控制速度,使反应平稳进⾏;反应过程中严格控制好反应温度。
3、苯有毒,是致癌物质之⼀,不要接触⽪肤或吸⼊蒸⽓。
4、注意反应终点和反应混合物处理时⼀定在通风橱内进⾏。
5、⽆⽔三氯化铝的质量是本实验成败的关键,以⽩⾊粉末打开盖冒⼤量的烟,⽆结块现象为好。

苏州大学化学化工学院课程教案[实验名称] 苯乙酮的制备[教学目标] 学习利用Friedel-Crafts酰基化反应制备芳香酮的原理和方法。
了解无水实验的操作要点,初步掌握电磁搅拌器的使用,学习安装尾气吸收装置和使用空气冷凝管的实验操作,掌握分液漏斗的使用和萃取操作。
[教学重点] Friedel-Crafts酰基化反应原理和特点,催化剂Lewis酸的种类和用量。
[教学难点] Friedel-Crafts酰基化反应原理和特点,实验装置(含尾气吸收装置)的安装,分液漏斗的正确使用。
[教学方法] 启发式,讨论法,演示法,归纳法[教学过程][引言]【实验内容】苯乙酮的制备。
【实验目的】学习利用Friedel-Crafts酰基化反应制备芳香酮的原理和方法;了解无水实验的操作要点;初步掌握电磁搅拌器的使用;学习安装尾气吸收装置和使用空气冷凝管的实验操作;掌握分液漏斗的使用和萃取操作。
[提问] 本次实验原理是什么?[讲述] (评价学生答案并复述原理)Friedel-Crafts酰基化反应制备芳香酮的最重要和最常用的方法之一,可用FeCl3、AlCl3、ZnCl2等Lewis酸作催化剂。
酰卤和酸酐是常用的酰化试剂,常用过量的液体芳烃等作为反应的溶剂。
Friedel-Crafts酰基化反应是一个放热反应,通常将酰基化试剂配成溶液后慢慢滴加到盛有芳烃溶液的反应瓶中,并需密切注意反应温度的变化。
由于芳香酮可与AlCl3形成配合物,故与烷基化反应相比,酰基化反应的催化剂用量要大得多。
烷基化反应中AlCl3/RX(摩尔比)是0.1,酰基化反应中两者摩尔比为1.1。
由于芳烃与酸酐反应产生的有机酸会与AlCl3反应,所以AlCl3/RCOX(摩尔比)是2.2。
无水AlCl3+ (CH3CO)2O[演示] 【实验装置】参见P.12图1-9(3)。
图1 苯乙酮制备装置图NaOH尾气吸收装置[讲述] 【投料】无水苯(16 mL,约14 g,0.18 mol,过量);无水AlCl3(13 g,0.097 mol);乙酐(4 mL,约4.3 g,0.04 mol)。

苯乙酮生产原材料
苯乙酮是一种重要的化工原料,被广泛用于制造染料、香料、农药等精细化学品。
生产苯乙酮需要使用多种原材料,其中包括:
苯胺:苯胺是生产苯乙酮的主要原料之一,它可以通过化学合成或生物转化等方法获得。
乙醛:乙醛是生产苯乙酮的中间体之一,它可以由石油裂解气或其他来源获得。
硫酸:硫酸是生产苯乙酮过程中必不可少的催化剂和氧化剂,可以由硫磺制酸或间接法合成得到。
其他辅助材料:在生产苯乙酮的过程中,还需要使用一些其他辅助材料,如甲苯、丙酮等有机溶剂,以及三氯化铝、四氯化锡等催化剂。
这些原材料都是经过严格筛选和处理的,以确保其质量和纯度符合生产要求。
同时,在生产过程中也需要严格控制工艺条件和操作规程,确保产品的质量和安全性。
总之,苯乙酮的生产过程涉及到多个环节和复杂的化学反应,需要使用多种原材料和催化剂。
只有掌握了正确的原材料选择和使用方法,才能保证生产的稳定性和可靠性,从而满足市场需求并提高企业的竞争力。

苯乙酮的制备研究苯乙酮是一种重要的化学原料,被广泛应用于医药、染料、香料、香精、树脂等领域。
其制备方法有多种,包括从苯乙烯、苯甲醛或苯乙酸等原料合成。
本文将探讨苯乙酮的制备研究,介绍不同方法的原理和优缺点,以期为相关领域的科研工作者提供参考。
一、苯乙酮的制备方法1. 从苯乙烯合成将苯乙烯和氧气在催化剂的存在下氧化反应,生成苯乙酮。
催化剂通常采用铜、铬、钴等金属氧化物,也可选择氧化硫酸亚铁等化合物。
该方法操作简便,但设备投资较大。
2. 从苯甲醛还原合成利用还原剂将苯甲醛还原得到苯乙醇,再经过氧化反应得到苯乙酮。
还原剂可选用金属钠、金属铝等。
该方法将苯甲醛作为原料,可利用多种合成途径制备苯乙酮。
首先将苯乙酸和氯化亚砜在氢氧化钠的存在下反应生成苯乙醛,然后再进行氧化反应制备苯乙酮。
该方法所需原料易得,操作简便,适合工业生产。
优点:原料易得,反应途径简单。
缺点:设备投资大,氧化反应选择催化剂需要谨慎,对环境要求高。
优点:利用多种还原剂可制备苯乙酮,适用性广。
缺点:苯甲醛原料价格较高,还原剂对环境有一定的影响。
3. 从苯乙酸酐羧化合成的优缺点优点:原料易得,操作简便,适合工业化生产。
缺点:反应条件要求严格,氯化亚砜等原料对人体有一定的毒性。
三、苯乙酮制备研究的发展趋势1. 利用生物技术随着生物技术的发展,利用酶、微生物等生物催化剂合成苯乙酮成为研究热点。
通过优化酶的反应条件和酶的特异性,可以提高合成效率,并减少对环境的污染。
2. 绿色合成方法在苯乙酮的合成过程中,绿色合成方法备受关注。
包括采用水为溶剂、利用可降解催化剂、减少废弃物产生等方法,致力于实现对环境友好的苯乙酮合成过程。
3. 新型催化剂研究新型催化剂对苯乙酮的合成具有重要作用,包括贵金属、过渡金属、离子液体等催化剂的研究。
这些催化剂不仅可以提高合成效率,还可以减少催化剂的使用量,降低成本。
实验十三: 苯乙酮的制备一、实验目的1、学习傅-克酰基化制备芳酮的原理和方法;2、初步掌握无水操作、吸收、搅拌、回流、滴加等基本操作。
二、实验原理Friedel-Crafts 酰基化反应是制备芳酮的重要方法之一,酰氯、酸酐是常用的酰基化试剂,无水FeCl 3,BF 3,ZnCl 2和AlCl 3等路易斯酸作催化剂,分子内的酰基化反应还可以用多聚磷酸(PPA )作催化剂,酰基化反应常用过量的芳烃、二硫化碳、硝基苯、二氯甲烷等作为反应的溶剂。
用苯和乙酐制备苯乙酮的反应方程式如下:(CH 3CO)2O3CH 3COOH++COCH 3具体过程:CH O CH 3O O ++33Cl 3δCH 3COOAlCl 2CH 3OAlCl 3红色溶液+CH 3COOAlCl 2CH 3OAlCl 3H 2OCOCH 3Al(OH)Cl +HCl2CH 3COOH +Al(OH)Cl 2Al(OH)Cl 2Al + 3Cl + H 2O三、实验药品及其物理常数四、主要仪器和材料升降台 木板 隔热垫 电炉 水浴锅 机械搅拌器 四氟搅拌套塞(19#) 玻璃搅拌 三口烧瓶(100mL、19#×3)恒压滴液漏斗(14#×2)大小头(口14#+塞19#)空心塞(14#) 球形冷凝管(19#)直形干燥管(19#×2)分液漏斗圆底烧瓶(100 mL、19#)蒸馏头(19#)螺帽接头(19#)温度计(300℃) 直形冷凝管(19#)空气冷凝管(19#)真空接引管(19#)锥形瓶(50 mL、19#)量筒(100 mL)三角漏斗冰五、实验装置⑴搅拌、滴加、回流、尾气吸收装置⑵萃取、洗涤装置⑶常压蒸馏回收低沸物装置⑷减压蒸馏提纯高沸物装置六、操作步骤【操作要点及注意事项】⑴搭装置:保持反应体系无水是实验成败之关键,所有仪器一定要烘干(除三角漏斗和烧杯)。
仪器的选用,搭配顺序,各仪器高度位置的控制要合理。
【精品】苯乙酮的制备
苯乙酮是一种重要的化学品,广泛应用于香精、药品、农药等行业中。
本文将介绍几
种制备苯乙酮的方法。
1. 酮化反应法
酮化反应法是苯乙酮制备的重要方法之一,反应条件简单,易于控制,适用于大规模
工业生产。
酮化反应一般用苯和乙酸为原料,催化剂为硫酸或磷酸。
反应物质比例要求苯
和乙酸之间的摩尔比为1:1.5-2。
反应温度为150℃左右,反应时间为4-5小时。
反应产物经过蒸馏分离,得到纯苯乙酮。
不同生产厂家的分离方法略有不同,但大多
采用水蒸汽蒸馏法进行分离。
将反应物加入至反应釜,升温至160℃-175℃,经过蒸馏分离,得到苯乙酮和副产物乙酸酯。
经过多级分离、净化,最终得到纯苯乙酮。
总之,以上几种方法都适用于苯乙酮的制备。
其中,酮化反应法应用最为广泛,适用
于大规模工业制备;氧化反应法适用于小规模实验室制备;而醇解反应法则原料价格低廉,能够实现大规模工业生产,成本低。
苯乙酮的制备研究苯乙酮是一种常见的芳香族酮类化合物,具有广泛的用途,如用于药物合成、杀虫剂合成以及香料和染料合成等。
因此,苯乙酮的制备研究一直受到广泛的关注和探讨。
传统的苯乙酮制备方法主要有两种,一种是通过酰化反应制备,另一种是通过芳环化反应制备。
酰化反应是一种将酸酐或酸与醇或季铵盐反应生成酯键的重要反应。
苯乙酮的制备可以通过苯甲酸与乙酸酐在硫酸催化下进行酰化反应而得到。
反应方程式为:C6H5COOH + (CH3CO)2O → C6H5COCH2COCCH3 + H2O该反应通常在恒温下进行,但需要不断搅拌以提高反应速度。
反应结束后,反应物混合物经蒸馏分离,得到苯乙酮。
芳环化反应是另一种制备苯乙酮的常用方法。
该方法是以苯及其衍生物为反应底物,在适当的催化剂存在下,发生芳香族分子间的亲核加成与失活后的芳香族碳自由基取代反应,形成由芳环与羰基化合物构成的新环。
在这种方法中,苯和丙酮在碘化铝(AlI3)的存在下进行反应,生成苯乙酮。
反应方程式为:该反应需要在干燥条件下进行,并且需要适当控制反应中反应的温度和时间以确保反应物充分转化。
除了传统的制备方法之外,还有一些新型的制备苯乙酮的方法。
近年来,高斯应用量子化学计算的方法,提出一种通过醛/酮转移氢化或不确定介质反应,从苯甲醛以及乙酮派生物中制备苯乙酮的方法。
因为这种方法无需使用有机溶剂,反应的催化剂也可以是较为廉价的金属催化剂。
总的来说,苯乙酮的制备方法主要包括酰化反应、芳环化反应以及其他新型方法。
随着科技的发展和人们对环保和资源的理解,新型方法会逐渐替代传统方法,开发更加绿色、环保的方法,提高制备效率和降低成本,以更好地满足市场需求。
苯乙酮的制备(6学时)
【实验目的】
学习利用Fridel-Crafts 酰基化反应制备芳香酮的原理和方法
【实验原理】
1877年法国化学家付瑞德和美国化学家克拉夫茨发现了制备烷基苯和芳酮的反应,简称为付—克反应。
制备烷基苯的反应叫付—克烷基化反应,制备芳酮的反应叫付—克酰基化反应。
Friedel —Craffs 烷基化反应可合成乙苯
许多Lewis 酸可作为Friedel —Craffs 反应的催化剂:无水AlCl 3、无水ZnCl 2、FeCl 3、SbCl 3、SnCl 4、BF 3等,因为酸是一种非质子酸,在反应中是电子对的接受者,形成碳正离子,便于向苯环进攻。
在烷基化反应中,AlCl 3可以重复使用,所以烷基化反应的AlCl 3用量只需催化剂用量。
由Friedel —Craffs 酰基化反应制苯乙酮的原理:
反应历程:
O C O CH 3
C O
CH 3+ AlCl 3
O
C CH 3
Cl + O
C CH 3
O AlCl 2
从反应历程可看出:
1. 酰基化反应:苯乙酮与当量的氯化铝形成络合物,副产物乙酸也与当量氯化铝形成盐,反应中一分子酸酐消耗两分子以上的氯化铝
2. 反应中形成的苯乙酮/氯化铝络合物在无水介质中稳定,水解时,络合物被破坏,析出苯乙酮。
氯化铝与苯乙酮形成络合物后,不再参与反应,因此,氯化铝的用量是在生成络合物后,剩余的作为催化剂
3. 氯化铝可以与含羰基的物质形成络合物,所以原料乙酸酐也与氯化铝形成分子络合物;另外,氯化铝的用量多时,可使醋酸盐转变为乙酰氯,作为酰化试剂,参与反应:
O
C CH 3
Cl O C CH 3
O AlCl 2
+ AlOCl
4. 苯用量是过量的,苯不但作为反应试剂,而且也作为溶剂,所以乙酸酐才是产率的基准试剂。
5. 酰基化反应特点:产物纯、产量高(因酰基不发生异构化,也不发生多元取代)
【实验仪器及药品】
药品:乙酸酐 苯 硫酸镁 盐酸 氯化铝 氢氧化钠
仪器:圆底烧瓶 冷凝管 滴液漏斗 蒸馏装置 干燥管 搅拌装置
【主要反应试剂及产物的物理常数】
【实验装置图】
图8-1 无水滴加搅拌气体吸收反应装置
【实验步骤】
向装有10ml 恒压滴液漏斗、机械搅拌装置和回流冷凝管(上端通过一氯化钙干燥管与氯化氢气体吸收装置相连)的100ml 三颈烧瓶中迅速加入13g (0.097mol )粉状无水三氯化铝和16ml(约14g, 0.18mol)无水苯。
在搅拌下将4ml (约4.3g,0.04mol )乙酐自滴液漏斗慢慢滴加到三颈烧瓶中(先加几滴,待反应发
生后再继续滴加),控制乙酐的滴加速度以使三颈烧瓶稍热为宜。
加完后(约10min),待反应稍和缓后在沸水浴中搅拌回流,直到不再有氯化氢气体逸出为止。
将反应混合物冷到室温,在搅拌下倒入18ml浓盐酸和30g碎冰的烧杯中(在通风橱中进行),若仍有固体不溶物,可补加适量浓盐酸使之完全溶解。
将混合物转入分液漏斗中,分出有机层(哪一层?),水层用苯萃取两次(每次8ml)。
合并有机层,依次用15ml10%氢氧化钠、15ml水洗涤,再用无水硫酸镁干燥。
先在水浴上蒸馏回收苯,然后在石棉网上加热蒸去残留的苯,稍冷后改用空气冷凝管(为什么?)蒸馏收集195~202℃馏分,产量约为4.1g(产率85%)。
纯苯乙酮为无色透明油状液体,bp为202℃,mp为20.5℃,n D20 1.5372
【注意事项】
1. 滴加苯乙酮和乙酐混合物的时间以10min为宜,滴的太快温度不易控制。
2. 无水三氯化铝的质量是本实验成败的关键,以白色粉末打开盖冒大量的烟,无结块现象为好。
若大部分变黄则表明已水解,不可用。
3. AlCl3要研碎,速度要快。
4. 加入稀HCl时,开始慢滴,后渐快;稀HCl(1:1,已配)用量约为140ml。
5. 吸收装置:约20%氢氧化钠溶液,自配,200mL,特别注意防止倒吸。
6. 苯以分析纯为佳,最好用钠丝干燥24小时以上再用。
7. 粗产物中的少量水,在蒸馏时与苯以共沸物形式蒸出,其共沸点为69.4℃
【思考题】
1. Friedel—Craffs酰基化反应与Friedel—Craffs烷基化反应各有何特点?在两反应中,AlCl3和芳烃的用量有何不同?为什么?
答:Friedel—Craffs烷基化反应中,Lweis酸仅作催化剂。
Friedel—Craffs酰基化反应中,无水AlCl3不仅做催化剂,还能与酰基苯中的羰基氧结合成盐。
故为了反应顺利进行,需要多加一些Lewis酸,AlCl3。
2. 反应完成后为什么要加入浓盐酸和冰水的混合物?
答:用酸处理是为了破坏酰基氧与AlCl3形成的络合物,析出产物苯乙酮,同时为了防止碱性铝盐产生沉淀析出,影响产品质量。
C Ar R AlCl 3
O Ar R
AlCl 3
+
由于分解络合物的反应是放热的,故用冰水分解降温。
3. 下列试剂在无水三氯化铝存在下相互作用,应得到什么产物?
①过量苯+ClCH2CH2Cl ;
CH 2CH 2
1,2-二苯乙烷
②氯苯和丙酸酐;③甲苯和邻苯二甲酸酐;④溴苯和乙酸酐
4. 为什么硝基苯可作为反应的溶剂?芳环上有OH 、NH 2等基团存在时对反应不利,甚至不发生反应,为什么?
5. 在苯乙酮的制备中,水和潮气对本实验有何影响?在仪器装置和操作中应注意哪些事项?
答:破坏试剂影响产率,导致失败因三个试剂都属无水。
应采取措施:⑴药品仪器均需干燥。
⑵回流冷凝管上装一个干燥管。
⑶整个装置密合不漏气。
【实验要求】
计算产率,上交实验报告。