称化学反应标准平衡常数32页PPT
- 格式:ppt
- 大小:2.37 MB
- 文档页数:32




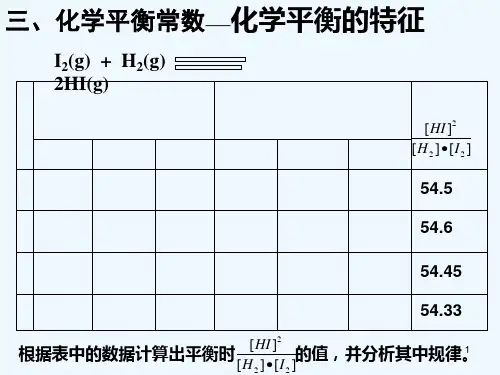
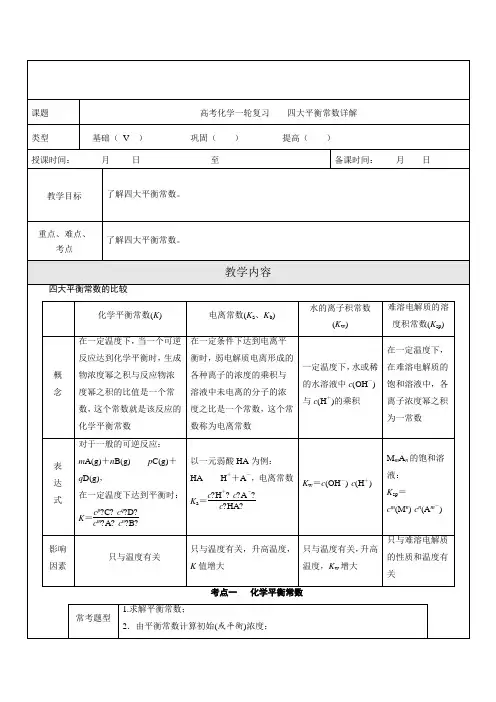
对于一般的可逆反应:m A(g)+n B(g)p C(g)+q D(g),在一定温度下达到平衡时:K=c p?C?·c q?D?c m?A?·c n?B?以一元弱酸HA为例:HA H++A-,电离常数K a=c?H+?·c?A-?c?HA?3.计算转化率(或产率);4.应用平衡常数K 判断平衡移动的方向(或放热、吸热等情况)。
对 策从基础的地方入手,如速率计算、“三阶段式”的运用、阿伏加德罗定律及其推论的应用、计算转化率等,这些都与化学平衡常数密不可分(严格讲电离平衡、水解平衡、沉淀溶解平衡也是化学平衡,只是在溶液中进行的特定类型的反应而已),要在练习中多反思,提高应试能力。
1.高炉炼铁过程中发生的主要反应为13Fe 2O 3(s)+CO(g)23Fe(s)+CO 2(g)。
已知该反应在不同温度下的平衡常数如下:温度/℃ 1 000 1 150 1 300 平衡常数4.03.73.5请回答下列问题:(1)该反应的平衡常数表达式K =________,ΔH ________0(填“>”“<”或“=”);(2)在一个容积为10 L 的密闭容器中,1 000 ℃时加入Fe 、Fe 2O 3、CO 、CO 2各1.0 mol ,反应经过10 min 后达到平衡。
求该时间范围内反应的平均反应速率v (CO 2)=________,CO 的平衡转化率=________。
2.已知可逆反应:M(g)+N(g)P(g)+Q(g) ΔH >0,请回答下列问题:(1)在某温度下,反应物的起始浓度分别为:c (M)=1 mol/L ,c (N)=2.4 mol/L ;达到平衡后,M 的转化率为60%,此时N 的转化率为________。
(2)若反应温度升高,M 的转化率________(填“增大”“减小”或“不变”)。
(3)若反应温度不变,反应物的起始浓度分别为:c (M)=4 mol /L ,c (N)=a mol/L ;达到平衡后,c (P)=2 mol/L ,a =________。
