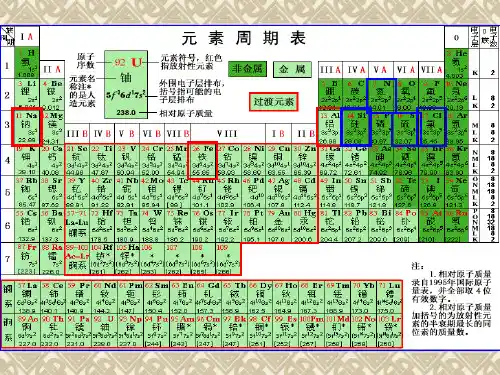
Fe2O3 不溶
相应酸或氢氧化物的制备 规律
CO2 SiO2 Na2O CaO
H2CO3 SiO32-
NaOH
Ca(OH)2
H2SiO3
若对应的氧化物可 溶,则直接与水反 应生成相应的酸或 碱;若对应的氧化 物不溶,可使氧化 物溶于酸或碱生成
Fe2O3 Fe3+ Fe(OH)3
盐,再加入碱或酸 生成对应的碱或酸
目标导航 预习导引
3.硅胶
知识梳理 典例透析
一、CO2与SiO2的比较 CO2
构成
CO2 分子
物理性质
与碱性氧 化物反应 与碱溶液 的反应
气体,熔点、沸点低,溶 于水
CaO+CO2 CaCO3
2NaOH+CO2 Na2CO3+H2O
SiO2 硅原子、氧原子,无 SiO2 分 子 固体,熔点、沸点高, 硬度大,不溶于水
二、二氧化硅的结构与性质 1.存在
石英、水晶、玛瑙、光导纤维、沙子的主要成分是SiO2。 2.结构
SiO2晶体是由Si和O按1∶2的比例组成的立体网状结构的晶体, 每个Si与4个O结合,每个O与2个Si结合。
目标导航 预习导引
3.物理性质 熔点 高
4.化学性质
硬度 大
溶解性 不溶于水
目标导航 预习导引
与碳反应 C+CO2 2CO
2C+SiO2 Si+2CO↑
与 H2O 作用
CO2+H2O H2CO3
不与水化合
与酸反应 不反应
只与氢氟酸反应 SiO2+4HF SiF4↑+2H2O
相同点 都是酸性氧化物,与碱反应生成盐和水
知识梳理 典例透析