初中化学第一章知识网络图精品PPT课件
- 格式:ppt
- 大小:242.00 KB
- 文档页数:41
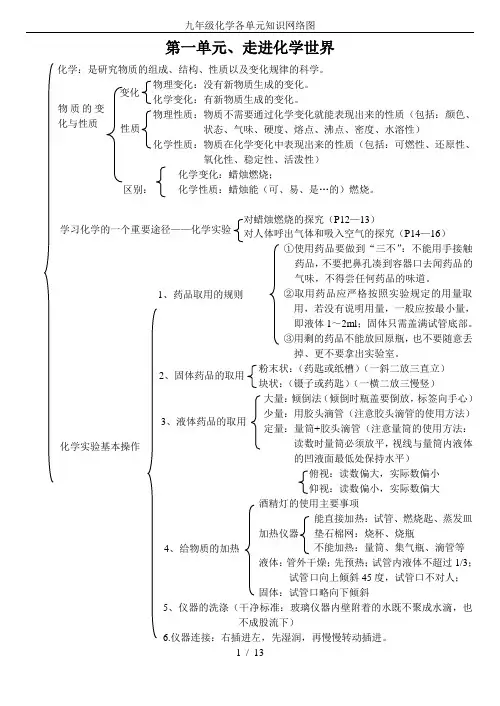
第一单元、走进化学世界化学:是研究物质的组成、结构、性质以及变化规律的科学。
物理变化:没有新物质生成的变化。
化学变化:有新物质生成的变化。
物理性质:物质不需要通过化学变化就能表现出来的性质(包括:颜色、状态、气味、硬度、熔点、沸点、密度、水溶性)化学性质:物质在化学变化中表现出来的性质(包括:可燃性、还原性、氧化性、稳定性、活泼性)化学变化:蜡烛燃烧;区别: 化学性质:蜡烛能(可、易、是…的)燃烧。
对蜡烛燃烧的探究(P12—13)对人体呼出气体和吸入空气的探究(P14—16) ①使用药品要做到“三不”:不能用手接触药品,不要把鼻孔凑到容器口去闻药品的气味,不得尝任何药品的味道。
②取用药品应严格按照实验规定的用量取用,若没有说明用量,一般应按最小量,即液体1~2ml ;固体只需盖满试管底部。
③用剩的药品不能放回原瓶,也不要随意丢掉、更不要拿出实验室。
粉末状:(药匙或纸槽)(一斜二放三直立) 块状:(镊子或药匙)(一横二放三慢竖)大量:倾倒法(倾倒时瓶盖要倒放,标签向手心) 少量:用胶头滴管(注意胶头滴管的使用方法) 定量:量筒+胶头滴管(注意量筒的使用方法:读数时量筒必须放平,视线与量筒内液体的凹液面最低处保持水平)俯视:读数偏大,实际数偏小 仰视:读数偏小,实际数偏大 酒精灯的使用主要事项能直接加热:试管、燃烧匙、蒸发皿 加热仪器 垫石棉网:烧杯、烧瓶不能加热:量筒、集气瓶、滴管等 液体:管外干燥;先预热;试管内液体不超过1/3;试管口向上倾斜45度,试管口不对人;固体:试管口略向下倾斜5、仪器的洗涤(干净标准:玻璃仪器内壁附着的水既不聚成水滴,也不成股流下)6.仪器连接:右插进左,先湿润,再慢慢转动插进。
变化 物质的变化与性质 性质 学习化学的一个重要途径——化学实验 1、药品取用的规则2、固体药品的取用3、液体药品的取用4、给物质的加热 化学实验基本操作第二单元、我们周围的空气、物性:无色无味的气体,密度比空气略小,难溶于水2、化性:不能燃烧,不支持燃烧,不能呼吸、用途:1、氧气含量的实验测定(用红磷在空气中燃烧)实验现象:①红磷燃烧,产生大量白烟;②水进入瓶中大约占瓶体积的1/5化学方程式:4P + 5O 2 ===== 2P 2O 5结论:氧气约占空气体积的1/5①红磷量不足②装置漏气 ③瓶未冷却就打开夹子2、物性:无色无味的气体,密度比空气大,不易溶于水,在一定条件下可液化为淡蓝色液态氧,也可固化为淡蓝色的固态氧。





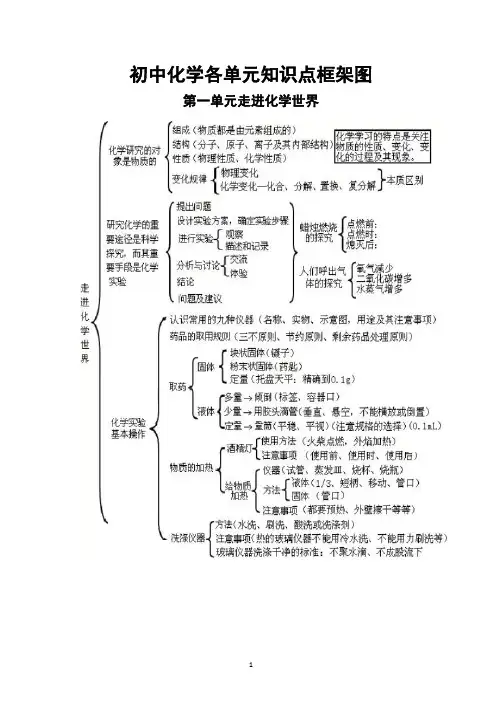
第一单元走进化学世界走进化学世界化学研究的领域:①制造新物质②合成新药物③开发新能源④防止环境污染。
物质变化性质化学一门实验基础科学化学验的本操作第二单元我们周围的空气我们周围的空气氮气(N2)(78%)性质用途:作化工原料;作保护气;作冷冻剂;制造低温环境。
物理性质:无色无味气体,不易溶于水。
化学性质:不活泼,一般不能燃烧,也不支持燃烧。
稀有气体(0.94%)性质:无色无味气体,化学性质不活泼。
用途:作保护气;作电光源;激光技术;冷冻剂;麻醉剂。
二氧化碳(0.03%);其他气体和杂质(0.03%)氧气(O2)(21%)物理性质:无色无味的气体,密度比空气大,不易溶于水。
化学性质(比较活泼,具有氧化性,是常用的氧化剂)C + O2点燃CO22C + O2点燃2COS + O2点燃SO24P + 5O2点燃2P2O53Fe + 2O2点燃Fe3O42Mg + O2点燃2MgO4Al + 3O2点燃2Al2O32H2 + O2点燃2H2O2CO + O2点燃2CO24+ 2O2点燃CO2 + 2H2O(白光、放热、澄清的石灰水变浑浊)(蓝紫色火焰、放热、有刺激性气味)(产生白烟、放热、白色固体)(剧烈燃烧,火星四射、黑色固体)(耀眼的白光、放热、白色固体)(耀眼的白光、放热、白色固体)(淡蓝色或蓝色火焰,干冷烧杯壁有无水滴,沾石灰水的烧杯壁是否浑浊)制法工业制法:分离液态空气法(物理变化)实验室制原理2H2O22H2O+O2↑2KClO32KCl + 3O2 ↑2KMnO4K2MnO4 + MnO2 + O2↑发生装置:固体+液体反应不需加热或固体+固体反应需要加热收集装置大)实验步骤:查、装、定、点、收、离、熄注意事项:先撤导管,后熄灭酒精灯等7点。
检验:将带火星的木条放入瓶中,木条复燃。
验满:将带火星的木条放入瓶口,木条复燃。
用途供给呼吸:动植物呼吸、潜水、登山、医疗、宇航。
支持燃烧:炼钢、气焊、化工生产、宇航。
初中化学各单元知识点框架图第一单元走进化学世界第二单元我们周围的空气第三单元自然界的水第四单元物质构成的奥秘第五单元化学方程式第六单元碳和碳的氧化物第七单元燃料及其利用第八单元金属和金属材料第九单元溶液第十单元 酸、碱、盐(一)化学用语1电离方程式:-++=24422SO H SO H ;-++=OH Na NaOH ;-++=24334232)(SO Al SO Al2物质的俗称和主要成分:生石灰CaO ;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO 3;食盐的主要成分NaCl ;纯碱、口碱Na 2CO 3;烧碱、火碱、苛性钠NaOH ;胆矾、蓝矾CuSO 4·5H 2O ;碳酸钠晶体Na 2CO 3·10H 2O ;氨水NH 3·H 2O 。
(二)金属活动性 1金属活动性顺序:K >Ca >Na >Mg >Al >Zn >Fe >Sn >Pb(H)Cu >Hg >Ag >Pt >Au 2金属活动性顺序的意义:在金属活动顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失去电子而变成离子,它的活动性就越强。
3金属活动性顺序的应用:⑴排在氢前的金属能置换出酸里的氢(元素)。
⑵排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K 、Ca、Na除外)。
(三)酸、碱、盐的溶解性1常见盐与碱的溶解性钾(盐)、钠(盐)铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2八个常见的沉淀物氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3四微溶物Ca(OH)2(石灰水注明:澄清“的原因)CaSO4(实验室制二氧化碳时不用稀硫酸的原因)Ag2SO4(鉴别-24SO和-Cl时,不用硝酸银的原因)MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4三个不存在的物质氢氧化银、碳酸铝、碳酸铁(四)复分解反应发生的条件反应有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)1、不溶性碱只能与酸性发生中和反应;2、不溶性盐,只有碳酸盐能与酸反应;3、KNO3、NaNO3、AgNO3、BaSO4不能做复分解反应的反应物。


第一单元走进化学世界1、锅炉爆炸、轮胎爆炸是物理变化,可燃性物质导致的爆炸是化学变化,如氢气爆炸,烟花爆炸等。
2、催化剂能加快和减慢反应速率,其质量和化学性质反应前后不变,物理性质,如形状、状态可能改变3、由一种元素组成的物质可能为单质,也可能为混合物。
如氧气O2和臭氧O3两种单质混合得到混合物,也只由氧(O)元素组成。
金刚石C和石墨C的混合物,只由碳(C)元素组成等。
只有说由一种元素组成的纯净物,才能说一定是单质。
冰水混合物是纯净物,冰是水的固态,还是水。
4、原子是化学变化中的最小粒子。
但不能说原子一定就比分子小。
原子是化学变化中的最小粒子,在化学变化中不可再分。
但是某些物理变化中是可再分(核裂变)的二、三、六、八、十、十一单元身边的化学物质七、十二单元化学能源和社会发展第二单元我们周围的空气测氧气含量实验失败原因:红磷量不足,装置漏气,未等到装置冷却就打开弹簧夹不是所有的燃烧都需氧气参与。
如氢气在氯气中能燃烧。
着火点是物质的固有属性,不能说降低物质的着火点,只能说把温度升高到物质的着火点。
燃烧需三个条件都具备,灭火只要破坏任一条件。
第三单元自然界的水沉淀有静置沉淀和吸附沉淀。
吸附沉淀是指加明矾生成胶体吸附大颗粒固体杂质,获得比静置沉淀更快的沉淀。
过滤是在沉淀后,把不溶于水的沉淀和水分离的操作。
若单独提到吸附,则是指加活性炭吸附色素和气体。
蒸馏后得到的水净化程度最高,为蒸馏水,是纯净物。
蒸馏操作可以使硬水软化第四单元物质构成的奥秘原子团的记忆找诀窍:如碳酸根CO3,就是二氧化碳CO2多1个O。
硫酸根SO4,是三氧化硫SO3多1个O。
硝酸根NO3,是二氧化氮NO2多1个O。
铵根NH4,是氨气NH3多1 个O.第五单元化学方程式1、如点燃A克氧气和B克氢气的混合气体,生成水的质量是小于或等于(A+B)克。
氧气和氢气要么恰好按质量比完全反应,都不剩余,则生成水质量等于(A+B)克。
要么,氢气过量剩余或者氧气过量剩余,有一种没有全部反应,则生成水质量小于(A+B)克。