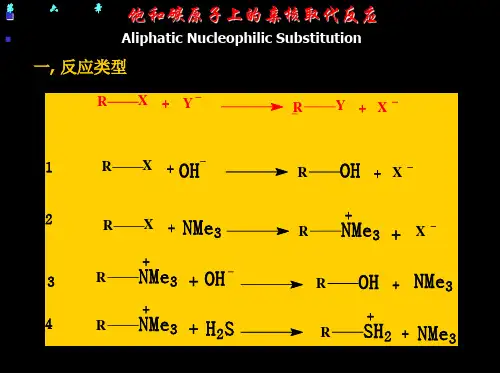
第八章 饱和碳原子上的亲核取代反应
- 格式:pdf
- 大小:2.65 MB
- 文档页数:59





有机化学基础知识点碳原子的亲核取代反应亲核取代反应是有机化学中重要的反应类型之一。
在这篇文章里,我将介绍碳原子的亲核取代反应的基础知识点。
亲核取代反应是一种化学反应,涉及到一个亲核试剂攻击一个电子云密度较低的碳原子,并将其取代。
这种反应可以发生在饱和碳原子上,也可以在环上的碳原子上发生。
1. 亲核试剂的选择亲核试剂是亲核取代反应中至关重要的一部分。
常见的亲核试剂包括卤代烷、醇、胺等。
选择适当的亲核试剂可以有效地促进反应的进行。
2. 亲核试剂的攻击在亲核取代反应中,亲核试剂攻击碳原子的位置非常重要。
碳原子可以通过两种方式进行亲核攻击:SN1和SN2机理。
- SN1机制:这是一种两步反应,首先,亲核试剂离去一个离子,形成一个带电的中间体。
然后,亲核试剂攻击中间体上的位点,取代离去的离子。
- SN2机制:这是一种一步反应,亲核试剂直接攻击碳原子,并同时取代离去的基团。
3. 碳原子的离去基团在亲核取代反应中,碳原子上的离去基团是影响反应速率和反应机理的重要因素。
常见的离去基团包括卤素原子、氨基和醇基等。
不同的离去基团会导致不同的反应速率和产物选择。
4. 反应条件的影响亲核取代反应的条件也会对反应的进行产生影响。
常见的反应条件包括溶剂的选择、温度和反应时间等。
选择合适的反应条件可以提高反应的收率和选择性。
5. 反应机理的解释了解亲核取代反应的机理对于理解反应过程和预测产物是非常重要的。
通过观察亲核试剂攻击碳原子的位置、反应速率以及产物选择等因素,可以确定反应机理。
在总结中,亲核取代反应是有机化学中基本的反应类型之一。
了解碳原子的亲核取代反应的基础知识点可以帮助我们理解反应机理、预测产物以及进行有机合成的设计。
当然,亲核取代反应还有很多细节和应用等待我们深入探索和学习。


影响亲核取代反应的因素摘要亲核取代反应是有机化学中一类重要的反应,饱和碳原子上的亲核取代反应可按S N1和S N2两种不同历程进行。
亲核取代反应的两种历程,在反应中同时存在,相互竞争。
对同一反应物来说,在不同的反应条件下反应速率是不同的;在相同的条件下,不同的反应物的活性也不同。
本文讨论了影响亲核取代反应的因素,并总结了某些规律。
关键词亲核取代反应速率影响因素卤代烃的亲核取代反应是一类重要的反应。
由于这类反应可用于各种官能团的转变以及碳碳键的形成,因此在有机合成中具有广泛用途。
本文将以卤代烃的亲核取代反应为例,讨论影响亲核取代反应的因素,即亲核取代反应的反应活性。
大量研究表明,亲核取代反应的活性与反应物的结构(包括烃基和离去基团的结构)、亲核试剂的亲核性和溶剂的性质等因素都有密切的联系。
1反应物的结构1.1烃基的结构烃基的影响体现在两个方面,一个是电子效应,另一个是空间(立体)效应。
一般来说,烃基的电子效应对S N1反应的影响更大,烃基的空间效应对S N2反应的影响更显著。
1.1.1在S N2反应中,烃基的空间效应影响占主导地位,α—碳或β—碳上支链增加,阻碍了亲核试剂从离去基团的背面进攻,且会造成过渡态拥挤程度增加,降低了过渡态的稳定性,使反应速率明显下降。
例如,不同的烷基发生S N2反应的平均相对速度如下:R-CH3-CH3CH2-(CH3)2CH-相对速度30 1 2.5⨯10-2卤代烃按S N2机理进行的活性次序是:烯丙型、苄基型、甲基卤代烷>伯>仲>叔>乙烯型、芳卤、桥头卤代烷在烯丙卤、苄卤的S N2反应中,当亲核试剂进攻α-碳原子时,其反应过渡态应该有p轨道的重叠,旁边的碳碳双键能帮助它分散电荷,起稳定作用。
在乙烯型、芳卤的S N2反应中,因其分子中存在着p-π共轭,使碳卤键键长缩短,键能增加,卤原子不易离去。
桥头卤代烷因桥环的立体障碍,亲核试剂不能从背面进攻α-碳原子,故不易发生S N2反应。


Nu +C LNu CNu C L 亲核取代反应一.概说:脂肪族亲核取代反应是指有机分子中与碳相连的某原子或基团被作为亲核试剂的某原子或基团取代的反应。
在反应过程中,取代基团提供形成新键的一对电子,而被取代的基团则带着旧键的一对电子离去(带着一对电子来,带着一对电子去)。
底物:受亲核试剂进攻的对象。
Nu:是亲核试剂,带有一对孤对电子。
与离去基团相连的碳原子叫做中心碳原子。
通式:R—L+Nu:R—Nu+L:二.亲核取代的反应速率与分类:按照机理的不同:如果反应速率只与底物浓度有关,那么这个反应是一级反应——S N1反应。
V=k[R—L]如果反应速率除了与底物浓度有关外,还与亲核试剂的浓度有关——S N2反应。
V=k[R—L][Nu:]按照底物一亲核试剂的性质来分:1.中性底物+ 中性亲核试剂2.中性底物+ 负离子亲核体3.正离子底物+ 中性亲核体4.正离子底物+ 负离子亲核体三.亲核取代的机理:反应速率呈现出两种情况,为了解释这两种情况,提出了两种机理——S N1,S N2。
1.S N2反应定义、机理、势能图定义:S N2反应又叫做双分子亲核取代反应。
有两种分子参与了决定反应速率关键步骤的亲核取代反应叫做双分子亲核取代反应。
可见该定义是从动力学角度来定义的。
机理:如图:亲核试剂从离去基团的背面进攻底物的中心碳原子,随着Nu:不断接近碳原子,Nu 上的负电荷逐渐减少到部分负电荷δ-,此时由于Nu:的不断接近C—L键不断延长L上有部分正电荷δ+,即在Nu…C键逐渐形成,C-L键逐渐裂解这时就形成了过渡态,这个过渡态由于5个原子所以很拥挤,可想该过渡态的能量很高。
随着反应进行,Nu和C成键,L作为离去基团从中心碳原子上离去,中心碳原子的杂化态也由sp2回到sp3。
特点:1) 从离去基团的背面进攻底物,协同的一步反应。
2)没有中间体产生。
3)旧键的断裂和新键的形成几乎同时发生对过渡态的描述:1. 当Nu向C逐渐进攻的同时,L以相反的方向逐渐离去,此过程中,Nu、C 和L在同一直线上,只有这样过渡态能量才能相对低。
影响亲核取代反应的因素2010-04-27 08:55饱和碳原子上的亲核取代反应可按SN1和SN2两种不同历程进行。
亲核取代反应的两种历程,在反应中同时存在,相互竞争。
但对一种反应物来说, 在一定条件下, 与亲核试剂作用时, 我们能否知道, 反应究竟按什么历程进行?如果对不同的反应物, 我们能否预计哪一个快, 哪一个慢?对于这样类似的一系列问题, 通过许多科学家的研究, 现在已经找到明确而肯定的答案。
研究表明, 反应历程和反应活性与反应物中的烃基结构, 离去基团性质, 亲核试剂性质以及溶剂性质等因素都有关系, 下面分别讨论。
5.5.1烃基结构的影响影响反应历程的因素很多,卤代烃本身结构是主要因素之一。
在卤代烃分子中,反应中心是a-C原子。
a-C原子上电子密度的高低,直接影响反应历程。
如果a-C原子上电子密度低,则有利于Nu-进攻,有利于反应按双分子历程进行。
反之,如果a-C原子上电子密度高,则有利于卤素夺取电子而以X-的形式离解,所以有利于按单分子历程进行反应.从反应中间体来看如果能形成稳定的正离子,则有利于反应按SN1历程进行。
反之,则有利于SN2历程。
烃基结构对亲核取代反应的影响, 可以通过分析烃基的电子效应和空间效应来确定。
先看看SN1和SN2两个决速步骤中过渡态的结构(见表5.8)。
表5.8 SN1和SN2过渡态结构反应历程SN2SN1过渡态结构电荷分散集中体积比反应物拥挤比反应物宽松在卤代烃的亲核取代反应中, 烃基的立体效应和电子效应对SN1和SN2影响程度不同。
对SN2历程,烃基的立体效应是主要的,而对SN1历程,烃基的电子效应是主要的。
5.5.1.1 烃基的立体效应由于SN2历程中形成的过渡态比较拥挤, 所以SN2历程对烃基的立体效应比较敏感。
(1)当中心碳原子上的支链增多时, 不利于SN2反应, 有利于SN1反应。
考虑立体因素时,伯卤代烃有利于SN2反应,叔卤代烃有利于SN1反应。