第九章 反应活性中间体-卡宾、乃春、芳炔
- 格式:ppt
- 大小:4.60 MB
- 文档页数:36




浅谈有机化学反应中的活性中间体王敏 2005110031 西北大学化学系化学专业摘要:有机反应活性中间体在有机化学中占有极其重要的地位。
本文简要的介绍了基础有机化学反应中涉及到的几种反应活性中间体——碳正离子、碳负离子和自由基。
关键词:活性中间体,碳正离子,碳负离子,自由基学习《有机化学》有一学期了,我个人觉得有机化学反应的机理非常有趣,现抽空将所学的有机化学反应机理里牵扯的一些活性中间体介绍给大家,希望能对大家以后的学习有所帮助。
研究反应机理时,需要用一组基元反应来解释反应过程。
要用几个基元反应才能描述整个反应过程的反应称为复杂反应,在这些反应中常经过一个或多个基元反应才能形成反应活性中间体,然后再经过一个或者几个基元反应达到最终产物。
在复杂反应中,沿着反应坐标常出现多个最高能垒,在每两个能垒之间有一个最低能垒,具有这种最低能垒的结构及称为反应活性中间体。
有机反应中的机理大多是分步进行的,在这些反应过程中常生成经典碳正离子、碳负离子、自由基等活性中间体。
下面就对以上几种活性中间体进行简单的描述。
1、 碳正离子1.1、碳正离子的结构碳正离子的中心碳原子为sp 2杂化,中心碳原子即与其相连的三个原子在同一平面内,在与平面垂直的方向,有一个空的p 轨道,如下图:C 23R 1NuC 2R R 1NuSP 2平面结构1.2、经典碳正离子是有机反应中的重要中间体。
S N 1亲核取代反应、双键亲电加成、芳香亲电取代反应等都能生成碳正离子中间体。
以下分几种情况对碳正离子的生成进行介绍。
1.2.1、当取代中心为叔碳原子时,易于形成碳正离子,按S N 1机理进行反应。
例如反应:CH 3C Br CH 3CH 3NaOH H 2OK CH 3CH 3CH 3C Br CH 3C OH CH 3CH 3NaBr+ν=+其反应机理为: BrCH 3C CH 3CH 3Br C Br CH 3CH 3CH 3CH 3C CH 3CH 3OH CH 3C CH 3CH 3CH 3C CH 3CH 3OH CH 3C CH 3CH 3OH 第一步慢过渡态1中间体+第二步+快过渡态2δδδδ1.2.2、在双键与卤化氢的加成反应中必须先生成碳正离子中间体,才能生成重排产物,例如对反应:CH 3C CH 3CH 3CH CH 2HClCH 3C CH 3CH 3CHCH 3Cl CH 3C Cl CH 3CH CH 3CH 3+17%83%CH 3C CH 3CH 3CH 3C CH 3CH 3CH CH 3ClCH 3C CH CH 3CH CH 3Cl CH 3C Cl CH 3CH CH 3CH 383%CH 3C CH 3CH 3CHCH 3Cl 17%重排主要产物为后者,这是因为反应过程中生成的仲碳正离子通过甲基的迁移,重排成了更稳定的叔碳正离子。





关于有机活性中间体乃春的研究摘要:乃春是合成含氮化合物的一类重要的有机活性中间体,具有反应活性高、反应类型多样等特点,在材料学、生命科学等高新科技领域中有着广泛的应用。
本文主要综述了有机活性中间体乃春的产生,以及各种化学反应反应。
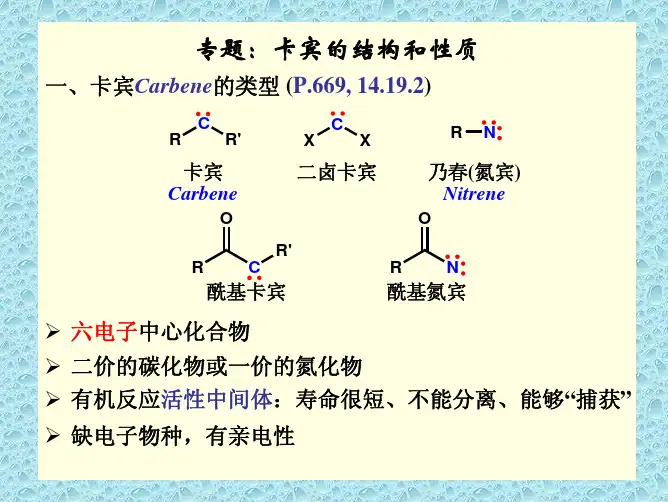
关键词:乃春乃春结构活性中间体乃春反应乃春是与碳烯等电子的类似物,是含有一价氮、不带电荷的活性中间体。
其氮原子周围只有6个价电子,属于缺电子体系。
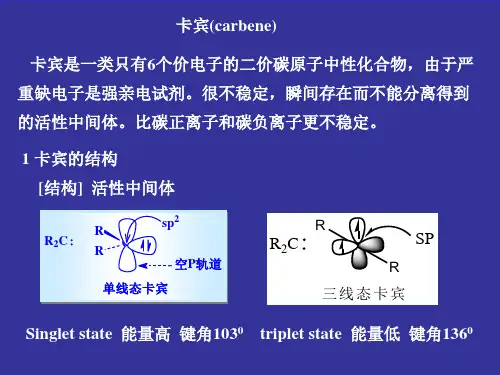
在乃春的氮原子中,一对电子与相连的原子生成6键,另外一对电子定域在氮原子的一个轨道上,剩下的两个电子则存在自旋反平行和自旋平行两种电子状态,分别为单重态和三重态。
乃春可通过叠氮化合物的分解、α-消除反应、伯氨基的氧化、硝基化合物的脱氧、羟胺磺酸酯分解反应以及酰胺降解等方法来得到[1、2]。
下面重点介绍关于乃春的反应性和应用的新近研究进展。
一,乃春的产生乃春可以看作是卡宾的氮类衍生物, 从讨论生成卡宾的反应途径类推有下述产生的可能性:1,直接生成:直线断裂,例如:2,以分步方式生成:先生成游离基再生成乃春例如:3,氧化作用:一级氨基的氧化作用是由原子团-NH2除去两个氢原子(或H+及H-)能生成乃春。
例如:4,还原作用:硝基化合物的脱氧作用是将硝基化合物和亚磷酸三乙醋共热, 则把氧转称给磷生成磷酸盐。
反应产物和由相应的氮化合物分解生成的产物相同, 这表明在此反应过程中生成乃春。
例如:二,乃春的反应1,加成反应:涉及到乃春的一个非常重要的反应就是与烯烃双键的加成反应,可形成用以合成含氮官能团化合物的多用途中间体—氮杂环丙烷,其所表现出的亲电反应性、立体选择性使之成为有机合成中的有用构件。
乃春与烯烃发生氮杂环丙烷化反应有很多种反应形式,该类反应是氮原子进攻双键发生环加成,因此随着乃春的电子自旋状态不同,加成产物也不完全相同。
单线态乃春与烯烃的加成具有立体专一性,而二线态乃春因是双自由基,故与烯烃加成时为非立体专一性。
Mansuy等[3、4]以对甲苯磺酰亚胺碘苯(Phi=NTs)为氮源,所使用的催化剂是四苯基卟啉(TPP)和四—(2,6-二氯)苯基(TDCPP)作为配体形成的以Mn、Fe为中心金属离子的配合物,催化反应合成N-对甲苯磺酰氮杂环丙烷,他们系统地研究了不同脂肪族烯烃和芳香族烯烃的氮杂环丙烷化反应。
2 有机反应活性中间体有4种含碳原子的有机活性物种,它们一般只成2或3键,非常活泼,寿命很短,仅以中间体的形式存在并迅速转化为稳定的分子(其中也有些稳定的中间体可以分离出来)。
这4种活性中间体是碳正离子、碳负离子、自由基和碳烯(卡宾),其中只有碳负离子具8电子结构。
除上述4种含碳的活性中间体之外,还有一些其它原子也因为带有电荷或孤对电子而成为有机反应的活性中间体,其中最重要的是氮烯(乃春)。
2.1碳正离子提示:命名自1902年以来,这些物种一直被称为碳鎓离子(carbonium ions)。
由于“鎓”(-nium)通常指成键数高于中性原子的离子,所以,这一叫法并不合理。
1971年,Olah提出将碳鎓离子(carbonium ions)保留给成5键带正电荷的碳,而用碳正离子(carbocations)命名3配位的带正电荷的碳。
1987年,IUPAC接受了上述定义。
2.1.1形成与反应(1)形成碳正离子,不论其稳定与否,一般通过两种途径形成:①直接离子化,与碳原子相连的基团带着原来共用的一对电子离去:②质子或其它正电荷物种加到不饱和体系的一个原子上,从而在其相邻的碳原子上形成正电荷:由于碳正离子是短寿命的过渡物种,所以,不论它以何种方式产生,一般都不经分离直接继续反应。
(2)反应碳正离子反应形成稳定产物的两种主要方式恰恰是其两种主要形成方式的逆反应。
①碳正离子可以和拥有孤对电子的物种反应(路易斯酸碱的反应)这些拥有孤对电子的物种可以是羟基负离子、卤素离子或其它负离子,也可以是带有可共享的孤对电子的中性物种(此时产生的中间产物也会带有正电荷)。
②碳正离子可以从相邻的原子上脱去氢或其它正离子(消除反应)除生成稳定产物外,碳正离子还可以通过反应得到新的碳正离子。
③重排重排后的碳正离子较原碳正离子稳定,之后,新碳正离子可能按①或②生成稳定的产物。
④加成碳正离子可以加到双键上,在新位置上再形成一个正离子,而这个新的碳正离子还可以继续往双键上加成,这也是烯烃聚合的机理之一。
有机化学试卷班级姓名分数一、选择题 ( 共 91 题 182 分 ) 1. 2分 (4002)4002(C H) C HCH C(CH ) C H CH3 2 2 3 2 2 3的 CCS 名称应是:(A) 1,4,三4-甲基己烷(B) 3,3,三5-甲基己烷(C)2甲-基辛烷(D) 2,4,三4-甲基己烷2. 2 分 (4003)4003CH3左式,CCS 名称应是:CH3(A)2,5二- 甲基萘(B) 1,6二- 甲基萘(C)1,5二- 甲基萘(D) 2,10二- 甲基萘3. 2 分 (4004)4004化合物 1-甲基-1,3环-十二碳二烯(如图),如需说明两个烯键的构型,应当在上述名称前加上:(A)1E,3Z(B)1Z,3Z(C)1E,3E(D)1Z,3ECH 324. 2 分 (4005) 4005(I 式)是 2-丁醇的一个构型异构体,它跟哪个式子构型一样? H(I 式)CH 3OH CH 2CH 3(A) OH (B) CH 3 (C) C 2H 5 (D) CH 2CH 3 C H 3 H H O H C H 3 OH OH CH 3CH 2C H 3 CH 2C H3 H H5. 2 分 (4006)4006以下分子两个手性碳的构型是: (A) 2R ,3R (B) 2R ,3S(C) 2S ,3R(D) 2S,3SH Br CH CH23BrCH 3H6. 2 分 (4007) 4007Cl CH 3 C C分子中,烯键的构型,可以加前缀:CH 3H(A ) E 或顺(B)Z 或顺(C)E 或反(D ) Z 或反7. 2 分 (4008) 4008H(CH 3)2CH C推断左式手性碳的构型,应是:CH CHOH(A) (CH ) C H ─ 比 CH = CH ─优先,所以是 R3 22CH 3(B) (CH) C H ─ 比 CH = CH ─优先,所以是 S3 2 2(C) CH = C H ─ 比 (CH ) C H ─优先,所以是 R 2 (D) C H= C H ─ 比 (CH 3 2 ) C H ─优先,所以是 S 23 28. 2 分 (4009) 4009ClOH共有几个立体异构体?(A) 2 个(B)3 个(C)4 个(D)5 个9. 2 分 (4012) 4012以下四个芳烃,熔点最高的是:(A )CH 2CH 3CH 3 ( ) (D )(B )CH 3CCH 3CH 3*. 2 分 (4013) 4013以下四个化合物,在水中溶解度最大的是:(A)CH 3COOCH 2CH 3(B)HCOOCH 2CH 2CH 3(C)CH 3CH 2CH 2COOH(D)OO11. 2 分 (4014)4014以下四个溶剂, 密度比水大的是:(A) CH(CH3) C H2 83(B)(C) CH NO6 52(D) CH OC H2 52CH 3512. 2 分 (4015)4015以下C H 的异构体,哪一个燃烧发热量(kJ/mol最)小?6 10(A)(C)13. 2 分 (4016)4016以下四种离子,碱性最强的是: (A)HO -(B)CH O -3(B)(D)(C)C H O -(D)CH COO- 6 5 314. 2 分 (4017)4017以下四个试剂,亲核性最强的是:(A)NH(B)NH -(C)CHNH(D)(CH )N H3 2 3 2 3 215. 2 分 (4018)4018以下四个试剂,亲核性最强的是:(A)p-CH C H -O -3 64 (B)p-NO C H -O -2 6 4(C)p-ClC H6-O -4(D)p-CHOC3H -O -6416. 2 分 (4019) 4019IBP以下四个卤代烃,R 是一样的烃基,其中卤原子最简洁成为负离子离去的是: (A) R─I (B) R─Br (C) R─Cl (D) R─F17. 2 分 (4020) 4020以下四个化合物,作为碳素酸(carbon acid 哪),一个的酸性(即 C ─H 键中氢的活性)最大? (A)环戊烷(B)环戊烯 (C)1,3环- 戊二烯 (D)1,4环- 己二烯18. 2 分 (4021)4021反响物(B) 中间体(I) 产物(P) 的能量曲线如以以下图所示, 可以认为本反响是:势能O(A) 放热反响,速率打算步骤是第一步 (B) 放热反响,速率打算步骤是其次步 (C) 吸热反响,速率打算步骤是第一步 (D) 吸热反响,速率打算步骤是其次步反响坐标19. 2 分 (4022) 0035以下哪些不是自由基反响的特征? (A) 酸碱对反响有明显的催化作用 (B) 光、热、过氧化物能使反响加速(C) 氧、氧化氮、酚对反响有明显的抑制作用 (D) 溶剂极性变化对反响影响很小20. 2 分 (4023) 4023以下反响经过的主要活性中间体是:(A) 碳正离子(或离子对中碳原子为正电一端)(B)碳负离子(及烯醇盐负离子碎片)(C)卡宾(即碳烯 Carbene)(D)氮宾(即氮烯 Nitrene)(E)苯炔(Benzyne)OEtOOC CH 2CH2CH2CH2CO2Et NaOEtEtOHCO2Et21. 2 分 (4024)4024以下反响经过的主要活性中间体是:(A)碳正离子(或离子对中,碳原子为正电一端) (B)碳负离子(及烯醇盐负离子碎片)(C)卡宾(即碳烯Carbene)(D)乃春(即氮烯 Nitrene) (E)苯炔(Benzyne)ClKNH2* NH 2NH3( ¨)+NH222. 2 分 (4025)4025以下反响经过的主要活性中间体是:(A)碳正离子(或离子对中,碳原子为正电一端)(B)碳负离子(及烯醇盐负离子碎片)(C)卡宾(即碳烯 Carbene)(D)乃春(即氮烯 Nitrene)(E)苯炔(Benzyne)CONH2NH2Br2 +NaOH+ CO 223. 2 分 (4026)4026以下反响经过的主要活性中间体是:CH3COCH N(1) Ag2O2(2) HO +CH3CH2COOH +N 2**3(A) 碳正离子(或离子对中,碳原子为正电一端) (B) 碳负离子(及烯醇盐负离子碎片) (C) 卡宾(即碳烯 Carbene) (D) 氮宾(即氮烯 Nitrene) (E) 苯炔(Benzyne)24. 2 分 (4027) 4027以下反响经过的主要活性中间体是:(A) 碳正离子(或离子对中碳原子为正电一端) (B) 碳负离子(及烯醇盐负离子碎片) (C) 卡宾(即碳烯 Carbene) (D) 乃春(即氮烯 Nitrene) (E) 苯炔(Benzyne)CH CH 2H +2CH 3Ph25. 2 分 (4028) 4028以下四个氯代烃,最简洁发生 S 2 的是:N(A) CH CH CH CH Cl(B) (CH ) C HCH Cl 3 22 23 22(C) CHCHCH(Cl)C H(D) (CH ) C Cl3233 326. 2 分 (4029)4029以下四个氯代烯烃,最简洁消去 HCl 的是:CH 2CH 2CH 2CH 2Cl CH 2CH 2CHCH 3(A)(B)Cl(C)CHCH 2CH 2CH 3 Cl(D)ClCH 327. 2 分 (4030) 4030用KOH/CH OH 处理(CH ) C HCHClCH CH ,主要产物可能是: 2 5 3 2 2 3(A)反-4-甲基-2-戊烯 (B)顺-4-甲基-2-戊烯 (C)2-甲基-2-戊烯 (D)反-2-甲基-2-戊烯28. 2 分 (4032)4032-甲基萘跟 Cl /Fe 反响得到的主要一氯取代产物是:2(A)(B)(C)Cl(D)Cl CH 2ClCl29. 2 分 (4033)4033用(1)CH CH MgBr (2)H O 处理乙酰乙酸乙酯得到的是:3 2 2(A) CH COCH (C H )COOEt (B) CHCOCH(CH )C(OH)(C H )32 532 5 2 5 2(C) CH CH3C(OH)(C H2)C H3COOEt(D) CH 2COCH3COOEt230. 2 分 (4034) 4034如以以下图化合物被EtONa/EtOH 作用,主要得到:H(A) C H 6 CH(C H5)CH = C H ( )3 2 H 3C OTs(B) C H 6 C(CH5 2)= C H52(C) E -C H 6 C(C H 5)= C H(CH ) 3 3 PhCH 3(D) Z -C H 6 C(C H5)= C H(CH )33CH 3CH 3HCl ClClCl ClCl(A)31. 2 分 (4036)4036CH C ≡C ─CH = CH 经 Lindlar 催化(Pd/BaSO /喹啉)加氢的产物是:32432. 2 分 (4037)4037先跟C H CO H 反响 , 再在OH -溶液中水解 , 主要产物是:6 52(A)(C)OH(±)(B)(D)OH(±)OH33. 2 分 (4038) 4038以下 1,2,3,4,5,六6-氯环己烷的四个异构体,消去 H Cl 最慢的是:Cl ClCl Cl(B)(C) Cl Cl Cl(D)Cl Cl ClClClClCl ClCl ClCl34. 2 分 (4039) 4039(CH 3)2C CHCH 3 与 1 ( 3)2)/TH (F BH , 2( ) Na 2O O H 2//H H 2O 反响的产物是:(A) (CH 3)2C(OH )CH(OH )CH 33)2C(OH )CH(OH (B ))C H(3CH(± ) (C) (CH 3)2C(OH )CH 2CH 3) (CH 3)2CH C H(OH )CH 3(D ± ( )OH O H O HNO 2NO 2NO 235. 2 分 (4040) 40402-甲氧基萘跟 HCONHCH /POCl反响后水解主要产物是:6 53(A) 2甲- 氧基-1-萘甲醛 (B)N -苯基-2-甲氧基-1-萘胺 (C) 6甲- 氧基-1-萘甲醛(D) N -苯基-6-甲氧基-1-萘胺36. 2 分 (4041)4041萘与CHCOCl/ 无水AlCl / PhNO在25℃反响,和萘与CHCOCl/AlCl/CS在-15℃332332反响。
关于有机活性中间体乃春的研究摘要:乃春是合成含氮化合物的一类重要的有机活性中间体,具有反应活性高、反应类型多样等特点,在材料学、生命科学等高新科技领域中有着广泛的应用。
本文主要综述了有机活性中间体乃春的产生,以及各种化学反应反应。
关键词:乃春乃春结构活性中间体乃春反应乃春是与碳烯等电子的类似物,是含有一价氮、不带电荷的活性中间体。
其氮原子周围只有6个价电子,属于缺电子体系。
在乃春的氮原子中,一对电子与相连的原子生成6键,另外一对电子定域在氮原子的一个轨道上,剩下的两个电子则存在自旋反平行和自旋平行两种电子状态,分别为单重态和三重态。
乃春可通过叠氮化合物的分解、α-消除反应、伯氨基的氧化、硝基化合物的脱氧、羟胺磺酸酯分解反应以及酰胺降解等方法来得到[1、2]。
下面重点介绍关于乃春的反应性和应用的新近研究进展。
一,乃春的产生乃春可以看作是卡宾的氮类衍生物, 从讨论生成卡宾的反应途径类推有下述产生的可能性:1,直接生成:直线断裂,例如:2, 以分步方式生成:先生成游离基再生成乃春例如:3, 氧化作用:一级氨基的氧化作用是由原子团-NH2除去两个氢原子(或H+及H-)能生成乃春。
例如:4, 还原作用:硝基化合物的脱氧作用是将硝基化合物和亚磷酸三乙醋共热, 则把氧转称给磷生成磷酸盐。
反应产物和由相应的氮化合物分解生成的产物相同, 这表明在此反应过程中生成乃春。
例如:1二,乃春的反应1,加成反应:涉及到乃春的一个非常重要的反应就是与烯烃双键的加成反应,可形成用以合成含氮官能团化合物的多用途中间体―氮杂环丙烷,其所表现出的亲电反应性、立体选择性使之成为有机合成中的有用构件。
乃春与烯烃发生氮杂环丙烷化反应有很多种反应形式,该类反应是氮原子进攻双键发生环加成,因此随着乃春的电子自旋状态不同,加成产物也不完全相同。
单线态乃春与烯烃的加成具有立体专一性,而二线态乃春因是双自由基,故与烯烃加成时为非立体专一性。
感谢您的阅读,祝您生活愉快。