有机化学第二版(高占先)第五章习题答案
- 格式:doc
- 大小:920.00 KB
- 文档页数:6

有机化学答案高占先全 GE GROUP system office room 【GEIHUA16H-GEIHUA GEIHUA8Q8-有机化学(第二版)课后习题参考答案第一章绪论1-1 扼要解释下列术语.(1)有机化合物 (2) 键能、键的离解能 (3) 键长 (4) 极性键 (5) σ键(6)π键 (7) 活性中间体 (8) 亲电试剂 (9) 亲核试剂 (10)Lewis碱(11)溶剂化作用 (12) 诱导效应 (13)动力学控制反应 (14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9) 亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。

第一章绪论1-1 扼要解释下列术语.(1)有机化合物(2) 键能、键的离解能(3) 键长(4) 极性键(5) σ键(6)π键(7) 活性中间体(8) 亲电试剂(9) 亲核试剂(10)Lewis碱(11)溶剂化作用(12) 诱导效应(13)动力学控制反应(14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9) 亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10) Lewis碱:能提供电子对的物种称为Lewis碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。

徐寿昌编《有机化学》第二版习题参考答案第二章烷烃1、用系统命名法命名下列化合物(1)2,3,3,4-四甲基戊烷(2)3-甲基-4-异丙基庚烷(3)3,3,-二甲基戊烷(4)2,6-二甲基-3,6-二乙基辛烷(5)2,5-二甲基庚烷(6)2-甲基-3-乙基己烷(7)2,2,4-三甲基戊烷(8)2-甲基-3-乙基庚烷2、试写出下列化合物的结构式(1) (CH3)3CC(CH2)2CH2CH3(2) (CH3)2CHCH(CH3)CH2CH2CH2CH3 (3) (CH3)3CCH2CH(CH3)2(4) (CH3)2CHCH2C(CH3)(C2H5)CH2CH2CH3(5)(CH3)2CHCH(C2H5)CH2CH2CH3(6)CH3CH2CH(C2H5)2(7) (CH3)2CHCH(CH3)CH2CH3(8)CH3CH(CH3)CH2CH(C2H5)C(CH3)33、略4、下列各化合物的系统命名对吗?如有错,指出错在哪里?试正确命名之。
均有错,正确命名如下:(1)3-甲基戊烷(2)2,4-二甲基己烷(3)3-甲基十一烷(4)4-异丙基辛烷(5)4,4-二甲基辛烷(6)2,2,4-三甲基己烷5、(3)>(2)>(5)>(1) >(4)7、用纽曼投影式写出1,2-二溴乙烷最稳定及最不稳定的构象,并写出该构象的名称。
8、构象异构(1),(3)构造异构(4),(5)等同)2),(6)9、分子量为72的烷烃是戊烷及其异构体(1) C(CH3)4(2) CH3CH2CH2CH2CH3 (3) CH3CH(CH3)CH2CH3(4) 同(1)10、分子量为86的烷烃是己烷及其异构体(1)(CH3)2CHCH(CH3)CH3(2) CH3CH2CH2CH2CH2CH3 , (CH3)3CCH2CH3(3)CH3CH2CH(CH3)CH2CH3(4)CH3CH2CH2CH(CH3)214、(4)>(2)>(3)>(1)第三章烯烃1、略2、(1)CH2=CH—(2)CH3CH=CH—(3)CH2=CHCH2—3、(1)2-乙基-1-戊烯(2) 反-3,4-二甲基-3-庚烯(或(E)-3,4-二甲基-3-庚烯(3) (E)-2,4-二甲基-3-氯-3-己烯(4) (Z)-1-氟-2-氯-2-溴-1-碘乙烯(5) 反-5-甲基-2-庚烯或(E)-5-甲基-2-庚烯(6) 反-3,4-二甲基-5-乙基-3-庚烯(7) (E) -3-甲基-4-异丙基-3-庚烯(8) 反-3,4-二甲基-3-辛烯5、略6、7、活性中间体分别为:CH3CH2+CH3CH+CH3(CH3)3C+稳定性: CH3CH2+>CH3CH+CH3>(CH3)3C+反应速度: 异丁烯>丙烯>乙烯8、略9、(1)CH3CH2CH=CH2(2)CH3CH2C(CH3)=CHCH3(有顺、反两种)(3)CH3CH=CHCH2CH=C(CH3)2(有、反两种)用KMnO4氧化的产物: (1) CH3CH2COOH+CO2+H2O(2)CH3CH2COCH3+CH3COOH(3) CH3COOH+HOOCCH2COOH+CH3COCH310、(1)HBr,无过氧化物(2)HBr,有过氧化物(3)①H2SO4,②H2O(4)B2H6/NaOH-H2O2(5)①Cl2,500℃②Cl2,AlCl3(6)①NH3,O2②聚合,引发剂(7)①Cl2,500℃,②Cl2,H2O ③NaOH11、烯烃的结构式为:(CH3)2C=CHCH3。

第五章饱和烃5-1 写出符合下列条件的C7H16的构造式,并各以系统命名法命名。
(1)庚烷(3)3-甲基已烷(4)2,2-二甲基戊烷(5)2,3-二甲基戊烷(6)2,4-二甲基戊烷(7)3,3-二甲基戊烷(8)3-乙基戊烷(9)2,2,3-三甲基丁烷5-2 写出下列烷基的名称及常用缩写符号。
(1)甲基(Me—);(2)乙基(Et—);(3)正丙基(n-Pr—);(4)异丙基(i-Pr—);(5)正丁基(n-Bu—);(6)异丁基(i-Bu—);(7)仲丁基(s-Bu—);(8)叔丁基(t-Bu—)。
5-3 比较下列化合物沸点的高低,并说明原因。
(1) CH3(CH2)4CH3(2) (CH3)2CH(CH2)2CH3(3)CH3CH2C(CH3)3(4) CH3CH2CH(CH3)CH2CH3(1)>(4) >(2)>(3)同碳数的烷烃异构体,含支链越多,分子间作用力越弱,沸点越低。
5-4 完成下列反应式:OSO3HBrBrBr(1)HO2C(CH2)4CO2HHNO3+(2)BrBr-60℃Br 2+(3)CH(CH 3)2CO 2H 2OCl+ClClCl碳正离子重排导致的产物++CH(CH 3)2BrC(CH 3)2Br+(4)BrHBr(5)5-5 比较下列化合物构象的稳定性大小。
1,4-二甲基环已烷的构象稳定性(1)<(2)。
原因是(1)中的二个甲基均处于a 键上,而(2)中的二个甲基则皆处于e 键上,后者构象能量较低,较稳定。
3H 33CH 3CH 3H 3CCH 3(1)(2)5-6 下列异构体中哪个最稳定?题目所示二甲基环已酮三个异构体对应的构象式如下,从中可看出(3)最稳定,因为其两个甲基均处于e 键上,体系能量较低。
O OO(1)(2)(3)5-7 环丙烷内能高是由哪些因素造成的?环丙烷分子中碳原子为不等性sp 3杂化,轨道重叠比开链烷烃的小,形成的碳碳共价键键能小(即有角张力),容易断裂,不如开链烷烃牢固;其次是环丙烷的三个碳原子共平面,相邻两个碳原子上的C —H 键是重叠式构象,存在扭转张力。
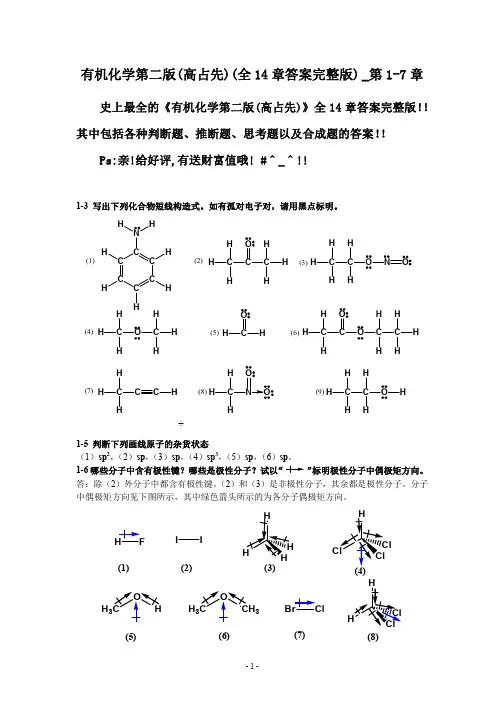

有机化学第二版(高占先)(全14章答案完整版)_第1-7章史上最全的《有机化学第二版(高占先)》全14章答案完整版!!其中包括各种判断题、推断题、思考题以及合成题的答案!!Ps:亲!给好评,有送财富值哦! #^_^!!1-3 写出下列化合物短线构造式。
如有孤对电子对,请用黑点标明。
1-5 判断下列画线原子的杂货状态(1)sp2,(2)sp,(3)sp,(4)sp3,(5)sp,(6)sp。
1-6哪些分子中含有极性键哪些是极性分子试以“”标明极性分子中偶极矩方向。
答:除(2)外分子中都含有极性键。
(2)和(3)是非极性分子,其余都是极性分子。
分子中偶极矩方向见下图所示,其中绿色箭头所示的为各分子偶极矩方向。
1-7 解释下列现象。
(1)CO2分子中C为sp杂化,该分子为直线型分子,两个C=O键矩相互抵消,分子偶极矩为零,是非极性分子;而SO2分子中S为sp2杂化,分子为折线型,两个S—O键矩不能抵消,是极性分子。
(2)在NH3中,三个N—H键的偶极朝向N,与电子对的作用相加;而NF3中三个N—F键的偶极朝向F,与N上的未成对电子的作用相反并有抵消的趋势。
(3)Cl和F为一同主族元素,原子共价半径是Cl比F大,而电负性是F 比Cl大。
键的偶极矩等于μ=qd,q为正电荷中心或负电荷中心上的电荷量,d为正负电荷中心的距离。
HCl键长虽比HF的长,但F-中心上的电荷量大大于Cl-上的电荷量,总的结果导致HF的偶极矩大于HCl。
所以键长是H—Cl较长,偶极矩是H—F较大。
1-8 将下列各组化合物中指定键的键长由长到短排列并说明理由。
答:(1)从乙烷,乙烯到乙炔,碳原子杂化态由sp3到sp2至sp,s成份提高,拉电子能力增强,虽同属于碳氢键但键长缩短。
(2)键长顺序为C—I>C—Br>C—Cl>C—F。
因为卤素原子核外电子层数为I>Br>Cl>F,即其范德华半径为I>Br>Cl>F,则其原子共价半径I>Br>Cl>F。
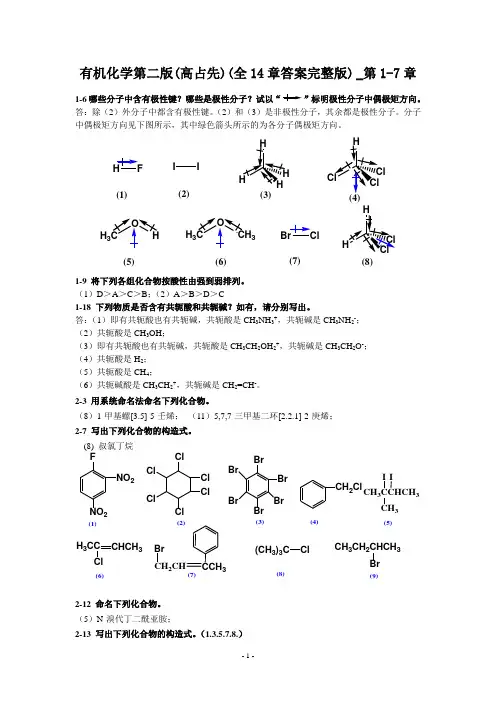
有机化学第二版(高占先)(全14章答案完整版) _第1-7章1-6哪些分子中含有极性键?哪些是极性分子?试以“”标明极性分子中偶极矩方向。
答:除(2)外分子中都含有极性键。
(2)和(3)是非极性分子,其余都是极性分子。
分子中偶极矩方向见下图所示,其中绿色箭头所示的为各分子偶极矩方向。
HH 33H 3I I(1)(2)(3)(5)(6)(7)(8)1-9 将下列各组化合物按酸性由强到弱排列。
(1)D >A >C >B ;(2)A >B >D >C1-18 下列物质是否含有共轭酸和共轭碱?如有,请分别写出。
答:(1)即有共轭酸也有共轭碱,共轭酸是CH 3NH 3+,共轭碱是CH 3NH 2-; (2)共轭酸是CH 3OH ;(3)即有共轭酸也有共轭碱,共轭酸是CH 3CH 2OH 2+,共轭碱是CH 3CH 2O -; (4)共轭酸是H 2; (5)共轭酸是CH 4;(6)共轭碱酸是CH 3CH 2+,共轭碱是CH 2=CH -。
2-3 用系统命名法命名下列化合物。
(8)1-甲基螺[3.5]-5-壬烯; (11)5,7,7-三甲基二环[2.2.1]-2-庚烯; 2-7 写出下列化合物的构造式。
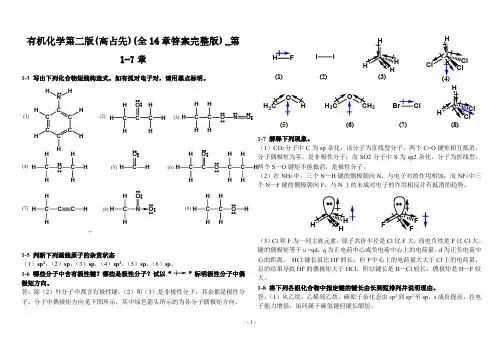
(8) 叔氯丁烷(1)(2)(3)(4)(5)(6)(7)(8)(9)FNO 22ClCl ClClClCl Br BrBrBrBr CH 2Cl CH 3CCHCH3I 3IH 3CCCHCH 3ClCH 2CHCCH 3Br (CH 3)3CClCH 3CH 2CHCH 3Br2-12 命名下列化合物。
(5)N-溴代丁二酰亚胺;2-13 写出下列化合物的构造式。
(1.3.5.7.8.)(1)(2)(3)(4)(6)(7)(8)C CH 2COCH 2CH 2CHCH 3ClO3CH 322H 5OOO OCO Cl C OCH 2CH 2CH 2CH 2CH 3CH 3C O NCH 3CH 3O C O C O OO OH 3CSO 2NH 22-15 写出下列化合物的构造式。
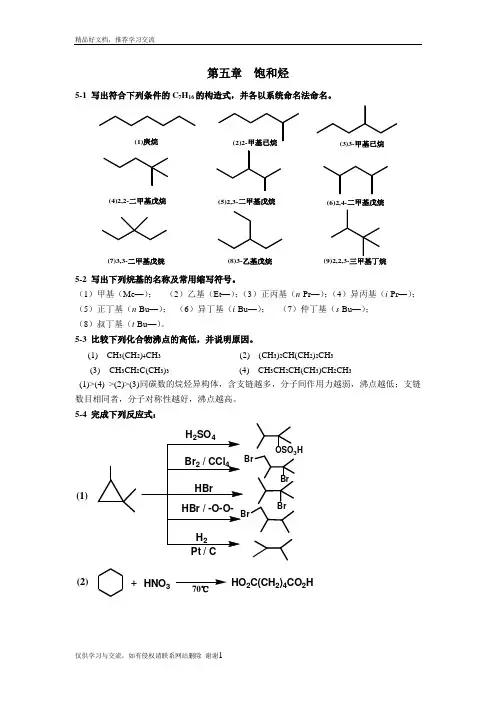
第五章饱和烃5-1 写出符合下列条件的C7H16的构造式,并各以系统命名法命名。
(1)庚烷(3)3-甲基已烷(4)2,2-二甲基戊烷(5)2,3-二甲基戊烷(6)2,4-二甲基戊烷(7)3,3-二甲基戊烷(8)3-乙基戊烷5-2 写出下列烷基的名称及常用缩写符号。
(1)甲基(Me—);(2)乙基(Et—);(3)正丙基(n-Pr—);(4)异丙基(i-Pr—);(5)正丁基(n-Bu—);(6)异丁基(i-Bu—);(7)仲丁基(s-Bu—);(8)叔丁基(t-Bu—)。
5-3 比较下列化合物沸点的高低,并说明原因。
(1) CH3(CH2)4CH3(2) (CH3)2CH(CH2)2CH3(3)CH3CH2C(CH3)3(4) CH3CH2CH(CH3)CH2CH3(1)>(4) >(2)>(3)同碳数的烷烃异构体,含支链越多,分子间作用力越弱,沸点越低;支链数目相同者,分子对称性越好,沸点越高。
5-4 完成下列反应式:OSO3HBrBr(1)HO2C(CH2)4CO2HHNO3+(2)BrBr-60℃Br 2+(3)CH(CH 3)2CO 2H 2OCl+ClClCl碳正离子重排导致的产物++CH(CH 3)2BrC(CH 3)2Br+(4)BrHBr(5)5-5 比较下列化合物构象的稳定性大小。
1,4-二甲基环已烷的构象稳定性(1)<(2)。
原因是(1)中的二个甲基均处于a 键上,而(2)中的二个甲基则皆处于e 键上,后者构象能量较低,较稳定。
3H 33CH 3CH 3H 3CCH 3(1)(2)5-6 下列异构体中哪个最稳定?题目所示二甲基环已酮三个异构体对应的构象式如下,从中可看出(3)最稳定,因为其两个甲基均处于e 键上,体系能量较低。
OOO(1)(2)(3)5-7 环丙烷内能高是由哪些因素造成的?环丙烷分子中碳原子为不等性sp3杂化,轨道重叠比开链烷烃的小,形成的碳碳共价键键能小,容易断裂,不如开链烷烃牢固;其次是环丙烷的三个碳原子共平面,相邻两个碳原子上的C —H 键是重叠式构象,存在扭转张力。

《有机化学》第二版习题参考答案第二章烷烃1、用系统命名法命名下列化合物(1)2,3,3,4-四甲基戊烷(2)3-甲基-4-异丙基庚烷(3)3,3,-二甲基戊烷(4)2,6-二甲基-3,6-二乙基辛烷(5)2,5-二甲基庚烷(6)2-甲基-3-乙基己烷(7)2,2,4-三甲基戊烷(8)2-甲基-3-乙基庚烷2、试写出下列化合物的结构式(1) (CH3)3CC(CH2)2CH2CH3(2) (CH3)2CHCH(CH3)CH2CH2CH2CH3(3) (CH3)3CCH2CH(CH3)2(4) (CH3)2CHCH2C(CH3)(C2H5)CH2CH2CH3(5)(CH3)2CHCH(C2H5)CH2CH2CH3(6)CH3CH2CH(C2H5)2(7) (CH3)2CHCH(CH3)CH2CH3(8)CH3CH(CH3)CH2CH(C2H5)C(CH3)33、略4、下列各化合物的系统命名对吗?如有错,指出错在哪里?试正确命名之。
均有错,正确命名如下:(1)3-甲基戊烷(2)2,4-二甲基己烷(3)3-甲基十一烷(4)4-异丙基辛烷(5)4,4-二甲基辛烷(6)2,2,4-三甲基己烷5、(3)>(2)>(5)>(1) >(4)6、略7、用纽曼投影式写出1,2-二溴乙烷最稳定及最不稳定的构象,并写出该构象的名称。
H交叉式最稳定重叠式最不稳定8、构象异构(1),(3)构造异构(4),(5)等同)2),(6)9、分子量为72的烷烃是戊烷及其异构体(1) C(CH3)4(2) CH3CH2CH2CH2CH3 (3) CH3CH(CH3)CH2CH3(4) 同(1)10、分子量为86的烷烃是己烷及其异构体(1)(CH3)2CHCH(CH3)CH3(2) CH3CH2CH2CH2CH2CH3 , (CH3)3CCH2CH3 (3)CH3CH2CH(CH3)CH2CH3(4)CH3CH2CH2CH(CH3)214、(4)>(2)>(3)>(1)第三章 烯烃1、略2、(1)CH 2=CH — (2)CH 3CH=CH — (3)CH 2=CHCH 2— CH 2CH CH 3M eH H i-P rE t M en-P rM e M e E t i-P rn-P r (4)(5)(6)(7)3、(1)2-乙基-1-戊烯 (2) 反-3,4-二甲基-3-庚烯 (或(E)-3,4-二甲基-3-庚烯 (3) (E)-2,4-二甲基-3-氯-3-己烯 (4) (Z)-1-氟-2-氯-2-溴-1-碘乙烯(5) 反-5-甲基-2-庚烯 或 (E)-5-甲基-2-庚烯 (6) 反-3,4-二甲基-5-乙基-3-庚烯 (7) (E) -3-甲基-4-异丙基-3-庚烯 (8) 反-3,4-二甲基-3-辛烯 4、略 5、略 6、CH 3CH 2CHC H 2CH 3CH 3CH 2CCHC H 3CH 3OH BrCH 3CH 2CCHC H3CH 3Cl ClCH 3CH 2C CHC H3CH 3OH OHCH 3CH 2CHCHC H 3CH 3OHCH 3CH 2COCH3CH 3CHOCH 3CH 2CHCHC H 3CH 3Br(1)(2)(3)(4)(5)(6)(7)7、活性中间体分别为:CH 3CH 2+ CH 3CH +CH 3 (CH 3)3C + 稳定性: CH 3CH 2+ > CH 3CH +CH 3 > (CH 3)3C + 反应速度: 异丁烯 > 丙烯 > 乙烯8、略9、(1)CH 3CH 2CH=CH 2 (2)CH 3CH 2C(CH 3)=CHCH 3 (有顺、反两种) (3)CH 3CH=CHCH 2CH=C(CH 3)2 (有、反两种)用KMnO 4氧化的产物: (1) CH 3CH 2COOH+CO 2+H 2O (2)CH 3CH 2COCH 3+CH 3COOH (3) CH 3COOH+HOOCCH 2COOH+CH 3COCH 310、(1)HBr ,无过氧化物 (2)HBr ,有过氧化物 (3)①H 2SO 4 ,②H 2O (4)B 2H 6/NaOH-H 2O 2 (5)① Cl 2,500℃ ② Cl 2,AlCl 3(6)① NH 3,O 2 ② 聚合,引发剂 (7)① Cl 2,500℃,② Cl 2,H 2O ③ NaOH 11、烯烃的结构式为:(CH 3)2C=CHCH 3 。

第一章绪论1-1 扼要解释下列术语.(1)有机化合物(2) 键能、键的离解能(3) 键长(4) 极性键(5) σ键(6)π键(7) 活性中间体(8) 亲电试剂(9) 亲核试剂(10)Lewis碱(11)溶剂化作用(12) 诱导效应(13)动力学控制反应(14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9) 亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10) Lewis碱:能提供电子对的物种称为Lewis碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。
5章思考题5.1 在不饱和卤代烃中,根据卤原子与不饱和键的相对位置,可以分为哪几类,请举例说明。
5.2 试比较S N2和S N1历程的区别。
5.3 什么叫溶剂化效应?5.4 说明温度对消除反应有何影响?5.5 卤代芳烃在结构上有何特点?5.6 为什么对二卤代苯比相应的邻或间二卤代苯具有较高的熔点和较低的溶解度?5.7 芳卤中哪种卤原子最能使苯环电子离域,为什么?解答5.1 答:可分为三类:(1)丙烯基卤代烃,如CH3CH=CHX(2)烯丙基卤代烃,如CH2=CH-CH2X(3)孤立式卤代烃,如CH2=CHCH2CH2X5.2 答:(略)5.3 答:在溶剂中,分子或离子都可以通过静电力与溶剂分子相互作用,称为溶剂化效应。
5.4 答:增加温度可提高消除反应的比例。
5.5 答:在卤代芳烃分子中,卤素连在sp2杂化的碳原子上。
卤原子中具有弧电子对的p轨道与苯环的π轨道形成p-π共轭体系。
由于这种共轭作用,使得卤代芳烃的碳卤键与卤代脂环烃比较,明显缩短。
5.6 答:对二卤代苯的对称性好,分子排列紧密,分子间作用力较大,故熔点较大。
由于对二卤代苯的偶极矩为零,为非极性分子,在极性分子水中的溶解度更低。
5.7 答:(略)习题5.15.1命名下列化合物。
5.25.2写出下列化合物的构造式。
(1)烯丙基溴(2)苄氯(3)4-甲基-5-溴-2-戊炔(4)偏二氟乙浠(5)二氟二氯甲烷(6)碘仿(7)一溴环戊烷(环戊基溴) (8)1-苯基-2-氯乙烷(9)1,1-二氯-3-溴-7-乙基-2,4-壬二烯(10)对溴苯基溴甲烷(11)(1R,2S,3S)-1-甲基-3-氟-2-氯环己烷(12)(2S,3S)-2-氯-3-溴丁烷5.3 完成下列反应式。
5.4用方程式表示CH3CH2CH2Br与下列化合物反应的主要产物。
(1)KOH(水)(2)KOH(醇)(3)(A)Mg ,乙醚;(B) (A)的产物+HC≡CH (4)NaI/丙酮(5)NH3 (6)NaCN (7)CH3C≡CNa(8)AgNO3(醇) (9) Na (10) HN(CH3)25.5用化学方法区别下列各组化合物。
有机化学答案高占先第1章结构与性能概论习题参考答案(P 31-32)1-5 判断下列画线原子的杂化状态(1) SP 2 (2) SP (3) SP (4) SP 3 (5) SP (6) SP 1-9 将下列各组化合物按酸性由强到弱排列。
(1) D >A >C >B (2) A >B >D >C 1-18下列物质是否有共轭碱和共轭酸?如有请分别写出。
(1) (2) (3) (4) (5) (6) 1-19将下列物种按碱性,由强至弱排列成序。
1-20 下列极限式中,哪个式子是错误的,为什么? (1) C 是错误的,因原子核的位置发生了改变。
(2) C 是错误的,因所有的共振体中要保持一致的单电子数。
(3) D 是错误的,因共振结构式必须符合价键理论,是路易斯结构式。
第2章分类及命名习题参考答案(P 55-59)2-1 用系统命名法命名下列烷烃(1)2,2,5-三甲基已烷(2)3,6-二甲基-4-丙基-辛烷(3)4-甲基-5-异丙基-辛烷(4)2-甲基-3-乙基庚烷(5)5-丙基-6-异丁基-十二碳烷(7)5-丁基-4-异丙基-癸烷(6)3,3-二甲基-4乙基-5-(1,2-二甲丙基)-壬烷(8)3,6,6-三甲基-4-丙基-壬烷2-2 用系统命名法命名下列不饱和烃(1)4-甲基-2-戊炔(2)2,3-二甲基-1-戊烯-4-炔(3)1-已烯-5-炔(4)3-异丁基-4-己烯-1-炔(5)3-甲基-2,4-庚二烯(6)2,3-已二烯(7)2-甲基-2,4,6-辛三烯(8)3-甲基-5-已烯-1-炔(9)亚甲基环戊烷(10)2,4-二甲基-1-戊烯(11)3-甲基-4-(2-甲基环已基)-1-丁烯 2-3用系统命名法命名下列化合物(1)3-甲基环戊烯(2)环丙基乙烯(3)4,4-二氯-1,1-二溴-螺[2,4]-庚烷(4)3-烯丙基环戊烯(5)1-甲基-3-环丙基-环戊烷(6)3,5-二甲基环己烯(7)螺[4,5]-1,6-癸二烯(8)1-甲基螺[3,5]-5-壬烯(9)2-甲基-1-环丁基戊烷(10)2,2-二甲基-1-环丁基二环[2,2,2]辛烷(11)5,7,7-三甲基二环[2,2,1]-2-庚烯(12)二环[4,2,0]-7-辛烯(13)1-甲基-4-乙基二环[3,1,0]己烷CH 3NH3CH 3OH CH 3CH 3OH 2H 2CH 4CH 2CH CH 3CH 2>>>NH 2C CH CH 3O OH>2-4 写出下列化合物的构造式答案见习题集2-5用系统命名法命名下列化合物答案见习题集2-6用系统命名法命名下列化合物(1) 3-甲基-1-溴丁烷其余答案见习题集 2-7写出下列化合物的构造式 (1) ~ (7) 答案见习题集 (8) (9) 2-8用系统命名法命名下列化合物(1) ~ (12) 答案见习题集 (13) 1,4-丁二醇 2-9写出下列化合物的构造式(1) ~ (8) 答案见习题集 (9) (10) (11)(12) (13) 2-10用系统命名法命名下列化合物(1) ~ (12) 答案见习题集 (13) 3-甲基-2,6-萘醌 2-11写出下列化合物的构造式答案见习题集 2-12命名下列化合物(1)(2)(5)(6)(7)(9)(10)(11)(12) 答案见习题集(3) 3-甲基丁内酯 (4) 环已基甲酸 (8) 2-甲基-N-苯基丙酰胺 (13) 4-甲基苯磺酸2-13写出下列化合物的构造式(1)(2)(4)(5) 答案见习题集 (3) (6) (7) (8)2-14命名下列化合物(3) 二甲氨基环丁烷(12) 丙亚氨基环戊烷(13) 1,6-已二腈(14) 1,4-苯二胺(15) 4-氨基-2-甲氧基己烷其余各题答案见习题集2-15写出下列化合物的构造式(8) (15)(16)其余各题答案见习题集C Cl CH 3H 3C 3CH 3CH 2CHCH 3Br (CH 3)3COH OHOHCH 2CH OH CH 2CH3OCH 2CH 2OCH 2CH 2OCH 3C O O C OC C O O OC C O O O COCl 3SO 2NH 2H 2C CH CH CH OCH C 2H 5C CH C C O O O CN CH 3SO 2Cl CH 3CHCH 23OH第3章同分异构现象习题参考答案3-1 下列化合物是否有顺反异构体?若有,试写出它们的顺反异构体。
第五章饱和烃5-1 写出符合下列条件的C7H16的构造式,并各以系统命名法命名。
(1)庚烷(3)3-甲基已烷(4)2,2-二甲基戊烷(5)2,3-二甲基戊烷(6)2,4-二甲基戊烷(7)3,3-二甲基戊烷(8)3-乙基戊烷(9)2,2,3-三甲基丁烷5-2 写出下列烷基的名称及常用缩写符号。
(1)甲基(Me—);(2)乙基(Et—);(3)正丙基(n-Pr—);(4)异丙基(i-Pr—);(5)正丁基(n-Bu—);(6)异丁基(i-Bu—);(7)仲丁基(s-Bu—);(8)叔丁基(t-Bu—)。
5-3 比较下列化合物沸点的高低,并说明原因。
(1) CH3(CH2)4CH3(2) (CH3)2CH(CH2)2CH3(3)CH3CH2C(CH3)3(4) CH3CH2CH(CH3)CH2CH3(1)>(4) >(2)>(3)同碳数的烷烃异构体,含支链越多,分子间作用力越弱,沸点越低。
5-4 完成下列反应式:OSO3HBrBrBr(1)HO2C(CH2)4CO2HHNO3+(2)BrBr-60℃Br 2+(3)CH(CH 3)2CO 2H 2OCl+ClClCl碳正离子重排导致的产物++CH(CH 3)2BrC(CH 3)2Br+(4)BrHBr(5)5-5 比较下列化合物构象的稳定性大小。
1,4-二甲基环已烷的构象稳定性(1)<(2)。
原因是(1)中的二个甲基均处于a 键上,而(2)中的二个甲基则皆处于e 键上,后者构象能量较低,较稳定。
3H 33CH 3CH 3H 3CCH 3(1)(2)5-6 下列异构体中哪个最稳定?题目所示二甲基环已酮三个异构体对应的构象式如下,从中可看出(3)最稳定,因为其两个甲基均处于e 键上,体系能量较低。
O OO(1)(2)(3)5-7 环丙烷内能高是由哪些因素造成的?环丙烷分子中碳原子为不等性sp 3杂化,轨道重叠比开链烷烃的小,形成的碳碳共价键键能小(即有角张力),容易断裂,不如开链烷烃牢固;其次是环丙烷的三个碳原子共平面,相邻两个碳原子上的C —H 键是重叠式构象,存在扭转张力。
基于上述原因,导致环丙烷的内能较高。
5-8 用费歇尔(Fischer )投影式表示下列化合物的构型,并用R / S 标记手性碳的构型。
3HCH 3BrHCH 3BrD2ClH 3C(1)(2)(3)三个化合物费歇尔投影式如下CH 2ClDH3CH 3HCl 2CH 3CH 3H Br CH 3HBr (1)(2)(3)SS RS5-9 下列四个纽曼投影式表示的化合物,哪些是对映体?哪些是非对映体?哪些是同一化合物的不同构象?CH 3H Cl 2H 5HBrH 32H 5C 2H 5BrHH3C Cl H(1)(4)(2)(3)32H 5C 2H H 332H 52H 5BrHCH 3Cl HC 2H 5BrH H Cl CH 32H 5Br HCH 3HClCH 3Cl H C 2H 5HBr C 2H 5Br H 3ClH H Cl H 3C C 2H 5HBrCH 3H ClC 2H 5HBrCH 3H Cl C 2H 5BrH C 2H 5HBr ClHCH 32H 5H BrCH 3ClH(1)(2S ,3R )-2-氯-3-溴戊烷; (2)(2R ,3R )-2-氯-3-溴戊烷; (3)(2S ,3R )-2-氯-3-溴戊烷; (4)(2S ,3S )-2-氯-3-溴戊烷。
∴(2)和(4)是对映体;(2)和(1)或(3)、(4)和(1)或是非对映体;(1)和(3)是同一化合物的不同构象。
5-10 写出环戊烷生成氯代戊烷的反应机理并画出链增长阶段的反应势能变化草图。
在图上标明反应物、中间体、过渡态和生成物的结构。
并指出哪一步是反应的控制步骤。
反应机理如下三式所示:(1)(2)(3)Cl h υ或△Cl2C 5H 10HCl C 5H 9+Cl++C 5H 9Cl C 5H 9+Cl+Cl 2C 5H 9C 5H9C 5H 9Cl+C 5H 9Cl链引发链增长链终止反应势能变化草图:从反应势能草图中可看出,反应机理(2)中第一步即环戊基自由基生成步的活化能较大,所以是整个反应的速率控制步骤。
5-11 2,2,4-三甲基戊烷可以生成哪些碳自由基?按稳定性由大到小的顺序排列这些自由基。
可生成下列自由基。
CH 3(CH 3)2CH(CH 3)3C(CH 3)2CHCH 2(CH 3)32H 2CC H 2C CH 3CH 3HCH 3CH 3H 3CC H CCH 3CH 3HCH 3CH 3H 3CC H 2C CH 3CH 3HCH 3CH 2H 3CC H 2C CH 3CH 3CCH 3CH 3CH 3CHCH 2C(CH 3)3其稳定性为:3°R ·>2°R ·>1°R ·>CH 3·C 5H 10+Cl •C 5H 9Cl+Cl •C 5H 9•+HCl中间体(自由基)过渡态1过渡态2能量5-12 下列反应 t -BuOCl + RH → RCl + t -BuOH 如果链引发反应为:t -BuOCl → t -BuO·+ Cl· ,写出链增长反应。
(2)+(1)RH+t -BuOHR+t -BuOClRRCl +t -BuO t -BuO5-13甲烷在用光照进行氯代反应时,可以观察到如下现象,试用烷烃的氯代反应机理解释这些现象。
(1) 将氯先经用光照,然后立即在黑暗中与甲烷混合,可以获得氯代产物。
(2) 将氯气先经光照,,然后在黑暗中放置一段时间再与甲烷混合,则不发生氯代反应。
(3) 将氯气先经光照,,然后在黑暗中与氯气混合,也不发生氯代反应。
(1) Cl 2先用光照,产生氯自由基·Cl ,迅速在黑暗中与CH 4混合,Cl·来不及相互结合,可与甲烷产生连锁反应得到氯化产物。
(2) Cl 2通过光照射虽产生自由基·Cl.,但在黑暗中经过一段时间后,又重新结合成Cl 2,Cl 2再与甲烷混合时,由于无自由基存在,也无产生自由基条件,故不发生反应。
(3) 甲烷解离能较大,光照不足以产生自由基,黑暗中Cl 2也不产生自由基,故不发生反应。
5-14 回答下列问题。
(1)为什么烷烃不活泼?(2)为什么在烷烃高温热解过程中,断裂的主要是C —C 键而不是C —H 键?(3)烷烃的燃烧是一个强烈的放热反应,但该反应并不在室温下发生。
(1)烷烃分子中只有C —C 键和C —H 键两种非极性σ键,σ键键能较大,化学性质稳定。
(2)经查表知C —C 键能347.3kJ·mol -1,而C —H 键能414.2kJ·mol -1,即前者键能较小,所以断裂的主要是C —C 键而不是C —H 键。
(3)由于其反应的活化能非常高,所以在室温下不易反应。
5-15 下列哪些化合物物可以用烷烃的卤代反应制备?哪些不适合?请说明理由。
(2)、(4)、(5)和(6)可用烷烃的卤代反应制备,而(1)和(3)不适合用烷烃的卤代反应制备。
原因是(2)、(5)和(6)对应的烷烃各只有一种H ,它们发生卤代反应时,仅生成一种一卤代产物;(4)中氢虽然有两种H ,但其叔H 和伯H 被溴取代的活性相差1600倍,所以,它发生溴代时仍然可得到高产率的目标产物。
而(1)对应的烷烃有5种H ,(3)对应的烷烃有11种H ,也即(1)和(3)对应的烷烃发生卤代反应会生成多种一卤代产物。
5-16 下列反应可以得到几种一溴代物(包括立体异构体)?如果伯氢和仲氢的反应速率比为1 :82,请估算各种产物的相对含量。
2h υ戊烷发生一溴代反应可得到3种构造异构产物。
(3)(2)(1)H 3CH 2CC H 2H 2CCH 2Br H 3CH 2CC H 2CHCH 3Br H 3CH 2CH H 23*其中(2)有一个手性碳,存在对映异构体。
所以共有4种一溴代物。
1-溴戊烷2-溴戊烷+3-溴戊烷伯氢的总数仲氢的总数伯氢的相对活性仲氢的相对活性×=66182×=182 =1-溴戊烷的含量==11+82×100% 1.2%2-溴戊烷的含量=821+82×100%65.9% 23=3-溴戊烷的含量=821+82×100%32.9% 13=2-溴戊烷中R型和S型是等量的(消旋化),即各为32.9%。