有机化学高占先第二版课后习题答案
- 格式:doc
- 大小:1.76 MB
- 文档页数:6

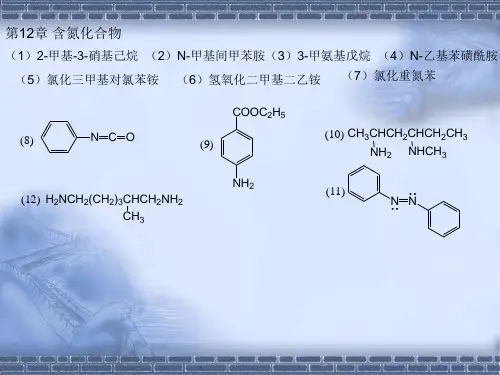

有机化学第二版高占先著第十一章课后答案(总8页)--本页仅作为文档封面,使用时请直接删除即可----内页可以根据需求调整合适字体及大小--第11章 羧酸及其衍生物11-1 将下列各组化合物按酸性由强至弱排列成序。
CH 3COOHClCH 2COOHCl 3CCOOHOHA. B. C.D.A.B.C.D.COOHBr COOHNO 2COOHOCH 3COOHNO 2NO 2COOHOHCOOHCOOHOHA. B.C.(1)(2)(3)(1)D >B >A >C ; (2)C >B >A >D ; (3)B >A >C 。
知识点:羧酸的酸性。
11-2 将下列各组化合物按水解反应速率由大至小排列成序。
CH 3COCl(CH 3CO)2OCH 3CONHCH 3A. B. C. D.COOCH 3NO 2COOCH 3CH 3COOCH 3A.B.C.(1)(2)CH 3COOC 2H 5(1)A >B >D >C ; (2)A >C >B 。
知识点:羧酸衍生物水解反应活性。
水解反应是亲核加成-消除反应,连有吸电子基有利于反应进行。
11-3 比较下列酸在H +催化下进行酯化反应的速率。
HCOOHCH 3COOHCH 3CH 2COOH(1)(2)(3)(CH 3)2CHCOOH (4)(1)>(2)>(3)>(4) 知识点:酸酯化反应活性。
11-4 完成下列反应。
(1)COOHOHOHOOO+(1) LiAlH 4(2)H 2CCOOH2H 2CCH 2OHSOCl 2(3)H 3C CH 2CH 23C CH 2CH 2COClH 3COAlCl 3(分子内酰基化)(1) Zn, CH 3CH(Cl)COOEt(Reformasky 反应)(4)(2) H 2OOOHCHCOOC 2H 5CH 3(5)Br 2/红磷CH 2COOHCHCOOHBr(酰胺还原)(6)NHO(Hofmann 降解)(7)22C 6H 5H 32C 6H 5H 3(8)H 3O(Claisen 酯缩合反应, Wittig 反应, Mannich 反应)(CH 3CO)2O (9)△O(10)3(酯与格氏试剂反应,羟醛缩合反应)HCOOC 2H 5NaOC 2H5(11)+C H OHCHO(12)O O333CH 3COOC 2H 5AlPO 4(13)CH 3COOH2CH 3CH 2OHH 2CC O知识点:羧酸及其衍生物的化学性质。
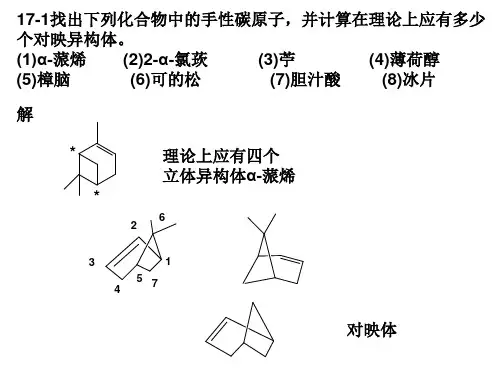

有机化学(第二版)课后习题参考答案第二章分类及命名2-1 用系统命名法命名下列烷烃。
(1)2,2,5-三甲基已烷;(2)3,6-二甲基-4-正丙基辛烷;(3)4-甲基-5-异丙基辛烷;(4)2-甲基-3-乙基庚烷;(5)5-正丙基-6-异丙基十二烷;(6)3,3-二甲基-4-乙基-5-(1,2-二甲基丙基)壬烷;(7)4-异丙基-5-正丁基癸烷;(8)3,6,6-三甲基-4-正丙基壬烷。
2-2 用系统命名法命名下列不饱和烃。
(1)4-甲基-2-戊炔;(2)2,3-二甲基-1-戊烯-4-炔;(3)1-已烯-5-炔;(4)3-异丁基-4-己烯-1-炔;(5)3-甲基-2,4-庚二烯;(6)2,3-已二烯;(7)2-甲基-2,4,6-辛三烯;(8)4-甲基-1-已烯-5-炔;(9)亚甲基环戊烷;(10)2,4-二甲基-1-戊烯;(11)3-甲基-4-(2-甲基环已基)-1-丁烯。
2-3 用系统命名法命名下列化合物。
(1)3-甲基环戊烯;(2)环丙基乙烯;(3)4,4-二氯-1,1-二溴螺[2.4]庚烷;(4)3-烯丙基环戊烯;(5)1-甲基-3-环丙基环戊烷;(6)3,5-二甲基环已烯;(7)螺[4.5]-1,6-癸二烯;(8)1-甲基螺[3.5]-5-壬烯;(9)2-甲基-1-环丁基戊烷;(10)2,2-二甲基-1-环丁基二环[2.2.2]辛烷;(11)5,7,7-三甲基二环[2.2.1]-2-庚烯;(12)二环[4.2.0]-7-辛烯;(13)1-甲基-4-乙基二环[3.1.0]已烷。
2-4 写出下列化合物的构造式。
(1) 3-甲基环己烯(2) 3,5,5-三甲基环己烯(3) 二环[2.2.1]庚烷(4) 二环[4.1.0]庚烷(5) 二环[2.2.1]-2-庚烯(6)二环[3.2.0]-2-庚烯(7) 螺[3.4]辛烷(8) 螺[4.5]-6癸烯(9) 2-甲基二环[3.2.1]-6-辛烯(10) 7,7-二甲基二环[2.2.1]-2,5-庚二烯33 H33H3H3(1)(2)(3)(4)(5)(6)(7)(8)(9)(10)2-5 用系统命名法命名下列化合物。

有机化学第二版(高占先)(全14章答案完整版)_第8-14章史上最全的《有机化学第二版(高占先)》全14章答案完整版!!其中包括各种判断题、推断题、思考题以及合成题的答案!!Ps:亲!给好评,有送财富值哦! #^_^!!第8章卤代烃8-2 完成下列各反应式。
(CH3)3CBr C2H5OH(CH3)2C=CH2+CH3CH=CH2HBr+O OCH3CH2CH2CH3CH2CH2CNNaCN(1)(2)(CH3)2CHCH=CH2Br+500℃(CH3)2CCH=CH2Br H2O(CH3)2C=CHCH2Br +(CH3)2CCH=CH2OH(CH3)2C=CHCH2OH +(3)NaCNKOH25(4)(5)(6)ClCH=CHCH2Cl CH3+ClCH=CHCH23OBrBrBrCNCH2CHCH3BrCH=CHCH3CH3 Br2NH3(l)CH3NH2CH32+ClCl NO2NaOH-H2OOHClNO2ZnCl2(HCHO + HCl)+CH2ClMgCH2MgCl CH2COOH ClCH2CHCH2CH2CH3PhCH2MgClCH3+PhCH2CH2CHCH2CH2CH3CH3(7)(8)(9)(10)3RC CLi(11)RC CR'RC CCOOHRC CCH2CH2OHCHBr3BrBr(12)8-3写出下列反应主要产物的构型式。
CC 2H 5CH 3NaI+CC 2H 5CH 3NaSCH 3+(S N 2)(S N 2)(S N 2)CH 3ICH 2(CH 2)4CH 3HH 2OCH 3H CH 2(CH 2)4CH 3HOC BrCH 2CH 2CH 3CCH 2CH 32Lindar 催化剂C HCCH 2CH 2CH 3H(1)(2)(3)(4)3KOH 253H 3t -BuOK H 3CPh PhHC 6H 5H 3C H 6H 5H Br C 6H 5H C 6H 5CH 32525Br(H 3C)2HCCH 3(H 3C)2HC3CH 3H Br CH 2CH 3HBr C 2H 5CH 325Znt -BuOK (E2反式消除)(E2反式消除)(E2反式消除)(顺式消除)(E2反式消除,但很慢)(5)(6)(7)(8)(9)8-4 比较下列每对亲核取代反应,哪一个更快,为什么 (1)B >A (亲核性C 2H 5O ->C 2H 5OH )(2)A>B (烯丙型卤代烃活泼)(3)B>A (极性非质子溶剂有利于S N2反应)(4)A>B (亲核性-SH>-OH)(5)A>B (亲核性硫比氮强)(6)B>A (离去能力I->Cl-)8-5卤代烷与NaOH在H2O-C2H5OH溶液中进行反应,指出哪些是S N2机理的特点,哪些是S N1机理的特点(1)产物发生Walden转化; S N2(2)增加溶剂的含水量反应明显加快; S N1(3)有重排反应产物; S N1(4)反应速率明显地与试剂的亲核性有关; S N2(5)反应速率与离去基的性质有关; S N2和S N1(6)叔卤代烷反应速度大于仲卤代烷。

有机化学第二版( 高占先)( 全14 章答案完整版) _第8-14 章史上最全的《有机化学第二版( 高占先) 》全14 章答案完整版!!其中包括各种判断题、推断题、思考题以及合成题的答案!!Ps: 亲! 给好评, 有送财富值哦! # ^_^!!第8 章卤代烃8-2 完成下列各反应式。
(1) (CH3)3CBr KCN+ C2H5OH (CH3)2C=CH 2(2) CH3CH=CH 2 + HBr O O NaCNCH3CH2CH2Br CH3CH2CH2CN(3) (CH3)2CHCH=CH 2 + Br 2500℃(CH3)2CCH=CH 2+(CH3)2C=CHCH 2BrH2O△(CH3)2CCH=CH 2OH+ Br(CH3)2C=CHCH 2OHO (4) ClCH=CHCH 2Cl + CH3COO ClCH=CHCH 2OCCH 3BrCN NaCN(5)BrBr(6)CH2CHCH 3BrKOHC2H5OH, △CH=CHCH 3(7)C H3Br NaNH 2NH3(l)CH3NH2+CH3NO2NH2 NO 2(8) Cl Cl NaOH-H 2O△C l OHCH2Cl CH2 MgCl CH2COOH(9) + (HCHO + HCl) ZnCl2Mg乙醚(1) CO2(2) H3O乙醚(10) PhCH 2MgCl ClCH 2CHCH 2CH2CH3 PhCH 2 CH2 CHCH 2CH2CH3+CH3 CH3R'ClRC CR'(11) RC CLi(1)CO2(2)H3ORC CCOOHO (1)(2)H3ORC CCH 2 CH 2OH(12)CHBr 350%NaOH(aq) BrBr8-3写出下列反应主要产物的构型式。
C2H5C2H5(1)丙酮C CH3 + CNaIHIBrHC H3(S N2)(2) Cl H H I+ NaSCH3Cl H H3CS H(S N 2)(3) H CH3IH2O(溶剂解)HOCH 3H(S N 2) CH2(CH2)4CH 3CH 2(CH2)4CH 3Br(4)C CH2CH2CH3(1) NaNH 2/NH 3(l)(2) H 3OC CCH 2CH3H2Lindar 催化剂BrCH 2CH2CH3C CHHCH3 CH3(5)H KOHHC2H5OH,△H(E2反式消除) BrHH3C Ph t-BuOK Ph Ph(6)(E2反式消除)t-BuOH, △Ph BrH3 C HH(7)C6H5H3C HH BrC6H5C2H5ONa / C2H5OHE2H C H6 5C6H5 CH3(E2反式消除)(H3C)2HC(H3C)2HC(8) Br t-BuOKt-BuOH, △(E2反式消除,但很慢)CH3CH3CH3(9) H BrH BrZnC2H5OHC2H5 CH3(顺式消除)H HCH2 CH38-4比较下列每对亲核取代反应,哪一个更快,为什么?(1)B>A (亲核性C2H5O2H5OH)->C(2)A>B (烯丙型卤代烃活泼)(3)B>A (极性非质子溶剂有利于S N2 反应)(4)A>B (亲核性-SH>-OH)(5)A>B (亲核性硫比氮强)- (6)B>A (离去能力I >Cl - )8-5卤代烷与NaOH 在H2O-C 2H5OH 溶液中进行反应,指出哪些是S N 2 机理的特点,哪些是S N 1 机理的特点?(1)产物发生Walden 转化;S N 2(2)增加溶剂的含水量反应明显加快;S N1(3)有重排反应产物;S N1(4)反应速率明显地与试剂的亲核性有关;S N2(5)反应速率与离去基的性质有关;S N2 和S N1(6)叔卤代烷反应速度大于仲卤代烷。

第二章分类及命名2-1 用系统命名法命名下列烷烃。
(1)2,2,5-三甲基已烷;(2)3,6-二甲基-4-正丙基辛烷;(3)4-甲基-5-异丙基辛烷;(4)2-甲基-3-乙基庚烷;(5)5-正丙基-6-异丙基十二烷;(6)3,3-二甲基-4-乙基-5-(1,2-二甲基丙基)壬烷;(7)4-异丙基-5-正丁基癸烷;(8)3,6,6-三甲基-4-正丙基壬烷。
2-2 用系统命名法命名下列不饱和烃。
(1)4-甲基-2-戊炔;(2)2,3-二甲基-1-戊烯-4-炔;(3)1-已烯-5-炔;(4)3-异丁基-4-己烯-1-炔;(5)3-甲基-2,4-庚二烯;(6)2,3-已二烯;(7)2-甲基-2,4,6-辛三烯;(8)4-甲基-1-已烯-5-炔;(9)亚甲基环戊烷;(10)2,4-二甲基-1-戊烯;(11)3-甲基-4-(2-甲基环已基)-1-丁烯。
2-3 用系统命名法命名下列化合物。
(1)3-甲基环戊烯;(2)环丙基乙烯;(3)4,4-二氯-1,1-二溴螺[2.4]庚烷;(4)3-烯丙基环戊烯;(5)1-甲基-3-环丙基环戊烷;(6)3,5-二甲基环已烯;(7)螺[4.5]-1,6-癸二烯;(8)1-甲基螺[3.5]-5-壬烯;( 9)2-甲基-1-环丁基戊烷;(10)2,2-二甲基-1-环丁基二环[2.2.2]辛烷;(11)5,7,7-三甲基二环[2.2.1]-2-庚烯;(12)二环[4.2.0]-7-辛烯;(13)1-甲基-4-乙基二环[3.1.0]已烷。
2-4 写出下列化合物的构造式。
(1) 3-甲基环己烯 (2) 3,5,5-三甲基环己烯 (3) 二环[2.2.1]庚烷 (4) 二环[4.1.0]庚烷(5) 二环[2.2.1]-2-庚烯 (6)二环[3.2.0]-2-庚烯 (7) 螺[3.4]辛烷(8) 螺[4.5]-6癸烯(9) 2-甲基二环[3.2.1]-6-辛烯(10) 7,7-二甲基二环[2.2.1]-2,5-庚二烯33 H33H3H3(1)(2)(3)(4)(5)(6)(7)(8)(9)(10)2-5 用系统命名法命名下列化合物。
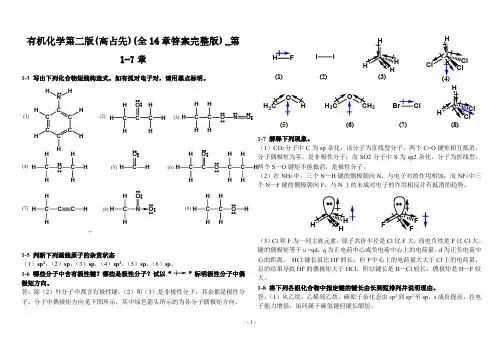

第一章绪论1-1 扼要解释下列术语.(1)有机化合物(2) 键能、键的离解能(3) 键长(4) 极性键(5) σ键(6)π键(7) 活性中间体(8) 亲电试剂(9) 亲核试剂(10)Lewis碱(11)溶剂化作用(12) 诱导效应(13)动力学控制反应(14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9) 亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10) Lewis碱:能提供电子对的物种称为Lewis碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。

第一章绪论1-1 扼要解释下列术语.(1)有机化合物(2) 键能、键的离解能(3) 键长(4) 极性键(5) σ键(6)π键(7) 活性中间体(8) 亲电试剂(9) 亲核试剂(10)Lewis碱(11)溶剂化作用(12) 诱导效应(13)动力学控制反应(14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9) 亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10) Lewis碱:能提供电子对的物种称为Lewis碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。
有机化学第二版(高占先)(全14章答案完整版)_第8-14章(1) -CAL-FENGHAI-(2020YEAR-YICAI)_JINGBIAN有机化学第二版(高占先)(全14章答案完整版) _第8-14章史上最全的《有机化学第二版(高占先)》全14章答案完整版!!其中包括各种判断题、推断题、思考题以及合成题的答案!!Ps:亲!给好评,有送财富值哦! #^_^!!第8章 卤代烃8-2 完成下列各反应式。
(CH 3)3CBr C 2H 5OH(CH 3)2C=CH 2+CH 3CH=CH 2HBr+O OCH 3CH 2CH 2CH 3CH 2CH 2CNNaCN(1)(2)(CH 3)2CHCH=CH 2Br +500℃(CH 3)2CCH=CH 2BrH 2O (CH 3)2C=CHCH 2Br+(CH 3)2CCH=CH 2OH(CH 3)2C=CHCH 2OH+(3)NaCNKOH 25(4)(5)(6)ClCH=CHCH 2Cl CH 3+ClCH=CHCH 23OBrBrBrCNCH 2CHCH 3BrCH=CHCH 3CH3 Br2NH3(l)CH3NH2CH32+ClCl NO2NaOH-H2OOHClNO2ZnCl2(HCHO + HCl)+CH2ClMgCH2MgCl CH2COOH ClCH2CHCH2CH2CH3PhCH2MgClCH3+PhCH2CH2CHCH2CH2CH3CH3(7)(8)(9)(10)3RC CLi(11)RC CR'RC CCOOHRC CCH2CH2OHCHBr3BrBr(12)8-3写出下列反应主要产物的构型式。
CC2H5CH3NaI+CC2H5CH3NaSCH3+(S N2)(S N2)(S N2)CH3ICH2(CH2)4CH3HH2OCH3HCH2(CH2)4CH3HOCBrCH2CH2CH3CCH2CH32Lindar催化剂CHCCH2CH2CH3H(1)(2)(3)(4)3KOH253H3t-BuOKt-BuOH, △H3CPh PhHC6H5H3C H6H5H BrC6H5H C6H5CH32525Br(H3C)2HCCH3(H3C)2HCCH3CH3H BrCH2CH3H BrC2H5CH325Znt-BuOK(E2反式消除)(E2反式消除)(E2反式消除)(顺式消除)(E2反式消除,但很慢)(5)(6)(7)(8)(9)8-4比较下列每对亲核取代反应,哪一个更快,为什么?(1)B>A (亲核性C2H5O->C2H5OH)(2)A>B (烯丙型卤代烃活泼)(3)B>A (极性非质子溶剂有利于S N2反应)(4)A>B (亲核性-SH>-OH)(5)A>B (亲核性硫比氮强)(6)B>A (离去能力I->Cl-)8-5卤代烷与NaOH在H2O-C2H5OH溶液中进行反应,指出哪些是S N2机理的特点,哪些是S N1机理的特点?(1)产物发生Walden转化; S N2(2)增加溶剂的含水量反应明显加快; S N1(3)有重排反应产物; S N1(4)反应速率明显地与试剂的亲核性有关; S N2(5)反应速率与离去基的性质有关; S N2和S N1(6)叔卤代烷反应速度大于仲卤代烷。
有机化学(第二版)课后习题参考答案第一章绪论1-1扼要解释下列术语.(1)有机化合物(2) 键能、键的离解能(3) 键长(4) 极性键(5) σ键(6)π键(7) 活性中间体(8) 亲电试剂(9) 亲核试剂(10)Lewis碱(11)溶剂化作用(12) 诱导效应(13)动力学控制反应(14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB 拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4)极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9)亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10) Lewis碱:能提供电子对的物种称为Lewis碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。
第五章饱和烃5-1 写出符合下列条件的C7H16的构造式,并各以系统命名法命名。
(1)庚烷(3)3-甲基已烷(4)2,2-二甲基戊烷(5)2,3-二甲基戊烷(6)2,4-二甲基戊烷(7)3,3-二甲基戊烷(8)3-乙基戊烷5-2 写出下列烷基的名称及常用缩写符号。
(1)甲基(Me—);(2)乙基(Et—);(3)正丙基(n-Pr—);(4)异丙基(i-Pr—);(5)正丁基(n-Bu—);(6)异丁基(i-Bu—);(7)仲丁基(s-Bu—);(8)叔丁基(t-Bu—)。
5-3 比较下列化合物沸点的高低,并说明原因。
(1) CH3(CH2)4CH3(2) (CH3)2CH(CH2)2CH3(3)CH3CH2C(CH3)3(4) CH3CH2CH(CH3)CH2CH3(1)>(4) >(2)>(3)同碳数的烷烃异构体,含支链越多,分子间作用力越弱,沸点越低;支链数目相同者,分子对称性越好,沸点越高。
5-4 完成下列反应式:OSO3HBrBr(1)HO2C(CH2)4CO2HHNO3+(2)BrBr-60℃Br 2+(3)CH(CH 3)2CO 2H 2OCl+ClClCl碳正离子重排导致的产物++CH(CH 3)2BrC(CH 3)2Br+(4)BrHBr(5)5-5 比较下列化合物构象的稳定性大小。
1,4-二甲基环已烷的构象稳定性(1)<(2)。
原因是(1)中的二个甲基均处于a 键上,而(2)中的二个甲基则皆处于e 键上,后者构象能量较低,较稳定。
3H 33CH 3CH 3H 3CCH 3(1)(2)5-6 下列异构体中哪个最稳定?题目所示二甲基环已酮三个异构体对应的构象式如下,从中可看出(3)最稳定,因为其两个甲基均处于e 键上,体系能量较低。
OOO(1)(2)(3)5-7 环丙烷内能高是由哪些因素造成的?环丙烷分子中碳原子为不等性sp3杂化,轨道重叠比开链烷烃的小,形成的碳碳共价键键能小,容易断裂,不如开链烷烃牢固;其次是环丙烷的三个碳原子共平面,相邻两个碳原子上的C —H 键是重叠式构象,存在扭转张力。
第六章 不饱和烃6-1 命名下列各化合物。
(CH 3)2CHCH 2CH 2CH 3CH 2CH(CH 3)2CC H 3C H C CH 2HH 3CH 2CH 3HCH 312345678912345678CC C 25H 3C C 3)3CC 2H 52,4-二甲基-1-戊烯3-异丁基环已烯(E )-1,3-戊二烯(S )-6-甲基-1,3-环辛二烯(3R ,4Z )-3,6-二甲基-5-丙基-4-壬烯(E )-3-甲基-4-叔丁基-3-辛烯-5-炔12345(1)(2)(3)(4)(5)(6)(2)也可命名为:3-(2-甲基丙基)环已烯 6-2 按要求比较反应活性。
(1)B >C >A ; (2)A >B >C >D >E ; (3)A >C >B >D ; (4)B >A >C >D . 6-3 将下列各组碳正离子按稳定性由大到小排列成序。
(1)B →A →C →D ; (2)A →C →B 。
(3)C →D → B →A 6-4 指出下列分子中各存在哪些类型的共轭体系?(1)、(3)和(4)都是p-π共轭体系;(2)π-π和p-π共轭体系。
(1)和(4)还有π-σ和p-σ超共轭。
6-5下列各对结构式是构造异构体系还是共振结构关系? (1)构造异构体; (2)、(3)和(4)共振结构。
6-6 下列各组极限结构式,哪一个极限结构对共振杂化体的贡献较大? (1) B 式(负电荷处在电负性较大的O 上比处在C 上稳定) ;(2) B 式(B 式中所有原子均有完整的价电子层,而在A 式中+C 上没有完整的价电子层); (3)A 式(A 式的正离子为三级碳正离子,正电荷较分散)。
6-7 将下列烯烃按稳定性由大至小排列。
稳定性由大至小顺序为:(2)→(4)→(1)→(3)反式烯烃比顺式烯烃稳定,内烯烃比端烯烃稳定,双键上取代基多的烯烃比取代基少的烯烃稳定。
6-8查阅并比较(Z )-2-丁烯与(E )-2-丁烯;(Z )-1,2-二氯乙烯与(E )-1,2-二氯乙烯的熔沸点、偶极矩,说明结构与熔沸点的关系。
经查阅(见下表),题中所给的二组顺反异构体中,Z 型的皆有一定偶极矩,是极性分子,分子间作用较大,因而沸点比E 型的高;而E 型的偶极矩为0,是非极性分子,但对称性较好,有对称中心。
熔点比Z 型的高。
分子的对称性好,熔点高;分子偶极矩大,沸点高。
6-9完成下列反应式,写出主要产物。
(C 2H 5)2CCHCH 3ICl +(C 2H 5)2C CHCH 3ClI+ClCC H 3C HCH 3H Br 24H 33CC t -Bu CH 32H 5Br 2432H 5(1)(2)(3)(4)H 3CH23t 即H +Pb-BaSO 4,(5)(6)(7)(8)喹啉H 2C=HC(H 2C)3(CH 2)3CH=CH 2HCl(1mol)+ClCOOH O+CH 2CH 3B 2H 6/THF 22①CH 2CH 3OH H(9)Br+H 3CH 2CHOH+(10)C 2CHO 3Cl 2/H 2OC O CO O(1mol)C O CO O+Cl OH(11)(12)(13)ClHO+CH 3CH=CH 2(15)+△(14)33CH 3CH 32Ru 催化剂CH 3CH=CHCH 3CH 2=CH 26-10 用化学方法鉴别下列化合物。
(1)(2)6-11用≤C 3的有机物为原料合成下列化合物。
CH 3C CH NaNH 2+液氨CH 3CCNaBrCH 2CH 2CH2CH 3CCNa 2+CH 3CC(CH 2)3C CCH 3(1)HCCH NaNH 2+液氨NaCCNa 2CH 3CH 2Br NaCCNa +CH 3CH 2CCCH 2CH3(2)22NH 3+A B C D E (+)(-)(+) (-) (-)↓白色 白色 褪色,并有CO 2褪色 (-)A B (-)褪色(+) 褪色(+) (-)A DB Br 2/CCl 4(-)褪色(+) (-)(+)白色H 2P-2催化剂CH 3CH 2CCCH 2CH 3+H 3CH 2CCH 2CH 3HCCH HC +CuCl-NH 4ClCCHCH H 2C CCH CH H 2C H +Lindlar cat.CH CH 2CHH 2CCH CH 2CHH 2CCH H 2C+C 6H 6CN(3)2CH 3HCCH NaNH 2+液氨NaCCNa NaCCNa +CC (4)22NH 3+H P-2催化剂+H 3C CH 3H 3C CH 3C C H 3C CH 3H 3C CH 3OsO 4+吡啶NaHSO 4CH 3HO H CH 3HO HCC H 3C CH Na/液氨HH 3C CH 3HCH 3CO 3H H 332OHCH 3OH H CH 3OH H 或HCCH NaNH 2+液氨CHCNa CH 3CH 2BrCHCNa+HC C (5)NH 3+CH 2CH 3H 2OHgSO 4,H 2SO 4HC C CH 2CH 3+CH 3COCH 2CH 3CCH NaNH 2+液氨+(6)NH 3+H 3CCCNa H 3C CCNa H 3C CH 3COCH3液氨H 3OC CH 3C C CH 3CH 3OH6-12用≤C 5的有机物为原料合成下列化合物(无机试剂任选)。
KMnO 4/H +(1)CO COCOC OO△COOHCOOHHOOC HOOCCH H 2CKMnO 4/H+(2)苯CN△COOHCNHOOCCH H 2C KMnO 4/HCl +(3)△苯Cl△HOOCCOOHCl6-13写出下列反应的合理反应机理。
(1)CH 2CH 33HCH 333CH 3CH 3CH 3CH 333CH 3CH 3CH 3H甲基迁移HCH 3CH 3CH 3+++(2)R-O-O-R h υ或△2RO RO HBr ROHBrBr+HBr+Br+Br+Br BrBr 2链引发链增长链终止(3)H 2SO 44H+Ph H HPhBr Br+Br BrBrBrPhBr H PhHBr PhH Br PhBrH+即(4)6-14分子式为C 7H 10的某开链烃A ,可发生下列 反应:A 经催化可生成3-乙基戊烷;A 与AgNO 3/NH 3溶液反应可产生白色沉淀;A 在Pd/BaSO 4作用下吸收1molH 2生成化合物B ;可以与顺丁烯二酸酐反应生成化合物C 。
试推测A ,B 和C 的构造式。
HCCCH CH 3CH 2CH 3H 2CCHCCH CH 3CH 2CH 3EtMeC CO O(A)(B)(C)6-15 某化合物A 的分子式为C 5H 8,在液NH 3中与NaNH 2作用后,再与1-溴丙烷作用,生成分子式为C 8H 14的化合物B ;用KMnO 4氧化B 得到分子式为C 4H 8O 2的两种不同的酸C 和D 。
A 在HgSO 4存在下与稀H 2SO 4作用,可得到酮E (C 5H 10O )。
试写出A~E 的构造式,并用反应式表示上述转变过程。
(A)(B)(C)HC C CH 3CH 3CH 3CH 2CH 2CC CH 3CH 3CH 3CH 2CH 2COOHCH 3CHCOOH3H 3CC CH CH 3CH 3(D)(E)(A)(B)(C)HC C CH 3CH 3CH 3CH 2CH 2CC CH 3CH CH 3CH 2CH 2COOH CH 3CHCOOH3H 3CC CH CH 3CH 3O (D)(E)NaNH 2+NaC C CH 3CH 322KMnO 4/H+(A)HC C CH 3CH 3H 2HgSO 4, H 2SO 4+6-16 写出下式中A~E 各化合物的构造式。
(A)(B)(C)C C C(CH 3)3(D)(E)H H 3C C C C(CH 3)3H 3H Br C C3)3HH 3C Br 2S,3R 2R ,3SC C C(CH 3)3H 3C HC C C(CH 3)3H 3C6-17 工业上主要有两种方法生产氯丁橡胶的单体2-氯丁二烯,分别为乙炔法和丁二烯氧化法。
请查阅文献,对比分析这两种生产方法的特点并写出两种方法的各步反应式及其各步反应的类型。
HC CH HC +CuCl-NH 4ClHCl C CHCH 2C HCl+HgCl 2/CC CH CH H 2C CCH 2CH H 2C Cl乙炔法乙炔法涉及反应:(1)乙炔二聚合;(2)共轭亲电加成反应。
NaOHCH CH 2CH H 2C CH CH 2CH H 2C Cl ClCH CH 2CH 2C Cl ClCl ++CH CH 2CH H 2C ClCl△CH 2CH H 2C Cl丁二烯法丁二烯氯化法:(1)亲电共轭加成;(2)亲电1,2-加成;(3)消除反应;(4)异构化。
6-18 请比较烯、炔、共轭二烯烃的结构及化学性质的异同点。
共同点:三者都为不饱和烃,结构中含有不饱和键(π键);化学性质上皆表现为能发生加成反应。
不同点:烯烃双键碳为sp 2杂化(双键由一个σ键和一个π键组成);而炔烃中的叁键碳为sp 杂化(叁键由一个σ键和两个π键组成);共轭二烯烃的双键碳也为sp 2杂化,但其中含π-π共轭体系。
化学性质上,炔烃能与两分子亲电试剂加成,且还能发生亲核加成;而烯烃只能与一分子试剂加成;共轭二烯烃能发生共轭加成(1,4-加成)。