重氮盐的反应.ppt
- 格式:ppt
- 大小:985.00 KB
- 文档页数:27
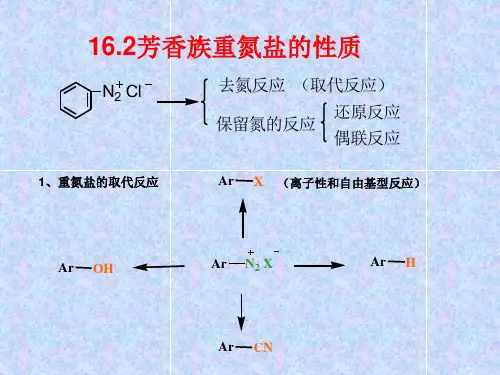









重氮盐偶联反应一、引言重氮盐偶联反应是有机合成中的一种重要反应,可以用于构建碳-碳键和碳-氮键。
该反应以芳香胺或其衍生物为原料,通过氧化亚氮生成重氮盐中间体,再与亲核试剂发生偶联反应。
该反应具有简单易行、高选择性、高效率等优点,在药物合成、材料科学等领域得到广泛应用。
二、机理重氮盐偶联反应的机理主要分为两步:生成重氮盐中间体和与亲核试剂发生偶联反应。
1. 生成重氮盐中间体首先,芳香胺经过亲电取代作用被氧化为亚硝基芳香胺,随后在酸催化下失去水分子形成重氮盐中间体。
2. 与亲核试剂发生偶联反应生成的重氮盐中间体进一步与亲核试剂发生偶联反应。
如与苯乙烯发生偶联反应时,重氮离子上的N-N键断裂,C-N键形成,同时苯环上的双键被还原为单键。
三、影响因素1. 反应物的选择芳香胺的结构和取代基对反应速率和产率有很大影响。
一般来说,含电子供体基团的芳香胺反应活性较高,而含电子吸引基团的芳香胺反应活性较低。
2. 酸催化剂的选择酸催化剂对反应速率和产率也有很大影响。
一般来说,强酸催化剂如硫酸、氯化亚铁等反应速率较快,但容易引起副反应;而弱酸催化剂如硼酸、乙酰氧化铝等则反应速率较慢,但产物纯度高。
3. 温度和溶剂的选择温度和溶剂也是影响重氮盐偶联反应的重要因素。
一般来说,在适当温度下进行该反应可以提高产率;而不同溶剂对该反应也有不同影响,如极性溶剂有利于离子中间体形成,而非极性溶剂则有利于亲核试剂与离子中间体发生偶联。
四、实例分析1. 苯甲醛与N-苯基-1-萘胺的偶联反应首先,N-苯基-1-萘胺在硫酸催化下被亚硝基化生成重氮盐中间体。
随后,重氮盐中间体与苯甲醛发生偶联反应,生成N-(2-苯乙酰基)-1-萘胺。
2. 苯甲醛与N,N-二甲基苯胺的偶联反应首先,N,N-二甲基苯胺在硼酸催化下被亚硝基化生成重氮盐中间体。
随后,重氮盐中间体与苯甲醛发生偶联反应,生成N,N-二甲基-N-(2-苯乙酰基)苯胺。
五、总结重氮盐偶联反应是一种简单易行、高选择性、高效率的有机合成方法,可以用于构建碳-碳键和碳-氮键。
实验九 重氮盐的制备及其反应一、实验目的1.掌握重氮化反应的原理和重氮盐的制备方法 2.掌握放氮反应的原理和操作方法3.掌握偶合反应的原理及偶氮化合物的制备方法二、实验原理重氮盐通常是伯芳胺在过量无机酸(常用盐酸和硫酸)的水溶液中与亚硝酸钠在低温作用而制得:ArNH 2NaNO 2HXArN 2+X -H 2O NaX低温++2+2+在制备重氮盐时,应注意以下几个问题:⑴ 严格控制在低温。
重氮化反应是一个放热反应,同时大多数重氮盐极不稳定,在室温时易分解,所以重氮化反应一般都保持在0~5℃进行。
但芳环上有强的间位取代基的伯芳胺,如对硝基苯胺,其重氮盐比较稳定,往往可以在较高的温度下进行重氮化反应。
⑵ 反应介质要有足够的酸度。
重氮盐在强酸性溶液重比较不活泼;过量的酸能避免副产物重氮化合物等的生成。
通常使用的酸量要比理论量多25%左右。
⑶ 避免过量的亚硝酸。
过量的亚硝酸会促进重氮盐的分解,会很容易和进行下一步反应所加入的化合物(例如叔芳胺)起作用,还会使反应终点难于检验。
加入适量的亚硝酸钠溶液后,要及时用碘化钾淀粉试纸检验反应终点。
过量的亚硝酸可以加入尿素来除去。
⑷ 反应时应不断搅拌。
反应要均匀地进行,避免局部过热,以减少副产物。
制得的重氮盐水溶液不易放置过久,要及时地用于下一步的合成中。
最常见的重氮盐的化学反应有下列两种类型:⑴ 作用时放出氮气的反应。
在不同的条件下,重氮基能被氢原子、羟基、氰基、卤原子等所置换,同时放出氮气。
例如,桑德迈耳(Sandmeyer )反应:ArN 2+Cl -CuCl 过量浓盐酸ArCl +N 2在实际操作中,往往将先制备的、冷的重氮盐溶液慢慢地加到冷的氯化亚铜的浓氢卤酸溶液中去,先生成深红色悬浮的复盐。
然后,缓缓加热,使复盐分解,放出氮气,生成卤代芳烃。
⑵ 作用时保留氮的反应,其中最重要的是偶合反应。
例如重氮盐与酚或叔芳胺在低温时作用,生成具有Ar —N=N —Ar '结构的稳定的有色偶氮化合物。