葡萄糖酸钙含量的测定
- 格式:doc
- 大小:30.00 KB
- 文档页数:2
1 感官要求取10g被测样品,置于洁净的白瓷盘中,用肉眼在自然光线下观察其色泽、组织形态、杂质,品尝其滋味,嗅其气味。
2一般规定本标准所用试剂除非另有说明,在分析中仅使用确认为分析纯的试剂和 GB/T 6682—2008中规定的三级水。
试验方法中所需标准滴定溶液、制剂及制品,在没有注明其他要求时,均按GB/T 601、GB/T 603之规定制备。
3 鉴别试验3.1 试剂和材料3.1.1 冰乙酸。
3.1.2 苯肼:临用时蒸馏。
3.2 鉴别试验3.2.1 钙盐鉴别3.2.1.1 方法原理钙盐与草酸铵试液反应,生成白色沉淀,沉淀在乙酸中不溶解,但可溶解于稀盐酸。
3.2.1.2 分析步骤取约 1.0 g实验室样品,精确至 0.01 g,加 40 mL水溶解,必要时加热使溶解,取此溶液按《中华人民共和国药典》 2005年版二部附录Ⅲ一般鉴别试验钙盐项下( 2),应显钙盐的鉴别反应。
3.2.2 葡萄糖的鉴别 3.2.2.1 方法原理样品在乙酸介质中,与苯肼共热,生成黄色葡萄糖酰苯肼结晶。
3.2.2.2 分析步骤取约 0.5 g 实验室样品,精确至 0.01 g ,置 10 mL 试管中,加 5 mL 水,溶解(必要时加热),加 0.7 mL 冰乙酸和 1 mL 苯肼,在水浴上加热 30min ,放至室温,用玻璃棒摩擦试管内壁,则析出黄色的结晶。
3.2.3 红外光吸收图谱鉴别采用溴化钾压片法测定,实验室样品的红外光吸收图谱应与对照的图谱《药品红外光谱集》465图)一致,对照图谱见附录 B 。
4 葡萄糖酸钙的测定 4.1 方法提要以钙紫红素为指示剂,用乙二胺四乙酸二钠标准滴定液滴定样品水溶液,根据乙二胺四乙酸二钠标准滴定液的用量,计算以 C12H22CaO14·H2O 计的葡萄糖酸钙的含量。
4.2 试剂与材料4.2.1 钙紫红素指示剂。
4.2.2 氢氧化钠溶液:40g/L 。
4.2.3 乙二胺四乙酸二钠标准滴定液:c(EDTA)=0.05mol/L 。


葡萄糖酸钙钙含量测定分析报告分析化学大型实验报告葡萄糖酸钙中钙含量的测定姓名学号学院班级自主设计试验,用两种滴定方法进行葡萄糖酸钙中钙含量的测定一、主要仪器试剂1.仪器:分析天平(0.1mg)酸式滴定管(50mL)锥形瓶(250 mL)洗耳球移液管(25mL)容量瓶(250mL)烧杯(100mL、600 mL)表面皿玻璃棒煤气灯石棉网2.药品:一、EDTA固体 CaCO3优级纯酚酞指示剂葡萄糖酸钙样品钙指试剂蒸馏水NaOH优级纯固体二、HCl (6 mol•L、浓盐酸) KMnO4分析纯NaOH优级纯固体 Na2C2O4基准试剂NH3.H2O-NH4Cl缓冲溶液(pH=10)甲基橙指示剂 H2SO43mol/L蒸馏水二、实验步骤I、用EDTA测定葡萄糖酸钙中钙的含量1、EDTA标准溶液的配置与标定⑴0.020mol/LEDTA溶液的配制称取4.0g乙二胺四乙酸二钠于500ml烧杯中,加200ml水,温热使其溶解完全,加水稀释至500ml,摇匀。
⑵配制0.020mol/L钙标准溶液准确称取110℃干燥过的CaCO30.50~0.55g,置于250ml锥形瓶中,用少量水润湿,盖上表面皿,慢慢滴加1:1 HCl 5 ml使其溶解,加少量水稀释,定量转移至250ml容量瓶中,用水稀释至刻度,摇匀,计算其准确浓度。
⑶EDTA溶液浓度的标定称取NaOH固体4.0g溶于100ml水中,配制成40g/LNaOH溶液。
移取25.00ml钙标准溶液置于250ml锥形瓶中,加5ml40g/LNaOH 溶液及少量钙指示剂,摇匀后,用EDTA溶液滴定至溶液由酒红色恰变为纯蓝色,即为终点。
平行滴定三份。
2、葡萄糖酸钙中钙含量的测定准确称取质量为2.0g的葡萄糖酸钙样品,置于100ml烧杯中,加入5ml6mol/L HCl,适当加热至完全溶解后冷至室温,定量转移至250ml容量瓶中,用水稀释至刻度,摇匀。
用移液管移取上述溶液25.00ml于锥形瓶中,加入5ml40g/LNaOH,再加少许钙指示剂,用EDTA标准溶液滴定至溶液由酒红色变为纯蓝色,记取EDTA耗用的体积,平行测定三份。
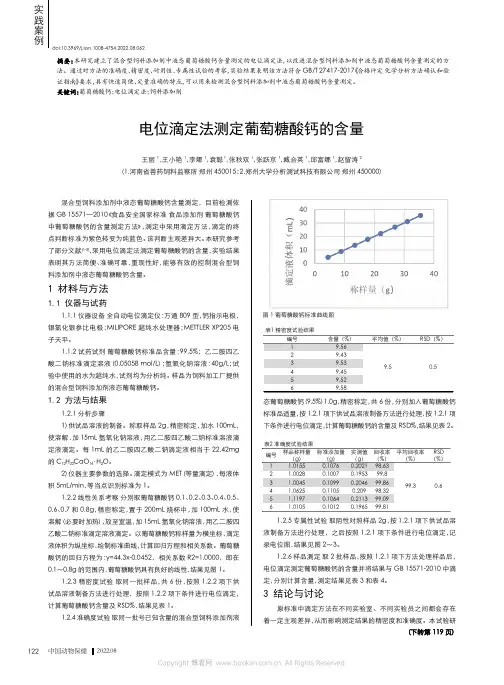
中国动物保健2022.08实践案例电位滴定法测定葡萄糖酸钙的含量王丽1,王小艳1,李娜1,袁聪1,张秋双1,张跃京1,臧合英1,邱富娜1,赵留涛2(1.河南省兽药饲料监察所郑州450015;2.郑州大学分析测试科技有限公司郑州450000)研究建立了混合型饲料添加剂中液态葡萄糖酸钙含量测定的电位滴定法,以改进混合型饲料添加剂中液态葡萄糖酸钙含量测定的方法。
通过对方法的准确度、精密度、耐用性、专属性试验的考察,实验结果表明该方法符合GB/T 27417-2017《合格评定化学分析方法确认和验证指南》要求,具有快速简便、定量准确的特点,可以用来检测混合型饲料添加剂中液态葡萄糖酸钙含量测定。
糖酸钙;电位滴定法;饲料添加剂混合型饲料添加剂中液态葡萄糖酸钙含量测定,目前检测依据GB 15571—2010《食品安全国家标准食品添加剂葡萄糖酸钙中葡萄糖酸钙的含量测定方法》,测定中采用滴定方法,滴定的终点判断标准为紫色转变为纯蓝色。
该判断主观差异大。
本研究参考了部分文献[1-3],采用电位滴定法测定葡萄糖酸钙的含量,实验结果表明其方法简便、准确可靠,重现性好,能够有效的控制混合型饲料添加剂中液态葡萄糖酸钙含量。
1材料与方法1.1仪器与试药1.1.1仪器设备全自动电位滴定仪:万通809型,钙指示电极,银氯化银参比电极;MILIPORE 超纯水处理器;METTLER XP205电子天平。
1.1.2试药试剂葡萄糖酸钙标准品含量:99.5%;乙二胺四乙酸二钠标准滴定溶液(0.05058mol/L );氢氧化钠溶液:40g/L ;试验中使用的水为超纯水,试剂均为分析纯。
样品为饲料加工厂提供的混合型饲料添加剂液态葡萄糖酸钙。
1.2方法与结果1.2.1分析步骤1)供试品溶液的制备。
称取样品2g ,精密称定,加水100mL ,使溶解,加15mL 氢氧化钠溶液,用乙二胺四乙酸二钠标准溶液滴定液滴定。
每1mL 的乙二胺四乙酸二钠滴定液相当于22.42mg 的C 12H 22CaO 14·H 2O 。

葡萄糖酸钙含量的测定思考题
1、传统的滴定法:葡萄糖酸钙可以与适当的指示剂配合使用滴定试剂进行滴定,通过观察滴定终点的变化来确定含量。
思考如何选择合适的滴定试剂和指示剂,并确定滴定过程的适当条件。
2、分光光度法:葡萄糖酸钙溶液的吸光度可以在特定波长下测量,可以利用标准曲线来计算含量。
思考如何选择合适的测量波长和建立准确的标准曲线。
3、离子色谱法:通过离子色谱仪分析样品中的葡萄糖酸钙离子。
思考如何选择合适的色谱柱和流动相,并优化分析条件以实现准确的测定。
4、原子吸收光谱法:使用原子吸收光谱仪测量样品中钙离子的浓度,从而计算葡萄糖酸钙的含量。
思考如何选择合适的工作波长和优化样品的制备条件。
5、红外光谱法:通过红外光谱仪对葡萄糖酸钙样品进行分析。
思考如何解读红外光谱图并确定葡萄糖酸钙的含量。

测定葡萄糖酸钙钙片中钙含量的方法比较贺琼【摘要】详细论述了EDTA滴定法与高锰酸钾间接滴定法测定钙片中钙含量的方法比较,从理论上来说,高锰酸钾法具有更高的准确度.通过对样品的测定结果表明,用EDTA滴定法测得钙含量为8.07%,用高锰酸钾间接滴定法测得钙含量为8.29%.经显著性检验,两种方法间不存在显著性差异,可以用EDTA配位滴定法代替高锰酸钾法进行钙含量的测定.【期刊名称】《广州化工》【年(卷),期】2013(041)009【总页数】3页(P159-160,183)【关键词】钙含量;测定;EDTA配位滴定法;高锰酸钾法;葡萄糖酸钙【作者】贺琼【作者单位】常州工程职业技术学院,江苏常州213164【正文语种】中文【中图分类】TQ462钙与身体健康息息相关,钙除成骨以支撑身体外,还参与人体的代谢活动,它是细胞的主要阳离子,还是人体最活跃的元素之一,因此,补钙越来越被人们所重视。
由于中国人的膳食结构因素,从儿童到老年普遍存在补钙问题,众多厂家抓住这一商机,大力宣传,全力推出补钙药品、保健品,目前国内市场有100 多种补钙剂。
我们有必要了解补钙剂中钙的含量。
根据人体需要选择适合自己的补钙方法。
钙片中钙含量的测定有滴定分析法、分光光度法和离子色谱法等很多种方法[1-7]。
鉴定于目前许多补钙制剂尚未收入国家药典,国家尚未提出补钙制剂中钙含量的统一方法[5]。
对此,采用EDTA 滴定法与高锰酸钾间接滴定法两种方法对钙片中钙含量进行测定。
由于钙片本身是颗粒状的,所以要研碎后才能作为试样,否则很难使钙片中的钙成分离解,影响对钙含量的测定。
用EDTA 滴定法是使指示剂与钙离子生成酒红色络合物,当EDTA滴定至终点时,游离出指示剂,溶液呈现蓝色。
用高锰酸钾间接滴定法是利用在弱酸性溶液中,,过滤洗涤后,用硫酸溶解,CaC2O4+2H+=Ca2++H2C2O4,生成用高锰酸钾标准溶液滴定,以高锰酸钾自身为指示剂,从而测得钙的含量。
葡萄糖酸钙检验操作程序目的:建立一个葡萄糖酸钙检验操作程序,以规范操作。
范围:适用于葡萄糖酸钙的质量检验。
责任人:化验员、QA检查员。
程序:检验依据:《中国药典》2010版二部第931页和企业标准。
1、简述:本品为D-葡萄糖酸钙盐-水合物。
含C12H22CaO14·H2O应为99.2%~103.0%。
2、性状:本品为白色颗粒性粉末;无臭,无味。
本品在沸水中易溶,在水中缓缓溶解,在无水乙醇、三氯甲烷或乙醚中不溶。
3、鉴别3.1、仪器与用具:试管、量筒、水浴锅、玻璃棒、天平、红外分光光度计薄层板、铂丝。
3.2、试剂:三氯化铁、。
乙醇-水浓氨溶液-乙酸乙酯(50:30:10:10)、钼酸铵-硫酸铈试液、盐酸、甲基红指示液、氨试液、草酸铵试液、醋酸、稀盐酸。
3.3、操作3.3.1、取本品约0.1g,加水5ml溶解后,加三氯化铁试液1滴,显深黄色。
3.3.2、取本品50mg,加水5ml,温水浴溶解,滤过,取滤液作为供试品溶液。
另取葡萄糖酸钙对照品,同法制成每1ml中含10mg的溶液,作为对照品溶液。
照薄层色谱法试验,吸取上述两种溶液各5µl,分别占于同一硅胶G薄层板上,以乙醇-水浓氨溶液-乙酸乙酯(50:30:10:10)为展开剂,展开,晾干,置110℃加热20分钟后,放冷,喷以钼酸铵-硫酸铈试液(取钼酸铵2.5g,加1mol/L硫酸溶液50ml使溶解,再加硫酸铈1.0g,加1mol/L硫酸溶液溶解并稀释至100ml,摇匀),再在110℃加热10分钟后,取也放冷,10分钟后检视。
供试品溶液所显主斑点的位置和颜色应与对照品溶液的主斑点相同。
3.3.3、本品的红外光吸收图谱应与对照的图谱(光谱集465图)一致。
3.3.4、本品的水溶液显钙盐的鉴别反应。
3.3.4.1、取铂丝,用盐酸湿润后,蘸取供试品,在无色火焰中燃烧,火焰即显砖红色。
3.3.4.2、取供试品溶液(1→20),加甲基红指示液2滴,用氨试液中和,再滴加盐酸至恰呈酸性,加草酸铵试液,即生成白色沉淀;分离,沉淀不溶于醋酸,但可溶于稀盐酸。

离子色谱法测定葡萄糖酸钙(锌)制剂的含量
刘文英;许茜;盛龙生;安登魁
【期刊名称】《中国药科大学学报》
【年(卷),期】1990(21)1
【摘要】采用Waters ILC-1离子液相色谱仪,IC-PAK A 50 mm×4.6 mm色谱柱,pH 6.1的1×10^(-3)mol/L邻苯二甲酸溶液为流动相,430型电导检测器检测,
由外标法和外标单点校正法测定了葡萄糖酸钙片和葡萄糖酸锌片的含量。
方法简便、快速,测定结果与中国药典法一致。
外标法和外标单点校正法测定葡萄糖酸钙注射
液的回收率分别为98.85%和99.59%,相关系数分别为0.9901(n=4)和
0.9911(n=4)。
外标单点校正法测定葡萄糖酸钙片和葡萄糖酸锌片的回收率分别为101.3%和101.4%,相关系数分别为0.9968(n=4)和0.9928(n=4)。
【总页数】4页(P31-34)
【关键词】葡萄糖酸钙;葡萄糖酸锌;离子色谱法
【作者】刘文英;许茜;盛龙生;安登魁
【作者单位】中国药科大学药物分析教研室
【正文语种】中文
【中图分类】R927.2
【相关文献】
1.离子色谱法测定氰化浸出液中金、银、铜、铁、钴、镍和锌的含量 [J], 叶艳清;马金晶;李银科;羊波;杨新周;胡秋芬
2.高效液相色谱法测定葡萄糖酸钙锌口服溶液中盐酸赖氨酸的含量 [J], 王艳芳;李琴;汪六英;李嘉楠
3.离子色谱法测定葡萄糖酸钙注射液中葡萄糖酸根的含量 [J], 李婕;韩春霞;黄海伟;张岩琛;何兰
4.离子色谱法测定雷尼替丁原料药及制剂中亚硝酸根含量 [J], 田珩;吴纯敏;贝琦华因版权原因,仅展示原文概要,查看原文内容请购买。

原子吸收法测定葡萄糖酸钙锌口服液的含量发布时间:2021-12-22T08:28:29.722Z 来源:《中国科技人才》2021年第27期作者:张丹丹[导读] 在难以获得量值准确的葡萄糖酸对照品的情况下,色谱方法会造成样品含量测定结果不够准确。
哈药集团三精制药有限公司黑龙江省哈尔滨市 150069摘要:采用原子吸收分光光度法测定葡萄糖酸钙锌口服液中钙和锌的含量,测钙的回归方程为A=0.0429C-0.0017(r=0.9999),测锌的回归方程为A=0.5743C-0.0082(r=0.9988),葡萄糖酸钙的平均回收率为101.4%,葡萄糖酸锌的平均回收率为99.07%。
建立的方法准确、简便、高效,不需要使用对照品,可用于葡萄糖酸钙锌口服溶液制剂中葡萄糖酸的绝对定量。
关键词:原子吸收;葡萄糖酸钙;葡萄糖酸锌;含量测定引言葡萄糖酸是葡萄糖分子中醛基经氧化生成的糖酸,可与钙锌离子通过配合形成水溶性的有机盐,与无机盐相比具有易吸收、对消化道无刺激的优点,儿童对于这种甜味的口服溶液依从性更好,是目前金属离子载体营养补充剂的首选。
葡萄糖酸钙锌口服溶液的市场定位人群主要为成长期儿童,其质量状况更应该成为关注的重点,以保证儿童用药安全。
各国药典收载的葡萄糖酸盐类制剂的质量标准仅针对钙离子或锌离子进行检测,葡萄糖酸仅采用鉴别反应进行考察,并未控制制剂中葡萄糖酸的含量。
制剂中葡萄糖酸的含量会影响到其与钙锌离子的配合,而且也会对产品的质量带来影响。
目前,葡萄糖酸含量测定方法有比色法、酶法、离子交换色谱(IEC)法、高效液相色谱(HPLC)法等。
比色法专属性较低;酶法操作过程繁琐,结果易受诸多因素影响不易控制,对操作人员的要求高;IEC和HPLC法是目前进行药物质量控制的常用方法,具有分析时间短、专属性强、样品处理简单等特点。
但IEC法中OH-淋洗液容易吸收空气中的二氧化碳,配制条件严苛;HPLC法中,葡萄糖酸保留不强,采用210nm波长检测,易受到背景干扰。
1 感官要求取10g 被测样品,置于洁净的白瓷盘中,用肉眼在自然光线下观察其色泽、组织形态、杂质,品尝其滋味,嗅其气味。
2 一般规定本标准所用试剂除非另有说明,在分析中仅使用确认为分析纯的试剂和GB/T 6682—2008中规定的三级水。
试验方法中所需标准滴定溶液、制剂及制品,在没有注明其他要求时,均按GB/T 601、GB/T 603 之规定制备。
3 鉴别试验3.1 试剂和材料3.1.1 冰乙酸。
3.1.2 苯肼:临用时蒸馏。
3.2 鉴别试验3.2.1 钙盐鉴别3.2.1.1 方法原理钙盐与草酸铵试液反应,生成白色沉淀,沉淀在乙酸中不溶解,但可溶解于稀盐酸。
3.2.1.2 分析步骤取约 1.0 g 实验室样品,精确至0.01 g,加40 mL水溶解,必要时加热使溶解,取此溶液按《中华人民共和国药典》2005 年版二部附录Ⅲ一般鉴别试验钙盐项下( 2 ),应显钙盐的鉴别反应。
3.2.2 葡萄糖的鉴别3.2.2.1 方法原理样品在乙酸介质中,与苯肼共热,生成黄色葡萄糖酰苯肼结晶。
3.2.2.2 分析步骤取约0.5 g 实验室样品,精确至0.01 g ,置10 mL 试管中,加 5 mL 水,溶解(必要时加热),加0.7 mL 冰乙酸和 1 mL 苯肼,在水浴上加热30min ,放至室温,用玻璃棒摩擦试管内壁,则析出黄色的结晶。
3.2.3 红外光吸收图谱鉴别采用溴化钾压片法测定,实验室样品的红外光吸收图谱应与对照的图谱《药品红外光谱集》465 图)一致,对照图谱见附录B。
4 葡萄糖酸钙的测定4.1 方法提要以钙紫红素为指示剂,用乙二胺四乙酸二钠标准滴定液滴定样品水溶液,根据乙二胺四乙酸二钠标准滴定液的用量,计算以C12H22CaO1·4 H2O计的葡萄糖酸钙的含量。
4.2 试剂与材料4.2.1 钙紫红素指示剂。
4.2.2 氢氧化钠溶液:40g/L 。
4.2.3 乙二胺四乙酸二钠标准滴定液:c(EDTA)=0.05mol/L 。

实验七葡萄糖酸钙含量的测定一、实训目的1.掌握EDTA滴定液的配制和标定方法。
2.了解酸度对配位平衡的影响,熟悉控制溶液酸度的方法。
3.掌握葡萄糖酸钙口服溶液的含量测定方法。
4.熟悉金属指示剂的变色原理。
二、实训原理葡萄糖酸钙口服溶液为D-葡萄糖酸钙盐-水合物(C12H22CaO14•H2O), 故可用配位滴定法滴定其中的钙离子,将供试品加水微热使溶解,加氢氧化钠试液与钙紫红素指示剂后用乙二胺四乙酸二钠滴定液滴定至溶液由紫色转变为纯蓝色即可:滴定前:Ca2++HIn2-+H+纯蓝色酒红色终点前:Ca2++H2Y2CaY2-+2H+终点时:CaIn-+H2Y2-CaY2-+HIn2-+H+酒红色纯蓝色三、仪器及试剂仪器:酸式滴定管(50ml)、容量瓶(250ml)、烧杯(1000ml)、试剂瓶(1000ml)、锥形瓶(250ml)、移液管(25ml)、托盘天平、分析天平或电子天平。
试剂:乙二胺四乙酸二钠盐(EDTA-2Na·2H2O,A·R)、ZnO(基准试剂)、铬黑T指示剂、钙紫红素指示剂、稀盐酸、甲基红指示剂、氨试液、氨-氯化铵缓冲液(pH=10),葡萄糖酸钙口服溶液(规格:10%)。
四、实训内容(一)EDTA滴定液的配制和标定称取EDTA二钠19g,加水适量使溶解,加水至1000ml(浓度约为0.05 mol/L),摇匀待标定。
取于800℃灼烧至恒重的基准氧化锌1.2g,精密称定,加稀盐酸30ml使溶解,定容于250 ml容量瓶中,用移液管精密吸取25ml 置锥形瓶中,加0.025%甲基红的乙醇溶液1滴,滴加氨试液至溶液显微黄色,加水25ml与氨-氯化铵缓冲液(pH=10.0)10ml,再加铬黑T指示剂少量,用本液滴定至溶液由紫色变为纯蓝色,并将滴定的结果用空白试验较正,平行测定3次取平均值。
每1ml EDTA滴定液(0.05000 mol/L)相当于4.069 mg的氧化锌。
案例一 尿素中氮含量的测定尿素CO (NH 2)2经浓硫酸消化后转化为(NH 4)2SO 4,过量的H 2SO 4 以甲基红作指示剂,用NaOH 标准溶液滴定至溶液从红色到黄色。
(NH 4)2SO 4为强酸弱碱盐,由于NH 4+ 的酸性太弱(K a =5.6×10-10 ),故不能用NaOH 标准溶液直接滴定。
但NH 4+可与甲醛作用定量地生成六次甲基四胺盐和H +,反应式为:4NH 4+ +6HCHO=(CH 2)6N 4H + +6H 2O+3H +由于生成的(CH 2)6N 4H + (K a =7。
1×10—6)和H +可用NaOH 标准溶液滴定,滴定终点生成的(CH 2)6N 4 是弱碱,,溶液的pH 值约为9,应选用酚酞为指示剂,滴定至溶液突现微红色即为终点。
试样中氮含量的计算式为:-3NaOH NaOH N N 10100%25.00250.0C V M m ω⨯=⨯⨯试样案例二 阿司匹林药片中乙酰水杨酸含量的测定 阿司匹林的主要成分是乙酰水杨酸。
乙酰水杨酸是有机弱酸(K a =1。
0×10—3),结构式,1r M 180.16g mol -=⋅,微溶于水,易溶于乙醇。
在强碱性溶液中溶解并水解为水杨酸和乙酸盐,反应式如下:乙酰水杨酸含量的计算式为:3NaOH NaOH HCl HCl 1)M 10210100%10.00250.0C V C V m ω-⨯-⨯⨯=⨯⨯乙酰水杨酸乙酰水杨酸试样( 由于药片中一般都添加一定量的赋形剂如硬脂酸镁、淀粉等不溶物,不宜直接滴定,可采用返滴定法进行测定.将药片研磨成粉末状后加入过量的NaOH 标准溶液,加热一段时间使乙酰基水解完全,再用HCl 标准溶液回滴过量的NaOH ,滴定至溶液由红色变为接近无色即为终点。
在这一滴定反应中,1mol 乙酰水杨酸消耗2molNaOH 。
案例三 离子交换树脂交换容量的测定离子交换树脂是一种高分子聚合物的有机交换剂,具网状结构,在水、酸、碱中难溶,对有机溶剂、氧化剂、还原剂及其它化学试剂具有一定的稳定性,对热也比较稳定.在离子交换树脂的网状结构的骨架上,有许多可以与溶液中离子起交换作用的活性基团,例如—SO 3H 、-COOH 等。
火焰原子吸收光谱法测定葡萄糖酸钙口服液的含量发布时间:2021-12-31T02:27:57.093Z 来源:《中国科技人才》2021年第25期作者:肖箫[导读] 钙元素被称为人体的生命元素,在人成长的各个阶段钙都起到极其重要的作用。
缺钙可引起钙代谢失调,导致儿童佝偻病和成人骨质疏松病,还会容易造成蛀牙、骨胳软化症、幼儿发育不良等。
哈药集团三精制药有限公司黑龙江省哈尔滨市 150069摘要:目的:通过火焰原子吸收影响下的测定光谱法来对葡萄糖酸钙药品在口服液状态下的成分含量。
方法:借助吸收火焰原子吸收的测定光谱法来对葡萄糖酸钙药品的主要成分含量进行测定,同时还采取了标准曲线的测定方法辅助测量分析工作。
结果:完成测量工作之后获取以下测量结果:钙元素的线性范围为1.7-11.75μg/mL(r=0.9992),葡萄糖酸钙药品的线性范围为25.8-132.4μg/mL(r=0.9981),平均回收率数值为102.11%(n=9)。
结论:对口服液状态下的葡萄糖酸钙药品的成分进行有效测定。
关键词:火焰原子吸收光谱法;葡萄糖酸钙口服液;含量测定钙元素被称为人体的生命元素,在人成长的各个阶段钙都起到极其重要的作用。
缺钙可引起钙代谢失调,导致儿童佝偻病和成人骨质疏松病,还会容易造成蛀牙、骨胳软化症、幼儿发育不良等。
给孩子补钙一直是这个时代的主题,由于人体中的钙有99%是存在于骨头及牙齿之中,一旦钙质不足,骨头就会变得易碎且不够坚固,极易产生骨折现象。
骨质疏松症虽是成人疾病,但发生原因可远朔至童年及青少年期的钙质摄取不足。
宝宝的牙齿发育也需要钙质,足够的钙可保持牙齿及牙龈的健康,并减少日后蛀牙的机会。
除了骨骼及牙齿外,还有剩余1%的钙质分散于各种软件组织和体液中,这些钙质在成人体内虽不超过10克,却在人体中扮演极重要的角色。
一、材料与方法1、材料。
WFX-120型火焰原子吸收分光光度计;钠空心阴极灯;葡萄糖酸钙口服溶液(规格为10mL/支,每mL含葡萄糖酸钙100mg;钙元素标准溶液(1000μg/mL;氯化锶;盐酸;硝酸;水为超纯水。
实验七葡萄糖酸钙含量的测定一、实训目的1.掌握EDTA滴定液的配制和标定方法。
2.认识酸度对配位均衡的影响,熟习控制溶液酸度的方法。
3.掌握葡萄糖酸钙口服溶液的含量测定方法。
4.熟习金属指示剂的变色原理。
二、实训原理葡萄糖酸钙口服溶液为 D-葡萄糖酸钙盐-水合物(C12H22CaO14?H2O),故可用配位滴定法滴定此中的钙离子,将供试品加水微热使溶解,加氢氧化钠试液与钙紫红素指示剂后用乙二胺四乙酸二钠滴定液滴定至溶液由紫色转变成纯蓝色即可:滴定前:Ca2++HIn2-CaIn-+H+纯蓝色酒红色终点前:Ca2++H2Y2-CaY2-+2H+终点时:CaIn-+H22-CaY-+HIn2-+H+酒红色纯蓝色三、仪器及试剂仪器:酸式滴定管(50ml)、容量瓶(250ml)、烧杯(1000ml)、试剂瓶(1000ml)、锥形瓶(250ml)、移液管(25ml)、托盘天平、剖析天平或电子天平。
试剂:乙二胺四乙酸二钠盐(EDTA-2Na·2H2O,A·R)、ZnO(基准试剂)、铬黑T指示剂、钙紫红素指示剂、稀盐酸、甲基红指示剂、氨试液、氨-氯化铵缓冲液(pH=10),葡萄糖酸钙口服溶液(规格: 10%)。
四、实训内容(一)EDTA滴定液的配制和标定称取EDTA二钠19g,加水适当使溶解,加水至1000ml(浓度约为mol/L),摇匀待标定。
取于800℃灼烧至恒重的基准氧化锌,精细称定,加稀盐酸30ml使溶解,定容于250ml容量瓶中,用移液管精细汲取25ml置锥形瓶中,加0.025%甲基红的乙醇溶液1滴,滴加氨试液至溶液显微黄色,加水25ml与氨-氯化铵缓冲液()10ml,再加铬黑T指示剂少许,用本液滴定至溶液由紫色变成纯蓝色,并将滴定的结果用空白试验较正,平行测定3次取均匀值。
每1mlEDTA滴定液(mol/L)相当于mg的氧化锌。
依据本液的耗费量与氧化锌的取用量,算出本液的浓度,即得。
葡萄糖酸钙含量测定【实验目的】1、熟悉掌握配位滴定法。
2、定量测出葡萄糖酸钙含量。
【实验原理】葡萄糖酸钙含有钙元素,可凭借配位滴定法测定钙元素含量来间接测定葡萄糖酸钙含量。
取适量样品溶解,加NH3-NH4Cl缓冲溶液与EBT(铬黑T)指示剂,用EDTA滴定液滴定至溶液由紫红色转变为纯蓝色。
此时读出EDTA滴定液使用量,计算可得样品中钙元素的含量,由此则可以计算出葡萄糖酸钙的质量,与取用样品质量对比,则可得出样品的葡萄糖酸钙含量。
反应式如下:Ca2++H2In-→CaIn-(红色)+2H+Ca2++H2Y2-→CaY2-+2H+H2Y2-+CaIn-→H2In-(蓝色)+CaY2-【试剂与仪器】试剂:蒸馏水、0.05mol/L EDTA滴定液、葡萄糖酸钙样品、0.100mol/LNH3-NH4Cl缓冲溶液、EBT(铬黑T)指示剂。
仪器:电子天平,200ml锥形瓶若干、三脚架、石棉网、酒精灯、25ml吸量管、酸碱两用滴定管、100ml量筒。
【实验步骤】1.用电子天平称取葡萄糖酸钙样品约0.500g,并记录准确称量数据为M。
2.加蒸馏水至100.0ml,微温,轻摇,使之溶解。
3.加0.100mol/L氢氧化钠试液15ml与钙紫红素指示剂约0.1g。
4.取装有0.05mol/LEDTA滴定液的滴定至溶液由紫色转变为纯蓝色,记录消耗EDTA滴定液的体积V1(ml)。
计算Ca2+含量:c(Ca2+)=c(EDTA)×V1(EDTA)/V(水样)×1000(mmol·L-1)5.计算得样品中Ca2+含量后可计算样品中的葡萄糖酸钙含量,记为m,计算百分含量,即m/M6.重复测定4~6次,求均值。
精品 Word 可修改欢迎下载精品 Word 可修改 欢迎下载【实验数据与表格】日期: 温度: 相对湿度:【思考题】1. 配位滴定中为什么要加入缓冲溶液?2. 通常使用乙二胺四乙酸二钠盐配制EDTA 标准溶液,为什么不用乙二胺四乙酸?3. 在配位滴定中,指示剂应具备什么条件?4. 如果只用铬黑T 指示剂,能否测定Ca 2+的含量?如何测定?5. 配位滴定法与酸碱滴定法相比,有哪些不同点?操作当中应注意哪些问题?【参考文献】[1]北京师范大学无机化学教研室编.无机化学实验.第3版.北京:高等教育出版社,2001 [2]李雪华.基础化学实验.北京:人民卫生出版社,2002 [3]唐中珅,陈清原.医用化学实验.北京:科学出版社,2010 [4]张枫,房晨婕.医用化学基础.北京:中国协和医科大学出版社,2010实验次数 1 2 3 4 5 6 样品质量M/g 0.100mol/LNaOH/ml 15.00 15.00 15.00 15.00 15.00 15.00 EBT(铬黑T)指示剂/g 约0.1 约0.1 约0.1 约0.1 约0.1 约0.1 0.05mol/LEDTA 用量/ml m (C 12H 22CaO 14·H 2O )/g百分含量(m/M)含量平均值1、最困难的事就是认识自己。
葡萄糖酸钙含量的测定
实验目的:
1.强化滴定法的操作
2.强化分析天平,容量瓶移液管,吸量管,滴定管 ,锥形瓶 ,溶液配制及转移
容量仪器的洗涤干燥,滴定分析操作
实验原理:
)/(1000)()()(22L mmol V EDTA V EDTA C ca C ⨯⨯=+水样
1,EDTA 是常用的螯合滴定剂,可滴定多种金属离子,与金属离子按1:1的比例
结合
2.在待测液中加入钙红指示剂(蓝色) 它与钙离子配位呈红色
3.滴定时,EDTA 先与游离钙离子配位,然后夺取已和指示剂配位的钙离子,从
而使指示剂被释放出来,达终点时,溶液由红色变为蓝色,此时可根据EDTA 标
准溶液消耗量计算出钙离子的含量
仪器与试剂:
仪器:分析天平,100ml 容量瓶,5ml 吸量管 滴定管,锥形瓶 ,烧杯,滴定台,药勺,洗耳球,玻璃棒,胶头滴管
试剂:待测葡萄糖酸钙粉末,钙红指示剂,蒸馏水,0.05 mol/L 的EDTA 标准溶
液
实验步骤:
1,用分析天平称量3g葡萄糖酸钙粉末
2.将葡萄糖酸钙粉末溶于10ml50~60℃的蒸馏水中
3. 将葡萄糖酸钙溶液转移到100ml容量瓶中,用胶头滴管加入蒸馏水至刻度线
4.从容量瓶中取出部分溶液到烧杯中,用吸量管吸取20.00ml溶液到锥形瓶中,
0.05mol/L的EDTA标准溶液加入到滴定管中,记下初始读数,
6.开始滴定,当溶液由红色变成蓝色时停止滴定,记下此时读数,
7.再重复滴定两次
数据记录与结果分析
日期:温度:
结实验编号 1 2 3 葡萄糖酸钙溶液
V(EDTA)/ml
V初(EDTA)/ml
平均(EFTA)/ml
相对平均偏差 /%
葡萄糖酸钙含量/%
讨论。