有机物分子中的原子共线共面(学案)
- 格式:doc
- 大小:237.03 KB
- 文档页数:4

如何分析有机物分子中原子共平面的问题有机物分子中原子共平面的问题,解决方法是:由简单到复杂。
首先要掌握以下几种最简单有机物的空间构型:(1)乙烯(CH 2CH 2)分子是平面结构,2个碳原子、4个氢原子共平面;(2)乙炔(C C H H )分子是直线型结构,4个原子在同一直线上;(3)苯()分子是平面正六边形结构,6个碳原子、6个氢原子共平面;(4)甲烷(CH 4)是正四面体结构,任意3个原子共平面;(5)甲醛(C H H O)分子是平面结构,4个原子共平面.在判断有机物分子中原子共平面情况时.要结合以上五种最简单物质的结构进行分析.例1请分析苯乙炔(C CH )分子中最多有多少个原子共平面? 分析:与C CH 直接相连的苯环上的碳原子相当于C C H H分子中1个氢原子所处的位置,应与C CH 在同一条直线上;与苯环相连的C CH 中碳原子相当于苯分子中氢原予所处的位置,应在苯环所在的平面内。
由此可知C CH 所在直线上有两点在苯环的平面内,所以苯己炔分子中所有原子均在同一平面,即苯乙炔分子中8个碳原子、6个氢原子均在同一平面内.,例2:有机物C CH 2CHO H分子中至少有多少个碳原子处于同一平面上?分析:由苯分子的空问构型可知,苯环上的6个碳原子、4个氢原子以及与苯环直接相连的两个碳原子一定共平面.由乙烯的分子结构可知,CH 2C H 中的原子在同一平面。
由乙醛分子结构可知,CHO 中的原子在同一平面。
由碳碳单键可以旋转,可知C CH 2CHO H分子中所有的原子可以共面。
例3:结构式为CH 3CH 3的烃,分子中至少有多少个碳原子处在同一平面上?分析:由苯分子的空间结构可知,苯环上的六个碳原子以及与它直接相邻的两个碳原子共面。
另外与苯环相连的另一苯环对位上的碳原子,处于两苯环旋转的轴线(两苯环之间的碳碳键可以旋转)上,也应该共面另外.与苯环相连的另一苯环对位上的碳原子,处于两苯环旋转轴线(两苯环之间的碳碳单键可以旋转)上,也应该共平面。
有机物分子中原子的共面共线问题有机分子中原子的共面共线是中学有机化学教学的一个难点。
此类题目的解题思维方法如下:原子共面共线问题思维的基础:甲烷的正四面体结构;乙烯、苯的平面结构;乙炔的直线结构。
1、甲烷的正四面体结构在甲烷分子中,一个碳原子和任意个氢原子可确定一个平面。
当甲烷分子中某氢原子被其他原子或原子团取代时,该代替原子的共面问题,可将它看作是原来氢原子位置。
丙烷其结构式可写成如图2所示,丙烷分子中最多原子可能共面。
2、乙烯的平面结构乙烯分子中的所有原子都在同一平面内,键角为120°。
当乙烯分子中某氢原子被其他原子或原子团取代时,则代替该氢原子的原子一定在乙烯的平面内。
CH3CH=CH2 原子一定共面,最多原子可能共面。
3.苯的平面结构苯分子所有原子在同一平面内,键角为120°。
当苯分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定在苯分子所在平面内。
甲苯如右下图所示,甲苯分子中最多有可能是个原子共面。
4.乙炔的直线结构乙炔分子中的2个碳原子和2个氢原子一定在一条直线上,键角为180°。
当乙炔分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定和乙炔分子的其他原子共线。
丙炔如图所示,丙炔分子中有个原子共线。
巩固练习:1、描述CH3-CH=CH-C≡C-CF3分子结构下列叙述中,正确的是A.6个碳原子有可能都在一条直线上B.6个碳原子不可能都在一条直线上C.6个碳原子有可能都在一个平面上D.6个碳原子不可能都在一个平面上2、甲烷分子中的4个氢原子全部被苯基取代,可得如图所示的分子,对该分子的描述不正确的是()A.分子式为C25H20B.分子中所有原子有可能处于同一平面C.该化合物分子中所有原子不可能处于同一平面D.分子中所有原子一定处于同一平面3、盆烯是近年合成的一种有机物,它的分子结构可简化表示为(其中C、H原子已略去),下列关于盆烯的说法中错误的是()A.盆烯是苯的一种同分异构体B.盆烯分子中所有的碳原子不可能在同一平面上C.盆烯是乙烯的一种同系物D.盆烯在一定条件下可以发生加成反应4、某烃的结构简式为CH3―CH2―CH=C(C2H5)―C≡CH分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数量最多为b,一定在同一平面内的碳原子数为c,则a、b、c分别为()A.4、3、5 B.4、3、6 C.2、5、4 D.4、6、45、观察以下有机物结构:CH3 CH2CH3(1) C = CH H (2) H—C≡C—CH2CH3 (3) CH=CF2思考:最多有几个碳原子共面、、最多有几个碳原子共线、、有几个不饱和碳原子、、不饱和度及其应用不饱和度又称为“缺氢指数”,用希腊字母Ω来表示,顾名思义,它是反映有机物分子不饱和程度的量化标志。

有机物中原子共平面、共线问题剖析有机物分子中原子共平面的问题,解决方法是:由简单到复杂,要联合以下五种最简单物质的结构进行剖析。
(1) 乙烯 ( CH2CH2)分子是平面构造,2个碳原子、4个氢原子共平面;(2) (2) 乙炔 ( H C C H )分子是直线型构造, 4 个原子在同向来线上;(3) (3) 苯 () 分子是平面正六边形构造, 6 个碳原子、 6 个氢原子共平面;(4)(4) 甲烷 (CH4) 是正四周体构造 , 随意 3 个原子共平面 ;O(5)(5) 甲醛 ( H C H) 分子是平面构造, 4 个原子共平面。
一、甲烷的空间构型 ---- 正四周体型构造式、分子构型如图一 :其键角 109 度 28 分,很明显甲烷中一个碳原子和四个氢原子不可以共面,在甲烷分子中, 1 个碳原子和随意 2 个氢原子可确立一个平面,其余的 2 个氢原子位于该平面的双侧,即甲烷分子中有且只有三原子共面 ( 称为三角形规则) 。
以甲烷母体模型衍变成-------一氯甲烷、乙烷当甲烷分子中某氢原子被其余原子或原子团取代时,该取代原子的共面问题,可将它看作是本来氢原子地点。
若将此中一个氢原子换成一个氯原子,因为C-H 键键长短于C-Cl 键长则以氯原子为极点的正三棱锥如图二(1),相同这五个原子不可以共面。
同理将甲烷中的一个氢原子换为甲基,则变成乙烷如图二( 2)所示:C-C 单键能够自由转动以,相同这些原子不可以共面。
可见凡是碳原子以单键形式存在其所连四个碳原子不可以共面。
二、乙烯的空间构型----平面型构造式、分子构型如图三:平面型构造,键角为120 度, C=C 所连的四个氢原子与这两个碳原子同在一个平面上。
当乙烯分子中某氢原子被其余原子或原子团取代时,则取代该氢原子的原子必定在乙烯的平面内。
需要注意的是:C=C 不可以转动, C-H 键能够转动。
以乙烯母体模型衍变成-------丙烯、2-丁烯若将此中的氢原子换成氯原子,其与全部碳氢原子共面。
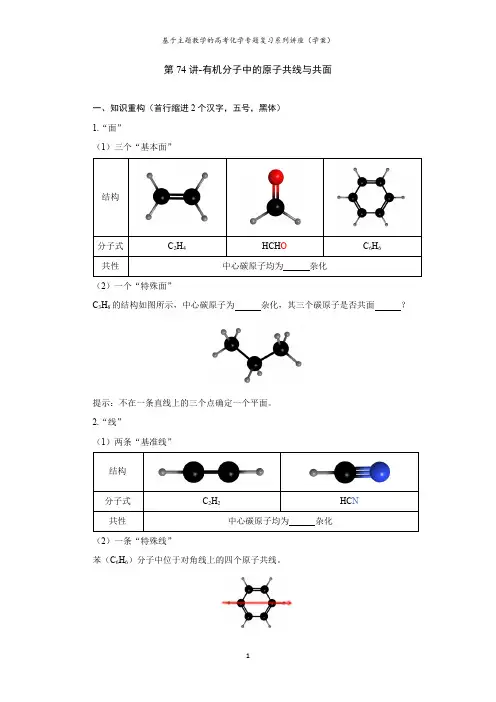
第74讲-有机分子中的原子共线与共面一、知识重构(首行缩进2个汉字,五号,黑体)1.“面”(1)三个“基本面”(2)一个“特殊面”C3H8的结构如图所示,中心碳原子为杂化,其三个碳原子是否共面?提示:不在一条直线上的三个点确定一个平面。
2.“线”(1)两条“基准线”(2)一条“特殊线”苯(C6H6)分子中位于对角线上的四个原子共线。
3. “面”组合结构分析(1)“甲基—基本面”组合(2)“甲基—特殊面”组合(3)“基本面—基本面”组合(4)“基本面—特殊面”组合正丙苯(C6H5CH2CH2CH3)分子中最多有个碳原子共面。
4. “线”组合结构分析(1)“甲基—基准线”组合(2)“甲基—特殊线”组合甲苯(C6H5CH3)分子中最多有个原子共线。
(3)“基准线—特殊线” 组合苯乙炔(C 6H 5C CH )分子中最多有 个原子共线;最多有 个原子共面。
5. “线—面”组合结构分析HCC CH CH 2分子中最多有 个原子共线;最多有 个原子共面。
6. 多元组合结构分析C C HH HC CHCH CCH 2HC分子中最多有 个原子共线;最多有 个原子共面。
二、重温经典1.(2022辽宁卷,8节选)下列关于苯乙炔(HC C )的说法正确的是B.分子中最多有5个原子共直线 【答案】错【解析】如图所示,苯乙炔分子中最多有 6 个原子共直线。
2.(2022浙江1月,6节选)关于如图化合物,下列说法正确的是CCHHCCN HO O CH 3A.分子中至少有7个碳原子共直线 【答案】错【解析】如图所示,化合物中1号碳原子为sp 3杂化,除本身位于图中所示直线上,其余均不在直线上,所以分子中有 6 个原子共直线。
3.(2022全国乙卷,8节选)一种实现二氧化碳固定及再利用的反应如下,下列叙述正确的是A .化合物1分子中的所有原子共平面 【答案】错 【解析】如图所示,化合物1中碳原子1和碳原子2均为sp 3杂化,所有原子一定不共面。
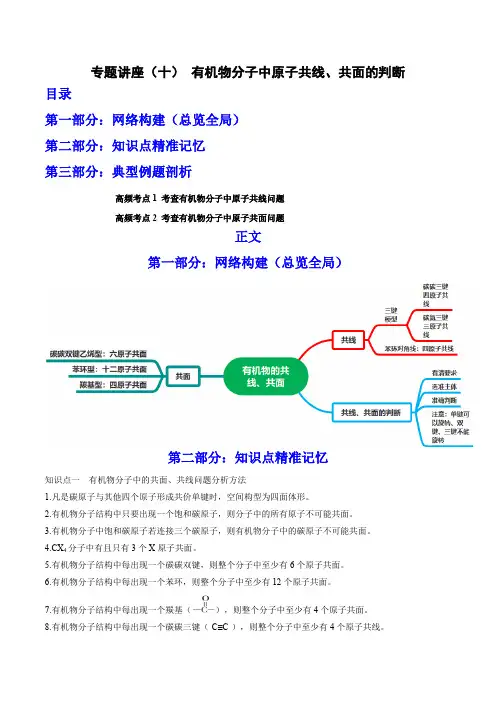
专题讲座(十)有机物分子中原子共线、共面的判断目录第一部分:网络构建(总览全局)第二部分:知识点精准记忆第三部分:典型例题剖析高频考点1 考查有机物分子中原子共线问题高频考点2 考查有机物分子中原子共面问题正文第一部分:网络构建(总览全局)第二部分:知识点精准记忆知识点一有机物分子中的共面、共线问题分析方法1.凡是碳原子与其他四个原子形成共价单键时,空间构型为四面体形。
2.有机物分子结构中只要出现一个饱和碳原子,则分子中的所有原子不可能共面。
3.有机物分子中饱和碳原子若连接三个碳原子,则有机物分子中的碳原子不可能共面。
4.CX4分子中有且只有3个X原子共面。
5.有机物分子结构中每出现一个碳碳双键,则整个分子中至少有6个原子共面。
6.有机物分子结构中每出现一个苯环,则整个分子中至少有12个原子共面。
7.有机物分子结构中每出现一个羰基(),则整个分子中至少有4个原子共面。
8.有机物分子结构中每出现一个碳碳三键(-C≡C-),则整个分子中至少有4个原子共线。
9.有机物分子结构中每出现一个苯环,则整个分子中至少有3条对角线,分别是4个原子共线。
10.有机物分子结构中每出现一个碳氮三键(-C≡N),则整个分子中至少有3个原子共线。
说明:单键可旋转,双键或三键不能旋转。
知识点二判断有机物分子中原子能否共面、共线的方法1.熟练掌握五种基本模型对比参照①分子中碳原子若以四条单键与其他原子相连(含有四面体结构C原子),则所有原子一定不能共平面,如CH3Cl、甲烷分子中所有原子一定不共平面,最多有3个原子处在一个平面上。
②含有,至少6个原子一定共平面,乙烯分子中所有原子一定共平面,若用其他原子代替其中的任何氢原子,如CH2===CHCl所得有机物中所有原子仍然共平面。
③含有结构,至少12个原子一定共平面,苯分子中所有原子一定共平面,若用其他原子代替其中的任何氢原子,所得有机物中所有原子也仍然共平面,如溴苯()。
含有结构的对角线一定有4个原子共线,若用其他原子代替对角线上的任何氢原子,所得有机物苯环对角线上所有原子也仍然共线。


有机物分子中的共线共面问题教案课1. 概述在有机化学中,有机物分子的共线共面问题是一个非常重要的概念。
它不仅涉及到有机物分子的空间构型,还关乎着化学反应的进行以及产物的选择性。
深入理解有机物分子的共线共面问题对于有机化学学习是至关重要的。
本文将结合有机化学的教学实际,以及学生的学习情况,探讨有机物分子中的共线共面问题教案课的设计。
2. 共线共面问题的基本概念共线共面问题是有机化学中的一个重要概念,它指的是在有机分子中,若两个或多个原子或基团位于同一直线上,则称它们是共线的;若多个原子或基团位于同一平面上,则称它们是共面的。
在有机化学中,共线共面问题不仅涉及到分子的空间构型,还紧密关联着反应的进行以及产物的选择性。
共线共面问题的探讨需要从简到繁地进行。
可以以最简单的烷烃分子为例,引导学生理解共线共面问题的基本概念。
通过分子模型的展示或是计算机模拟的方式,让学生直观地感受分子中原子的排布及其共线共面关系。
可以逐步引入含有双键、环状结构等有机物分子,让学生应用共线共面的概念来分析分子构型,理解其在反应中的作用。
3. 教学内容设计在设计有机物分子中的共线共面问题教案课时,需要根据学生的实际情况和教学大纲来合理安排教学内容。
可以从以下几个方面展开教学内容:3.1. 共线共面问题概念的引入首先需要向学生介绍共线共面问题的基本概念,包括定义、特点以及在有机化学中的应用。
可以通过实例或案例分析的方式,让学生从直观的角度认识共线共面问题,建立概念的基础。
3.2. 共线共面问题在反应中的影响可以引导学生探讨共线共面问题在不同有机反应中的作用。
在亲核加成反应中,分子中的双键和亲核试剂的相对位置就涉及到共线共面问题,影响着反应的进行和产物的选择性。
通过分子模型的展示或实验数据的分析,让学生理解共线共面问题在反应中的重要性。
3.3. 拓展与应用可以引导学生应用共线共面问题的概念,对一些常见的有机化合物进行分析和讨论。
对于含有多个不同取代基的环状化合物,学生可以根据共线共面问题来预测其可能的立体异构体和反应活性。

有机物分子中原子共线、共面问题教学目标1.掌握典型代表物甲烷、乙烯、乙炔、苯,这四种物质的空间构型2.2.以五种常见物质(甲烷、乙烯、乙炔、苯)的分子构型推断一些简单分子中的原子数共面问题或者共线问题。
3.3.学生借助分子模型加深理解典型物质的分子构型4.4.学生通过动手搭建有机物分子模型,加深理解碳四价的特点。
教学过程一. 基本空间构型1、熟记五类分子空间构型代表物空间构型结构球棍模型结构特点CH4正四面体任意3点(原子)共面C—C键可以旋转C2H4平面结构6点共面C=C键不能旋转C2H2直线型4点共线(面) C≡C键不能旋转C6H6平面正六边形12点共面HCHO 平面4点共面二、结构不同的基团连接后原子共面分析1.直线与平面连接:直线结构中如果有2个原子(或者一个共价键)与一个平面结构共用,则直线在这个平面上。
如CH2=CH-C≡CH,其空间结构为,中间两个碳原子既在乙烯平面上,又在乙炔直线上,所以直线在平面上,所有原子共平面。
2.平面与平面连接:如果两个平面结构通过单键(σ键)相连,则由于单键的旋转性,两个平面不一定重合,但可能重合。
如苯乙烯分子中共平面原子至少12个,最多16个。
3.平面与立体连接:如果甲基与平面结构通过单键相连,则由于单键的旋转性,甲基的一个氢原子可能暂时处于这个平面上。
如丙烯分子中,共面原子至少6个,最多7个。
4.直线、平面与立体连接:分析时要注意:观察大分子的结构,先找出甲烷、乙烯、乙炔和苯分子的“影子”,再将甲烷“正四面体”、乙烯“平面型”、乙炔“直线形”和苯“平面型”等分子构型知识迁移过来即可。

复习(共面、共线问题)班级姓名小组【学习目标】1.通过回顾甲烷、苯、乙烯的结构,能准确说出分子中共线、共面原子个数;2.通过小组讨论,能准确说出—CH3、-CH═CH2、-C≡C H、-CN、-C6H5相互组合中的原子共线、共面的个数;3.通过小组讨论,能根据反应的特点,确定给定反应的化学反应类型;4.通过小组讨论,以CH4、CH2═CH2、C6H6为例,能够准确说出其同系物典型的化学性质。
【重点难点】重点:有机物分子中共线、共面原子个数;化学反应类型的区分;有机物典型的化学性质。
难点:有机物分子中共线、共面原子个数;陌生反应的化学反应类型的确定。
【导学流程】一、基础感知知识链接:①CH≡C H、HCN分子结构为直线型。
②双键(如:C═C、C═O等)不可扭转,单键可扭转。
③三点确定一个平面;一条直线与线外一点定一平面;两点确定一条直线。
1.CH4的空间构型_________,最多_______个原子共面;2.CH2═CH2的空间构型_________,最多_______个原子共面;3.的空间构型_________,最多_______个原子共面,___个原子共线;4. 确定下列物质的共线、共面原子个数:最多_______个原子共面,一定存在________个原子共面;①②CH2═CH-CH═CH2,最多_______个原子共面,一定存在________个原子共面;③由CH3--CH═CH-C≡C-CH3可知,最多_______个原子共面,最多_______个原子共线。
④最多_______个原子共面;⑤CH2═CH-CN,最多_______个原子共面;| |<思考>只要有—CH3、—CH2—(亚甲基)、—CH—、—C—等的所有原子不可能全部共面。
|。
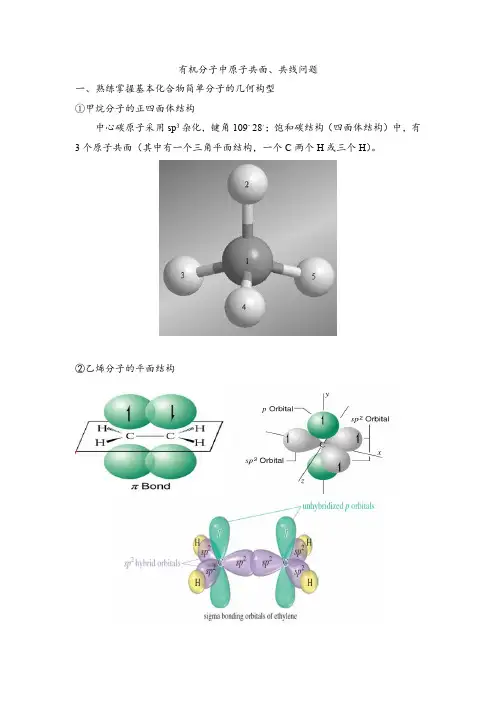
有机分子中原子共面、共线问题一、熟练掌握基本化合物简单分子的几何构型①甲烷分子的正四面体结构中心碳原子采用sp3杂化,键角109。
28,;饱和碳结构(四面体结构)中,有3个原子共面(其中有一个三角平面结构,一个C两个H或三个H)。
②乙烯分子的平面结构烯烃结构中6个原子均在同一平面上。
双键碳采用sp2杂化,三个sp2杂化轨道处在同一平面,还剩下一个未杂化的p轨道与该平面垂直。
碳原子用杂化轨道与其他碳原子、氢原子形成σ键,各用一个未杂化p轨道“肩并肩”重叠形成π键。
③乙炔分子的直线结构炔烃结构中4个原子在同一条直线上(当然共面)。
三键碳原子为sp杂化,两个sp轨道处在同一直线上,每个三键碳还各有两个相互垂直的p轨道。
每个三键碳原子各用一个杂化轨道与其他碳原子、氢原子形成σ键,各用两个未杂化的p轨道“肩并肩”重叠形成两个相互垂直的π键。
④苯分子的平面正六边形结构苯环结构中12个原子共平面,4个原子共线。
苯环上的六个碳原子均为sp2杂化,每个碳的三个sp2杂化轨道之间的键角均为120。
每个碳原子用杂化轨道分与相邻两个碳原子和氢原子形成σ键,由于sp2杂化轨道均处在同一平面上,因此六个氢原子和六个碳原子共平面。
每个碳原子上还有一个未杂化的垂直于环平面的p轨道,六个p轨道彼此形成离域键(大π键)。
⑤1,3-丁二烯分子的结构四个碳原子均采用sp2杂化,四个碳原子中未杂化的p轨道肩并肩重叠,形成离域键。
离域键的存在,使键长平均化、分子稳定性增加。
二、不同结构连接的共面分析单键可旋转:即两个结构通过一个单键相连,共用2个原子。
单键可旋转,即两个平面共有一条线,两个平面可能重合,也可能不重合。
(1)直线与平面连接CH2=CH−C≡CH共面原子至少8个,最多8个苯乙炔共面原子至少14个,最多14个(2)平面与平面苯乙烯分子中共平面原子至少12个,最多16个。
联苯苯环与苯环相连,共面原子最多22个,至少14个(不管单键如何旋转,10 C、20 H总是处于另一个苯环平面上。
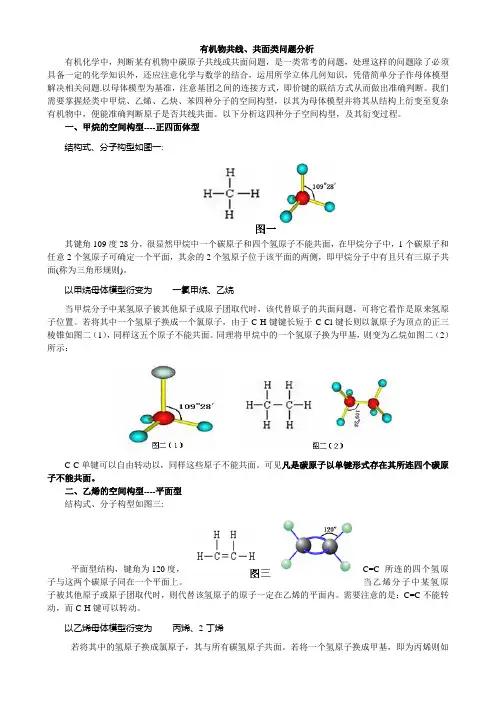
有机物共线、共面类问题分析有机化学中,判断某有机物中碳原子共线或共面问题,是一类常考的问题,处理这样的问题除了必须具备一定的化学知识外,还应注意化学与数学的结合,运用所学立体几何知识,凭借简单分子作母体模型解决相关问题.以母体模型为基准,注意基团之间的连接方式,即价键的联结方式从而做出准确判断。
我们需要掌握烃类中甲烷、乙烯、乙炔、苯四种分子的空间构型,以其为母体模型并将其从结构上衍变至复杂有机物中,便能准确判断原子是否共线共面。
以下分析这四种分子空间构型,及其衍变过程。
一、甲烷的空间构型----正四面体型结构式、分子构型如图一:其键角109度28分,很显然甲烷中一个碳原子和四个氢原子不能共面,在甲烷分子中,1个碳原子和任意2个氢原子可确定一个平面,其余的2个氢原子位于该平面的两侧,即甲烷分子中有且只有三原子共面(称为三角形规则)。
以甲烷母体模型衍变为-------一氯甲烷、乙烷当甲烷分子中某氢原子被其他原子或原子团取代时,该代替原子的共面问题,可将它看作是原来氢原子位置。
若将其中一个氢原子换成一个氯原子,由于C-H键键长短于C-Cl键长则以氯原子为顶点的正三棱锥如图二(1),同样这五个原子不能共面。
同理将甲烷中的一个氢原子换为甲基,则变为乙烷如图二(2)所示:C-C单键可以自由转动以,同样这些原子不能共面。
可见凡是碳原子以单键形式存在其所连四个碳原子不能共面。
二、乙烯的空间构型----平面型结构式、分子构型如图三:平面型结构,键角为120度,C=C 所连的四个氢原子与这两个碳原子同在一个平面上。
当乙烯分子中某氢原子被其他原子或原子团取代时,则代替该氢原子的原子一定在乙烯的平面内。
需要注意的是:C=C不能转动,而C-H键可以转动。
以乙烯母体模型衍变为-------丙烯、2-丁烯若将其中的氢原子换成氯原子,其与所有碳氢原子共面。
若将一个氢原子换成甲基,即为丙烯则如图四(1):将两个氢原子换成甲基则为2-丁烯如图四(2)显然,实线框内所有原子共面,由于C-C单键转动,实线框外的氢原子有一个可能转到纸面与框内所有原子共面, 可见凡与C=C直接相连的原子连同自身两个碳原子共面。
例析有机物分子中原子的共面共线问题有机物分子里原子共线共面问题,其实质就是分子的空间几何构型问题。
对有机物分子空间几何构型的考查,符合《考试说明》中“将化学问题抽象成数学问题,利用数学工具解决化学问题”这一能力要求的精神。
同时考查了学生对有机分子立体形象的观察能力和空间想象能力。
绝大多数有机物分子的构型都是复杂的,但总是以一些简单分子的几何构型为模型。
解决有机物分子里原子共线共面问题可采用模型假借的方法。
即假借简单分子的几何构型来解决复杂有机物分子里原子的共线共面问题。
因此,熟练地掌握好一些简单分子的几何构型是解决这类问题的关键。
常见简单分子的几何构型有:①CH4是正四面体构型;任意三个原子在同一个平面内;②CH2═CH2是平面四边形构型,两个碳原子和四个氢原子在同一个平面内;③CH≡CH是直线型,四个原子在同一条直线上;④是平面正六边形结构,6个碳原子和6个氢原子在同一个平面内;⑤是平面结构,四个原子在同一个平面内(但两条碳氢键不在一直线上)。
⑥萘()和蒽()均为平面结构等。
其次要掌握好共价型分子里;形成共价单键的原子可以绕轴旋转,如苯分子中苯环可以任一碳氢键为轴旋转。
形成双键和叁键的原子不能绕轴旋转的特点。
结合上述简单有机物的结构特点和价键特点对组成和结构较复杂的有机物分子进行分析、对比和综合,就可容易的解决有机物分子里原子共线共面问题。
再有,审题时需注意题干是碳原子数还是所有原子数(包括氢原子等)。
还需注意“可能”、“一定”、“最多”、“最少”、“共面”、“共线”等关键词。
试举几例加以分析:例1:下列关于的说法正确的是A.所有碳原子有可能都在同一平面上B.最多只可能有9个碳原子在同一平面上C.最多有7个碳原子可能在同一条直线上D.最多只可能有5个碳原子在同一直线上解析:本题的分子以CH2═CH2、CH≡CH、苯为模型,根据它们的各自构型,可以判断,所有碳原子有可能都在同一平面上。
根据CH2═CH2的平面四边形构型,共线的碳原子只能有HC≡C-中的两个碳原子、苯环对位上的两个碳原子及双键左端的一个碳原子,共5个。
高中化学必修二有机化学共线共面辅导教案高中化学必修二有机共线共面辅导讲义授课主题共线共面教学目的共线共面问题教学内容课程引入:思考?中间的5个C原子共面,且使得6个H原子与这5个碳共面,共有11个原子共面。
②乙烯分子中所有原子共平面。
乙烯型:平面结构。
六个原子均在同一平面上凡是位于乙烯结构上的六个原子共平面③乙炔分子中所有原子共直线。
乙炔型:直线型结构。
四个原子在同一条直线上凡是位于乙炔结构上的四个原子共直线。
④苯分子中所有原子共平面。
苯型:平面正六边形结构。
六个碳原子和六个氢原子共平面凡是位于苯环上的12个原子共平面。
⑤H—CHO分子中所有原子共平面。
(1)熟记四类空间构型中学有机化学空间结构问题的基石是甲烷、乙烯、乙炔和苯的分子结构。
(2)理解三键三角三键:C—C键可以旋转,而C=C键、C≡C键不能旋转。
三角:甲烷中的C—H键之间的夹角为109°28′,乙烯和苯环中的C—H键之间的夹角为120°,乙炔中的C—H键之间的夹角为180°。
2.单键的转动思想有机物分子中的单键,包括碳碳单键、碳氢单键、碳氧单键等可转动。
例题解析丙烷中最多有 3 个碳原子共面,最多有 5 个原子共面。
乙烯中有 6 个C原子共面和 6 个H原子一定共面。
巩固练习丙烯中有 3 个C原子共面和 3 个H原子一定共面。
丙烯中至少有 3 个C原子共面和 3 个H原子共面。
丙烯中最多有 3 个C原子共面和 4 个H原子共面。
丙烯中可能有 3 个C原子共面和 4 个H原子共面。
本知识点小结结构不同的基团连接后原子共面分析1.直线与平面连接:直线结构中如果有2个原子(或者一个共价键)与一个平面结构共用,则直线在这个平面上。
如CH2=CH-C≡CH,其空间结构为,中间两个碳原子既在乙烯平面上,又在乙炔直线上,所以直线在平面上,所有原子共平面。
2.平面与平面连接:如果两个平面结构通过单键相连,则由于单键的旋转性,两个平面不一定重合,但可能重合。
有机物中的原子共线共面问题(学 案)
一、巩固练习
【练习1】(09年浙江高考题).一种从植物中提取的天然化合物α-damascone 可用于制作香水,其结构
为:
O , 有关该化合物的下列说法不正确...
的是( ) A .分子式为C 13H 20O 。
B .该化合物可发生聚合反应。
C .1 mol 该化合物完全燃烧消耗19 mol O 2。
D .与Br 2的CCl 4溶液反应生成的产物经水解、稀硝酸酸化后可用AgNO 3溶液检验。
【练习2】(09年上海高考)奥运吉祥物福娃外材为纯羊毛线,内充物为无毒的聚酯纤维:
下列说法不正确...
的是 A .羊毛与聚酯纤维的化学成分不相同。
B .由单体合成聚酯纤维的反应属加聚反应。
C .该聚酯纤维单体为对苯二甲酸和乙二醇。
D .聚酯纤维和羊毛一定条件下均能水解。
二、基础知识的回顾
典型有机物的空间构型
空 间 结 构 典 型 代 表 物
正四面体结构 平面型结构 直线型结构
H
'28109 H H H
C C H
H C H
H 120°
120°
图3 乙烯结构
H C
C H
180 180
三、知识的拓展
【问题1】 在丙烷分子中,最多有多少个原子共面?
C
H
图2 丙烷的分子结构
H
H
① ⑤
H
C
H
②
H
C H H ④③
【问题2】在丙烯分子(23CH CH CH =)中,至少有多少个原子共面?最多有多少个原子共面?。
图4 丙烯的分子结构
②H
①H ⑤④③
C
H C
H
H
⑦⑥
C H
【问题3】 (1)2323)()(CH C C CH = (2)
3323()()(CH C CH C C CH =【问题4】 (1)在
C
H
H
H
①③
②
分子中,至少有多少个原子共面?最多有多少个原子共面?
(2)CH 2
②
③
①
分子中,共面的原子有多少个?
【问题5】
(1) 在H
C C CH C
C H
H
3
② ③ ④
①
分子中,至少有多少原子共面?最多有多少个原子共面?
(2) 分子中,最多有多少个原子共面?
四、课堂练习
1(05年全国高考)已知碳碳单键可以绕键轴自由旋转,结构简式为如下图所示的烃,下列说法中正确的是()
(A)分子中至少有9个碳原子处于同一平面上。
(B)分子中至少有10个碳原子处于同一平面上。
(C)分子中至少有11个碳原子处于同一平面上。
(D)该烃属于苯的同系物。
2(08年江苏高考题)香兰素是重要的香料之一,它可由丁香酚经多
步反应合成。
OH
OCH3
CH2CH CH 2……
OH
OCH3
CHO
丁香酚香兰素
有关上述两种化合物的说法正确的是()
A.常温下,1mol丁香酚只能与1molBr2反应。
B.丁香酚不能FeCl3溶液发生显色反应。
C.1mol香兰素最多能与3mol氢气发生加成反应。
D.香兰素分子中至少有12个原子共平面。
五、课堂作业
1(04年高考题)在分子中处于同一平面上的原子数最多可能是()。
A. 18
B. 20
C. 21
D.23
2 (08年宁夏高考题)在①丙烯②氯乙烯③苯④甲苯四种有机化合物中,分子内所有原子均在同一平
面的是( )。
A.①②B.②③C.③④D.②④
3 (09年海南高考题)下列化合物分子中的所有碳原子不可能处于同一平面的是()。
A.甲苯 B.硝基苯 C.2-甲基丙烯 D.2-甲基丙烷
4 (06重庆高考题)利尿酸在奥运会上被禁用,其结构简式如题12图所示。
下列叙述正确的是()。
A、利尿酸衍生物利尿酸甲酯的分子式是C14H14Cl2O4 。
B、利尿酸分子内处于同一平面的原子不超过10个。
C、1mol利尿酸能与7mol氢气发生加成反应。
D、利尿酸能与氯化铁溶液发生显色反应。
5 (09年全国Ⅰ高考题)现有乙酸和两种链状单烯烃混合物,其中氧的质量分数为a,则碳的质量分数是()
A.(1)
7
a
-
B.
3
4
a
C.
6
(1)
7
a
- D.
12
(1)
13
a
-。