《生物指示剂培养记录》
- 格式:doc
- 大小:55.00 KB
- 文档页数:1

0.9%氯化钠注射液(100ml软袋)灭菌工艺验证报告验证工艺0.9%氯化钠注射液(100ml软袋)灭菌工艺验证车间输液 3 线验证方案制订:部门姓名日期品管部验证方案审核:部门姓名日期研发部生产部品管部验证方案批准:日期:验证结果审核:部门姓名日期研发部生产部品管部验证结果批准:日期:1.概述为了改善输液软袋外部的洁净度,本品种采取了双袋灭菌工艺。
内袋灌注药液后,再进行套外袋,内袋和外袋共同进行灭菌,避免了内袋和输液塞与外界环境的接触,给患者增加了安全感,也方便了医务人员,双袋输液进入手术室内即可使用。
本品为临床上常用的输液品种。
用于各种原因所致的失水,包括低渗性、等渗性和高渗性失水;高渗性非酮症糖尿病昏迷,应用等渗或低渗氯化钠可纠正失水和高渗状态;低氯性代谢性碱中毒等。
本公司按最终灭菌药品的工艺进行生产。
鉴于本品化学性能稳定,故采用115℃、35分钟的灭菌温度进行灭菌(Fo≥12),现将灭菌情况报告如下。
灭菌釜的型号:PSMD7280生产厂家:山东新华医疗器械股份有限公司本公司设备编号:灭菌釜的结构:PSMD型大输液水浴灭菌器为圆形筒体结构,灭菌室最高可承受0.27MPa压力。
筒体材料为8mm厚耐酸不锈钢,支座材料为碳钢板Q235B。
水浴灭菌器将蒸汽通过热交换器间接加热纯化水,并以循环喷淋方式对输液瓶进行加热灭菌,灭菌结束后,冷却水通过热交换器冷却纯化水,对输液瓶进行冷却,使产品温度降到60℃左右。
通常将待灭菌的产品放置在不锈钢架子里,软袋每车为18层,每层30袋,装载后用车子推入灭菌机内。
100ml软袋产品装载12车(约6480袋/批)。
灭菌柜采用计算机与程序逻辑控制器(PLC)进行自动化控制。
灭菌程序中的主要参数,如灭菌加热速率、压力、温度、时间及冷却速率都可根据不同产品的要求设定。
温度控制系统使用Pt 100探头6只。
一个探头测定循环水入口处的温度,另一个探头测量循环水出口处的温度,其余4个探头直接插入瓶内测定瓶内温度,与计算机控制系统相连,用于灭菌温度控制,只有当4个瓶内探头中的3只达到设定温度时,才开始记录灭菌时间。
全自动配液系统性能确认方案目录1.1 目的 (3)1.2 范围 (3)1.3 职责 (3)1.4 确认前培训 (3)1.5 文件记录要求 (3)1.6 确认对象描述 (4)1.7 可接受标准 (4)1.8 性能确认步骤及结果 (4)1.9 偏差 (20)1.10 变更 (20)1.11 术语 (21)1.12 参考文献 (21)1.13 修订历史 (21)1.1目的1.1.1本性能确认方案的目的是提供文件证据证明江苏复旦复华药业有限公司无菌配液过滤系统的性能确认方法与标准,能基于批准的工艺方法和产品标准,作为组合或分别进行有效的重复的运行。
1.1.2性能测试应在真实生产条件或模拟生产条件下进行,应收集确认数据并记录在附件的测试报告上。
性能确认是正式测试的最后步骤,以及确认需求矩阵中识别为进行性能确认测试的系统正式运行前正确性能的文件证据。
当最终性能确认报告批准后,系统可用于正常生产操作或用于工艺验证。
1.2范围本确认方案适用于江苏复旦复华药业有限公司冻干粉针剂车间二层无菌配液系统的性能确认工作。
1.3职责1.3.1设备使用部门负责确认文件的起草,确认工作的组织与实施。
1.3.2QC负责样品的检测。
1.3.3QA负责现场取样及确认工作实施的监督。
1.3.4QA经理负责相关确认文件的审核。
1.3.5质量管理负责人负责相关确认文件的批准。
1.3.6QA文档管理员负责给出确认文件的文件编号,以及相关文件的发放、回收及归档。
1.4确认前培训确认小组应在本确认方案批准后进行本确认方案的专项培训,并确保所有参加本确认工作的人都已熟知本方案要求,并记录在《培训记录表》(QA-MAN-005-H)。
1.5文件记录要求1.5.1严格按照《良好的文件记录规范》(QA-MAN-003)中对质量记录填写的要求进行确认报告的填写及记录。
1.5.2确认操作及记录应至少两人进行,确保所有的确认测试均完成,并有足够的确认数据被提供。
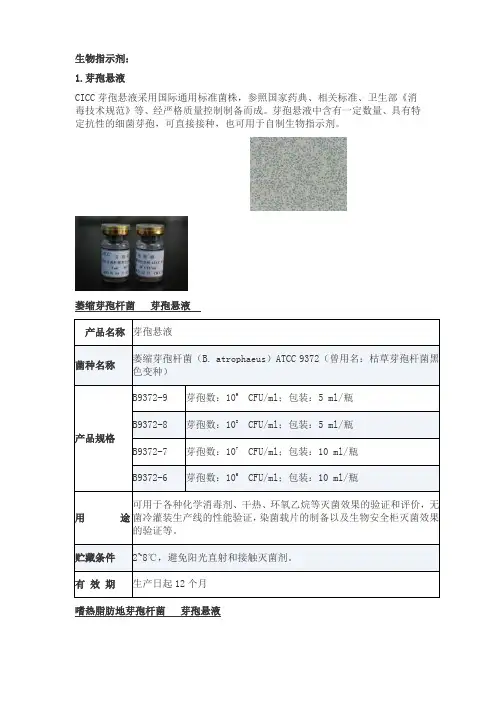
生物指示剂:1.芽孢悬液CICC芽孢悬液采用国际通用标准菌株,参照国家药典、相关标准、卫生部《消毒技术规范》等、经严格质量控制制备而成。
芽孢悬液中含有一定数量、具有特定抗性的细菌芽孢,可直接接种,也可用于自制生物指示剂。
萎缩芽孢杆菌芽孢悬液产品名称芽孢悬液菌种名称萎缩芽孢杆菌(B. atrophaeus)ATCC 9372(曾用名:枯草芽孢杆菌黑色变种)产品规格B9372-9 芽孢数:109CFU/ml;包装:5 ml/瓶B9372-8 芽孢数:108CFU/ml;包装:5 ml/瓶B9372-7 芽孢数:107CFU/ml;包装:10 ml/瓶B9372-6 芽孢数:106CFU/ml;包装:10 ml/瓶用途可用于各种化学消毒剂、干热、环氧乙烷等灭菌效果的验证和评价,无菌冷灌装生产线的性能验证,染菌载片的制备以及生物安全柜灭菌效果的验证等。
贮藏条件2~8℃,避免阳光直射和接触灭菌剂。
有效期生产日起12个月嗜热脂肪地芽孢杆菌芽孢悬液短小芽孢杆菌芽孢悬液注:CICC亦可按照客户要求提供不同规格包装。
另外根据客户要求可提供:生孢梭菌(Clostridium sporogenes),枯草芽孢杆菌(B. subtilis),巨大芽孢杆菌(B. megaterium),蜡状芽孢杆菌(B. cereus)等的芽孢悬液。
2.工业生物指示剂工业生物指示剂是根据工业企业实际情况,按照标准要求定制加工而成,以满足企业的特殊需求,通常采用不同的载体材料和包装形式,例如钢片、钢线、纸片、棉线、塑料片和滑石粉等,它与芽孢条、自含式等标准生物指示剂相比更具优势。
CICC可按照客户要求提供定制工业生物指示剂。
染菌滑石粉CICC研制的标准专用染菌滑石粉,以符合标准要求的滑石粉为载体,选用CICC 自行生产的微生物材料萎缩芽孢杆菌ATCC 9372芽孢悬液,按标准要求精制而成,每批染菌滑石粉产品均经过芽孢含量检验,确保质量稳定。

文件编号:/MR/6.4-12版次/修订:A/0 微生物检测操作规程制定者:审核者:批准者:2022-09-29发布2022-09-29实施本程序由XXXX医疗器械有限公司提出页次1/11微生物检测操作规程1. 目的通过规定产品微生物性能方面的检测方法和要求,达到规范操作,保障产品质量的目的。
2. 范围合用于XXXX医疗器械有限公司的生产的产品。
3. 职责3.1品质管理部:严格按照本规程执行检验操作。
包括对产品的初始污染菌、细菌内毒素、无菌性报考相应培养基的合用性等进行检测。
3.2其他部门:提供检测样品4. 操作规程4.1 无菌测试方法4.1.1 生物指示剂法将灭菌后的生物指示剂的塑料内管捏碎,将生物指示剂放置于电热恒温培养箱内,37℃ ± 2℃培养48h。
培养液颜色保持绿色不变,表示灭菌通过;培养液呈黄色,表示灭菌不通过,阴阳性对照。
4.1.2 薄膜过滤法4.1.2.1 试验前期准备a) 培养基(硫乙醇酸盐流体培养基,胰酪大豆胨液体培养基) 配制:用药匙取培养基粉末,按标签要求配制好培养基后,放在加热炉加热溶解,加热至沸腾。
分装至适宜的容器中。
其中,硫乙醇酸盐流体培养基的装量与容器髙度的比例应符合培养结束后,培养基氧化层(粉红色)不超过培养基深度的1/2。
灭菌。
在供试品接种前,培养基氧化层的高度不得超过培养基深度的1/5,否则,须经100℃水浴加热至粉红色消失(不超过2 0分钟),迅速冷却,只限加热一次,并防止被污染。
页次2/11b) 培养基灭菌:依据培养基要求,使用压力蒸汽灭菌器进行灭菌。
硫乙醇酸盐流体培养基灭菌参数设为121℃灭菌15分钟,胰酪大豆胨液体培养基灭菌参数设为121℃灭菌15分钟。
c) 器皿等清洗与灭菌:所有试验过程使用的培养皿、烧瓶、试管、镊子、剪刀、过滤杯、移液管、生理盐水等在使用前用纯化水清洗,然后烘干,放在灭菌桶内,置于压力蒸汽灭菌器中进行灭菌。
灭菌参数通常设为121℃灭菌30分钟。
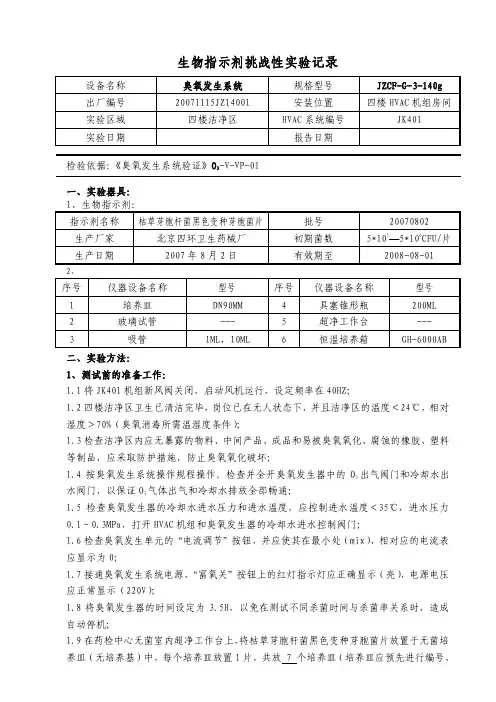
生物指示剂挑战性实验记录检验依据:《臭氧发生系统验证》O3-V-VP-01一、实验器具:二、实验方法:1、测试前的准备工作:1.1将JK401机组新风阀关闭,启动风机运行,设定频率在40HZ;1.2四楼洁净区卫生已清洁完毕,岗位已在无人状态下,并且洁净区的温度<24℃,相对湿度>70%(臭氧消毒所需温湿度条件);1.3检查洁净区内应无暴露的物料、中间产品、成品和易被臭氧氧化、腐蚀的橡胶、塑料等制品,应采取防护措施,防止臭氧氧化破坏;1.4按臭氧发生系统操作规程操作。
检查并全开臭氧发生器中的O3出气阀门和冷却水出水阀门,以保证O3气体出气和冷却水排放全部畅通;1.5检查臭氧发生器的冷却水进水压力和进水温度,应控制进水温度<35℃,进水压力0.1~0.3MPa,打开HVAC机组和臭氧发生器的冷却水进水控制阀门;1.6检查臭氧发生单元的“电流调节”按钮,并应使其在最小处(mix),相对应的电流表应显示为0;1.7接通臭氧发生系统电源,“富氧关”按钮上的红灯指示灯应正确显示(亮),电源电压应正常显示(220V);1.8将臭氧发生器的时间设定为3.5H,以免在测试不同杀菌时间与杀菌率关系时,造成自动停机;1.9在药检中心无菌室内超净工作台上,将枯草芽胞杆菌黑色变种芽胞菌片放置于无菌培养皿(无培养基)中,每个培养皿放置1片,共放 7 个培养皿(培养皿应预先进行编号,以确定杀菌时间),盖上平皿盖,用牛皮纸包扎好;2、杀菌实验:2.1将包扎好的枯草芽胞杆菌黑色变种芽胞菌片培养皿,通过传递窗传入洁净区,放置在内包间正中央地面上;2.2全部移开平皿盖(注意防止对培养基平皿污染),人员撤离出洁净区,准备臭氧消毒;2.3按下绿色“富氧开”启动按钮,“富氧开”绿色按钮指示灯亮,相应的“富氧关”红色按钮指示灯灭,“臭氧关”红色按钮指示灯亮,“时间定时器”通电开始计时;2.4打开外接压缩空气阀门,调节并控制气源静态压力应≤0.25MPa(气源静态压力是指臭氧发生单元未工作时,压缩空气压力。

2020版药典要来了,生物指示剂孢子含量测定
一、计数生物指示剂分类:
1、滤纸片类:孢子载体为滤纸
1)与培养液分离,灭菌完毕将培养液与滤纸片接触,依据培养液颜色变化确认灭菌效果。
2)不含培养液,灭菌完毕接种至指定培养基培养,依据培养基浑浊与否确认灭菌效果。
2、孢子悬液类:孢子载体为液体,直接分散于培养液中,一般整体为安瓿包装,灭菌完毕直接培养,依据培养液颜色变化确认灭菌效果。
3、不锈钢片类:孢子载体为不锈钢片(圆形或长条形),不含培养液,灭菌完毕接种至指定培养基培养,依据培养基浑浊与否确认灭菌效果。
二、滤纸片类生物指示剂计数方法
1、检验所需仪器及物品:
1)仪器:
生物安全柜、通用水浴、振荡器、培养箱、100~1000μl移液枪、计时器。
2)培养基:
胰酪大豆胨琼脂培养基(TSA),至少200ml/瓶×1瓶,融化后45~50℃水浴保温不超过8h
3)灭菌物品:
a)90mm平皿×8个、1ml带滤芯枪头×1盒(含枪头至少20个,灭菌前先用剪刀剪短枪头约2mm,防止滤纸堵塞影响计数结果)、直径4-6mm玻璃珠24个、50ml平底试管×4支,经湿热灭菌124℃、50min后备用,效期内。
b)无菌纯化水:9ml/支试管×12支,100ml/瓶三角瓶×1瓶,经湿热灭菌121℃、15min后备用,效期内。
c)具体灭菌程序按各灭菌器使用及维护标准操作规程进行。

本发明公开了一种常压蒸汽灭菌生物指示剂及其制备方法,它包括有干培养基、指示菌片。
所述的指示菌片为指示菌的芽孢附着在染菌载体片上,在该染菌载体片表面涂布有石蜡、石蜡乳液或脂肪酸。
制备方法为:将指示菌接种至生芽孢细菌培养基斜面上培养,芽孢生成后制成指示菌悬液;吸取指示菌芽孢悬液,滴加在染菌载体片上,即制成染菌载体片;将染菌载体片放置在融化的石蜡或脂肪酸液体或石蜡乳液中浸渍,然后干燥即制成防水指示菌片;将防水指示菌片与干培养基组合成一体。
本发明指示剂进行常压蒸汽灭菌效果测定时,不论指示剂瓶内加水时间早晚,都能够保证指示菌芽孢实际接触水的时间是基本一致,从而有效避免了同一灭菌锅的指示剂由于加水时间前后不一,而导致通过指示剂指示灭菌能力不一的问题。

生物指示剂LT另外根据客户要求可提供:生孢梭菌(Clostridium sporogenes),枯草芽孢杆菌(B. subtilis),巨大芽孢杆菌(B. megaterium),蜡状芽孢杆菌(B. cereus)等的芽孢悬液。
2.工业生物指示剂工业生物指示剂是根据工业企业实际情况,按照标准要求定制加工而成,以满足企业的特殊需求,通常采用不同的载体材料和包装形式,例如钢片、钢线、纸片、棉线、塑料片和滑石粉等,它与芽孢条、自含式等标准生物指示剂相比更具优势。
CICC可按照客户要求提供定制工业生物指示剂。
染菌滑石粉CICC研制的标准专用染菌滑石粉,以符合标准要求的滑石粉为载体,选用CICC 自行生产的微生物材料萎缩芽孢杆菌ATCC 9372芽孢悬液,按标准要求精制而成,每批染菌滑石粉产品均经过芽孢含量检验,确保质量稳定。
该产品适用于评定屏障材料对携菌微粒阻穿透性的实验方法,适用于国家医药行业手术衣标准《病人、医护人员和器械用手术单、手术衣和洁净服》(YY/T 0506-2009)、国际标准ISO 22612:2005 Clothing for protection against infectious agents -- Test method for resistance to dry microbial penetration(传染介质防护服--防干微生物渗入的试验方法)。
产品参数:产品名称染菌滑石粉微生物材料萎缩芽孢杆菌(B. atrophaeus)ATCC 9372芽孢含量108 CFU/g规格0.5g+0.1 g /瓶粒度<800目(95%<15μm)贮藏条件2~8℃,避免阳光直射和接触灭菌剂。
有效期生产日起12个月染菌石英粉CICC研制的标准专用染菌石英粉,以符合标准要求的石英粉为载体,选用CICC 自行生产的微生物材料萎缩芽孢杆菌ATCC 9372芽孢悬液,按标准要求精制而成,每批染菌石英粉产品均经过芽孢含量检验,产品质量稳定。

环氧乙烷生物指示剂培养试验通过半周期法,在保持其它灭菌工艺参数不变的条件下,将灭菌作用时间进行变化,并将不同灭菌作用时间的灭菌生物指示物(枯草杆菌的黑色芽孢变种——Atcc9372)在无菌环境下进行培养,检测微生物生长,找出细胞全部杀灭的时间临界值(最短有效灭菌时间)。
应至少重复进行2次该时间临界值的有效确认。
1.按供方提供的资料初步设定灭菌工艺参数1.灭菌温度——50±3℃2.保温时间——60min3.预真空——7min (0—— -20KPa)4.保压时间——10min5.湿度——60±20%RH6.加药量——0.800Kg/m³(7Kg)7.灭菌时间——480min8.换气时间——30min ,换气真空度0- -5KPa9.换气次数——至少5 次,换气真空度 -5 KPa2.灭菌过程的有效试验为证明灭菌过程的有效性,按照半周期请在保持上述灭菌工艺参数的不变的条件下,将灭菌作用时间进行变化并将不同灭菌作用时间的灭菌生物指示物在无菌环境下进行培养。
按其结果作为对无菌过程和无菌工艺有效性的评判。
其记录如下表:试验记录菌片培养原始记录(3小时)检验人/日期:复核人/日期:菌片培养原始记录(4小时)检验人/日期:复核人/日期:菌片培养原始记录(4小时)检验人/日期:复核人/日期:菌片培养原始记录(4小时)检验人/日期:复核人/日期:菌片培养原始记录(5小时)检验人/日期:复核人/日期:菌片培养原始记录(8小时)检验人/日期:复核人/日期:菌片培养原始记录(8小时)检验人/日期:复核人/日期:。
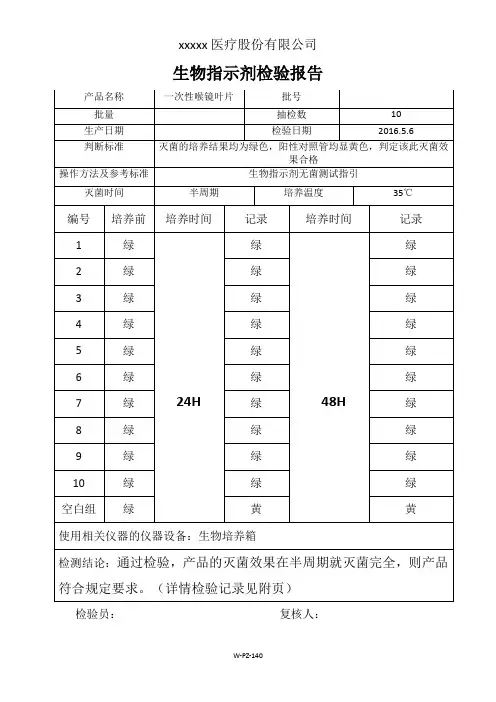
xxxxx 医疗股份有限公司
W-PZ-140
生物指示剂检验报告
检验员: 复核人:
产品名称 一次性喉镜叶片
批号 批量 抽检数 10 生产日期
检验日期
2016.5.6
判断标准
灭菌的培养结果均为绿色,阳性对照管均显黄色,判定该此灭菌效
果合格
操作方法及参考标准 生物指示剂无菌测试指引
灭菌时间
半周期
培养温度
35℃
编号 培养前 培养时间 记录 培养时间
记录 1 绿
24H
绿
48H
绿 2 绿 绿 绿 3 绿 绿 绿 4 绿 绿 绿 5 绿 绿 绿 6 绿 绿
绿
7 绿 绿 绿 8 绿 绿 绿 9 绿 绿 绿 10 绿 绿 绿 空白组
绿
黄
黄
使用相关仪器的仪器设备:生物培养箱
检测结论:通过检验,产品的灭菌效果在半周期就灭菌完全,则产品
符合规定要求。
(详情检验记录见附页)。
可编辑修改精选全文完整版《医院感染消毒灭菌效果监测取样指导》根据《消毒技术规范》的要求,现将我院消毒灭菌效果监测、环境微生学监测的采样方法、结果判定、质控标准等规范如下:第一章环境卫生学监测包括空气、物体表面、医务人员手的监测采样及检查原则。
采样应具有一定数量和代表性,采样后必须尽快对样品按要求指标进行检测,送检时间不得﹥6小时,若样品保存在冰箱内送检时间不得﹥24小时。
一、空气监测:1、采样时间:消毒处理后,操作前2、采样方法:平板沉降法(1)布点方法。
室内面积≤30m²,设内、中、外对角线3点,两端距墙1米;室内面积>30m²,设东、西、南、北4角及中央5点,其中东、西、南、北均距墙1米。
(2)采样方法。
将直径为9cm普通营养琼脂平板在室内各采样点处,采样高度为距地面1.5米,采样时将平板盖打开,扣放于平板旁,暴露5分钟,盖好立即送检。
(3)计算公式:空气细菌菌落总数(cfu/m³)=50000n/(a×t)式中a为平板面积(cm2);t为平板暴露时间(min);n为平均菌落数(cfu)。
(4)注意事项:采样前,关好门、窗,在无人走动的情况下,静止110min进行采样。
(5)质控标准。
Ⅰ类区域:细菌总数≤10cfu/m3(或0.2cfu/平板),未检出金黄色葡萄球菌、溶血性链球菌为消毒合格;Ⅱ类区域:细菌总数≤200cfu/m3(或4cfu/平板),未检出金黄色葡萄球菌、溶血性链球菌为消毒合格;Ⅲ类区域。
细菌总数≤500cfu/m3(或10cfu/平板),未检出金黄色葡萄球菌、溶血性链球菌为消毒合格。
二、医务人员手的监测:1、采样时间。
在接触病人和从事医疗活动前进行采样或消毒后立即采样。
2、采样面积及方法:手的采样:被检人五指并拢,用浸有含相应中和剂的无菌洗脱液的棉拭子在双手指屈面从指根到指端往返涂擦2次(一只手涂擦面积约30cm2),并随之转动采样棉拭子,剪去操作者手接触部位,将棉拭子投入10ml含相应中和剂的无菌洗脱液试管内,立即送检。
麦康凯液体培养基配制灭菌程序验证方案一、目的验证微生物检测室购买的由广东环凯微生物科技有限公司生产的麦康凯液体培养基的配制和灭菌方法,验证该配制灭菌程序适合于检测室麦康凯液体培养基的配制和灭菌,为培养基配制和灭菌提供正确的操作方法,使培养基配制和灭菌标准化、程序化。
二、适用范围麦康凯液体培养基的配制和灭菌三、职责1.技术负责人1.1为验证组长,负责组织编写并审核验证方案及报告。
负责组织方案及报告的执行。
2.检测室负责人2.1负责验证方案的起草和方案的具体实施;负责验证过程的记录。
3.检测员3.1负责验证方案的具体实施;负责验证过程的记录。
4.经理4.1负责批准方案及报告。
四、作业标准1.概述培养基是微生物试验的基础,直接影响微生物试验结果。
一般采用商品脱水培养基,临用时按使用说明或相关规定进行称量、配制、调节pH、分装、灭菌等。
应按照生产商提供参数进行培养基的灭菌。
培养基若采用不适当的加热和灭菌条件,有可能引起颜色变化、透明度降低、琼脂凝固力或pH 的改变。
因此,培养基应采用验证的灭菌程序灭菌,培养基灭菌方法和条件,应通过无菌性试验和促生长能力、抑制能力试验进行验证。
灭菌器中培养基的容积和装载方式也将影响加热的速度。
因此,应根据灭菌培养基的特性,进行全面的灭菌程序验证。
本公司现在检验用培养基的灭菌方法均为湿热灭菌方法。
2.验证实施计划年月至年月3.培训报告审批后,由验证小组组长对报告实施过程中涉及人员进行培训,以保证报告顺利实施,并做好培训记录,培训记录见附件1:《培训情况确认表》。
4.仪器确认4.1确认内容:确认过程所用仪器是否经校验,并有校验合格证且在校验有效期内。
确认所用试剂及菌液是否在有效期内。
4.2标准要求:仪器应已校验,有校验合格证并在校验有效期内。
4.3仪器及试剂的确认记录见附件2:《仪器确认记录》及附件3:《试剂确认记录》5.验证内容5.1取同一批干粉培养基配制三批进行以下验证。