4第四章 酶活力的测定
- 格式:ppt
- 大小:1.64 MB
- 文档页数:23

、酶活测定方法还原法酶与底物在特定的条件下反应,酶可以促使底物释放出还原性的基团。
在此反应体系中添加化学试剂,酶促反应的产物可与该化学试剂发生反应,生成有色物质。
通过在特定的波长下比色,即可求出还原产物的含量,从而计算出酶活力的大小。
色原底物法通过底物与特定的可溶性生色基团物质结合,合成人工底物。
该底物与酶发生反应后,生色基团可被释放出来,用分光光度法即可测定颜色的深浅,在与已知标准酶所做的曲线比较后,即可求出待测酶的活力。
粘度法该法常用于测定纤维素酶、木聚糖酶和β-葡聚糖酶的活力。
木聚糖和β-葡聚糖溶液通常情况下可形成极高的粘度,当酶作用于粘性底物时木聚糖和β-葡聚糖会被切割成较小的分子使其粘度大为降低。
基于Poiseuille定律我们知道,只要测定一定条件下溶剂和样品溶液的运动粘度,便可计算特性粘数,并以此来判断酶的活力。
高压液相色谱法酶与其底物在特定的条件下充分反应后,在一定的色谱条件下从反应体系中提取溶液进行色谱分析,认真记录保留时间和色谱图,测量各个样的峰高和半峰高,计算出酶促反应生成物的含量,从而换算出酶活力的数值。
免疫学方法常用于酶活性分析的免疫学方法包括:免疫电泳法、免疫凝胶扩散法。
这两种方法都是根据酶与其抗体之间可发生特定的沉淀反应,通过待测酶和标准酶的比较,最终确定酶活力。
免疫学方法检侧度非常灵敏,可检侧出经过极度稀释后样品中的酶蛋白,但其缺点是不同厂家生产的酶产品需要有不同特定的抗体发生反应。
琼脂凝胶扩散法将酶作用的底物与琼脂混合熔融后,倒入培养皿中或载波片上制成琼脂平板。
用打孔器在琼脂平面上打出一个约4-5mm半径的小孔。
在点加酶样并培养24h以后,用染色剂显色或用展开剂展开显出水解区,利用水解直径和酶活力关系测定酶活力。
蛋白酶活力测定法本方法适用于酿造酱油时在制品菌种、成曲的蛋白酶活力测定。
1 福林法1.1 试剂及溶液: 以下试剂都为分析纯1.1.1 福林试剂(Folin试剂):于2000mL磨口回流装置内,加入钨酸钠(Na2WO4·2H2O)100g,钼酸钠(Na2MoO4·2H2O)25g,蒸馏水700mL,85%磷酸50mL,浓盐酸100mL,文火回流10h。

酶活力测定
酶是一种能够催化生物体内化学反应的蛋白质,广泛存在于动植物、微生物、真菌等
生物体内。
酶在生理代谢、免疫系统、消化系统等方面扮演着重要的角色。
因此,对于酶
的活力测定十分重要。
下面将详细介绍酶活力测定方法。
酶活力测定的基本原理是通过测定一个给定反应体系下酶所催化的底物转化速度来确
定酶的活力。
酶活力的测定通常采用标准曲线法、比色法、荧光法、放射性同位素标记法、酶电极法等多种方法。
其中,比色法和荧光法是最为常用的两种方法。
二、比色法
比色法是通过反应体系中某一底物和产物的比色反应来测定酶的活力。
常用的比色反
应有蛋白质和氨基酸比色法、尿素酶测定法等。
以蛋白质和氨基酸比色法为例,其测定步骤如下:
1. 选定底物,例如眼镜蛇毒素,反应物为酸性的巴氏液
2. 选定测定时点,例如反应20分钟之后
3. 加入颜色试剂,例如Folin验液,使反应产生深色络合体
4. 测定吸光度,根据标准曲线计算出反应深度,从而计算出酶的活力值
三、荧光法
荧光法是通过酶催化的底物转化产生的荧光信号来测定酶活力。
荧光法具有高灵敏度、高精度、高速度、低误差等优点,越来越受到人们的关注。
1. 选择荧光素为底物,荧光素在激发光的作用下会发出荧光信号
2. 酶催化荧光素转化为羟基荧光素,生产出更强的荧光信号
四、注意事项
酶活力测定的过程中需要注意以下几个方面:
1. 选择适当的反应体系、底物和试剂
2. 在测定前保持合适的反应条件(例如pH、温度等)
3. 为了获得比较准确的测定结果,需要进行多次测定
4. 保证测定设备和试剂的质量和准确性。




实验四、蛋白酶活力的测定1.实验目的掌握用Folin-酚法测定蛋白酶活力的方法,与Azocasein(偶氮酪蛋白)法作为比较。
2.实验原理蛋白酶在一定的温度和pH下,水解酪素底物产生含有酚基的氨基酸(如酪氨酸、色氨酸),在碱性条件下,将福林试剂还原,生成钼蓝和钨蓝,其颜色的深浅与酚基氨基酸含量成正比,通过在660nm测定其吸光度,可得到酶解产生的酚基氨基酸的量,计算出蛋白酶活力,以此代表蛋白酶的总酶活力。
酶活单位定义:在37℃、相应的pH条件下,在1min内水解酪蛋白底物,产生相当于1µg酚类化合物(由酪氨酸等同物表示)的酶量,为1个酶活单位。
3.主要仪器和试剂试剂:0.1mg/mL L-酪氨酸标准贮备溶液、0.55mol/LNa2CO3、福林试剂、Casein溶液、TCA 溶液仪器设备:恒温水浴锅、分光光度计、pH计,分析天平、秒表。
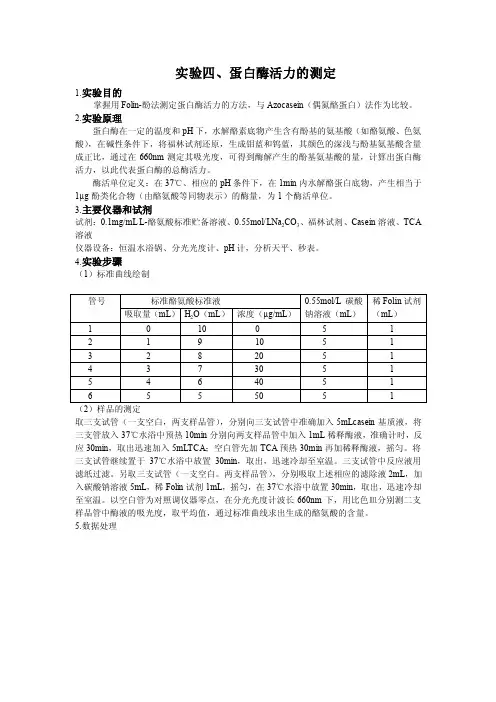
4.实验步骤(1)标准曲线绘制取三支试管(一支空白,两支样品管),分别向三支试管中准确加入5mLcasein基质液,将三支管放入37℃水浴中预热10min分别向两支样品管中加入1mL稀释酶液,准确计时,反应30min,取出迅速加入5mLTCA;空白管先加TCA预热30min再加稀释酶液,摇匀。
将三支试管继续置于37℃水浴中放置30min,取出,迅速冷却至室温。
三支试管中反应液用滤纸过滤。
另取三支试管(一支空白。
两支样品管),分别吸取上述相应的滤除液2mL,加入碳酸钠溶液5mL,稀Folin试剂1mL,摇匀,在37℃水浴中放置30min,取出,迅速冷却至室温。
以空白管为对照调仪器零点,在分光光度计波长660nm下,用比色皿分别测二支样品管中酶液的吸光度,取平均值,通过标准曲线求出生成的酪氨酸的含量。
5.数据处理。


酶活力测定实验报告一、实验目的酶活力测定实验的主要目的是了解酶的活性及其影响因素,掌握测定酶活力的基本方法和原理,以及学会使用相关仪器和试剂进行实验操作。
二、实验原理酶是生物体内具有催化作用的蛋白质或核酸。
酶活力是指酶催化一定化学反应的能力,通常用在一定条件下酶催化反应的速度来表示。
本实验采用分光光度法测定酶活力,其原理是基于酶催化反应所产生的产物在特定波长下具有光吸收特性,通过测定反应体系在该波长下吸光度的变化,可以计算出酶催化反应的速度,从而反映酶的活力。
以过氧化氢酶为例,过氧化氢酶能够催化过氧化氢分解为水和氧气。
在本实验中,通过加入一定量的过氧化氢溶液,使其与过氧化氢酶反应,然后使用高锰酸钾溶液滴定剩余的过氧化氢,根据高锰酸钾溶液的用量计算出过氧化氢酶的活力。
三、实验材料与仪器1、实验材料新鲜的猪肝或土豆等富含过氧化氢酶的组织。
过氧化氢溶液(3%)。
高锰酸钾溶液(002 mol/L)。
磷酸缓冲液(pH 70)。
2、实验仪器研钵。
离心机。
移液器。
分光光度计。
恒温水浴锅。
试管、量筒、容量瓶等玻璃仪器。
四、实验步骤1、酶液的制备称取新鲜的猪肝或土豆组织_____g,置于研钵中,加入适量的磷酸缓冲液(pH 70),研磨成匀浆。
将匀浆转移至离心管中,以_____rpm 的转速离心_____min,取上清液即为粗酶液。
2、酶活力的测定取_____支试管,分别标记为 1、2、3。
在 1 号试管中加入_____mL 磷酸缓冲液(pH 70)作为空白对照,在 2、3 号试管中分别加入_____mL 粗酶液。
向 1、2、3 号试管中分别加入_____mL 过氧化氢溶液(3%),立即摇匀,并同时开始计时。
在反应进行_____min 后,迅速向 1、2、3 号试管中分别加入_____mL 浓度为 2 mol/L 的硫酸溶液终止反应。
用移液器吸取_____mL 反应液,加入到另一支装有_____mL 高锰酸钾溶液(002 mol/L)的试管中,摇匀。

测定酶活的原理
测定酶活的原理是基于酶与底物的特异性结合及催化活性。
一种常用的测定方法是通过测量底物转化为产物的速度来间接衡量酶的活性。
该方法的基本步骤包括:
1. 准备一定浓度的底物溶液,使其与酶反应时达到酶的最佳工作浓度。
2. 添加一定量的酶溶液到底物中,使它们充分混合。
3. 在一定时间间隔内,取出反应液样本,并停止反应,例如通过加入酸性或碱性溶液。
4. 采用一种合适的分析方法,如光度法、荧光法或电化学法,测定样本中产生的产物的浓度。
5. 根据样本中产物浓度的变化,计算出酶的活性,通常以单位时间内产生的产物量来表示。
此外,也可以采用其他方法来直接测定酶的活性,例如测定酶的催化反应速率常数(Kcat)、酶对底物的亲和力(Km)等。
这些方法需要更复杂的实验步骤和数据处理。
总的来说,测定酶活的原理就是利用酶对底物的催化作用,通过测量底物转化为产物的速度或其他相关参数来间接或直接衡量酶的活性水平。

酶活测定方法还原法酶与底物在特定的条件下反应,酶可以促使底物释放出还原性的基团。
在此反应体系中添加化学试剂,酶促反应的产物可与该化学试剂发生反应,生成有色物质。
通过在特定的波长下比色,即可求出还原产物的含量,从而计算出酶活力的大小。
色原底物法通过底物与特定的可溶性生色基团物质结合,合成人工底物。
该底物与酶发生反应后,生色基团可被释放出来,用分光光度法即可测定颜色的深浅,在与已知标准酶所做的曲线比较后,即可求出待测酶的活力。
粘度法该法常用于测定纤维素酶、木聚糖酶和β-葡聚糖酶的活力。
木聚糖和β-葡聚糖溶液通常情况下可形成极高的粘度,当酶作用于粘性底物时木聚糖和β-葡聚糖会被切割成较小的分子使其粘度大为降低。
基于Poiseuille定律我们知道,只要测定一定条件下溶剂和样品溶液的运动粘度,便可计算特性粘数,并以此来判断酶的活力。
高压液相色谱法酶与其底物在特定的条件下充分反应后,在一定的色谱条件下从反应体系中提取溶液进行色谱分析,认真记录保留时间和色谱图,测量各个样的峰高和半峰高,计算出酶促反应生成物的含量,从而换算出酶活力的数值。
免疫学方法常用于酶活性分析的免疫学方法包括:免疫电泳法、免疫凝胶扩散法。
这两种方法都是根据酶与其抗体之间可发生特定的沉淀反应,通过待测酶和标准酶的比较,最终确定酶活力。
免疫学方法检侧度非常灵敏,可检侧出经过极度稀释后样品中的酶蛋白,但其缺点是不同厂家生产的酶产品需要有不同特定的抗体发生反应。
琼脂凝胶扩散法将酶作用的底物与琼脂混合熔融后,倒入培养皿中或载波片上制成琼脂平板。
用打孔器在琼脂平面上打出一个约4-5mm半径的小孔。
在点加酶样并培养24h以后,用染色剂显色或用展开剂展开显出水解区,利用水解直径和酶活力关系测定酶活力。
蛋白酶活力的测定随着生物技术的发展及环保要求的提高,越来越多的酶制剂应用于制革生产中。
比如浸水,脱毛,软化,脱脂等工序都用到大量的酶制剂,从酶的作用性质来看制革生产中用到的主要是蛋白酶和脂肪酶。
酶活力测定的方法
酶活力测定的方法有多种,下面列举常用的几种方法:
1. 比色法:通过测定酶反应产生的可见光吸收或色素形成来间接测定酶活力。
常用的比色法有尼林蓝法、间苯二酚法、对苯二酚法等。
2. 发光法:利用酶催化的氧化还原反应产生的发光信号来测定酶活力。
常用的发光法有荧光发光法、葡萄糖氧化酶法等。
3. 毛细管电泳法:通过测定酶催化反应产生的电荷变化、离子浓度变化或pH 值的变化来测定酶活力。
4. 毛细管电泳法:通过测定酶催化反应产生的电荷变化、离子浓度变化或pH 值的变化来测定酶活力。
5. 凝胶电泳方法:通过观察酶在凝胶上的迁移距离或酶活性的带状图案的强度来测定酶活力。
6. 标记物法:利用酶催化与标记物反应产生的物质变化来测定酶活力,常用的标记物有放射性同位素、酶标记物等。
以上是常用的酶活力测定方法,不同方法适用于不同类型的酶和反应体系。
在实
际应用中,需要根据具体情况选择最合适的方法来测定酶活力。
④分光光度法利用底物和产物光吸收性质的不同,可直接测定反应混合物中底物的减少量或产物的增加量。
几乎所有的氧化还原酶都使用该法测定。
如还原型辅酶Ⅰ(NADH2)和辅酶Ⅱ(NADPH2)在340nm有吸收,而NAD和NADP在该波长下无吸收,脱氢酶类可用该法测定。
该法测定迅速简便,自动扫描分光光度计的使用对酶活力的快速准确的测定提供的极大的方便。
酶在食品加工中的作用就像一把双刃剑,我们要趋利避害。
酶的积极作用我们要加强,在食品加工过程中添加酶制剂,使其作用充分发挥;消极作用我们要尽量避免,可以通过加热等方法将酶灭活,消除其不利影响。
为了将酶更好地应用于食品加工,研究酶的性质是十分必要的。
而紫外-可见分光光度法是研究酶性质的重要方法之一。
下面我们来介绍用-可见分光光度计测定酶活的具体方法。
紫外-可见分光光度法测定酶活:1. β一半乳糖苷酶β一半乳糖苷酶,又称乳糖酶(Lactase)。
能水解乳糖来降低乳制品的乳糖含量,从而提高乳制品的可消化性,用于低乳糖牛奶和非结晶型浓缩牛奶的生产及奶酪风味的改变,同时还可用于生产低聚半乳糖。
【酶活测定】以ONPG为底物测定β-半乳糖苷酶活力。
【酶活定义】以ONPG为底物,37℃保温酶解,每分钟释放lμmol/L邻硝基酚的酶量,定义为1个酶活力单位。
2. 超氧化物歧化酶超氧化物歧化酶(Superoxide Dismutase,简称SOD)是一种十分重要的生物体防止氧化损伤的酶类,是生物体内超氧阴离子清除剂,保护细胞免受损伤。
SOD广泛存在于各类生物体内,所有好氧微生物细胞中都含有SOD。
自1969年Mccord等人首次发现了SOD 生物活性后,医学界对其医疗作用做了许多研究,证明它具有抗衰老、抗肿瘤、抗辐射、抗缺血、提高人体免疫力等作用,被专家称为21世纪最有前途的药用酶。
欧美国家已开始将其应用于医疗、食品、保健、化妆品等领域。
【酶活测定】在25℃4.5ml 50mmol/L pH8.3的K2HPO4- KH2PO4缓冲液中加入待测SOD样液,再加入10ul 50mmol/L的连苯三酚,迅速摇匀,倒人光径lcm 的比色杯,在325nm波长下每隔30s测一次A值。