初三化学生产实际分析2017.12
- 格式:doc
- 大小:1.75 MB
- 文档页数:6

2017年中考化学质量分析报告2017年中考化学质量分析报告一、试卷命题情况分析2017年中考化学试题与2016年相比,总体比较平稳,紧扣教材,侧重基础,无偏题、怪题、难题,试题有一定的区分度,总体难度适中,充分体现了我市中考化学命题一贯坚持的“平稳为主、稳中求变、变中求新”的原则。
试题能结合教材注重基础知识的考查,偏重于化学基础知识和化学实验运用的考查,较好地体现了新标三维目标的考查要求。
试题中知识点分布更加合理,学科特点突出。
在试题的呈现形式上,字叙述更加简洁明了,同时更多应用了图像、表格等灵活多样的方式,使得试题信息更加直观、指向性更强,便于考生阅读理解。
纵观2017年xx市中考化学试题,我们不难发现以下三个特点:1.紧扣双基,重视考查化学基本素养基础知识和基本技能是初中化学程的基本内容,是学生终身学习和发展的基础,是学生适应现代社会及未社会生活所必需的,也是对学生进行能力培养和情感教育的必要载体。
2017年xx市中考化学试题内容考查知识面宽、覆盖面大,减少了考查的偶然性和片面性。
试题将化学的基本知识放在真实的情境中,通过学生对问题情境的分析和解决的过程,考查学生利用所学的化学知识分析和解决具体问题的能力,考查了学生的化学基本素养。
如第一大题1-7小题,第二大题11、12、13小题,第三大题16、17小题,第四大题19小题等都是基础题。
2.立足教材,紧密联系社会生活实际试题紧密联系社会生活实际,以学生的生活实际为切入点,以日常生活所用到的化学知识为背景,融入社会生活中的实际问题,让考生在熟悉的生活情景中,运用最基础的化学知识解决生活中的一些实际问题。
这些试题为学生体验化学与社会、生活的紧密联系创设了丰富多彩的生产生活情境,既考查了学生运用化学知识解决实际问题的能力,又促使学生体验化学的应用价值,感到学有所得,学有所用,体现了“生活中处处有化学”,有助于学生建立社会可持续发展的意识,这也是化学程的重要功能。

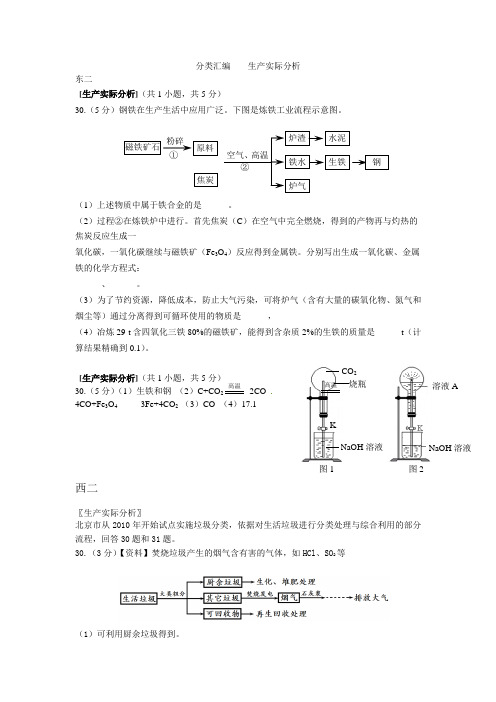
分类汇编------生产实际分析东二[生产实际分析](共1小题,共5分)30.(5分)钢铁在生产生活中应用广泛。
下图是炼铁工业流程示意图。
(1)上述物质中属于铁合金的是______。
(2)过程②在炼铁炉中进行。
首先焦炭(C )在空气中完全燃烧,得到的产物再与灼热的焦炭反应生成一氧化碳,一氧化碳继续与磁铁矿(Fe 3O 4)反应得到金属铁。
分别写出生成一氧化碳、金属铁的化学方程式: ______、______。
(3)为了节约资源,降低成本,防止大气污染,可将炉气(含有大量的碳氧化物、氮气和烟尘等)通过分离得到可循环使用的物质是______,(4)冶炼29 t 含四氧化三铁80%的磁铁矿,能得到含杂质2%的生铁的质量是______t (计算结果精确到0.1)。
[生产实际分析](共1小题,共5分)30.(5分)(1)生铁和钢 (2)C+CO22CO 4CO+Fe 3O 4 3Fe+4CO 2 (3)CO (4)17.1西二〖生产实际分析〗北京市从2010年开始试点实施垃圾分类,依据对生活垃圾进行分类处理与综合利用的部分流程,回答30题和31题。
30.(3分)【资料】焚烧垃圾产生的烟气含有害的气体,如HCl 、SO 2等(1)可利用厨余垃圾得到。
CO 2 NaOH 溶液K溶液ANaOH 溶液烧瓶图1 图2高温高温(2)1 t塑料瓶可回炼600 kg的无铅汽油和柴油。
塑料瓶属于垃圾分类中的类。
(3)石灰浆的作用是吸收CO2和。
31.(3分)②绿矾(FeSO4·7H2O)是一种浅绿色晶体,加热至70℃以上易分解(1)I中主要发生3个反应,其中生成气体的化学方程式是。
(2)II中向FeSO4溶液里加入铁屑,依次经过:加热浓缩、过滤、降温结晶、(填操作名称),得到绿矾。
其中铁屑的作用是。
〖生产实际分析〗30.(3分)(1)肥料 ( 2 ) 可回收物(3)SO2和HCl31.(3分)(1)Fe+H2SO4FeSO4+H2↑ ( 2 ) 过滤防止FeSO4被氧化海二29. (2分)(1)物理(2)A C30.(3分)(1)Cu (2)CuSO4H2SO4(3)B C D朝二〖生产实际分析〗(共1道小题,共5分)29.(5分) 工业上利用电石(CaC2)制备高纯碳酸钙的流程如下:已知:①CaC2+2H2O=Ca(OH)2+C2H2↑②CaCl2+H2O+CO2+2NH3=CaCO3↓+2NH4Cl(1)乙炔(C2H2)是一种常见的燃料,写出乙炔完全燃烧的化学方程式________________。
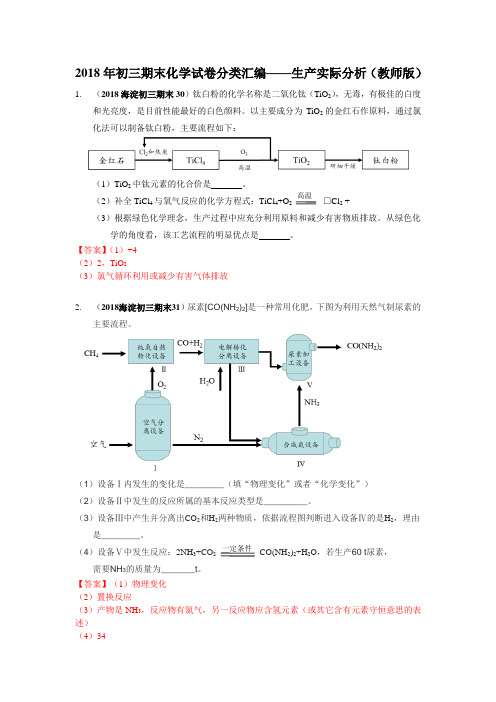
2018年初三期末化学试卷分类汇编——生产实际分析(教师版)1. (2018海淀初三期末30)钛白粉的化学名称是二氧化钛(TiO 2),无毒,有极佳的白度和光亮度,是目前性能最好的白色颜料。
以主要成分为TiO 2的金红石作原料,通过氯化法可以制备钛白粉,主要流程如下:(1)TiO 2中钛元素的化合价是。
(2)补全TiCl 4与氧气反应的化学方程式:TiCl 4+O 2 □Cl 2 +________(3)根据绿色化学理念,生产过程中应充分利用原料和减少有害物质排放。
从绿色化 学的角度看,该工艺流程的明显优点是 。
【答案】(1)+4(2)2,TiO 2(3)氯气循环利用或减少有害气体排放2. (2018海淀初三期末31)尿素[CO(NH 2)2]是一种常用化肥。
下图为利用天然气制尿素的主要流程。
(1)设备Ⅰ内发生的变化是________(填“物理变化”或者“化学变化”)(2)设备Ⅱ中发生的反应所属的基本反应类型是_________。
(3)设备Ⅲ中产生并分离出CO 2和H 2两种物质,依据流程图判断进入设备Ⅳ的是H 2,理由 是________。
(4)设备Ⅴ中发生反应:2NH 3+CO 2 CO(NH 2)2+H 2O ,若生产60 t 尿素, 需要NH 3的质量为_______t 。
【答案】(1)物理变化(2)置换反应(3)产物是NH 3,反应物有氮气,另一反应物应含氢元素(或其它含有元素守恒意思的表述)(4)34高温一定条件3.(2018西城初三期末39)某课外小组用废弃白铜(Cu、Ni)粉末分离得到Cu、Ni两种金属,其主要流程如下(部分反应产物在图中已略去):已知:Ni与Fe化学性质相似,常见化合价为+2价。
(1)固体A的化学式是______。
(2)ZnSO4中硫元素的化合价是______。
(3)I中反应的化学方程式是______。
(4)II中分离出固体C的操作名称是______。
(5)由上述流程得出Cu、Ni、Zn的金属活动性由强到弱的顺序是______。

2017年中考化学质量分析报告2017年中考化学质量分析报告一、试卷命题情况分析2017年中考化学试题与2016年相比,总体比较平稳,紧扣教材,侧重基础,无偏题、怪题、难题,试题有一定的区分度,总体难度适中,充分体现了我市中考化学命题一贯坚持的“平稳为主、稳中求变、变中求新”的原则。
试题能结合教材注重基础知识的考查,偏重于化学基础知识和化学实验运用的考查,较好地体现了新标三维目标的考查要求。
试题中知识点分布更加合理,学科特点突出。
在试题的呈现形式上,字叙述更加简洁明了,同时更多应用了图像、表格等灵活多样的方式,使得试题信息更加直观、指向性更强,便于考生阅读理解。
纵观2017年xx市中考化学试题,我们不难发现以下三个特点:1.紧扣双基,重视考查化学基本素养基础知识和基本技能是初中化学程的基本内容,是学生终身学习和发展的基础,是学生适应现代社会及未社会生活所必需的,也是对学生进行能力培养和情感教育的必要载体。
2017年xx市中考化学试题内容考查知识面宽、覆盖面大,减少了考查的偶然性和片面性。
试题将化学的基本知识放在真实的情境中,通过学生对问题情境的分析和解决的过程,考查学生利用所学的化学知识分析和解决具体问题的能力,考查了学生的化学基本素养。
如第一大题1-7小题,第二大题11、12、13小题,第三大题16、17小题,第四大题19小题等都是基础题。
2.立足教材,紧密联系社会生活实际试题紧密联系社会生活实际,以学生的生活实际为切入点,以日常生活所用到的化学知识为背景,融入社会生活中的实际问题,让考生在熟悉的生活情景中,运用最基础的化学知识解决生活中的一些实际问题。
这些试题为学生体验化学与社会、生活的紧密联系创设了丰富多彩的生产生活情境,既考查了学生运用化学知识解决实际问题的能力,又促使学生体验化学的应用价值,感到学有所得,学有所用,体现了“生活中处处有化学”,有助于学生建立社会可持续发展的意识,这也是化学程的重要功能。

生产实际分析生产实际分析【生产实际分析】1. (3分)我国制碱工业先驱侯德榜发明了“侯氏制碱法”。
其模拟流程如下:(1)操作a的名称是_______________________ 。
(2)写出NHCI 的一种用途(3)反应①的微观示意图如下,请在方框中补全相应微粒的图示。
条件的工艺流程如下:-1 "I~ OCH C 2H4CO乙烯制备装置__________________________________________________________ o )海洋中蕴藏着丰富的化学资源,如NaCl 、MgCl 2、( ____ -取金属镁的主要流程如下:」CaCi 2等物质。
从海水中提 2. (123分)利用燃煤烟气生产太阳N 2S Q和化工原料 乙烯(烟岁)■+(SO C Q)-_II_ 0 —心黠』•1厂NaSQ 和HCl 的溶液NaSQ 制备装置(1) N a 2SO 制备装置中,参加反应的物质有(2) NaSQ 制备装置中,反应前后化合价发 生改变的元素是(3)乙烯制备装置中,反应的化学方程式 为 3 (3 分 百操作[[氯化钱晶悴]操作川无水I 通电 夏(MgCl ;*6H 2O ; - MgCljMgCl 2的溶解度曲 线(1) 电解熔融的无水MgCb 可以得到金属镁。
该反应属于基本反应类型中的 __________________ 反 应。
(2) 将海水中的镁提取出来,首先要让海水 中的镁离子形成沉淀而富集起来。
结合 表中数据分析,为了使氯化镁转化为沉gci 淀,应加入的 /g溶液A 可能是 。
温度厂。
(3) 结合MgCb 的溶解度曲线分析,操作I : 蒸发浓缩、 _______ 、过滤。
4. (3分)“煤化工”是以煤为原料,经过化学加 工使煤转化为气体、液体、固体燃料以及各 种化工产品的工业过程。
请回答下列问题:(1) 煤的加工产品有很多用途,其中焦炭广 泛应用于炼铁。
解生产实际分析题的策略本文介绍生产实际分析题的题型特点和答题策略。
此模块取自社会生活、现代科技、新材料合成等,往往表现“高起点、低落点”的特点。
主要考查学生运用化学反应原理及相关知识来解决工业生产中实际问题的能力。
【知识点睛】生产实际分析题通常考查两种题型: (1)工业流程图 例如:回收利用是保护金属资源的一条有效途径.某工业废料含氧化铜和氧化铁,经过处理后可得到铜和硫酸亚铁溶液,主要流程如下.已知:2442CuO+H SO CuSO +H O ═ ()2443Fe+Fe SO 3FeSO ═ 解题策略:①画出题干重点:原料、产物。
②从左到右依次分析流程图,圈划要点(量、条件、操作等)并用化学语言标注关键信息,遇到不会的查阅已知或到问题中寻找已知条件。
③将问题代入框图中相应部位,再思考。
如:回收利用是保护金属资源的一条有效途径.某工业废料含氧化铜和氧化铁,经过处理后可得到铜和硫酸亚铁溶液,主要流程如下.解题技巧:①若考查回收利用金属问题,大多情况下加入的药品中不引入新的金属元素。
②关注“量”,如果固体过量,那么下一步的固体中一定有剩余,液体同理! (2)装置流程图工业上用闪锌矿(主要成分是ZnS 、FeS )冶炼锌,主要流程如下:(1)焙烧炉中,ZnS 转化为ZnO .补全该反应的化学方程式.(2)酸浸槽中,硫酸与锌焙砂反应得到用于电解的酸浸液,反应过程中需不断搅拌,其目的是___________________.(3)酸浸渣的主要成分是铁酸锌(ZnFe 2O 4,其中Fe 为+3价),底吹炉中,主要发生如下反应:①24343ZnFe O +C 2Fe O +3ZnO+CO −−−→↑高温 ②242ZnFe O +CO 2FeO+ZnO+CO −−−→高温 ③2ZnO+CO Zn +CO −−−→高温 (蒸汽)反应①-③中,化合价发生改变的元素有________________. (4)最终可以获得锌的设备有________________. 解题策略:装置流程图的分析和工业流程图分析方法大体相同。
生产实际分析【化合价计算】1.烟道脱硫的工艺不仅能消除SO2,还能将其转化为石膏(CaSO4·2H2O)等产品,实现“变废为宝”。
主要物质转化关系如下:回答下列问题:(1)反应①的基本反应类型是__________。
(2)反应①中化合价发生变化的元素有__________。
(3)下列说法正确的是_________。
a.为更好的脱硫应使用石灰石粉末b.反应①为复分解反应,有CO2生成c.脱硫后的烟气对环境无害2.近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。
过程如下:(1)反应①中化合价发生变化的元素是_________。
(2)反应①属于基本反应类型中的。
3.“打好蓝天保卫战、治理大气污染”是提升人民生活质量的重要工作。
二氧化硫是一种大气污染物。
工业上可以利用海水对二氧化硫进行吸收利用,变害为宝。
其工艺流程见图:(1)流程中将石灰石加水制成石灰石浆的目的是___________________。
(2)其中硫元素的化合价在反应前后的变化为___________。
4.燃油汽车安装的触媒转换器可以将有害气体转化成无害气体,其过程可表示如下:(1)触媒转换器可以将等有害气体转化为无害气体。
(2)在转化过程中化合价变化的元素是。
5.氢气是最理想的清洁能源,煤制氢是目前解决大规模氢来源的重要途径。
煤制氢过程中发生的主要反应为:①C+H2O==== CO+H2①CO+H2O==== CO2+H2(1)上述反应中的各物质,碳元素呈现种化合价。
(2)从上述反应①或①中任选一个....,在两个方框中补全其反应物和生成物相应微粒的图示。
生产实际分析【方程式书写】1.铁矿石炼成铁是一个复杂的过程。
把铁矿石、焦炭和石灰石一起加入高炉,在高温下利用炉内反应生成的一氧化碳把铁从铁矿石里还原出来,如图所示:(1)高炉内发生的主要化学反应:①C+O2高温CO2②C+CO2高温2CO③一氧化碳还原氧化铁____________________________(2)高炉气体中一定含有的成分为______________________2.高纯氧化铁[Fe2O3]又称“引火铁”,在现代工业上有广泛应用前景。
33.(3分)海水中含有丰富的资源,下图是从海水中提取镁的简单流程。
(1)操作①的名称为。
(2)沉淀B与试剂C发生中和反应,该反应的化学方程式为。
(3)由无水MgCl2电解制取Mg的化学反应方程式为。
34.(3分)氨碱法生产纯碱工艺如下图所示,图中生成的NaHCO3受热后会转化成纯碱。
(已知碳酸钙在设备甲中高温分解生成二氧化碳和氧化钙)(1)设备丙中发生反应的化学方程式为。
(2)设备乙中反应物所含元素除C、H、O外,还有(用元素符号表示)。
(3)设备丁中反应后的产物是。
30.(3分)乙炔(C2H2)是一种极易燃的气体,是生产聚氯乙烯的重要原料。
工业上用电石(主要成分为CaC2)制取乙炔的流程如下。
(1)C2H2中碳、氢元素的质量比为。
(2)电石渣可以处理含硫酸的废水,反应的化学方程式为。
(3)根据上述生产流程分析,下列说法正确的是。
①盛放电石的仓库着火,可用水灭火②电石生产乙炔反应的化学方程式为 CaC2 + H2O === Ca(OH)2 + C2H2↑③若将电石长期露置于空气中,可能会有碳酸钙生成31.(3分)工业上用22%~24%的稀硫酸清洗钢材后的废液称为酸洗液,酸洗液中含硫酸和硫酸亚铁,可用来生产铁红(氧化铁),其主要流程表示如下(其中溶液A中投加NaOH时发生复分解反应)。
(1)酸洗液中加入铁皮反应的化学方程式为_____ _。
(2)向Fe(OH)2浑浊液中通空气的目的是。
(3)溶液B中溶质一定含有___ ___。
29.(2分)联合钢铁工业的基本生产流程示意图如下:请回答下列问题:(1)以赤铁矿(Fe2O3)为原料在高温下与一氧化碳反应的化学方程式是。
(2)炼钢炉中通入氧气的目的是。
30.(3分)炼铁产生的废渣中含有大量CuS及少量铁和铁的化合物,工业上以该废渣为原料生产CuCl2的流程图如图所示:(1)②中Cu S、NaCl和O2在高温条件下反应生成了CuCl2和Na2SO4,其反应化学方程式是。
化 学 中 考 专 项 训 练生产实际分析(一)1. 工业上利用硫磺(S )制取硫酸的主要转化过程如下:(1)Ⅱ中发生化合反应的化学方程式为 。
(2)98%的硫酸中溶质与溶剂的质量比为 。
(3)上述流程中的含硫物质有S 、 和H 2SO 4。
2. 氯化钙常用作干燥剂。
工业生产氯化钙主要流程如下:(1)反应器中发生反应的化学方程式为 。
(2)酸浸槽中的反应属于基本反应类型中的 。
(3)脱色池中利用了活性炭的 作用。
3. 海水中含有MgCl 2,可用于提取金属镁,主要流程如右图。
整个生产过程中,主要发生的反应有: ①MgCl 2Mg + Cl 2 ↑②MgCl 2 + Ca(OH)2 == CaCl 2 + Mg(OH)2↓ ③Mg(OH)2 + 2HCl == MgCl 2 + 2H 2O(1)其中反应池中发生的反应是_________(填序号,下同)。
(2)属于复分解反应的是___________。
4. 臭氧(O 3)可用于医用消毒,生产臭氧的主要过程如下。
(1)从微粒..的角度解释,O 2与O 3化学性质不同的原因是________________________。
(2)Ⅰ中发生反应的化学方程式是___________________________。
(3)Ⅱ中发生的变化属于___________(填“物理”或“化学”)变化。
反应器 过滤器酸浸槽 脱色池5. 以粗盐(主要成分NaCl 、MgCl 2等)为原料的氯碱工业的主要工艺流程如下。
已知: Mg(OH)2难溶于水。
(1)溶解池中搅拌的目的是______________________________________________。
(2)处理池中发生复分解反应,该反应的化学方程式是_______________________________________。
(3)电解池中参加反应的物质的化学式为_____________________。