根据化合价书写化学式交叉约简法
- 格式:ppt
- 大小:203.50 KB
- 文档页数:6
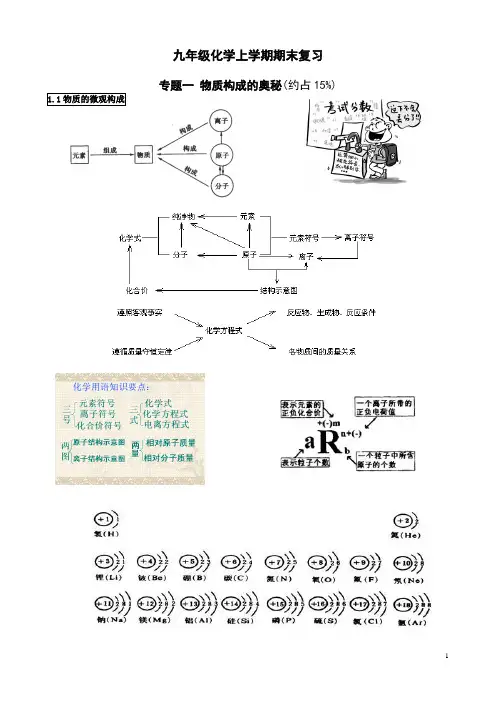
九年级化学上学期期末复习专题一物质构成的奥秘(约占15%)一:分子1.分子、原子的区别和联系2.用原子、分子的观点解释常见现象⑴物质变化:构成物质的 没有改变,只是运动速率、分子间间隔等发生改变,如挥发、扩散、蒸发、三态变化、热胀冷缩、酒精与水等体积混合后总体积变小等。
⑵化学变化: 发生了改变,分裂成原子,原子重新组合成新分子,分子再构成新的物质。
●化学反应的实质:在化学反应中分子 ,原子 。
二:原子1.构成物质的基本微粒有 、 、 ,构成原子的微粒是 、 、 三种。
如:铁是由 构成 ,氯化钠是由 构成,水是由 构成。
分子是保持物质 的最小微粒,而 是化学变化中的最小微粒。
2.五决定:原子的质量主要集中在 上 ;相对原子质量大小取决于 和 之和;与元素化学性质关系最密切的是 ;元素种类 (或元素间的本质区别)决定于 ;元素的化合价与 关系密切。
3.原子的结构①每个质子相对原子质量约等于1,约等于一个 原子的质量。
质子 ②每个质子带一个单位的 电荷。
③决定 种类。
原子核 ①每个中子相对原子质量约等于1,约等于一个氢原子的质量。
原 中子 ② 电荷。
③决定同类元素中的不同种原子。
子 ①质量约等于 (或 )质量的1/1836。
②每个电子带一个单位的 电荷。
③核外电子分层排布, 最外层电子数决定 的性质。
原子中:核电荷数 = 数 = 数 相对原子质量≈质子数 + 中子数。
(为什么?) 阳离子:核电荷数=质子数>核外电子数 阴离子:核电荷数=质子数<核外电子数 三:离子1.概念:带电的原子或原子团叫 。
带正电的离子叫 , 叫阴离子。
2.Fe 、 Fe 2+ 、Fe 3+ 具有相同的 ,属于同一种 ,但它们的 不同因而化学性质也不同。
3.一种元素的原子变成离子:一定改变的是 ,一定不变的 ,可能改变的是 。
(有几个填几个)4.同种元素的原子和离子一定具有相同的 。
一:物质的组成——元素1.元素定义:具有 (或 )的一类 的总称。

(一)、原子(1)由于原子核所带电量与核外电子的电量相等,电性相反,故整个原子不显电性,即核电荷数=质子数=核外电子数。
(2)除相对原子质量为1的普通氢原子不含中子外,其他原子都是由质子、中子、电子三种粒子构成的。
(3)核电荷数(即质子数)决定了元素的种类。
(4)电子的质量很小,可以忽略不计,所以原子的质量主要集中在原子核上。
(二)、相对原子质量以一种碳原子的质量的1/12(约1.66×10-27kg)作为标准,其他原子的质量跟它相比较所得的比值,就是这种原子的相对原子质量,即1、为什么要引入相对原子质量?原子的实际质量很小,一般只有10-27kg左右,这样小的数字,记忆、书写都很不方便,就像用吨作单位来表示一粒稻谷的质量一样,为了解这一问题,就引入了相对原子质量。
2、相对原子质量与原子的质量有什么区别?原子的质量是原子的实际存在的物质的多少,是实际质量或称为真实质量,相对原子质量是以12C原子质量的1/12为标准来表示物质质量多少的相对质量,原子质量的单位是kg,相对原子质量的单位是1。
3、原子质量与相对原子质量的区别与联系4、A、B两原子的相对原子质量之比=A、B两原子的质量之比。
(四)、元素具有相同核电荷数(即核内质子数)的一类原子总称为元素1、地壳中元素的含量地壳中含量较多的四种元素是氧(O)、硅(Si)、铝(Al)、铁(Fe)2、元素符号(1)来源:是这种元素拉丁文名称的第一个大写字母,如果几种元素名称的第一个大写字母相同时,再附加一个小写字母来区别。
(2)书写:第一个字母大写,第二个字母小写,如钙Ca、铜Cu。
(3)表示意义:①表示一种元素;②表示这种元素的一个原子,既有宏观意义,也有微观意义。
如H表示氢元素,也表示一个氢原子,但2H只表示2个氢原子。
3、元素周期表简介元素周期表共有7个横行,18个纵行,每个横行叫做一个周期,每个纵行叫做一个族,所以元素周期表有7周期,16个族(8、9、10三个纵行共同组成一个族)。

班级 姓名 学号 使用时间:2013年 月 日 计划 专题二 物质构成的奥秘2.4化学式及有关计算(2013年)【中考导航仪】【教材放大镜】用 和 的组合表示物质组成的式子,如H 2O 表示水。
2.每种纯净物的组成是,所以表示每种物质组成的化学式只有 个。
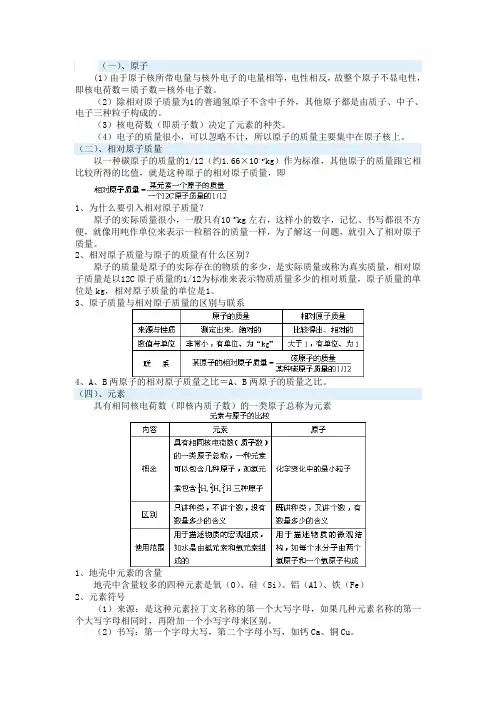
3.4.元素符号周围数字的意义a :表示有a 个R 粒子(原子、分子或离子等)b :表示一个粒子中含有b 个某原子c :表示一个R 离子带c 个正(或负)电荷d :表示(某化合物中)R 元素的化合价为±d 价 5.化学式的书写:6.化学式的读法:①固态单质直接读名称:如Cu读作铜;气态单质在名称后加“气”,如H2读作氢气。
②化合物一般从右向左读“某化某”,例如:ZnS读作硫化锌。
有时还要读出化学式中各元素的个数,如Fe3O4读作四氧化三铁。
数目,是不同元素的原子时表现出来的一种。
它与原子最外层电子数有非常密切关系。
●化合价的实质:元素的一个原子与其他元素的原子化合时,得失电子的数目或共用电子对的数目。
2.化合价的规律:⑴在化合物中氢通常显____价,氧元素通常显______价;⑵在金属化合物中金属元素一般显____价,非金属元素一般显____价;⑶单质中元素的化合价为_______;⑷在化合物里各元素的正负化合价的代数和为____;⑸一些元素在不同物质中可显______的化合价。
3.化合价的表示方法:书写在元素符号的。
【练习】试着标出下列物质中各元素的化合价:CaO Fe2O3H2KOH CO2CO4.例题:求高锰酸钾中锰元素的化合价(KMnO4)①标出常见元素的化合价:KMnO4②设锰元素的化合价为X,列出方程:(+1)×1+X×1+(-2)×4=0③求得X=7 所以:锰元素的化合价为+7价。
⑶根据原子团计算某元素的化合价计算硝酸铵中氮元素的化合价■原子团是指,又叫。
1.元素化合价口诀氢+1,氧-2,银锂钠钾+l价,锌镁钙钡+2价,铝+3,硅+4;只遇金属或是氢,氮磷-3、硫-2,氯碘氟溴总-1。

巧写化学式
作者:郝玉香
来源:《新课程·中旬》2015年第02期
学好化学的基础是熟练掌握化学语言,而化学式的书写是重中之重,下面我们就来看一下如何根据化合价写出化学式。
一、根据化合价书写化学式
例1.已知硫元素为+4价,氧元素为-2价,写出化学式。
步骤一:先排序(正价在前,负价在后)
SO
步骤二:后标价(标出各元素的化合价)
步骤三:约最简(把化合价的绝对值进行化简)
步骤四:再交叉(交叉相乘,把数字写在元素符号的右下角,“1”可省略)
例2.已知铁元素的化合价为+3价,硫酸根为-2价,写出化学式。
注意:把原子团当成一个整体,当原子团的个数大于1时,原子团要加上括号。
二、巧读化学式
例.读出下列化学式。
1.CO2、P2O5、Al2O3、NaCl
读作:二氧化碳、五氧化二磷、氧化铝、氯化钠
2.H2SO4、HNO3、HCl、H2CO3
读作:硫酸、硝酸、盐酸、碳酸
3.NaOH、Ca(OH)2
读作:氢氧化钠、氢氧化钙
4.Na2CO3、Mg(NO3)2、NH4NO3
读作:碳酸钠、硝酸镁、硝酸铵
小结化学式的读法:
从右往左,读作“某化某”(“几氧化几某”)“某酸”“氢氧化某”“某酸某”等。
编辑范昕欣。



十字交叉法写化学式
利用化合价写化学式
根据化合价写化学式的依据:
化合物中各元素正负化合价的代数和为零
常见的方法:最小公倍数法和十字交叉法
1、最小公倍数法写化学式
最小公倍数法———“一写、二求、三标、四验”
一写:一般把正价元素的符号(或根)写在左边,负价元素的符号(或根)写在右边,并把化合价写在元素符号(或根)的正上方
二求:求两种元素(或根)的最小公倍数,然后求出每种元素(或根)的原子个数。
即原子个数=最小公倍数÷∣化合价∣
三标:将原子个数写在相应元素符号(或根)的右下角
四验:检验各种元素正负化合价的代数和是否为零,确定化学式的正确性
2、十字交叉法写化学式
十字交叉法———“一排、二标、三交、四约、五查”
一排:元素符号(或根)一般按正价左,负价右顺序排列
二标:标出各元素的化合价,如果有根只需标出根的化合价
三交:将元素化合价(或根)的绝对值交叉写在另一元素符号(或根)的右下角
四约:将各元素(或根)的原子数约成最简整数比
五查:检查正负化合价代数和是否为零,确定化学式的正确性
这种方法也可以简单记忆为“正左负右标价数,十字交叉写个数”
说明:
①、只有确切知道某物质存在才能根据化合价书写化学式
②、一般把正价写在左边,负价写在右边。
但也有例外。
如NH3
③、如果标明根的个数时,应把根加上括号,再把数字写在右下角
1 / 11 / 1。

怎样书写化合物的化学式与九年级上册化学必须记住的化学式化合价是元素(原子团)相互化合时所表现出的一种性质,因此,熟悉化合价是正确书写化合物化学式的必要条件,书写化学史的方法你想了解吗?小编整理了相关资料,希望能帮助到您。
怎样书写化合物的化学式一、熟记常见元素(原子团)的化合价化合价是元素(原子团)相互化合时所表现出的一种性质,因此,熟悉化合价是正确书写化合物化学式的必要条件。
我们可以先将常见元素(原子团)的化合价编成下列韵语:-1氢硝根和氯;-2氧和碳硫根;+1铵钾钠银氢;+2钙镁钡铜锌(注:“氢硝根”是指氢氧根和硝酸根;“碳硫根”是指碳酸根和硫酸根)。
然后,用口念韵语、手写符号相结合的方法,手、口、脑并用,使常见元素(原子团)的符号、化合价数值深深印记在脑海中,为运用时快速提取这部分知识打下坚实的基础。
(敬请关注“九年级化学”微信公众号)二、了解化合物的组成特点每一类化合物都有其相应的组成特点。
“某化某”类化合物由两种元素组成,如,氯化钾(KCl),硫化氢(H2S),氧化镁(MgO);“氢氧化某”类化合物由金属元素和氢氧根组成,如,氢氧化钠(NaOH),氢氧化铜[Cu(OH)2];“某酸”类化合物由氢和酸根组成,如,硫酸(H2SO4),碳酸(H2CO3);“某酸某”类化合物一般由金属和酸根组成,如,硫酸锌(ZnSO4),碳酸钙(CaCO3)。
(敬请关注“九年级化学”微信公众号) 书写化合物的化学式时,首先要根据化合物的名称对其进行归类,然后根据其组成特点和组成元素的化合价去书写化学式,谨防将KCl(某化某)写成KClO3(某酸某)一类错误的发生。
三、掌握化学式的书写步骤(敬请关注“九年级化学”微信公众号)化合物化学式的书写一般要经历以下步骤:归类→定序→标价→交叉→约简。
归类:根据化合物的名称,确定化合物所属类别;定序:将组成化合物的元素、原子团,按照“正左负右”(显正价的元素或原子团写在左边,显负价的元素或原子团写在右边)的原则写出;标价:在元素或原子团的上方标出相应的化合价(化学式书写到达熟练程度之后,可将这一过程改为在头脑中回忆化合价);交叉:将正价一方的化合价数值写在负价一方的右下角,将负价一方的化合价数值写在正价一方的右下角;(敬请关注“九年级化学”微信公众号)约简:交叉后所得的右下角的两数字间,如有公约数,通常要进行约简,使右下角两数字之间的比值成为最简比【如果某一方是原子团,且原子团数目为2及2以上时,要在原子团外加括号,如Al2(SO4)3】。
常用的化学方程式书写及配平的口诀常用的化学方程式书写及配平的口诀书写口诀:重客观,量守恒;左反应,右生成。
化学式,请写对;计量数,来配平;连等号,条件清;标气沉,用箭头。
配平口诀:一找元素见面多,二将奇数变成偶,三按连锁先配平,四用观察配其它;有氢找氢无氢找氧,奇数配偶变单成双,出现分数去掉分母,调整系数使支配平。
配平方法:1、岐化反应的简捷配平法口诀:三种价态先标记,两者相减第三系。
若有约数需约简,悠然观察便配齐。
说明:1、岐化反应又称自身氧化还原反应,在岐化反应中,同一种元素的一部分原子(或离子)被氧化,另一部分原子(或离子)被还原。
如:KCIO3 → KCIO4+KCIS+KOH → K2S+K2SO3+H2O2、三种价态先标记:意思是说岐化反应简捷配平法的第一部是首先标记清楚反应式中不同物质分子中发生岐化反应的元素的化合价。
如:S0+KOH → K2S+K2SO3+H2O3、两者相减第三系:意思是说任意两个化合价的变化值(绝对值),即为第三者的系数。
4、若有约数需约简:意思是说由第二步得到的三个系数若有公约数,则需要约分后再加到反应式中去。
根据诗意的要求分析如下:在S和K2S中,S0 →S-2,化合价变化值为∣0-(-2)∣= 2,所以K2SO3前的系数为2。
在S和K2SO3中,S0→S+4,化合价变化值为∣0-4∣= 4,所以K2S前的系数为4。
在K2S和K2SO3中,S-2→S+4,化合价变化值为∣(-2)-4∣= 6,所以S前的系数为6。
又因为2、4、6有公约数2,所以约简为1、2、3,将约简后的系数代入反应式得:3S+KOH → 2K2S+K2SO3+H2O5、悠然观察便配齐:意思是说将约简后的系数代入反应式后,悠然自在地观察一下就可以配平。
观察可知:右边为6个K,所以KOH前应加6,加6后左边为6个H,所以H2O前应加3,于是得到配平后的化学反应方程式:3S+6KOH = 2K2S+K2SO3+3H2O双水解反应简捷配平法口诀:谁弱选谁切记清,添加系数电何等。
(一)常见元素的化合价口诀:钾钠氢银正一价,钙镁钡锌正二价;铝是正三氧负二,氯负一价最常见;硫有负二正四六,正二正三铁可变;正一二铜二四碳,单质零价永不变;其它元素有变价,先死后活来计算。
(二)常见原子团(根)的化合价:磷酸根3PO-4铵根1NH+4硫酸根24SO-亚硫酸根23SO-碳酸根23CO-锰酸根24MnO-氢氧根1OH-硝酸根13NO-氯酸根13ClO-高锰酸根14MnO-一价铵根硝酸根;氢卤酸根氢氧根。
高锰酸根氯酸根;高氯酸根醋酸根。
二价硫酸碳酸根;氢硫酸根锰酸根。
暂记铵根为正价;负三有个磷酸根二、化合物化学式的书写(一)根据化合价书写化学式:(二)根据名称书写化学式常见的化合物有四种读法,不论是哪一种读法,从化合价角度看,都只有正价和负价两部氯酸钾锰酸钾亚硫酸钠硫酸铝作业:1、熟记并书写第1页上化学基本用语2、按物质名称书写化学式:氧化铵硫化铵(3)硫酸铜碳酸镁磷酸铵高锰酸钾氯酸钙硝酸银氯酸钾锰酸钾亚硫酸钠硫酸铝硝酸汞亚硫酸铵硫酸锌硝酸铜硫酸钡碳酸铵磷酸钙氯酸钾(5)氢氧化铝氧化铁氧化钙硫化铁氯化钙硫化铵3、过关检测(要求:在掌握已学知识情况下用考试的要求来完成)第一组写出下列物质的化学式:硫化钾氧化亚铁氢氧化钙氢氧化钡硫酸铜氯化铁碳酸镁磷酸铵氯酸高锰酸钾氯酸钙硝酸银氯酸钾锰酸钾亚硫酸钠硫酸铝氟化铜碳酸氯化锌硝酸汞第二组写出下列物质的化学式:氯化钾锰酸亚硫酸铵硫酸铝氟化铵磷酸氯化铝硝酸铜硫化铝硫化亚铁氢氧化钠氢氧化镁硫酸钡氯化氢碳酸铵磷酸钙氯酸高锰酸铵氢氧化铝硝酸银。
化学式化合价【主要内容】化学式化合价【知识要点】一.化学式1.定义:用元素符号和数字的组合表示物质组成的式子。
2.写法和读法:(1)单质的化学式双原子:H2、N2、O2、Cl2(氯气)等多原子:O3(臭氧)、P4(白磷)等(2)化合物的化学式①氧化物的写法和读法:写法:氧元素写在后面,另一种元素写在前面,并标出角码,当角码为“1”时省略。
读法:角码为1时,读作“氧化某”,如:ZnO(氧化锌)、MgO(氧化镁)等。
角码不为1时,读作“几氧化几某”,如:Fe3O4(四氧化三铁)、P2O5(五氧化二磷)等。
特殊:H2O(水)、CO(一氧化碳)、Fe2O3(氧化铁)、FeO(氧化亚铁)、H2O2(过氧化氢)等②由一种金属元素和一种非金属元素组成的化合物的写法和读法:写法:金属元素在前,非金属元素在后,并标出角码,当角码为“1”时省略。
读法:读作“某化某”,如:NaCl(氯化钠)、MgCl2(氯化镁)、ZnS(硫化锌)等特殊:FeCl2(氯化亚铁)、FeCl3(氯化铁)3.化学式表示的含义:以H2O为例:(1)从组成上看:宏观:水是由氢元素和氧元素组成的;微观:水是由许多水分子构成的,一个水分子是由两个氢原子和一个氧原子构成的。
(2)从它代表的物质看:宏观:水这种物质;微观:一个水分子。
说明:只要化学式前有化学计量数(旧称“系数”),只表示微观。
如:3H2O 表示三个水分子、2Fe 表示两个铁原子等。
二.相对分子质量(M r)1.定义:化学式中所有原子相对原子质量之和说明:是一个比值,单位为“1”2.有关化学式的相关计算:(1)相对分子质量、相对分子质量总和的计算:例如:水(H2O)的相对分子质量为:2×1+1×16 = 18 或Mr(H2O) = 2×1+1×16 = 18CuSO4·5H2O的相对分子质量为:64+32+16×4 + 5×(2×1+16) = 250(说明:化学式中的“·”此时表示“+”,而不是数学中的“×”)2CO2的相对分子质量总和为:2×(12×1+16×2) = 88(2)化合物中原子个数比或元素质量比的计算:例如:求NH4NO3中各原子个数比、各元素的质量比NH4NO3中氮原子、氢原子、氧原子的个数比为2∶4∶3;NH4NO3中氮元素、氢元素、氧元素的质量比为(2×14)∶(4×1)∶(3×16)= 7∶1∶12 或者NH4NO3中m(N)∶m(H)∶m(O) = (2×14)∶(4×1)∶(3×16)= 7∶1∶12(3)化合物中元素质量分数的计算例如:求NH4NO3中氮元素的质量分数三.化合价1.定义:一种元素的一定数目的原子与其它元素一定数目的原子化合时所表现出的性质。