七年级科学:身边的溶液(溶液、水以外的溶液)
- 格式:ppt
- 大小:5.75 MB
- 文档页数:20
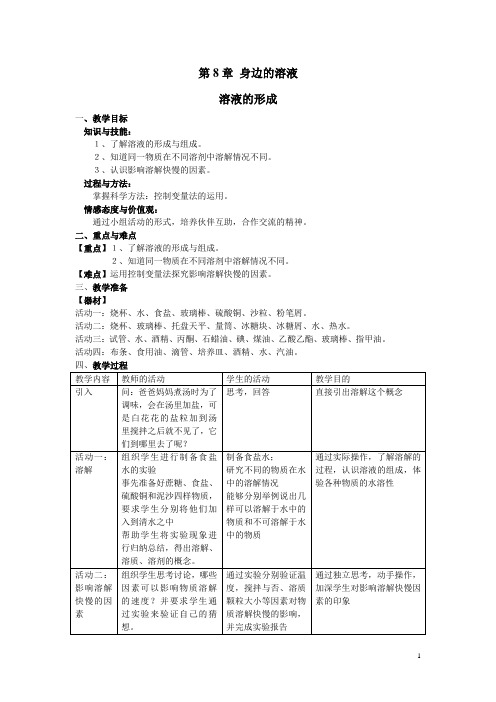
第8章身边的溶液溶液的形成一、教学目标知识与技能:1、了解溶液的形成与组成。
2、知道同一物质在不同溶剂中溶解情况不同。
3、认识影响溶解快慢的因素。
过程与方法:掌握科学方法:控制变量法的运用。
情感态度与价值观:通过小组活动的形式,培养伙伴互助,合作交流的精神。
二、重点与难点【重点】1、了解溶液的形成与组成。
2、知道同一物质在不同溶剂中溶解情况不同。
【难点】运用控制变量法探究影响溶解快慢的因素。
三、教学准备【器材】活动一:烧杯、水、食盐、玻璃棒、硫酸铜、沙粒、粉笔屑。
活动二:烧杯、玻璃棒、托盘天平、量筒、冰糖块、冰糖屑、水、热水。
活动三:试管、水、酒精、丙酮、石蜡油、碘、煤油、乙酸乙酯、玻璃棒、指甲油。
活动四:布条、食用油、滴管、培养皿、酒精、水、汽油。
四、教学过程生活中常见的溶液常见的酸碱指示剂(一)一、教学目标1.知道对溶液的科学分类可以按照其酸碱性分为酸性、碱性和中性溶液。
2.认识实验室常用的两种指示剂:石蕊和酚酞遇不同酸碱性溶液的变色情况。
3.懂得要移取少量的溶液进行酸碱性测定而不能污染待测溶液。
4.学会用石蕊和酚酞判断和区分溶液的酸碱性,认识常见的酸性溶液和碱性溶液。
5.了解指示剂发现过程中所体现的科学精神,激发从生活中发现不同的指示剂。
二、重点与难点【重点】1.学会用石蕊和酚酞两种指示剂判断溶液的酸碱性。
【难点】1.正确记录石蕊和酚酞遇不同酸碱性溶液的颜色变化。
2.实验操作中防止对待测溶液的污染和指示剂滴管的交叉污染。
三、教学准备【器材】活动一:生活中的一些溶液图片。
活动二:紫色石蕊试液、无色酚酞试液、试管架、小试管6、2试管酸性溶液(稀盐酸)、2试管中性溶液(蒸馏水)、2试管碱性溶液(稀氢氧化钠)。
活动三:紫色石蕊试液、无色酚酞试液、试管架、小试管3、溶液A(稀盐酸或稀硫酸)、溶液B(稀氢氧化钠或石灰水)、溶液C(蒸馏水)、学生自带待测溶液2-3种。
【资源】活动三:补充实验报告活动四:PPT课件。

中考化学复习身边的化学物质:水和溶液1.水:①认识水的组成。
②知道纯水与矿泉水、硬水与软水等的区别。
③了解吸附、沉淀、过滤和蒸馏等净化水的常用方法。
④理解水对生命活动的重要意义,认识水是宝贵的自然资源,形成保护水资源和节约用水的意识。
2.溶液:①认识溶解现象。
②知道水是最重要的溶剂,酒精、汽油也是常见的溶剂。
③了解饱和溶液和溶解度的含义。
④能配制一定溶质质量分数的溶液。
⑤了解结晶现象。
⑥能说出一些常见的乳化现象。
⑦了解溶液在生产、生活中的重要作用。
⑧能进行溶质质量分数的简单计算。
围绕考纲我们应掌握如下要点:1.水:①正确描述水的组成、性质及用途。
知道水组成的测定方法。
②能区分纯水与矿泉水、硬水与软水,掌握鉴别硬水与软水的方法。
③学会吸附、沉淀、过滤和蒸馏等净化水的常用方法。
④理解水对生命活动的重要意义,了解保护水资源和节约用水的常见措施。
2.溶液:①能正确描述溶液的组成,理解溶液和溶质、溶剂的概念,明确它们的关系。
②通过实验认识水溶液的一些性质。
③了解饱和溶液和溶解度的含义。
④认识溶液由溶质和溶剂组成,水是常用的溶剂。
⑤正确领会饱和溶液、不饱和溶液的概念,知道它们在一定的条件下是可以相互转化的。
⑥记住溶解性和溶解度的概念,明确它们的关系。
认识固体物质溶解度曲线,正确描述温度对固体溶解度的影响规律,并会简单的应用。
⑦结晶方法及其在生产生活中的应用。
⑧学会溶质质量分数的计算及一定溶质质量分数的溶液的配制。
考点①对水的综合认识水②电解水③水的净化考情回顾(河北省)①溶液②饱和溶液&不饱和溶液溶液③溶解度、溶解度曲线年份2021年4题(2分)单选考查方式考查对水的认识中考说明解读考纲2021年30题(4分)考查水电解实验2021年14题(2分)单选以水的组成、净化、软硬水综合2021年29题(3分)填空认识水2021年29题(2分)填空考查溶液形成、乳化作用2021年14题(2分)选填以图示形式考查溶解热量变化2021年6题(2分)单选2021年6题(2分)选择2021年7题(2分)选择2021年36题(5分)考查饱和与不饱和的转化、结晶以溶解度曲线考查溶解度及应用利用守恒关系解方程式计算表格沉淀利用守恒关系解方程式计算图示气体④溶质的质量分数2021年36题(5分)计算命题预测创设具体情景,以“节约用水,防止水污染”为主题的信息题、开放题是中考的热点之一;围绕水的组成和性质、水的电解实验、水的净化设计考题是有关水的知识又是一个热点。

初中概念详解之——溶液一、溶液概念:一种或一种以上的物质以分子或离子形式分散于另一种物质中形成的均一、稳定的混合物。
【定义扩展:分散质的粒子直径<1nm(1×10^-9m)的分散系。
分散质是分子或离子,具有透明、均匀、稳定的宏观特征。
通常情况下,我们把分散质粒子的直径大于10的负7次方米{100nm}的分散系叫做浊液(悬浊液或乳浊液),分散质粒子的直径在10的负9次方米~10的负7次方米{1nm~100nm}之间的分散系叫做胶体(colloid),分散质粒子的直径小于10负9次方{1nm}的分散系叫做溶液。
乳浊液:一种很细的液体分散于另一种(或数种)与之互不溶的液体中所形成的乳状液。
分散质粒子的直径大于100nm,为很多分子的集合体。
乳浊液不透明、不均一、不稳定,能透过滤纸不能透过半透膜。
静置后会出现液体上下分层的现象。
如油水混合物、石油原油、橡胶的乳胶、油漆就是乳浊液。
悬浊液:大于100纳米的固体小颗粒悬浮于液体里形成的混合物。
分散质粒子直径大于100nm,多为很多分子的集合体。
悬浊液不透明、不均一、不稳定,不能透过滤纸,静置后会出现分层(即分散质粒子在重力作用下逐渐沉降下来)如面糊,泥水,氢氧化铜,碳酸钙。
】二、溶液按聚集态不同分类:气态溶液:气体混合物,简称气体(如空气)。
液态溶液:气体或固体在液态中的溶解或液液相溶,简称溶液(如盐水)。
固态溶液:彼此呈分子分散的固体混合物,简称固溶体(如合金)。
读法:一般读作“某某(溶质)的某(溶剂)溶液”,如酒精可读作“乙醇的水溶液”说明:如果溶剂是水,可以简称为某溶液如“乙醇的水溶液”可以叫做乙醇溶液如果两种液体互溶,有水则以水为溶剂,否则以质量大的为溶剂三、组成成份:1.溶质:被溶解的物质(例如:用盐和水配置盐水盐就是溶质)2.溶剂:能溶解其他物质的物质(例如:用盐和水配置盐水,水就是溶剂)3.两种溶液互溶时,一般把量多的一种叫溶剂,量少的一种叫溶质。

牛津上海版七年级第一学期科学第八章身边的溶液第一节溶解1.溶液:是一种或一种以上的物质分散到另一种物质里,形成均一、稳定的混合物。
如:消毒酒精;生理盐水;碘酒等等可溶物质:在水中溶解的物质。
不可溶物质:不可在水中溶解的物质。
2.溶质:溶解在液体里的物质。
固体、液体或气体。
3.溶剂:溶解溶质的液体。
液体,常见的如水、酒精,汽油。
4.影响溶解快慢的因素:溶质颗粒大小(颗粒越小溶解速度越快)搅拌与否(搅拌使溶解速度加快)温度高低(加温使溶解速度加快)第二节水以外的溶剂1.生活中除了水,酒精,汽油等也可以作为一些物质的溶剂使用。
2.水是常用的溶剂,但它不能溶解所有的物质。
碘和指甲油等不能溶于水,但却可以溶于其它溶剂。
3.干洗:利用水以外的更容易溶解污渍的溶剂,清洗衣物,并且该溶剂不会溶解衣物。
第三节生活中常见的溶液溶液的分类:酸性溶液;中性溶液;碱性溶液第四节常见的酸碱指示剂1. 常用酸碱指示剂:石蕊是酸红、碱蓝,水紫(原)色酚酞是碱红、酸和水无(原)色。
2. pH试纸:遇酸变红色,遇碱变蓝色,遇蒸馏水变淡绿色3. pH试纸特点:pH值在0—14之间pH值小于7是酸性 pH值等于7是中性 pH值大于7是碱性pH值越小,酸性越强 pH值越大,碱性越强第五节酸碱溶液混合后的变化1.在碱溶液中加入酸溶液后,溶液的碱性减弱。
2.在酸溶液中加入碱溶液后,溶液的酸性减弱。
3.中和作用:酸碱混合时,会使对方的酸性和碱性减弱生成盐类物质和水。
4.酸碱溶液在日常生活中的运用。
第六节酸雨1. 酸雨是pH小于5.6的雨水2. 引起酸雨的主要物质是二氧化硫和氮氧化物3. 酸雨的危害:(1)河流、湖泊酸化,导致水生物、植物死亡。
(2)土壤酸化,导致森林死亡,农作物枯萎。
(3)加速建筑物和文物古迹的腐蚀和风化过程。
(4)影响人体健康。
4. 预防酸雨的措施:控制二氧化硫和氮氧化物第七节酸碱溶液的腐蚀性1. 稀盐酸的腐蚀性:(1)稀盐酸可以与除铜以外的金属发生反应,反应速度快慢不一,生成氢气等,所以不能将稀盐酸存放在金属容器中。

第八章牛津上海版科学七上《身边的溶液》教学村料
王沁怡
一、学情分析、教材分析
1.学情分析:
学生对水以外的溶剂可能了解不多,通过本课的学习,帮助学生了解更多溶剂。
而对于常见的溶液,应该能举出较多例子,这部分内容比较简单。
2.教材分析:
本课的前半部分“水以外的溶剂”是对前一课“溶解”的延伸,而后半部分“生活中常见的溶液和其分类”则是为下节课学习“用酸碱指示剂测定溶液酸碱性”作准备。
二、教学目标
1.知识与技能
1)知道同一物质在不同溶剂中溶解情况不同。
2)认识日常生活中的一些酸性和碱性溶液,知道对溶液的科学分类可以按照其酸碱性分为酸性、碱性和中性溶液。
2.过程与方法
通过观察教师演示实验,知道同一物质在不同溶剂中溶解情况不同。
3.情感、态度和价值观
体会科学与生活的密切关系
三、重点和难点
1.重点:知道同一物质在不同溶剂中溶解情况不同
2.难点:讨论如何找出清除油渍的最佳溶剂
四、教学工具
试管(8支)、试管架、药匙、滴管水、酒精、丙酮、石蜡油、碘、煤油、乙酸
乙酯、玻璃棒(4根)、指甲油、布条(3条)、培养皿(3个)、汽油。
六、教学板书
第八章溶液的形成第2课时
1.水以外的溶剂:酒精、丙酮、煤油、乙酸乙酯、汽油。
2.同一物质在不同溶剂中的溶解情况不同。
3.常见溶液的分类:按酸碱性分为酸性溶液、中性溶液和碱性溶液。
七、教学反思。

第八章身边的溶液溶解(dissolving)教学设计:本节课是新学期的第一节课,如何提高学生的学习兴趣是本节课的关键,运用直观的方法使学生明白什么是溶解,得到后的物质是溶液,引出溶剂和溶质,找出影响溶解快慢的因素,要注意引导学生设计方案,控制变量,并且要设计好实验步骤,再进行实验,最后由学生自己进行总结。
教学目标:知识和技能:1、知道溶质、溶剂和溶液的区别。
2、知道物质可分为可溶物质和不可溶物质。
》科学方法和能力:通过对影响溶解快慢的因素探究,培养学生的制定计划和动手动脑的实践能力。
情感、态度和价值观:1、培养能独立思考、又能乐于与他人合作、交流能力。
2、培养学生的猜测精神和想象能力和实事求是的科学态度。
教学准备:食盐、硫酸铜、沙粒、粉笔屑、冰糖块、冰糖屑、水、热水、烧杯、玻璃棒、电子天平、胶头滴管。
[剂可溶物质结论}快慢的因素教学过程:教学后记:',-水以外的溶剂和生活中常见的溶液教学设计:》本节课的内容比较简单,与学生的生活实际联系紧密,学生比较感兴趣,也容易理解,通过演示实验和学生的探究活动,学生的感性认识得到加强,有利于同学合作和交流。
教学目标知识和技能:1、知道一些除水之外的其他常用溶剂。
2、知道生活中常见溶液的用途。
过程和方法:1、熟练掌握移取溶液的技巧。
2、培养学生的社会调查及生活实践能力。
~情感、态度和价值观1、通过实验、培养严谨相信的学习态度。
2、在实验中,培养同学之间合作和交流。
教学方法实验探究法,讨论法。
教学设备试管、药匙、滴管、牙签、布条、胶头滴管、培养皿、酒精、汽油、水、丙酮、石蜡油、煤油、乙酸乙酯、指甲油、碘。
教学流程:】活动(1)五、教学后记'.…常见的酸碱指示剂一、教学设计*掌握酸碱指示剂的种类与使用方法的是学生学好酸和碱的前提,也是本节以后几节的基础。
要在一节课中让学生记住指示剂及与酸碱溶液反应的颜色是较困难的,可教材第8页表格,让学生讨论寻找酸碱指示剂遇酸碱溶液颜色变化的规律。
水和溶液初中科学知识点提纲水和溶液初中科学知识点提纲1溶液的形成一溶液1. 定义:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物,叫做溶液。
2. 基本特征① 均一性:指溶液中各部分的浓度和性质都相同。
② 稳定性:外界条件不变温度、压强不改变,溶剂不蒸发时,溶质、溶剂不分层,也不会析出固体。
3. 组成——溶液由溶质和溶剂两部分① 溶剂:能溶解其他物质的物质叫做溶剂,常见的溶剂有水、酒精、汽油。
水能溶解很多物质,汽油能溶解油脂,酒精能溶解碘等;通常不指明溶剂的溶液,一般指的是水溶液。
② 溶质:被溶解的物质叫做溶质,可以是固体、液体或气体。
③ 区分溶剂和溶质:固体或气体与液体混合时,固体或气体是溶质,液体是溶剂;液体和液体混合时,质量小的为溶质,质量大的为溶剂,如果其中一种液体是水,那么水是溶剂。
④ 同一物质在不同溶剂中的溶解性是不同的,不同物质在同一溶剂中的溶解性也是不同的。
例如:碘几乎不溶于水,却可以溶解在汽油中;高锰酸钾几乎不溶于汽油,却可以溶解在水中。
⑤ 溶液中溶质可以有一种或多种,但溶剂只能有一种。
⑥ 水和酒精能以任意体积互溶。
4. 关系① 溶液、溶质、溶剂的质量关系:溶液的质量=溶质的质量+溶剂的质量② 溶液、溶质、溶剂的体积关系:溶液的体积溶质的体积+溶剂的体积原因:分子之间存在间隔二溶解时的吸热或放热现象1. 物质在溶解时,通常伴随着热量的变化,会使溶液的温度相应发生变化。
2. 有的物质溶解放热:氢氧化钠固体、浓硫酸、氧化钙等。
3. 有的物质溶解吸热:硝酸钾等。
4. 有的物质溶解没有明显的热现象:氯化钠等。
三悬浊液和乳浊液1. 悬浊液:固体小颗粒分散到液体里形成的混合物叫做悬浊液,例如钡餐硫酸钡的悬浊液、粉刷墙壁用的涂料、黄河水等。
2. 乳浊液:小液滴分散到液体里形成的混合物叫做乳浊液,例如在农业上,一般把不溶于水的液体农药配制成乳浊液;植物油和水混合形成乳浊液。
3. 溶液、悬浊液与乳浊液的对比① 溶液均一稳定;悬浊液不稳定,静置一段时间后,固体小颗粒会沉降下来;乳浊液不稳定,静置后会分层。
《身边的溶液》复习青浦区实验中学麻妍劼一、背景及教学任务分析1、教学内容分析《身边的溶液》是牛津上海版《科学》七年级第一学期第八章(主题十)的内容。
这一章包括了“溶液的形成”、“形形色色的溶液”、“安全使用溶液”三大主题板块,“溶液的形成”涉及溶液的组成、溶解等有关知识;“形形色色的溶液”包含酸碱指示剂、酸雨等相关内容;“安全使用溶液”涵盖了酸碱腐蚀等方面知识,其中,“形形色色的溶液”是本章教学重点。
在上一学期,学生已经学习了第八章的所有内容,本节课通过复习,帮助学生回忆基础知识,梳理结构脉络,提升综合能力。
教师通过课堂启发,使学生能在交流、讨论、实验等活动中达到“正确区分溶液的组成,巩固酸碱指示剂的使用方法,理解酸雨的相关知识”的目的,在此基础上,学生能用所学知识分析实验与生活中和溶液有关的问题并作出评价,掌握科学的实验方法,提高分析问题和评价问题的能力。
2、教学对象分析学生在七年级第一学期已经学习过《身边的溶液》,对本章的大部分知识是有记忆的。
然而,很多学生对酸雨的概念和对酸碱溶液的鉴别方法还比较模糊,对诸如溶质、溶剂等概念容易产生混淆,对“控制变量”方法没有深入理解,无法灵活运用。
七年级2班的学生有较强的语言表达能力,他们也愿意通过小组合作的方式进行学习,根据这一特点,本节课的教学重点在小组合作中展开,通过合作方式调动积极性,使所有学生参与其中。
二、教学目标1、通过课前课中对溶液知识的梳理,初步学会搭建知识框架,理解溶液知识间的内在联系,在活动中提高表达交流能力。
2、通过对“酸碱指示剂”和“酸雨”重点知识的强化加深,巩固实验技能,提高对问题的辨析能力和逻辑论述能力。
3、通过对溶液相关的综合例题分析交流,理解“控制变量”的科学方法,能够对问题形成合理的观点,树立辩证的科学态度。
三、教学重点与难点重点:1、搭建知识框架,建立知识间内在联系2、用酸碱指示剂辨别溶液的酸碱性难点:区分溶质和溶剂四、教学设计思路本节课的设计有两个意图:巩固基础知识和提高学生能力。