高中化学-碳硅知识
- 格式:docx
- 大小:287.33 KB
- 文档页数:14

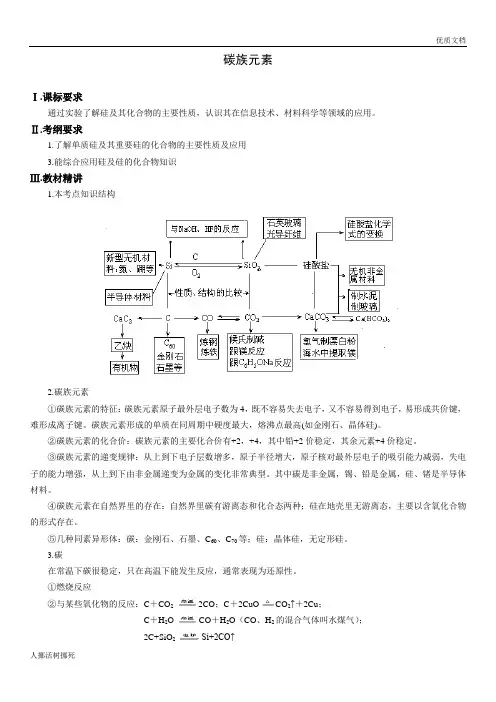
碳族元素Ⅰ.课标要求通过实验了解硅及其化合物的主要性质,认识其在信息技术、材料科学等领域的应用。
Ⅱ.考纲要求1.了解单质硅及其重要硅的化合物的主要性质及应用3.能综合应用硅及硅的化合物知识Ⅲ.教材精讲1.本考点知识结构2.碳族元素①碳族元素的特征:碳族元素原子最外层电子数为4,既不容易失去电子,又不容易得到电子,易形成共价键,难形成离子键。
碳族元素形成的单质在同周期中硬度最大,熔沸点最高(如金刚石、晶体硅)。
②碳族元素的化合价:碳族元素的主要化合价有+2,+4,其中铅+2价稳定,其余元素+4价稳定。
③碳族元素的递变规律:从上到下电子层数增多,原子半径增大,原子核对最外层电子的吸引能力减弱,失电子的能力增强,从上到下由非金属递变为金属的变化非常典型。
其中碳是非金属,锡、铅是金属,硅、锗是半导体材料。
④碳族元素在自然界里的存在:自然界里碳有游离态和化合态两种;硅在地壳里无游离态,主要以含氧化合物的形式存在。
⑤几种同素异形体:碳:金刚石、石墨、C60、C70等;硅:晶体硅,无定形硅。
3.碳在常温下碳很稳定,只在高温下能发生反应,通常表现为还原性。
①燃烧反应②与某些氧化物的反应:C+CO22CO;C+2CuO CO2↑+2Cu;C+H2O CO+H2O(CO、H2的混合气体叫水煤气);2C+SiO2Si+2CO↑③与氧化性酸反应:C+2H2SO4(浓)CO2↑+2SO2↑+2H2O;C+4HNO3(浓)CO2↑+4NO2↑+2H2O4.CO不溶于水,有毒(CO和血红蛋白结合,使血红蛋白无法和O2结合,而使细胞缺氧引起中毒),但由于CO无色无味因此具有更大的危险性。
①可燃性②还原性:CO+CuO CO2+Cu,CO+H2O(g)CO2+H2O5.CO2直线型(O=C=O)非极性分子,无色能溶于水,密度大于空气,可倾倒,易液化。
固态CO2俗称干冰,能升华,常用于人工降雨。
实验室制法:CaCO3+2HCl=CaCl2+CO2↑+H2O。

一、知识点一、碳、硅及其化合物1.碳碳在常温下非常稳定,但在高温条件下活动性增强,主要表现为还原性(1)与单质反应2C+O22CO C+O2CO2(2)与某些氧化物反应C+CO22CO C+H2O(g)CO+H22C+SiO2Si+2CO↑C+2CuO2Cu+CO2↑(3)与氧化性酸反应C+2H2SO4(浓)CO2↑+2SO2↑+2H2OC+4HNO3(浓)CO2↑+4NO2↑+2H2O2.碳的氧化物(1)CO物理性质:无色无味、难溶于水,有剧毒的气体。
具有可燃性和还原性。
化学性质:2CO+O22CO23CO+Fe2O32Fe+3CO2CO+H2O CO2+H2(2)CO2物理性质:无色无味,能溶于水(1∶1)的气体。
密度比空气大,易液化。
化学性质:①氧化性:CO2+C2CO②酸性氧化物的通性CO2+H2O H2CO3CO2+Ca(OH)2=CaCO3↓+H2OCO2+H2O+CaCO3=Ca(HCO3)22CO2+Ca(OH)2=Ca(HCO3)2CO2+CaO CaCO33.碳酸盐(1)溶解性正盐中只有碱金属的碳酸盐和铵盐溶于水,所有酸式盐均溶于水。
一般酸式盐比相应正盐易溶,但碱金属的碳酸氢盐比正盐溶解度小。
(2)热稳定性一般规律:可溶性碳酸正盐>不溶性碳酸正盐>酸式碳酸盐。
Na2CO3>CaCO3>NaHCO3(3)正盐与酸式盐的相互转化4.硅(1)与单质反应Si+2Cl2SiCl4(无色液体)Si+O2SiO2(2)硅的制取:SiO2+2C Si+2CO↑(得到粗硅)精制:Si+2Cl2SiCl4 SiCl4+2H2Si+4HCl5.二氧化硅(1)酸性氧化物的通性SiO2+CaO CaSiO3SiO2+2NaOH=Na2SiO3+H2O(2)氧化性SiO2+2C Si+2CO↑(3)和HF反应:SiO2+4HF=SiF4↑+2H2O6.硅酸和硅酸盐(1)硅酸是不溶于水的白色固体,酸性比碳酸还弱。
高考总复习《碳硅》【考纲要求】1.了解C 、Si 及其化合物的主要性质及应用。
2.掌握CO 2的实验室制取。
3.了解玻璃、水泥、陶瓷等硅酸盐材料的制备原料、原理和特性,能用氧化物形式表示硅酸盐的组成。
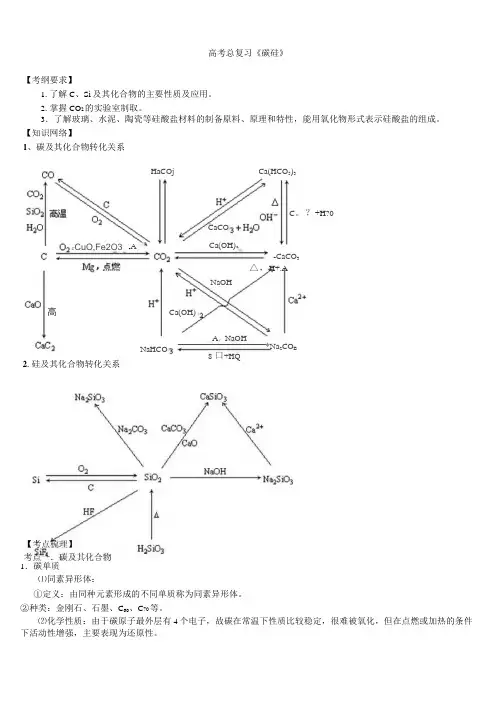
【知识网络】1、碳及其化合物转化关系1.碳单质⑴同素异形体:①定义:由同种元素形成的不同单质称为同素异形体。
②种类:金刚石、石墨、C 60、C 70等。
⑵化学性质:由于碳原子最外层有4个电子,故碳在常温下性质比较稳定,很难被氧化,但在点燃或加热的条件下活动性增强,主要表现为还原性。
CaCONaOH高A ,NaOH*Na 2CO BNaHCO8口+HQ2.硅及其化合物转化关系HaCOjCa(HCO 5)3C 。
?+H ?0r CuO ,Fe2O3,ACa(OH)a-CaCO 3 △,H+.ACa(OH)②与某些氧化物反应C+CO 2=2COC+H 2O (g )邈CO+H 2(水煤气) 2C+SiO 2臭逞Si+2COf△C+2CuO2Cu+COJ (CuO 足量) C+CuO △Cu+CO f (C 足量)③与氧化性酸反应C+2H 2SO 4(浓)△COJ+2SOJ+2H 2O C+4HNO 3(浓)△COJ+4NOJ+2H 2O 2.一氧化碳⑴物理性质:无色无味气体,有毒,不溶于水。
⑵化学性质①可燃性:2CO+O 2型2CO 2(用点燃的方法除去CO ); ②还原性(与Fe 3O 4、CuO 、H 2O 的反应)Fe 3O 4+4CO △3Fe+4CO 2; CuO+CO △Cu+CO ;2H 2O +CO ^L H 2+CO 2(工业制H 2)⑶毒性:CO 有剧毒,与血液里的血红蛋白结合,使人体缺氧而死亡;主要来自汽车尾气、煤和石油燃烧及钢铁冶炼等。
3.二氧化碳⑴物理性质:无色无味,密度比空气大的气体,微溶于水,固体CO 2叫做“干冰”。
⑵分子结构:电子式:6•二c ::6:;结构式O =C =O 。

碳、硅及其化合物教学目标:1.了解碳元素、硅元素的单质的主要性质及应用。
2.了解碳元素、硅元素的重要化合物的主要性质及应用。
3.了解碳元素、硅元素的单质及其重要化合物对环境质量的影响。
教学重难点:了解碳元素、硅元素的重要化合物的主要性质及应用教学过程:考点一碳、硅及其重要化合物的性质1.碳、硅元素的存在形态(1)碳元素在自然界中既有游离态又有化合态。
碳的同素异形体有金刚石、石墨、无定形碳、C60等。
(2)硅元素在地壳中的含量占第二位,仅次于氧元素,全部以化合态存在,是一种亲氧元素,单质硅有晶体和无定形两种。
2.碳、硅单质的结构、物理性质与用途的比较(1)碳⎩⎪⎪⎪⎨⎪⎪⎪⎧与O 2反应⎩⎨⎧O 2(足量):C +O 2=====点燃CO 2O 2(不足):2C +O 2=====点燃2CO与氧化物反应⎩⎪⎨⎪⎧CuO :2CuO +C=====△2Cu +CO 2↑(冶炼金属)SiO 2:SiO 2+2C=====高温Si +2CO ↑(制取粗硅)H 2O :C +H 2O (g )=====高温CO +H 2(制取水煤气)与强氧化性酸反应⎩⎨⎧浓H 2SO 4:C +2H 2SO 4(浓)=====△CO 2↑+2SO 2↑+2H 2O 浓HNO 3:C +4HNO 3(浓)=====△CO 2↑+4NO 2↑+2H 2O(2)硅①与F 2反应:Si +2F 2===SiF 4。
②与氢氟酸反应:Si +4HF===SiF 4↑+2H 2↑。
③与NaOH 溶液反应:Si +2NaOH +H 2O===Na 2SiO 3+2H 2↑。
④与O 2反应:Si +O 2=====△SiO 2。
⑤与Cl 2反应:Si +2Cl 2=====△SiCl 4。
硅的工业制法碳、硅单质的特殊性1.一般情况下,非金属元素的单质熔、沸点低,硬度小,但晶体硅、金刚石熔、沸点高,硬度大,其中金刚石为自然界中硬度最大的物质。

高中化学碳和硅的知识点介绍在高中的化学学习中,学生过会学习到很多的知识点,下面店铺的小编将为大家带来化学中关于碳和硅的知识点的介绍,希望能够帮助到大家。
高中化学碳和硅的知识点(一)碳族元素1、组成和结构特点(1)碳族元素包括碳、硅、锗、锡、铅五种元素,位于元素周期表的IVA族。
(2)碳族元素原子最外层有4个电子,在化学反应中不易得到或失去电子,易形成共价键。
主要化合价有+2和+4价,其中碳和硅有负价。
碳族元素在化合物中多以+4价稳定,而铅在化合物中则以+2价稳定。
碳族元素中碳元素形成的单质(金刚石)硬度最大;碳元素形成的化合物种类最多;在所有非金属形成的气态氢化物中,CH4中氢元素的质量分数最大;12C是元素相对原子质量的标准原子;硅在地壳中的含量仅次于氧,其单质晶体是一种良好的半导体材料。
2、性质的递变规律随着原子序数的增大,碳族元素的原子半径依次增大,由非金属元素逐渐转变为金属元素,即金属性逐渐增强,非金属性逐渐减弱;最高价氧化物对应水化物的酸性逐渐减弱,碱性逐渐增强;气态氢化物的稳定性逐渐减弱,还原性逐渐增强。
(二)碳及其化合物1、碳单质(1)碳的同素异形体(2)碳的化学性质常温下碳的性质稳定,在加热、高温或点燃时常表现出还原性,做还原剂,温度越高,还原性越强,高温时的氧化产物一般为一氧化碳。
溶解性不同:一般情况下,所有的钾盐、钠盐和铵盐是可溶的,所有的酸式盐是可溶的,正盐的溶解度小于酸式盐的溶解度,但碳酸钠的溶解度大于碳酸氢钠的溶解度。
热稳定性不同:一般情况下,难溶的正盐和酸式盐受热易分解,可溶性碳酸盐稳定不易分解。
与酸反应的剧烈程度不同:两者都能与强酸(H+)反应产生CO2,但反应的剧烈程度不同,根据反应的剧烈程度可鉴别两者。
可溶性盐的水解程度不同:相同浓度的正盐溶液的pH值大于酸式盐溶液的pH值。
与碱反应不同:弱酸的酸式盐可与碱反应生成正盐。
与盐反应不同:碳酸钠可与氯化钙或氯化钡反应生成难溶性碳酸盐,但碳酸氢钠不反应。

态度决定高度细节决定成败无机非金属材料的主角——碳、硅一、碳族元素:①碳族元素的特征:碳族元素原子最外层电子数为4,既不容易失去电子,又不容易患到电子,易形成共价键,难形成离子键。
碳族元素形成的单质在同周期中硬度最大,熔沸点最高(如金刚石、晶体硅)。
②碳族元素的化合价:碳族元素的主要化合价有+2,+4,其中铅+2价稳定,其余元素+4价稳定。
③碳族元素的递变规律:从上到下电子层数增多,原子半径增大,原子查对最外层电子的吸引能力减弱,失电子的能力增强,从上到下由非金属递变成金属的转变超级典型。
其中碳是非金属,锡、铅是金属,硅、锗是半导体材料。
④碳族元素在自然界里的存在:自然界里碳有游离态和化合态两种;硅在地壳里无游离态,主要以含氧化合物的形式存在。
⑤几种同素异形体:碳:金刚石、石墨、C60、C70等;硅:晶体硅,无定形硅。
2、碳:在常温下碳很稳定,只在高温下能发生反映,通常表现为还原性。
①燃烧反映②与某些氧化物的反映:(CO、H2的混合气体叫水煤气);③与氧化性酸反映:3、一氧化碳:不溶于水,有毒(CO 和血红蛋白结合,使血红蛋白无法和O 2结合,而使细胞缺氧引发中毒),但由于CO 无色无味因此具有更大的危险性。
①可燃性②还原性: ;4、二氧化碳:直线型(O =C =O )非极性分子,无色能溶于水,密度大于空气,可倾倒,易液化。
固态CO 2俗称干冰,能升华,常常利用于人工降雨。
实验室制法:①酸性氧化物一—酸酐(用于查验CO 2)②氧化性: ;六、碳酸盐:①溶解性: ;②热稳定性: ;碱金属正盐>碱金属酸式盐:③彼此转化:碳酸正盐碳酸酸式盐(除杂用)二、硅1.硅元素的存在硅元素在地壳中的含量仅次于氧元素,居第二位,硅酸盐及二氧化硅组成了地壳中大部份的岩石、沙子和土壤。
2.硅的原子结构示用意: 其原子既不易失去电子也不易患到电子,所以性质不活泼,较难形成离子化合物,主要形成四价化合物。
注意:①在地壳中的元素含量排前五位是“氧硅铝铁钙”2 8 4 +14②硅元素虽然比较稳定,但因为其为亲氧元素,故自然界中只有化合态无游离态。

碳、硅元素是高中化学中非常重要的元素之一,对于理解有机化学和无机化学都具有重要的意义。
下面将围绕碳、硅元素的单质及其重要化合物展开讨论。
碳元素是自然界中广泛存在的元素之一,其存在形式有三种:石墨、金刚石和富勒烯。
其中,石墨是由碳原子层层排列而成的,具有层间力较弱的特点,因此比较容易在垂直于层面的方向上滑动,使其具有一定的润滑性;金刚石则是由碳原子通过共价键构成的晶体,因其键的强度大而具有非常高的硬度;富勒烯是由碳原子组成的球状结构,呈现出球状和管状两种形态,具有独特的光学、电学和化学性质。
在化学中,碳元素的重要化合物有三种:碳酸盐、石油和有机化合物。
碳酸盐是一类由碳酸根离子(CO32-)和金属离子或氢离子组成的化合物,常用的碳酸盐有钙、镁和铁等。
碳酸盐在地壳中广泛存在,是构成大部分岩石的重要成分。
此外,碳酸盐还是碳酸氢盐的重要原料,常用于制备一些药品和化工产品。
有机化合物是由碳原子和氢原子以及其他元素原子通过共价键连接而成的化合物。
有机化合物广泛存在于自然界中,其种类多达数百万种。
有机化合物在生活中和工业中起着至关重要的作用,包括食品、药物、燃料、塑料、合成纤维等等,几乎所有涉及到碳元素的化学物质都可以归入有机化合物范畴。
硅元素是位于周期表第14族的元素,是一种典型的无机非金属元素。
硅元素主要以二氧化硅(SiO2)的形式存在于自然界中,是地壳中最广泛的元素之一、此外,硅元素还能与氧、氟等元素形成氧化物、氟化物等化合物。
硅元素的重要化合物有氧化硅、硅酸盐、硅烷等。
氧化硅是一种重要的无机化合物,常见的有结晶硅(SiO2)和非晶硅(SiOx)两种形态。
结晶硅具有硬度高、熔点高等特点,是制备半导体材料的重要原料。
非晶硅则具有较高的抗氧化性能,可用于制备耐热玻璃和陶瓷材料等。
硅酸盐是硅元素与氧、氢、金属离子等组成的化合物,是构成硅酸盐岩石的主要成分。
硅酸盐在建筑材料、玻璃、陶瓷等行业具有广泛应用。
硅烷是硅元素与氢原子构成的化合物,是有机硅化合物的基础。

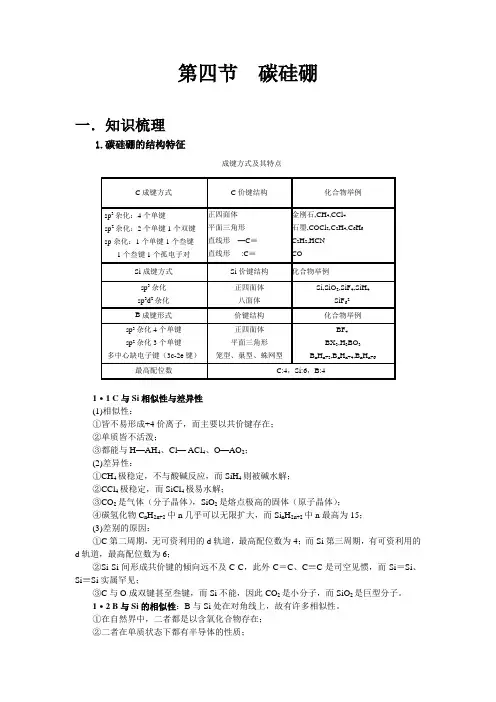
第四节碳硅硼一.知识梳理1.碳硅硼的结构特征成键方式及其特点1·1 C与Si相似性与差异性(1)相似性:①皆不易形成+4价离子,而主要以共价键存在;②单质皆不活泼;③都能与H—AH4、Cl— ACl4、O—AO2;(2)差异性:①CH4极稳定,不与酸碱反应,而SiH4则被碱水解;②CCl4极稳定,而SiCl4极易水解;③CO2是气体(分子晶体),SiO2是熔点极高的固体(原子晶体);④碳氢化物C n H2n+2中n几乎可以无限扩大,而Si n H2n+2中n最高为15;(3)差别的原因:①C第二周期,无可资利用的d轨道,最高配位数为4;而Si第三周期,有可资利用的d轨道,最高配位数为6;②Si-Si间形成共价键的倾向远不及C-C,此外C=C、C≡C是司空见惯,而Si=Si、Si≡Si实属罕见;③C与O成双键甚至叁键,而Si不能,因此CO2是小分子,而SiO2是巨型分子。
1·2 B与Si的相似性:B与Si处在对角线上,故有许多相似性。
①在自然界中,二者都是以含氧化合物存在;②二者在单质状态下都有半导体的性质;③B-O键和Si-O键都很稳定;④氢化物多种多样,都有挥发性,且可自燃(在空气中),并能水解;⑤卤化物均易水解;⑥H3BO3、H4SiO4都是弱酸,都能形成多酸盐,结构都很复杂⑦氧化物都能熔解金属氧化物,生成特殊颜色的盐2.碳硅硼的单质2·1 碳的同素异形体碳有三种同素异形体:金刚石、石墨、碳原子簇(富勒烯)。
(1)金刚石:金刚石是巨型共价分子,碳原子以sp3杂化轨道成键,形成空间网状结构,是原子晶体,属立方晶系面心立方晶体,C-C键能为345.6kJ.mol-1。
分子中无自由运动的电子,是绝缘体;(2)石墨:又称“黑铅”,碳原子以sp2杂化方式成键,形成层状结构,属于混合型晶体,层与层间以分子间力结合。
无定形碳和碳黑都是石墨微晶。
石墨软,能导电,属于导体,高熔点、高沸点,这些性质都与其独特的结构相关。

第四章 非金属及其化合物第一讲 碳、硅及无机非金属材料考点1 碳、硅单质及其重要化合物的性质一、碳、硅的单质1.存在:自然界中碳元素既有游离态,又有化合态,而硅元素因有亲氧性,所以仅有化合态。
碳单质主要有金刚石、石墨、C 60等同素异形体,硅单质主要有晶体硅和无定形硅两大类。
2.碳、硅单质的结构、物理性质与用途的比较碳、硅在参与化学反应时,一般表现还原性。
碳⎩⎪⎪⎨⎪⎪⎧与O 2反应⎩⎪⎨⎪⎧O 2(足量):C +O 2=====点燃CO 2O 2(不足):2C +O 2=====点燃2CO 与氧化物反应⎩⎪⎨⎪⎧CuO :2CuO +C=====△2Cu +CO 2↑(冶炼金属)SiO 2:SiO 2+2C=====高温Si +2CO ↑(制取粗硅)H 2O :C +H 2O (g )=====高温CO +H 2(制取水煤气)与强氧化性酸反应⎩⎪⎨⎪⎧浓H 2SO 4:C +2H 2SO 4(浓)=====△CO 2↑+2SO 2↑+2H 2O 浓HNO 3:C +4HNO 3(浓)=====△CO 2↑+4NO 2↑+2H 2O 二、碳、硅的氧化物 1.CO 的性质(1)物理性质:无色无味的气体,难溶于水。
能使人中毒的原因是其与人体中血红蛋白相结合,因缺氧而中毒。
(2)化学性质①可燃性:2CO +O 2=====点燃2CO 2。
②还原性:CO 还原Fe 2O 3的反应为Fe 2O 3+3CO=====高温2Fe +3CO 2。
2.二氧化碳与二氧化硅的比较 (1)物理性质①熔、沸点:CO 2的熔、沸点比SiO 2的熔、沸点低。
②溶解性:CO 2可溶于水,SiO 2不溶于水。
(2)化学性质CO 2+H 2OH 2CO 3CO 2:化工原料、灭火剂。
干冰用作制冷剂,人工降雨。
SiO 2:制光学仪器、石英玻璃。
水晶可制作饰品,常用来制造通讯材料光导纤维。
考点2 硅酸盐及无机非金属材料一、硅酸和硅酸钠 1.硅酸(H 2SiO 3)硅酸不溶于水,其酸性比碳酸弱,不能使紫色石蕊试液变红色。
知识清单12碳、硅及无机非金属材料知识点01碳及其化合物1.碳单质(1)存在形式:有金刚石、石墨、无定形碳、足球烯,它们互为同素异形体。
金刚石石墨足球烯①金刚石:正四面体空间网状结构。
物理性质:熔点高,硬度大,不导电。
②石墨:层状结构,每层为正六边形的平面网状结构。
物理性质:熔点高,硬度小,能导电,具有润滑性。
③足球烯(C60):笼状分子,由正五边形和正六边形排列而成。
不导电。
(2)主要化学性质——还原性可燃性O2不足:2C+O2(不足)=====点燃2COO2充足:C+O2(足量)=====点燃CO2与氧化物反应CuO:C+2CuO=====△2Cu+CO2↑(冶炼金属);SiO2:2C+SiO2=====高温Si+2CO↑(制取粗硅);H2O:C+H2O(g)=====高温H2+CO(制取水煤气)与强氧化性酸反应浓H2SO4:C+2H2SO4(浓)=====△CO2↑+2SO2↑+2H2O;浓HNO3:C+2H2SO4(浓)=====△CO2↑+2SO2↑+2H2O。
2.CO、CO2的性质对比CO CO2物理性质无色无味气体,密度比空气小,难溶于水无色无味气体,密度比空气大,可溶于水毒性有毒(易结合血红蛋白)无毒(温室效应)化学性质还原性可燃性:2CO+O2=====点燃2CO2还原氧化铁:Fe2O3+3CO=====高温2Fe+3CO2无(灭火)氧化性①与炽热炭反应:CO2+C=====高温2CO②Mg在CO2中燃烧:CO2+2Mg=====点燃2MgO+C与水反应无CO2+H2O H2CO3与碱反应无Ca(OH)2+CO2===CaCO3↓+H2O相互转化CO2C,△①O2,②CuOCO用途燃料、冶炼金属灭火、制汽水、植物肥料、化工原料等3.碳酸的正盐和酸式盐的比较正盐(CO2-3)酸式盐(HCO-3)溶解性只有钾、钠、铵盐可溶一般都可溶溶解度一般而言,在相同温度下,难溶性正盐溶解度小于其酸式盐溶解度,如溶解度Ca(HCO3)2>CaCO3;可溶性正盐溶解度大于其酸式盐溶解度,如溶解度Na2CO3>NaHCO3。
2019年高考化学碳硅物理性质及用途总结
碳和硅属于同一主族,化学性质相似,而且在自然界中,硅的含量远大于碳。
以下是碳硅物理性质及用途总结,请考生及时进行学习。
1.碳、硅单质的存在形态、物理性质及用途
(1)自然界中碳元素既有游离态,又有化合态,而硅元素因有亲氧性,所以仅有化合态。
碳单质主要有金刚石、石墨、C60等同素异形体,硅单质主要有晶体硅和无定形硅两大类。
(2)单质的结构、物理性质与用途比较
?碳硅结构金刚石:空间网状结构
石墨:层状结构晶体硅:与金刚石类似的空间网状结构物理性质金刚石熔点高、硬度大
石墨熔点高、质软,有滑腻感晶体硅为灰黑色固体,有金属光泽、硬度大、熔点高用途金刚石用作切割刀具,石墨用作电极、铅笔芯[来源:高[考试﹤题库GkStK] 晶体硅用作半导体材料、硅芯片和硅太阳能电池 2.碳、硅单质的化学性质
碳、硅在参与化学反应时,一般表现还原性。
碳硅物理性质及用途总结的全部内容就是这些,查字典化学网希望考生可以取得满意的成绩。
2019年高考第一轮复习备考专题已经新鲜出炉了,专题包含高考各科第一轮复习要点、复习方法、复习计划、复习试题,
大家来一起看看吧~。
碳、硅及其化合物教学目标:1.了解碳元素、硅元素的单质的主要性质及应用。
2.了解碳元素、硅元素的重要化合物的主要性质及应用。
3.了解碳元素、硅元素的单质及其重要化合物对环境质量的影响。
教学重难点:了解碳元素、硅元素的重要化合物的主要性质及应用教学过程:考点一碳、硅及其重要化合物的性质1.碳、硅元素的存在形态(1)碳元素在自然界中既有游离态又有化合态。
碳的同素异形体有金刚石、石墨、无定形碳、C60等。
(2)硅元素在地壳中的含量占第二位,仅次于氧元素,全部以化合态存在,是一种亲氧元素,单质硅有晶体和无定形两种。
2.碳、硅单质的结构、物理性质与用途的比较碳硅结构金刚石:空间网状结构石墨:层状结构晶体硅:与金刚石类似的空间网状结构物理性质金刚石熔点高、硬度大石墨熔点高、质软,有滑腻感晶体硅为灰黑色固体,有金属光泽、硬度大、熔点高用途金刚石用于制造切割刀具,石墨用作电极、铅笔芯晶体硅用作半导体材料,制造硅芯片和硅太阳能电池(1)碳⎩⎪⎪⎪⎨⎪⎪⎪⎧与O 2反应⎩⎨⎧O 2足量:C +O 2=====点燃CO 2O2不足:2C +O 2=====点燃2CO与氧化物反应⎩⎪⎨⎪⎧CuO :2CuO +C=====△2Cu +CO 2↑冶炼金属SiO 2:SiO 2+2C=====高温Si +2CO↑制取粗硅H 2O :C +H 2O g =====高温CO +H 2制取水煤气与强氧化性酸反应⎩⎨⎧浓H 2SO 4:C +2H 2SO 4浓=====△CO 2↑+2SO 2↑+2H 2O 浓HNO 3:C +4HNO 3浓=====△CO 2↑+4NO 2↑+2H 2O(2)硅①与F 2反应:Si +2F 2===SiF 4。
②与氢氟酸反应:Si +4HF===SiF 4↑+2H 2↑。
③与NaOH 溶液反应:Si +2NaOH +H 2O===Na 2SiO 3+2H 2↑。
④与O 2反应:Si +O 2=====△SiO 2。
⑤与Cl2反应:Si+2Cl2=====△SiCl4。
硅的工业制法碳、硅单质的特殊性1.一般情况下,非金属元素的单质熔、沸点低,硬度小,但晶体硅、金刚石熔、沸点高,硬度大,其中金刚石为自然界中硬度最大的物质。
2.一般情况下,非金属单质为绝缘体,但硅为半导体,石墨为电的良导体。
3.Si的还原性大于C,但C在高温下能还原出Si:SiO2+2C=====高温Si+2CO↑。
4.非金属单质与碱反应一般既作氧化剂又作还原剂,且无氢气放出,但硅与强碱溶液反应只作还原剂,且放出氢气:Si+2NaOH+H2O===Na2SiO3+2H2↑。
5.非金属单质一般不与非氧化性酸反应,但硅能与HF反应:Si+4HF===SiF4↑+2H2↑。
6.一般情况下,金属(Na、K)能置换出水中的氢,但C在高温下也能置换出H2O中的氢:C+H2O(g)=====高温H 2+CO。
CO2+H2O H2CO3碳、硅单质的特殊性1.一般情况下,非金属元素的单质熔、沸点低,硬度小,但晶体硅、金刚石熔、沸点高,硬度大,其中金刚石为自然界中硬度最大的物质。
2.一般情况下,非金属单质为绝缘体,但硅为半导体,石墨为电的良导体。
3.Si的还原性大于C,但C在高温下能还原出Si:SiO2+2C=====高温Si+2CO↑。
4.非金属单质与碱反应一般既作氧化剂又作还原剂,且无氢气放出,但硅与强碱溶液反应只作还原剂,且放出氢气:Si+2NaOH+H2O===Na2SiO3+2H2↑。
5.非金属单质一般不与非氧化性酸反应,但硅能与HF反应:Si+4HF===SiF4↑+2H2↑。
6.一般情况下,金属(Na、K)能置换出水中的氢,但C在高温下也能置换出H2O中的氢:C+H2O(g)=====高温H2+CO。
1.判断正误,正确的划“√”,错误的划“×”(1)用活性炭去除冰箱中的异味,没有发生化学反应( )(2)大量燃烧化石燃料是造成雾霾的一种重要原因( )(3)硅胶可作袋装食品的干燥剂( ) (4)金刚石、白磷都属于单质( )(5)由于晶体硅熔点高硬度大,则可用于制作半导体材料( ) (6)甲――→丁乙丁甲丙,若甲为焦炭,则丁可能是O 2( )(7)SiO 2可与HF 反应,因而氢氟酸不能保存在玻璃瓶中( ) (8)高温下用焦炭还原SiO 2制取粗硅( ) (9)单质硅是将太阳能转变为电能的常用材料( ) (10)合成纤维和光导纤维都是新型无机非金属材料( )(11)SiO 2有导电性,所以SiO 2可用于制备光导纤维( ) (12)(12)硅酸钠溶液应保存在带玻璃塞的试剂瓶中( )答案 (1)√ (2)√ (3)√ (4)√ (5)× (6)√ (7)√ (8)√ (9)√ (10)× (11)× (12)×题组1 碳、硅单质的性质1.下列关于碳和硅的叙述中,正确的是( )。
A .其氧化物都能与NaOH 溶液反应B .其单质在加热时都能跟O 2反应C .其氧化物都能溶于水生成相应的酸D .碳和硅两种元素共有两种单质 2.下列物质间的转化不能通过一步反应完成的是( )。
A .SiO 2―→Si B .CO 2―→C C .SiO 2―→H 2SiO 3 D .Si ―→Na 2SiO 3题组2 碳、硅氧化物的性质 3.下列说法正确的是( )。
A .反应:SiO 2+Na 2CO 3=====高温Na 2SiO 3+CO 2↑,说明H 2SiO 3的酸性大于H 2CO 3的酸性 B .可在试管内完成焦炭和石英砂(SiO 2)制取硅的反应 C .二氧化硅是生产光导纤维、玻璃的基本原料 D .CO 2、CH 4、N 2是温室气体4.向含有0.2 mol NaOH 和0.1 mol Ba(OH)2的溶液中持续稳定地通入CO 2气体,当通入气体为8.96 L(0 ℃,1.01×105 Pa)时立即停止,则这一过程中,溶液中离子的物质的量与通入CO 2气体的体积关系图像正确的是(气体的溶解和离子的水解忽略不计)( )。
B C C C考点二硅酸盐及无机非金属材料1.硅酸硅酸难溶于水,其酸性比碳酸弱,硅酸不能(填“能”或“不能”)使紫色石蕊试液变红色。
(1)硅酸不稳定,受热易分解,其化学方程式为:H2SiO3=====△SiO2+H2O。
(2)硅酸能与碱溶液反应,如与NaOH溶液反应的化学方程式为H2SiO3+2NaOH===Na2SiO3+2H2O。
(3)硅酸在水中易聚合形成胶体,硅胶有很强的吸水能力,常用作干燥剂。
2.硅酸盐(1)概念:由硅、氧和金属元素组成的化合物的总称,是构成地壳岩石的主要成分。
(2)表示方法:硅酸盐矿物的成分复杂,常用氧化物的形式表示它们的组成,如硅酸钠(Na2SiO3)写成Na2O·SiO2,钾云母(KH2Al3Si3O12)写成K2O·3Al2O3·6SiO2·2H2O。
(3)硅酸钠(Na2SiO3)①白色、可溶于水的粉末状固体,其水溶液俗称水玻璃,有黏性,水溶液显碱性。
②它能与较强的酸反应,如与盐酸反应的化学方程式为:Na2SiO3+2HCl===2NaCl+H2SiO3↓;与CO2水溶液反应的化学方程式为:Na2SiO3+CO2+H2O===H2SiO3↓+Na2CO3。
③用途:黏合剂(矿物胶),耐火阻燃材料。
3.无机非金属材料(1)传统无机非金属材料①三种硅酸盐工业生产的比较:②主要用途:陶瓷、玻璃、水泥是主要建筑材料,也广泛应用于生活中。
(2)新型无机非金属材料①高温结构陶瓷:如氮化硅陶瓷具有较高的硬度和耐磨性、较强的抗化学侵蚀性和电绝缘性等。
②生物陶瓷:对机体无排异反应,不会引起代谢作用异常。
③压电陶瓷:具有压电效应。
2.判断正误,正确的划“√”,错误的划“×”。
(1)玻璃是一种晶体,有较高的熔点。
( )(2)水玻璃是一种特殊的玻璃,泡花碱属于碱。
( )(3)向一定浓度的Na2SiO3溶液中通入适量CO2出现白色沉淀,证明H2CO3的酸性比H2SiO3的酸性强。
( )(4)传统无机非金属材料是指玻璃、水泥、陶瓷等硅酸盐材料( )(5)新型无机非金属材料克服了传统无机非金属材料的许多缺点( )(6)高温结构材料具有耐高温、耐酸碱腐蚀、硬度大、耐磨损、密度小等优点( )(7)水泥、玻璃、青花瓷、水晶、玛瑙都属于硅酸盐工业产品( )(8)2MgO·SiO2中的酸根阴离子为SiO2-4( )答案(1)×(2)×(3)√(4)√(5)√(6)√(7)×(8)×[示向题组]1.(2014·济南联考)下列有关硅及硅酸盐材料的说法正确的是( )。
A.硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在磨口玻璃塞试剂瓶中B.反应①Na2SiO3+H2O+CO2===Na2CO3+H2SiO3↓,反应②Na2CO3+SiO2=====高温Na2SiO3+CO2↑,两反应是相互矛盾的,不可能都能发生C.普通玻璃、石英玻璃,水泥等均属于硅酸盐材料D.祖母绿的主要成分为Be3Al2Si6O18,用氧化物形式表示为3BeO·Al2O3·6SiO22.(2014·郑州一模)材料与化学密切相关,表中对应关系错误的是( )。
中有广泛应用。
回答下列问题:(1)1810年瑞典化学家贝采利乌斯在加热石英砂、木炭和铁时,得到一种“金属”。
这种“金属”可能是________。
(2)陶瓷、水泥和玻璃是常用的硅酸盐材料。
其中,生产普通玻璃的主要原料有________。
(3)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。
工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:发生的主要反应①用方程式为____________________;碳化硅又称________,其晶体结构与________相似。
②在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如下表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和________________________________________________________________________。
3(4)氯碱工业可为上述工艺生产提供部分原料,这些原料是____________。
5.(2014·济南四校期中联考)单晶硅是信息产业中重要的基础材料。
通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500 ℃),四氯化硅经提纯后用氢气还原可得高纯硅。