高中化学-碳硅知识
- 格式:docx
- 大小:299.41 KB
- 文档页数:16


高考总复习《碳硅》【考点梳理】考点一.碳及其化合物1.碳单质⑴同素异形体:①定义:由同种元素形成的不同单质称为同素异形体。
②种类:金刚石、石墨、C60、C70等。
⑵化学性质:由于碳原子最外层有4个电子,故碳在常温下性质比较稳定,很难被氧化,但在点燃或加热的条件下活动性增强,主要表现为还原性。
①与单质反应2C+O22CO C+O2CO2②与某些氧化物反应C+CO22COC+H2O(g) CO+H2(水煤气)2C+SiO2Si+2CO↑C+2CuO △2Cu+CO2↑(CuO足量)C+CuO △Cu +CO↑(C足量)③与氧化性酸反应C+2H2SO4(浓)△CO2↑+2SO2↑+2H2OC+4HNO3(浓)△CO2↑+4NO2↑+2H2O2.一氧化碳⑴物理性质:无色无味气体,有毒,不溶于水。
⑵化学性质①可燃性:2CO+O22CO2(用点燃的方法除去CO);②还原性(与Fe3O4、CuO、H2O的反应)Fe3O4+4CO △2;CuO+CO △Cu+CO2;H2O+CO H2+CO2(工业制H2)⑶毒性:CO有剧毒,与血液里的血红蛋白结合,使人体缺氧而死亡;主要来自汽车尾气、煤和石油燃烧及钢铁冶炼等。
3.二氧化碳⑴物理性质:无色无味,密度比空气大的气体,微溶于水,固体CO2叫做“干冰”。
⑵分子结构:电子式;结构式O=C=O。
⑶化学性质:①弱氧化性CO2+C2CO;CO2+2Mg2MgO+C②酸性氧化物的通性CO2+ H2O=H2CO3CO2+Ca(OH)2=CaCO3↓+H2O;CO2+CaCO3+H2O=Ca(HCO3)2CO2+CaO=CaCO3③与盐的反应(相对较强的酸制取较弱的酸):(A)往漂白粉溶液中不断通入CO2气体的反应为:Ca(ClO)2+CO2+H2O==CaCO3↓+2HClO,CaCO3+CO2+H2O==Ca(HCO3)2(B)在NaAlO2溶液中不断通入CO2气体至过量时,反应为:2AlO2-+CO2 (少量)+3H2O==2Al(OH)3↓+CO32―AlO2―+CO2 (过量)+2H2O==Al(OH)3↓+HCO3-(C)往Na2SiO3溶液中不断通入CO2气体至过量时,反应为:SiO32―+CO2+H2O==H2SiO3 (胶体)+CO32―,SiO32―+2CO2+2H2O==H2SiO3 (胶体)+2HCO3―(D)往饱和Na2CO3溶液中通入CO2气体,反应为:2Na++CO32―+CO2+H2O==2NaHCO3↓(E)C6H5ONa+CO2+H2O→C6H5OH↓+NaHCO3⑷制法:①工业制法:煅烧石灰石CaCO3CaO+CO2↑②实验室制法:石灰石和稀盐酸反应原理:CaCO3+2HCl=CaCl2+CO2↑+H2O装置:“固+液→气”或启普发生器及其简易装置知识拓展——除杂:4.碳酸盐(1)溶解性正盐中只有碱金属的碳酸盐和铵盐溶于水,所有酸式盐均溶于水。


碳、硅及其化合物教学目标:1.了解碳元素、硅元素的单质的主要性质及应用。
2.了解碳元素、硅元素的重要化合物的主要性质及应用。
3.了解碳元素、硅元素的单质及其重要化合物对环境质量的影响。
教学重难点:了解碳元素、硅元素的重要化合物的主要性质及应用教学过程:考点一碳、硅及其重要化合物的性质1.碳、硅元素的存在形态(1)碳元素在自然界中既有游离态又有化合态。
碳的同素异形体有金刚石、石墨、无定形碳、C60等。
(2)硅元素在地壳中的含量占第二位,仅次于氧元素,全部以化合态存在,是一种亲氧元素,单质硅有晶体和无定形两种。
2.碳、硅单质的结构、物理性质与用途的比较(1)碳⎩⎪⎪⎪⎨⎪⎪⎪⎧与O 2反应⎩⎨⎧O 2(足量):C +O 2=====点燃CO 2O 2(不足):2C +O 2=====点燃2CO与氧化物反应⎩⎪⎨⎪⎧CuO :2CuO +C=====△2Cu +CO 2↑(冶炼金属)SiO 2:SiO 2+2C=====高温Si +2CO ↑(制取粗硅)H 2O :C +H 2O (g )=====高温CO +H 2(制取水煤气)与强氧化性酸反应⎩⎨⎧浓H 2SO 4:C +2H 2SO 4(浓)=====△CO 2↑+2SO 2↑+2H 2O 浓HNO 3:C +4HNO 3(浓)=====△CO 2↑+4NO 2↑+2H 2O(2)硅①与F 2反应:Si +2F 2===SiF 4。
②与氢氟酸反应:Si +4HF===SiF 4↑+2H 2↑。
③与NaOH 溶液反应:Si +2NaOH +H 2O===Na 2SiO 3+2H 2↑。
④与O 2反应:Si +O 2=====△SiO 2。
⑤与Cl 2反应:Si +2Cl 2=====△SiCl 4。
硅的工业制法碳、硅单质的特殊性1.一般情况下,非金属元素的单质熔、沸点低,硬度小,但晶体硅、金刚石熔、沸点高,硬度大,其中金刚石为自然界中硬度最大的物质。

高中化学碳和硅的知识点介绍在高中的化学学习中,学生过会学习到很多的知识点,下面店铺的小编将为大家带来化学中关于碳和硅的知识点的介绍,希望能够帮助到大家。
高中化学碳和硅的知识点(一)碳族元素1、组成和结构特点(1)碳族元素包括碳、硅、锗、锡、铅五种元素,位于元素周期表的IVA族。
(2)碳族元素原子最外层有4个电子,在化学反应中不易得到或失去电子,易形成共价键。
主要化合价有+2和+4价,其中碳和硅有负价。
碳族元素在化合物中多以+4价稳定,而铅在化合物中则以+2价稳定。
碳族元素中碳元素形成的单质(金刚石)硬度最大;碳元素形成的化合物种类最多;在所有非金属形成的气态氢化物中,CH4中氢元素的质量分数最大;12C是元素相对原子质量的标准原子;硅在地壳中的含量仅次于氧,其单质晶体是一种良好的半导体材料。
2、性质的递变规律随着原子序数的增大,碳族元素的原子半径依次增大,由非金属元素逐渐转变为金属元素,即金属性逐渐增强,非金属性逐渐减弱;最高价氧化物对应水化物的酸性逐渐减弱,碱性逐渐增强;气态氢化物的稳定性逐渐减弱,还原性逐渐增强。
(二)碳及其化合物1、碳单质(1)碳的同素异形体(2)碳的化学性质常温下碳的性质稳定,在加热、高温或点燃时常表现出还原性,做还原剂,温度越高,还原性越强,高温时的氧化产物一般为一氧化碳。
溶解性不同:一般情况下,所有的钾盐、钠盐和铵盐是可溶的,所有的酸式盐是可溶的,正盐的溶解度小于酸式盐的溶解度,但碳酸钠的溶解度大于碳酸氢钠的溶解度。
热稳定性不同:一般情况下,难溶的正盐和酸式盐受热易分解,可溶性碳酸盐稳定不易分解。
与酸反应的剧烈程度不同:两者都能与强酸(H+)反应产生CO2,但反应的剧烈程度不同,根据反应的剧烈程度可鉴别两者。
可溶性盐的水解程度不同:相同浓度的正盐溶液的pH值大于酸式盐溶液的pH值。
与碱反应不同:弱酸的酸式盐可与碱反应生成正盐。
与盐反应不同:碳酸钠可与氯化钙或氯化钡反应生成难溶性碳酸盐,但碳酸氢钠不反应。


非金属及其化合物知识梳理----碳和硅及其化合物间的相互转化关系第一节无机金属材料的主角——硅基础巩固一、硅单质1.元素的存在形态、单质的物理性质及其用途(1)结构:与金刚石相似,为_________结构。
(2)物理性质:熔点和沸点_______,导电性介于_______和_______之间。
(3)用途:制造________(信息材料)、制造________等。
2.化学性质:在常温下,除与F2、HF和强碱溶液反应以外,硅不易和其他物质反应。
有关化学反应方程式为:________________________;___________________________;________________________________。
3.制取:________________________;________________________;_____________________________________。
【思考交流1】硅的性质有哪些特殊性?提示:(1)硅的还原性比碳强,而碳在高温下却能从二氧化硅中还原出硅。
SiO2+2C==Si+2CO↑(2)非金属单质一般不与弱氧化性酸反应,而硅不但能与氢氟酸反应,而且还有H2生成(与酸反应产生氢气是活泼金属的性质)。
Si+4HF==SiF4↑+2H2↑(3)非金属单质与强碱溶液反应一般不生成氢气,而硅却不然。
Si+2NaOH+H2O====Na2SiO3+2H2↑二、二氧化硅1.存在:广泛存在于自然界中(_______、_______、_______的主要成分均是二氧化硅)。
2.物理性质:纯SiO2是___色透明的晶体,硬度______,熔沸点_______。
3.化学性质:(1)酸性氧化物:与NaOH反应____________________________。
(2)和氢氟酸反应:____________________________。
(3)在高温下,可与Na2CO3、CaCO3等碳酸盐反应。
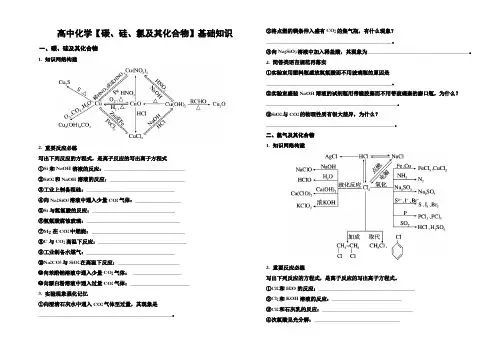
高中化学【碳、硅、氯及其化合物】基础知识一、碳、硅及其化合物1. 知识网络构建2. 重要反应必练写出下列反应的方程式,是离子反应的写出离子方程式①Si和NaOH溶液的反应:______________________________②SiO2和NaOH溶液的反应:____________________________③工业上制备粗硅:_________________________________④向Na2SiO3溶液中通入少量CO2气体:_________________⑤Si与氢氟酸的反应:_______________________________⑥氢氟酸腐蚀玻璃:___________________________________⑦Mg在CO2中燃烧:___________________________________⑧C与CO2高温下反应:_________________________________⑨工业制备水煤气:_________________________________⑩Na2CO3与SiO2在高温下反应:_______________________⑪向苯酚钠溶液中通入少量CO2气体:__________________⑫向漂白粉溶液中通入过量CO2气体:______________________3. 实验现象强化记忆①向澄清石灰水中通入CO2气体至过量,其现象是__________________________________________________。
②将点燃的镁条伸入盛有CO2的集气瓶,有什么现象?_______________________________________________。
③向Na2SiO3溶液中加入稀盐酸,其现象为______________________________________。
4. 简答类语言规范再落实①实验室用塑料瓶盛放氢氟酸而不用玻璃瓶的原因是_______________________________________________。



碳、硅及无机非金属材料考点一 碳、硅单质及其重要化合物[知识梳理]1.碳、硅单质的结构、物理性质及用途碳硅原子结构 示意图元素在自然界中的存在形式 既有游离态又有化合态 只有__化合__态结构金刚石:空间网状结构, 石墨:层状结构 晶体硅:与金刚石类似的__空间网状__结构物理性质金刚石熔点高、硬度大,石墨熔点高、质__软__,有滑腻感,能导电晶体硅为灰黑色固体,有金属光泽、硬度大、熔点__高__用途金刚石用作切割刀具,__石墨__用作电极、铅笔芯晶体硅用作__半导体__材料、硅芯片和硅太阳能电池碳、硅在参与化学反应时,一般表现还原性。
3.硅的工业制法及提纯石英砂――→①焦炭高温粗硅――→②氯气加热SiCl 4――→③氢气加热高纯硅反应①: SiO 2+2C=====高温Si +2CO ↑ 反应②: Si +Cl 2△,SiCl 4 反应③: SiCl 4+2H 2△,Si +4HCl 4.二氧化碳和二氧化硅二氧化碳二氧化硅类别 均为__酸性__氧化物结构 特点 由__二氧化碳分子__构成,属于__分子__晶体由氧原子与硅原子构成__立体网状__结构,属于__原子__晶体 主要物 理性质熔、沸点__低__,常温下为气体,能溶于水硬度__大__,熔、沸点__高__,常温下为固体,不溶于水化 学 性 质①与水 反应CO 2+H 2OH 2CO 3不反应②与酸 反应 不反应只与氢氟酸反应: SiO 2+4HF=== SiF 4↑+2H 2O__③与碱 反应 CO 2少量:CO 2+2OH -===CO 2-3+H 2OCO 2过量: CO 2+OH -===HCO -3 SiO 2+2NaOH===Na 2SiO 3+H 2O (盛碱性溶液的试剂瓶用__橡胶__塞)用途 制饮料、制碳酸盐光导纤维、光学仪器、电子部件归纳总结硅及其化合物的特殊性质[对点检测]1.判断正误,正确的划“√”,错误的划“×”。
第四章 非金属及其化合物第一讲 碳、硅及无机非金属材料考点1 碳、硅单质及其重要化合物的性质一、碳、硅的单质1.存在:自然界中碳元素既有游离态,又有化合态,而硅元素因有亲氧性,所以仅有化合态。
碳单质主要有金刚石、石墨、C 60等同素异形体,硅单质主要有晶体硅和无定形硅两大类。
2.碳、硅单质的结构、物理性质与用途的比较碳、硅在参与化学反应时,一般表现还原性。
碳⎩⎪⎪⎨⎪⎪⎧与O 2反应⎩⎪⎨⎪⎧O 2(足量):C +O 2=====点燃CO 2O 2(不足):2C +O 2=====点燃2CO 与氧化物反应⎩⎪⎨⎪⎧CuO :2CuO +C=====△2Cu +CO 2↑(冶炼金属)SiO 2:SiO 2+2C=====高温Si +2CO ↑(制取粗硅)H 2O :C +H 2O (g )=====高温CO +H 2(制取水煤气)与强氧化性酸反应⎩⎪⎨⎪⎧浓H 2SO 4:C +2H 2SO 4(浓)=====△CO 2↑+2SO 2↑+2H 2O 浓HNO 3:C +4HNO 3(浓)=====△CO 2↑+4NO 2↑+2H 2O 二、碳、硅的氧化物 1.CO 的性质(1)物理性质:无色无味的气体,难溶于水。
能使人中毒的原因是其与人体中血红蛋白相结合,因缺氧而中毒。
(2)化学性质①可燃性:2CO +O 2=====点燃2CO 2。
②还原性:CO 还原Fe 2O 3的反应为Fe 2O 3+3CO=====高温2Fe +3CO 2。
2.二氧化碳与二氧化硅的比较 (1)物理性质①熔、沸点:CO 2的熔、沸点比SiO 2的熔、沸点低。
②溶解性:CO 2可溶于水,SiO 2不溶于水。
(2)化学性质CO 2+H 2OH 2CO 3CO 2:化工原料、灭火剂。
干冰用作制冷剂,人工降雨。
SiO 2:制光学仪器、石英玻璃。
水晶可制作饰品,常用来制造通讯材料光导纤维。
考点2 硅酸盐及无机非金属材料一、硅酸和硅酸钠 1.硅酸(H 2SiO 3)硅酸不溶于水,其酸性比碳酸弱,不能使紫色石蕊试液变红色。
知识清单12碳、硅及无机非金属材料知识点01碳及其化合物1.碳单质(1)存在形式:有金刚石、石墨、无定形碳、足球烯,它们互为同素异形体。
金刚石石墨足球烯①金刚石:正四面体空间网状结构。
物理性质:熔点高,硬度大,不导电。
②石墨:层状结构,每层为正六边形的平面网状结构。
物理性质:熔点高,硬度小,能导电,具有润滑性。
③足球烯(C60):笼状分子,由正五边形和正六边形排列而成。
不导电。
(2)主要化学性质——还原性可燃性O2不足:2C+O2(不足)=====点燃2COO2充足:C+O2(足量)=====点燃CO2与氧化物反应CuO:C+2CuO=====△2Cu+CO2↑(冶炼金属);SiO2:2C+SiO2=====高温Si+2CO↑(制取粗硅);H2O:C+H2O(g)=====高温H2+CO(制取水煤气)与强氧化性酸反应浓H2SO4:C+2H2SO4(浓)=====△CO2↑+2SO2↑+2H2O;浓HNO3:C+2H2SO4(浓)=====△CO2↑+2SO2↑+2H2O。
2.CO、CO2的性质对比CO CO2物理性质无色无味气体,密度比空气小,难溶于水无色无味气体,密度比空气大,可溶于水毒性有毒(易结合血红蛋白)无毒(温室效应)化学性质还原性可燃性:2CO+O2=====点燃2CO2还原氧化铁:Fe2O3+3CO=====高温2Fe+3CO2无(灭火)氧化性①与炽热炭反应:CO2+C=====高温2CO②Mg在CO2中燃烧:CO2+2Mg=====点燃2MgO+C与水反应无CO2+H2O H2CO3与碱反应无Ca(OH)2+CO2===CaCO3↓+H2O相互转化CO2C,△①O2,②CuOCO用途燃料、冶炼金属灭火、制汽水、植物肥料、化工原料等3.碳酸的正盐和酸式盐的比较正盐(CO2-3)酸式盐(HCO-3)溶解性只有钾、钠、铵盐可溶一般都可溶溶解度一般而言,在相同温度下,难溶性正盐溶解度小于其酸式盐溶解度,如溶解度Ca(HCO3)2>CaCO3;可溶性正盐溶解度大于其酸式盐溶解度,如溶解度Na2CO3>NaHCO3。
2019年高考化学碳硅物理性质及用途总结
碳和硅属于同一主族,化学性质相似,而且在自然界中,硅的含量远大于碳。
以下是碳硅物理性质及用途总结,请考生及时进行学习。
1.碳、硅单质的存在形态、物理性质及用途
(1)自然界中碳元素既有游离态,又有化合态,而硅元素因有亲氧性,所以仅有化合态。
碳单质主要有金刚石、石墨、C60等同素异形体,硅单质主要有晶体硅和无定形硅两大类。
(2)单质的结构、物理性质与用途比较
?碳硅结构金刚石:空间网状结构
石墨:层状结构晶体硅:与金刚石类似的空间网状结构物理性质金刚石熔点高、硬度大
石墨熔点高、质软,有滑腻感晶体硅为灰黑色固体,有金属光泽、硬度大、熔点高用途金刚石用作切割刀具,石墨用作电极、铅笔芯[来源:高[考试﹤题库GkStK] 晶体硅用作半导体材料、硅芯片和硅太阳能电池 2.碳、硅单质的化学性质
碳、硅在参与化学反应时,一般表现还原性。
碳硅物理性质及用途总结的全部内容就是这些,查字典化学网希望考生可以取得满意的成绩。
2019年高考第一轮复习备考专题已经新鲜出炉了,专题包含高考各科第一轮复习要点、复习方法、复习计划、复习试题,
大家来一起看看吧~。
碳、硅及其化合物教学目标:1.了解碳元素、硅元素的单质的主要性质及应用。
2.了解碳元素、硅元素的重要化合物的主要性质及应用。
3.了解碳元素、硅元素的单质及其重要化合物对环境质量的影响。
教学重难点:了解碳元素、硅元素的重要化合物的主要性质及应用教学过程:考点一碳、硅及其重要化合物的性质1.碳、硅元素的存在形态(1)碳元素在自然界中既有游离态又有化合态。
碳的同素异形体有金刚石、石墨、无定形碳、C60等。
(2)硅元素在地壳中的含量占第二位,仅次于氧元素,全部以化合态存在,是一种亲氧元素,单质硅有晶体和无定形两种。
2.碳、硅单质的结构、物理性质与用途的比较碳硅金刚石:空间网状结构结构晶体硅:与金刚石类似的空间网状结构石墨:层状结构物理金刚石熔点高、硬度大石墨熔点晶体硅为灰黑色固体,有金属光泽、硬度大、熔性质高、质软,有滑腻感点高金刚石用于制造切割刀具,石墨用晶体硅用作半导体材料,制造硅芯片和硅太阳能用途作电极、铅笔芯电池3.碳、硅单质的化学性质与O2反应点燃O2足量:C+O2=====CO2点燃O2不足:2C+O2=====2CO△CuO:2CuO+C=====2Cu+CO2↑冶炼金属(1)碳与氧化物反应高温SiO2:SiO2+2C=====Si+2CO↑制取粗硅高温H2O:C+H2O g=====CO+H2制取水煤气与强氧化△浓H2SO4:C+2H2SO4浓=====CO2↑+2SO2↑+2H2O 性酸反应△浓HNO3:C+4HNO3浓=====CO2↑+4NO2↑+2H2O(2)硅①与F2反应:Si+2F2===SiF4。
②与氢氟酸反应:Si+4HF===SiF4↑+2H2↑。
③与NaOH溶液反应:Si+2NaOH+H2O===Na2SiO3+2H2↑。
△④与O2反应:Si+O2=====SiO2。
△⑤与Cl2反应:Si+2Cl2=====SiCl4。
硅的工业制法碳、硅单质的特殊性1.一般情况下,非金属元素的单质熔、沸点低,硬度小,但晶体硅、金刚石熔、沸点高,硬度大,其中金刚石为自然界中硬度最大的物质。
2.一般情况下,非金属单质为绝缘体,但硅为半导体,石墨为电的良导体。
高温3.Si的还原性大于C,但C在高温下能还原出Si:SiO2+2C=====Si+2CO↑。
4.非金属单质与碱反应一般既作氧化剂又作还原剂,且无氢气放出,但硅与强碱溶液反应只作还原剂,且放出氢气:Si+2NaOH+H2O===Na2SiO3+2H2↑。
5.非金属单质一般不与非氧化性酸反应,但硅能与 HF 反应:Si +4HF===SiF 4↑+2H 2↑。
6.一般情况下,金属 (Na 、K)能置换出水中的氢,但 C 在高温下也能置换出 H 2O 中的氢:C +高温H 2O(g)=====H 2+CO 。
物质 二氧化硅 二氧化碳 空间立体网状结构,结构 存在单个分子不存在单个分子 硬度大,熔、沸点高, 主要物理常温下为固体,不溶熔、沸点低,常温下为气体,微溶于水性质于水①与水不反应CO 2+H 2OH 2CO 3 反应只与氢氟酸反应:②与酸 反应SiO 2+4HF===SiF 4↑ +2H 2O不反应SiO 2+化2NaOH===Na 2SiO 3+CO 2 少量:CO 2+2NaOH===Na 2CO 3+H 2O 、 ③与碱 学H 2O(盛碱液的试剂瓶CO 2 过量:CO 2+NaOH===NaHCO 3 反应性用橡胶塞 )质如与 Na 2CO 3 反应:④与盐 反应高温SiO Na CO ===== +223量SiO 2NaHCO )===H ↓+2 33Na SiO CO2 32如与 Na 2SiO 3 反应:Na 2SiO 3+H 2O +CO 2(不 足)===H 2SiO 3↓+Na 2CO 3 或 Na 2SiO 3+2H 2O +2CO 2(足+↑⑤与碱如与CaO 反应:SiO2性氧化物反应高温+CaO=====CaSiO3如与Na2O 反应:Na2O+CO2===Na2CO3光导纤维、光学仪器、用途制饮料、制碳酸盐电子部件碳、硅单质的特殊性1.一般情况下,非金属元素的单质熔、沸点低,硬度小,但晶体硅、金刚石熔、沸点高,硬度大,其中金刚石为自然界中硬度最大的物质。
2.一般情况下,非金属单质为绝缘体,但硅为半导体,石墨为电的良导体。
高温3.Si 的还原性大于C,但C 在高温下能还原出Si:SiO2+2C=====Si+2CO↑。
4.非金属单质与碱反应一般既作氧化剂又作还原剂,且无氢气放出,但硅与强碱溶液反应只作还原剂,且放出氢气:Si+2NaOH+H2O===Na2SiO3+2H2↑。
5.非金属单质一般不与非氧化性酸反应,但硅能与HF 反应:Si+4HF===SiF4↑+2H2↑。
6.一般情况下,金属(Na、K)能置换出水中的氢,但 C 在高温下也能置换出H2O 中的氢:C+高温H2O(g)=====H2+CO。
1.判断正误,正确的划“√”,错误的划“×”(1)用活性炭去除冰箱中的异味,没有发生化学反应( )(2)大量燃烧化石燃料是造成雾霾的一种重要原因( )(3)硅胶可作袋装食品的干燥剂( )(4)金刚石、白磷都属于单质( )(5)由于晶体硅熔点高硬度大,则可用于制作半导体材料( )丁(6)甲――→乙丁甲丙,若甲为焦炭,则丁可能是O2( )(7)SiO2 可与HF 反应,因而氢氟酸不能保存在玻璃瓶中( )(8)高温下用焦炭还原SiO2 制取粗硅( )(9)单质硅是将太阳能转变为电能的常用材料( )(10)合成纤维和光导纤维都是新型无机非金属材料( )(11)SiO2 有导电性,所以SiO2 可用于制备光导纤维( )(12)(12)硅酸钠溶液应保存在带玻璃塞的试剂瓶中( )答案(1)√(2)√(3)√(4)√(5)×(6)√(7)√(8)√(9)√(10)×(11)×(12)×题组1 碳、硅单质的性质1.下列关于碳和硅的叙述中,正确的是( )。
A.其氧化物都能与NaOH 溶液反应B.其单质在加热时都能跟O2 反应C.其氧化物都能溶于水生成相应的酸D.碳和硅两种元素共有两种单质2.下列物质间的转化不能通过一步反应完成的是( )。
A.SiO2―→Si B.CO2―→CC.SiO2―→H2SiO3 D.Si―→Na2SiO3题组2 碳、硅氧化物的性质3.下列说法正确的是( )。
高温A.反应:SiO2+Na2CO3=====Na2SiO3+CO2↑,说明H2SiO3 的酸性大于H2CO3 的酸性B.可在试管内完成焦炭和石英砂(SiO2)制取硅的反应C.二氧化硅是生产光导纤维、玻璃的基本原料D.CO2、CH4、N2 是温室气体4.向含有0.2 mol NaOH 和0.1 mol Ba(OH)2 的溶液中持续稳定地通入CO2 气体,当通入气体为8.96L(0 ℃,1.01×105 Pa)时立即停止,则这一过程中,溶液中离子的物质的量与通入CO2 气体的体积关系图像正确的是(气体的溶解和离子的水解忽略不计)( )。
B C C C考点二硅酸盐及无机非金属材料1.硅酸硅酸难溶于水,其酸性比碳酸弱,硅酸不能(填“能”或“不能”)使紫色石蕊试液变红色。
△(1)硅酸不稳定,受热易分解,其化学方程式为:H2SiO3=====SiO2+H2O。
(2)硅酸能与碱溶液反应,如与NaOH 溶液反应的化学方程式为H2SiO3+2NaOH===Na2SiO3+2H2O。
(3)硅酸在水中易聚合形成胶体,硅胶有很强的吸水能力,常用作干燥剂。
2.硅酸盐(1)概念:由硅、氧和金属元素组成的化合物的总称,是构成地壳岩石的主要成分。
(2)表示方法:硅酸盐矿物的成分复杂,常用氧化物的形式表示它们的组成,如硅酸钠(Na2SiO3)写成Na2O·SiO2,钾云母(KH 2Al3Si3O12)写成K2O·3Al2O3·6SiO2·2H2O。
(3)硅酸钠(Na2SiO3)①白色、可溶于水的粉末状固体,其水溶液俗称水玻璃,有黏性,水溶液显碱性。
②它能与较强的酸反应,如与盐酸反应的化学方程式为:Na2SiO3+2HCl===2NaCl+H2SiO3↓;与CO2 水溶液反应的化学方程式为:Na2SiO3+CO2+H2O===H2SiO3↓+Na2CO3。
③用途:黏合剂(矿物胶),耐火阻燃材料。
3.无机非金属材料(1)传统无机非金属材料①三种硅酸盐工业生产的比较:水泥玻璃陶瓷生产原料石灰石、黏土纯碱、石灰石和石英黏土主要设备水泥回转窑玻璃窑陶瓷窑3CaO·SiO2 Na2SiO3主要成分2CaO·SiO2 CaSiO3硅酸盐3CaO·Al 2O3 SiO2生产条件高温②主要用途:陶瓷、玻璃、水泥是主要建筑材料,也广泛应用于生活中。
(2)新型无机非金属材料①高温结构陶瓷:如氮化硅陶瓷具有较高的硬度和耐磨性、较强的抗化学侵蚀性和电绝缘性等。
②生物陶瓷:对机体无排异反应,不会引起代谢作用异常。
③压电陶瓷:具有压电效应。
2.判断正误,正确的划“√”,错误的划“×”。
(1)玻璃是一种晶体,有较高的熔点。
( )(2)水玻璃是一种特殊的玻璃,泡花碱属于碱。
( )(3)向一定浓度的Na2SiO3 溶液中通入适量CO2 出现白色沉淀,证明H2CO3 的酸性比H2SiO3 的酸性强。
( )(4)传统无机非金属材料是指玻璃、水泥、陶瓷等硅酸盐材料( )(5)新型无机非金属材料克服了传统无机非金属材料的许多缺点( )(6)高温结构材料具有耐高温、耐酸碱腐蚀、硬度大、耐磨损、密度小等优点( )(7)水泥、玻璃、青花瓷、水晶、玛瑙都属于硅酸盐工业产品( )2-(8)2MgO·SiO2 中的酸根阴离子为SiO4 ( )答案(1)×(2)×(3)√(4)√(5)√(6)√(7)×(8)×[示向题组]1.(2014 ·济南联考)下列有关硅及硅酸盐材料的说法正确的是( )。
A.硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在磨口玻璃塞试剂瓶中高温B.反应①Na2SiO3+H2O+CO2===Na2CO3+H2SiO3↓,反应②Na2CO3+SiO2=====Na2SiO3+CO2↑,两反应是相互矛盾的,不可能都能发生C.普通玻璃、石英玻璃,水泥等均属于硅酸盐材料D.祖母绿的主要成分为Be3Al 2Si6O18,用氧化物形式表示为3BeO·Al 2O3·6SiO22.(2014 ·郑州一模)材料与化学密切相关,表中对应关系错误的是( )。