Tris-乙酸电泳缓冲液
- 格式:pdf
- 大小:98.41 KB
- 文档页数:1

tris-acetate buffer作用Trisacetate buffer是一种常用的缓冲液,主要用于调节溶液的酸碱性。
本文将以Trisacetate buffer作用为主题,从何为缓冲液、Trisacetate buffer的组成、Trisacetate buffer的酸碱性调节机制、Trisacetate buffer的优点和应用等方面,详细介绍Trisacetate buffer的作用。
第一部分:缓冲液的概述缓冲液是一种可以维持溶液酸碱性不易受外界影响的溶液。
在生化实验和许多生物学实验中,维持溶液的酸碱平衡是重要的,而缓冲液的作用就是起到这个平衡的作用。
缓冲液可以通过吸收或释放氢离子来维持溶液的酸碱平衡,并使溶液的pH值保持在一个稳定的范围内。
第二部分:Trisacetate buffer的组成Trisacetate buffer是一种由三羟甲基氨基甲烷(Tris)和乙酸钠(sodium acetate)组成的缓冲液。
Tris是一种弱碱,可以和酸反应,吸收氢离子,使溶液保持在碱性条件下。
乙酸钠是一种弱酸,可以和碱反应,释放氢离子,使溶液保持在酸性条件下。
这两种物质的组合可以在一定pH范围内维持溶液的中性。
第三部分:Trisacetate buffer的酸碱性调节机制Tris和乙酸钠之间的反应可以用以下方程式表示:Tris + H+ ↔ TrisH+乙酸钠↔乙酸 + Na+酸性条件下,乙酸钠离解,释放出乙酸和Na+离子,乙酸与Tris反应,生成TrisH+,以吸收氢离子,维持溶液的酸碱平衡。
碱性条件下,Tris与H+反应,生成TrisH+,以吸收氢离子,维持溶液的酸碱平衡。
通过Tris和乙酸钠之间的反应,Trisacetate buffer可以在一定pH范围内稳定溶液的酸碱性。
第四部分:Trisacetate buffer的优点和应用Trisacetate buffer具有以下几个优点:1. 在生理pH范围内(pH 7.27.6)表现出良好的缓冲能力,减小了溶液的pH值受外界变化的影响;2. 具有良好的溶解性,可以在生化实验中稳定有效地工作;3. 不对大多数生物分子具有毒性和抑制作用,适用于生物学实验。

te缓冲液1. 简介TE缓冲液是一种常用于核酸研究中的缓冲液。
TE缓冲液的全称为Tris-EDTA 缓冲液,其中Tris是三羟甲基氨基甲烷(Tris(hydroxymethyl)aminomethane),EDTA是乙二胺四乙酸(Ethylenediaminetetraacetic Acid)的缩写。
TE缓冲液常被用于核酸的储存、稀释和DNA的电泳分析。
2. 组成TE缓冲液的组成为:•10mM Tris-Cl•1mM EDTA3. 功能TE缓冲液具备以下功能:•维持等电点:TE缓冲液的pH值约为8.0,可在理想pH范围内维持核酸的等电点,保持其稳定性。
•稀释和储存:由于TE缓冲液中的EDTA可以与金属离子结合,阻止金属离子的催化作用,因此经TE缓冲液稀释储存的核酸可以减少降解和酶催化反应的发生。
•DNA电泳:TE缓冲液可用于DNA电泳分析,使DNA保持在双链状态,减少DNA降解和断裂。
4. 制备方法制备TE缓冲液的步骤如下:1.加入800mL去离子水或蒸馏水到一个无菌的容器中。
2.加入6.06g Tris-Cl固体,搅拌至完全溶解。
3.加入0.372g EDTA固体,搅拌至完全溶解。
4.调节pH值至8.0,可以用盐酸(HCl)或氢氧化钠(NaOH)进行调节。
5.加入去离子水或蒸馏水直至总体积为1L。
6.混匀,用0.2μm滤器过滤消除杂质,得到TE缓冲液。
5. 注意事项在制备和使用TE缓冲液时,需要注意以下事项:•使用无菌的实验室器具、试剂和培养基。
•严格遵循实验室的安全操作规程,避免对人身和环境造成伤害。
•储存TE缓冲液时,使用无菌密封容器,避免污染和杂质的进入。
•注意TE缓冲液的pH值,需要在8.0附近,可以使用pH计进行测量和调节。
•TE缓冲液供实验使用前,需要用0.2μm滤器过滤消除杂质。
6. 结论TE缓冲液是核酸研究中必备的一种缓冲液,具备维持核酸稳定性、稀释储存和DNA电泳的功能。
在制备和使用TE缓冲液时,需要注意无菌操作、安全操作和pH值的调节。

PCR 各种缓冲液的配方1. 电泳缓冲液50×Tris-乙酸(TAE)缓冲液终浓度配制1L溶液成分2mol/L Tris碱 242g1mol/L 冰乙酸 57.1 mlEDTA (pH=8.0) 18.622g (200ml的0.5 mol/L EDTA(pH 8.0))水补足1L2. 5×Tris-硼酸(TBE)缓冲液成分及终浓度配制1L溶液各成分的用量445 mmol/L Tris碱54g445 mmol/L 硼酸盐 27.5g 硼酸10 mmol/L EDTA 20 ml的0.5 mol/L EDTA(pH 8.0)水补足1L染料1%溴酚蓝(bromophenol blue)加1g水溶性钠型溴酚蓝于100ml水中,搅拌或涡旋混合直到完全溶解。
1%二甲苯青FF(xylene cyanole FF)溶解1g二甲苯青FF于足量水中,定容到100ml。
10mg/ml的溴化乙锭(ethidium bromide)小心称取1g溴化乙锭,转移到广口瓶中,加100ml水,用磁力搅拌器搅拌直到完全溶解。
用铝箔包裹装液管,于4℃贮存。
3. 凝胶上样液(gel loading solutions)6×碱性凝胶上样液(室温贮存)成分及终浓度配制10ml溶液各成分用量0.3 N 氢氧化钠 300ul 10N 氢氧化钠6 mmol/L EDTA 120ul 0.5mol/L EDTA(pH8.0)18%聚蔗糖(400型) 1.8g0.15%溴甲酚绿 15mg0.25%二甲苯青FF 25mg水 10ml4. 6×聚蔗糖凝胶上样液(室温贮存)成分及终浓度配制10ml溶液各成分用量0.15%溴酚蓝 1.5ml 1%溴酚蓝0.15%二甲苯青FF 1.5ml 1%二甲苯青FF5 mmol/L EDTA 100ul 0.5mol/L EDTA(pH8.0)15%聚蔗糖(400型) 1.5g水补足到10ml5.6×溴酚蓝/二甲苯青/聚蔗糖凝胶上样液(室温贮存)成分及终浓度配制10ml溶液各成分用量0.25%溴酚蓝 2.5ml 1%溴酚蓝0.25%二甲苯青FF 2.5ml 1%二甲苯青FF15%聚蔗糖(400型) 1.5g水补足到10ml6.6×甘油凝胶上样液(4℃贮存)成分及终浓度配制10ml溶液各成分用量0.15%溴酚蓝 1.5ml 1%溴酚蓝0.15%二甲苯青FF 1.5ml 1%二甲苯青FF5 mmol/L EDTA 100ul 0.5mol/L EDTA(pH8.0)50%甘油3ml水 3.9ml7. 6×蔗糖凝胶上样液(室温贮存)成分及终浓度配制10ml溶液各成分用量0.15%溴酚蓝 1.5ml 1%溴酚蓝0.15%二甲苯青FF 1.5ml 1%二甲苯青FF5 mmol/L EDTA 100ul 0.5mol/L EDTA(pH8.0)40%聚蔗糖 4g水补足到10ml8.10×十二烷基硫酸钠/甘油凝胶上样液(室温贮存)成分及终浓度配制10ml溶液各成分用量0.2%溴酚蓝20mg0.2%二甲苯青FF 20mg200 mmol/L EDTA 4ml 0.5mol/L EDTA(pH8.0) 0.1%SDS 100ul 10% SDS50%甘油 5ml水补足到10ml。
2.测序凝胶加样缓冲液98%去离子甲酰胺10mol/L EDTA(pH8.0)0.025%二甲苯青FF0.025%溴酚蓝甲酰胺:许多批号的试剂级甲酰胺,其纯度符合使用要求,无须再进行处理。
不过,一旦略呈黄色,则应用在磁力搅拌器上将甲酰胺与D owexXG8混合床树脂共同搅拌1小时进行去离子处理,并用What man 1号滤纸过滤2次,去离子甲酰胺分装成小份,充氮存于-70℃。
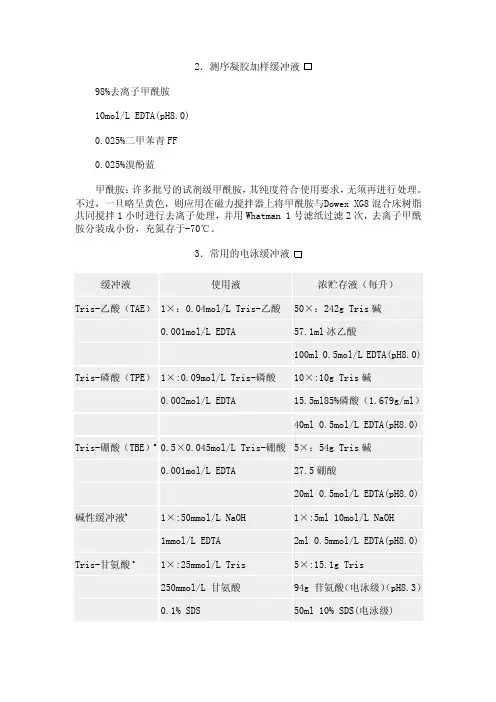
3.常用的电泳缓冲液说明:①TBE溶液长时间存放后会形成沉淀物,为避免这一问题,可在室温下用玻璃瓶保存5×溶液,出现沉淀后则予以废弃。
以片都以1×TBE作为使用液(即1:5稀释浓贮液)进行琼脂糖凝胶电泳。
但0.5×的使用液已具备足够的缓冲容量。
目前几乎所有的琼脂糖胶电泳都以1:10稀释的贮存液作为使用液。
进行聚丙烯酰胺凝胶垂直槽的缓冲液槽较小,故通过缓冲液的电流量通常较大,需要使用1×TBE以提供足够的缓冲容量。
②碱性电泳缓冲液应现用现配。
③Tris-甘氨酸缓冲液用SDS聚丙烯酰胺凝胶电泳。
4.2×SDS凝胶加样缓冲液100mmo l/L Tris·HCl(6.8)200mmo l/L二硫苏糖醇(DTT)4%SDS(电泳级)0.2%溴酚蓝20%甘油不含DTT的2×SDS凝胶加样缓冲液可保存于室温,应在临用前取1mol/L贮存液现加于上述缓冲液中。
5.凝胶加样缓冲液使用以上凝胶加样缓冲液的目的有三:增大样品密度;以确保DNA均匀进入样品孔内;使样品呈现颜色,从而使加样操作更为便利,含有在电块中能以可预知速率向阳极泳动的染料。
溴酚蓝在琼脂糖中移动的速率约为二甲苯青FF的2. 2倍,而与琼脂糖浓度无关。

常用缓冲液配方及缓冲范围缓冲液是一种水溶液,其中含有在酸性或碱性条件下能够保持pH稳定的化学物质。
缓冲液广泛应用于生物化学、分子生物学、生物技术和医学等领域的实验和研究中。
下面是一些常用的缓冲液配方及其应用范围。
1. Tris缓冲液Tris缓冲液是一种中性缓冲液,常用于生物化学和分子生物学实验。
它的配方通常为:- 10 mM Tris base-1mMEDTA-向溶剂中调整pH至7.4Tris缓冲液可用于DNA和RNA的电泳、酶反应、细胞培养等实验中。
2.PBS缓冲液PBS(磷酸盐缓冲液)是一种常用的生物学缓冲液,具有缓冲能力强和与生物体液成分相似的特点。
它的配方通常为:-137mMNaCl-2.7mMKCl-10mMNa2HPO4-2mMKH2PO4-向溶剂中调整pH至7.4PBS缓冲液可用于细胞培养、免疫荧光染色、蛋白质凝胶电泳等实验中。
3.TAE缓冲液TAE(三乙酸缓冲液)是一种常用的核酸电泳缓冲液,其配方为:- 40 mM Tris base-20mM醋酸-1mMEDTA-向溶剂中调整pH至8.0TAE缓冲液可用于DNA和RNA的琼脂糖凝胶电泳,如聚丙烯酰胺凝胶电泳()和琼脂糖凝胶电泳(agarose gel electrophoresis)。
4. Tris-HCl缓冲液Tris-HCl缓冲液是一种常用的酸性或碱性缓冲液。
它的配方基于Tris缓冲液,在Tris缓冲液基础上调整pH的方法是在配方中加入稀盐酸或稀氢氧化钠。
例如,对于Tris-HCl缓冲液的配方为:- 50 mM Tris base-向溶剂中加入HCl调整pH至所需的值(通常为7.2至9.0)Tris-HCl缓冲液可用于酶反应、蛋白质组学研究、PCR等实验中。
这只是一些常用的缓冲液配方,根据不同实验需求和物质稀释要求,还有其他许多缓冲液的配方。
对于缓冲液的选择,关键在于根据实验要求选取适当的缓冲体系,并对缓冲液中所需的化学物质浓度、pH值等进行精确调整。

Tris-HCl缓冲液的优点是:①因为Tris碱的碱性较强,所以可以只用这一种缓冲体系配制pH范围由酸性到碱性的大范围pH值的缓冲液;②对生物化学过程干扰很小,不与钙、镁离子及重金属离子发生沉淀。
其缺点是:①缓冲液的pH值受溶液浓度影响较大,缓冲液稀释十倍,pH值的变化大于0.1;②温度效应大,温度变化对缓冲液pH值的影响很大,即:△pKa/℃=-0.031 ,例如:4℃时缓冲液的pH=8.4,则37℃时的pH=7.4,所以一定要在使用温度下进行配制,室温下配制的Tris-HCl缓冲液不能用于0℃~4℃。
③易吸收空气中的CO2,所以配制的缓冲液要盖严密封。
④此缓冲液对某些pH电极发生一定的干扰作用,所以要使用与Tris溶液具有兼容性的电极。
Question about Tris-Hcl and PBS buffer - (Jan/22/2007 )Hello..Maybe it is a very stupid question..but i would like to ask what is usage of buffer...and what is the difference between the Tris-Hcl and PBS...How can i choose buffer for the experiment? What is the basis of sele cting a buffer solution?-hana_angel-Remember that biological reactions work well only in a very narrow ra nge of pH (around 7.4). Many of that ractions generate or consume pro tons, so a buffer must have the capability of compensate that variati ons of pH. Tris has pros and cons about it. Its pKa is 8.0, so its bu ffering capacity is around 7.5-9.0, enough to most of biological reac tions. Despite its high buffering capacity, being highly soluble in w ater and being inert for enzimatic reactions, Tris is a toxic polyami ne, and that's why we use PBS for living cells experiments. PBS is ma de of phosphates so it's cheap and easy to prepare (an important poin t for a good buffer). It's no toxic for cells, compatible in osmolari ty and it's insensitive to temperature changes (Tris don't). Phosphat es have a high buffering capacity too but may inhibit enzymatic react ions because they can sequester divalent cations like calcium and mag nesium, then we use Tris for enzymatic reactions.Choosing a buffer depends upon the objective of your experiment and t he nature of your method (enzymatic reactions, histological procedure, live/dead cell detection methods, etc). Take a look on the literatur e about the experiment you want to do and check is buffers used there are compatible with your experiment or protocol. Some basic books ab out cell culture or molecular biology technics are useful too. Even b rochures or catalogs from manufacturers could be a good source of information.Good Luck!-aleruiz-三羟甲基氨基甲烷(tris(hydroxymethyl)aminomethane,一般简称为Tris)是一种有机化合物,其分子式为(HOCH2)3CNH2。

电泳缓冲液母液的配制
50×TAE
称取242g Tris溶于800ml双蒸水中,加57.1ml冰乙酸和100ml 0.5mol/L EDTA(pH 8.0),再加水定容至1L,室温保存备用。
50×TAE简易配制方案
称量242gTris,EDTANa2·2H2O37.2g于1L烧杯中,向烧杯中加入约800ml双蒸水,充分搅拌均匀;加入57.1ml的冰乙酸,充分溶解;用NaOH调pH至8.3,加去离子水定容至1L后,室温保存。
注:开始溶解药品的双蒸水量一定要小于800ml,否则加药后会发现总体积超过1L,加入水后,常会发现药品很难完全溶解,此时可先将烧杯放在磁力搅拌器上充分搅拌且适当加热液体(≤80℃),并继续后续配制;用NaOH调节pH时,推荐使用固体(粉末或颗粒)试剂,由于缓冲液的缓冲作用,需要加入较大量的NaOH,并且随着NaOH的加入,前面未溶解的药品会慢慢溶解,当pH>8.0后,溶液即会变为无色澄清的液体。
此种配方方便快捷,且可保证稀释后1×TAE的pH值在8.0左右,是理想的TAE配制方案。
5×TBE
称取54g Tris,27.5g硼酸溶于800ml双蒸水中,加入20ml 0.5mol/L EDTA(pH 8.0),再加水定容至1L,室温保存备用。
![[VIP专享]TAE缓冲液](https://uimg.taocdn.com/bbb09e0c3b3567ec112d8a4f.webp)

Tris缓冲液的特性Tris中文品名为三羟甲基氨基甲烷;氨基丁三醇;又名缓血酸胺;2-氨基-2-(羟甲基)-1,3-丙二醇。
是一种白色结晶或粉末,溶于乙醇和水,微溶于乙酸乙酯、苯,对铜、铝有腐蚀作用,是一种有刺激性的化学物质。
Tris有很高的缓冲能力,在水中溶解度高,对很多酶呈惰性反应,它的这一特性使得Tris成为用于许多生化目的非常满意的缓冲液。
一般用于稳定反应体系的pH,在pH7.5-9.0之间有较强的缓冲能力。
三羟甲基氨基甲烷Tris白色粉末状一、Tris缓冲液的优点①因为Tris碱的碱性较强,所以可以只用这一种缓冲体系配制pH范围由酸性到碱性的大范围pH值的缓冲液;②对生物化学过程干扰很小,不与钙、镁离子及重金属离子发生沉淀。
二、Tris缓冲液的缺点①缓冲液的pH值受溶液浓度影响较大,缓冲液稀释十倍,pH值的变化大于0.1;②温度效应大,温度变化对缓冲液pH值的影响很大,△pKa/℃=-0.031,例如:4℃时缓冲液的pH=8.4,则37℃时的pH=7.4,所以一定要在使用温度下进行配制,室温下配制的Tris-HCl缓冲液不能用于0℃~4℃;③易吸收空气中的CO2,所以配制的缓冲液要盖严密封;④此缓冲液对某些pH电极发生一定干扰作用,所以要使用与Tris溶液具有兼容性的电极。
三、Tris缓冲液pH范围Tris缓冲液在生物化学研究中使用较广泛的一种缓冲剂,它的常用有效pH范围是在“中性”范围,如:Tris-HCl缓冲液:pH=7.5~8.5Tris-磷酸盐缓冲液:pH=5.0~9.0除TRIS-hcl外,TRIS还有多种衍生化缓冲:TBS=Tris-HCl+NaCl+KCl常用来清洗免疫染色组织或Western blotting中的Western blotting膜;TBST=Tris-HCl+NaCl+tween20,一种常用于Western Blotting的膜缓冲液;TE=Tris-HCl+EDTA,对DNA碱基具有保护作用,常用于DNA的稳定和储存;TAE=Tris碱+乙酸+EDTA,是一种广泛应用于短片段DNA电泳的缓冲体系;TBE=三碱基+硼酸+EDTA,适用于长期DNA电泳,对小片段有较好的分离效果。

北京雷根生物技术有限公司
Tris-硼酸电泳缓冲液(5×TBE)
产品简介:
Tris-硼酸电泳缓冲液简称TBE。
0.5×TBE工作液中含有45mM Tris-硼酸、1mM EDTA(pH8.0)。
TBE是常用的DNA电泳缓冲液。
一般情况下,DNA电泳常使用0.5×TBE工作液,Tris-乙酸电泳缓冲液的优点:缓冲能力弱,适宜分离相对较小(小于2000bp)的DNA片段。
亦可以使用0.5~1×TBE工作液,该工作液缓冲能力相对较强。
本试剂是10倍浓缩的TBE,使用时需用蒸馏水或去离子水稀释为0.5×TBE后使用。
主要成分:主要由450mM Tris-硼酸,10mM EDTA等组成。
操作步骤(仅供参考):
1、用蒸馏水或去离子水稀释到0.5×后使用。
注意事项:
1、10×TBE储存液不稳定,容易产生沉淀,建议采用5×TBE,因为5×TBE储存起来更稳定。
2、工作液使用0.5×TBE,亦可以使用0.5~1×TBE工作液,该工作液缓冲能力相对较强。
3、为了您的安全和健康,请穿实验服并戴一次性手套操作。
有效期:12个月有效。
相关产品:
产品编号 产品名称
NA0006DNA凝胶加样缓冲液(6×DNA Loading Buffer)
NA0015MOPS电泳缓冲液(1×,RNase free)
NA0030Tris-乙酸电泳缓冲液(50×TAE)
PE0092Tris-甘氨酸电泳缓冲液(5×SDS-PAGE)。

缓冲液缓冲溶液(英文:buffer solution)是一种能在加入少量酸或碱和水时大大减低pH变动的溶液。
pH缓冲系统对维持生物的正常pH值和正常生理环境起到重要作用。
多数细胞仅能在很窄的pH范围内进行活动,而且需要有缓冲体系来抵抗在代谢过程中出现的pH变化。
在生物体中有三种主要的pH缓冲体系,它们是蛋白质缓冲系统、重碳酸盐缓冲系统以及磷酸盐缓冲系统。
每种缓冲体系所占的分量在各类细胞和器官中是不同的。
在生化研究工作中,常常需要使用缓冲溶液来维持实验体系的酸碱度。
研究工作的溶液体系pH值的变化往往直接影响到研究工作的成效。
如果“提取酶”实验体系的pH值变动或大幅度变动,酶活性就会下降甚至完全丧失。
所以配制缓冲溶液是一个不可或缺的关键步骤。
常用作缓冲溶液的酸类由弱酸及其共轭酸盐组合成的溶液具有缓冲作用。
生化实验室常用的缓冲系主要有磷酸、柠檬酸、碳酸、醋酸、巴比妥酸、Tris(三羟甲基氨基甲烷)等系统,生化实验或研究工作中要慎重地选择缓冲体系,因为有时影响实验结果的因素并不是缓冲液的pH值,而是缓冲液中的某种离子。
如硼酸盐、柠檬酸盐、磷酸盐和三羟甲基甲烷等缓冲剂都可能产生不需要的化学反应。
硼酸盐:硼酸盐与许多化合物形成复盐、如蔗糖。
柠檬酸盐:柠檬酸盐离子容易与钙结合,所以存在有钙离子的情况下不能使用。
磷酸盐:在有些实验,它是酶的抑止剂或甚至是一个代谢物,重金属易以磷酸盐的形式从溶液中沉淀出来。
而且它在pH7.5以上时缓冲能力很小。
三羟甲基氨基甲烷:它可以和重金属一起作用,但在有些系统中也起抑制作用。
其主要缺点时温度效应。
这点往往被忽视,在室温pH是7.8的Tris缓冲液,4℃时是8.4,37℃时是7.4,因此,4℃配制的缓冲液在37℃进行测量时,其氢离子浓度就增加了10倍。
在pH7.5以下,其缓冲能力极为不理想。
缓冲溶液组成缓冲体系由1、弱酸和它的盐(如HAc---NaAc)2、弱碱和它的盐(NH3.H2O---NH4Cl)3、多元弱酸的酸式盐及其对应的次级盐(如NaH2PO4---Na2HPO4)的水溶液组成。
琼脂糖凝胶电泳的试剂
琼脂糖凝胶电泳是一种常用于生物化学和分子生物学实验的技术,用于分离和鉴定DNA、RNA和蛋白质等生物大分子。
在进行琼脂糖凝胶电泳实验时,需要使用以下试剂:
1.琼脂糖:作为凝胶基质,用于制作凝胶板。
2.缓冲液:用于维持样品和电泳过程中的pH值稳定。
常用的缓冲液有Tris-乙酸(TAE)和Tris-甘氨酸(TG)等。
3.核酸染料:用于染色和可视化核酸样品。
常用的核酸染料有乙酰胺蓝、考马斯亮蓝、荧光染料(如SYBR Green)等。
4.蛋白质染料:用于染色和可视化蛋白质样品。
常用的蛋白质染料有考马斯亮蓝、银染料等。
5.电泳缓冲液:用于在电泳过程中提供离子和能量。
常用的电泳缓冲液有Tris-乙酸(TAE)和Tris-甘氨酸(TG)等。
6.琼脂糖凝胶制备试剂:用于制备琼脂糖凝胶,如凝胶板。
常用的试剂有TAE缓冲液、琼脂糖、DNA酶抑制剂等。
7.样品加载试剂:用于将样品加载到凝胶板上,如DNA Loading Buffer、Protein Loading Buffer等。
8.终止剂:用于终止电泳过程,如琼脂糖凝胶电泳终止剂(如Ethidium bromide)。
9.洗涤剂:用于清洗实验器材,如70%乙醇、缓冲液等。
10.其他辅助试剂:如移液器、吸头、离心管、DNA Marker、蛋白质Marker等。
常用的电泳缓冲液
说明:
①tbe溶液长时间存放后会形成沉淀物,为避免这一问题,可在室温下用玻璃瓶保存5×溶液,出现沉淀后则予以废弃。
以片都以1×tbe作为使用液(即1:5稀释浓贮液)进行琼脂糖凝胶电泳。
但0.5×的使用液已具备足够的缓冲容量。
目前几乎所有的琼脂糖胶电泳都以1:10稀释的贮存液作为使用液。
进行聚丙烯酰胺凝胶垂直槽的缓冲液槽较小,故通过缓冲液的电流量通常较大,需要使用1×tbe以提供足够的缓冲容量。
②碱性电泳缓冲液应现用现配。
③tris-甘氨酸缓冲液用sds聚丙烯酰胺凝胶电泳。
2×sds凝胶加样缓冲液:
100mmol/l tris·hcl(6.8)
200mmol/l二硫苏糖醇(dtt)
4%sds(电泳级)
0.2%溴酚蓝
20%甘油
不含dtt的2×sds凝胶加样缓冲液可保存于室温,应在临用前取1mol/l贮存液现加于上述缓冲液中。
常用电泳试剂配制方法电泳试剂是在蛋白质或核酸电泳实验中使用的一系列化学试剂。
常用的电泳试剂包括缓冲液、凝胶、加载缓冲液、电泳盐溶液等。
以下是常用电泳试剂的配制方法。
一、缓冲液的配制方法:1.TAE缓冲液TAE缓冲液配方:0.04M缩醛酸,0.001M乙酸,0.001MEDTA,pH8.0。
配制方法:将缩醛酸溶解在适量的蒸馏水中,调节pH值为8.0,加入乙酸和EDTA,再用蒸馏水稀释至适量。
2.TBE缓冲液TBE缓冲液配方:0.089M缩醛酸,0.089M硼酸,0.002MEDTA,pH8.3配制方法:将缩醛酸溶解在适量的蒸馏水中,调节pH值为8.3,加入硼酸和EDTA,再用蒸馏水稀释至适量。
3. Tris-EDTA缓冲液 (TE缓冲液)TE缓冲液配方:10mM缩醛酸,1mMEDTA,pH8.0。
配制方法:将缩醛酸溶解在适量的蒸馏水中,调节pH值为8.0,然后加入EDTA,再用蒸馏水稀释至适量。
二、凝胶的配制方法:1.聚丙烯酰胺凝胶聚丙烯酰胺凝胶配方:30%丙烯酰胺,0.8%季铵盐,1M缓冲液,10%过硫酸铵。
配制方法:将丙烯酰胺溶解在适量的蒸馏水中,加入季铵盐,搅拌均匀后加入缓冲液,最后加入过硫酸铵,混合均匀后注射到凝胶板中,等待凝固。
2.熔融琼脂糖凝胶熔融琼脂糖凝胶配方:1%琼脂糖,1×TAE缓冲液。
配制方法:将琼脂糖溶解在适量的蒸馏水中,加热至完全融化,冷却至60-70°C后加入TAE缓冲液,混合均匀后倒入凝胶板中,等待凝固。
三、加载缓冲液的配制方法:1.6×加载缓冲液6×加载缓冲液配方:40%甘露醇,0.25%溴酚蓝,一定量的TAE或TBE缓冲液。
配制方法:先将甘露醇溶解在适量的蒸馏水中,加入溴酚蓝,搅拌均匀后加入适量的TAE或TBE缓冲液,混合均匀后即可。
四、电泳盐溶液的配制方法:1.DNA电泳盐溶液DNA电泳盐溶液配方:1×TAE缓冲液。
TAE缓冲液:电泳缓冲液Tris-乙酸TAE缓冲液成分及终浓度:1、2mol/L Tris碱2、1mol/L 乙酸3、100 mmol/L EDTA4、水配制1L的50×TAE缓冲液各成分用量:1、 Tris碱(242g)2、冰乙酸(57.1 ml)3、EDTA【200ml的0.5 mol/L EDTA(pH 8.0)】4、水(补足1L)50×TAE缓冲液的配制方法:称下列试剂,1L烧杯Tris 242g Na2EDTA.2H2O 37.2g然后加入800ml的去离子水,充分搅拌溶解。
加入57.1ml的醋酸,充分混匀。
加去离子水定容至1L,室温保存。
AE是使用最广泛的缓冲系统。
其特点是超螺旋在其中电泳时更符合实际相对分子质量(TBE 中电泳时测出的相对分子质量会大于实际分子质量),且双链线状DNA在其中的迁移率较其他两种缓冲液快约10%,电泳大于13kb的片段时用TAE缓冲液将取得更好的分离效果,此外,回收DNA片段时也易用TAE缓冲系统进行电泳。
TAE的缺点是缓冲容量小,长时间电泳(如过夜)不可选用,除非有循环装置使两极的缓冲液得到交换。
loading bufferloading buffer 的中文名字叫上样缓冲液,6*的缓冲液中可以显示两条带,前面的蓝色的条带是溴酚蓝,代表的片段大小是300bp,后面的有点绿色的条带是二甲苯青,代表的片段大小在4000bp左右。
loading buffer的功能主要有两个。
第一,里边的指示剂溴酚蓝和二甲苯酚起到指示的作用,显示电泳的进程,以便我们适时终止电泳;第二,里边的成分甘油可以加大样品密度,使样品密度大于TAE,从而沉降到点样孔中,防止样品飘出点样孔。
另外,有的Buffer是加有SDS的,一般都会写明。
SDS主要是促使聚合酶变性,因为没有除尽的聚合酶会结合在DNA双链上影响它的迁移速率。
细胞裂解后的裂解液,加loading 100℃加热,也是为了中止酶促反应,防止提取的蛋白质降解。
TAE缓冲液:电泳缓冲液Tris-乙酸TAE缓冲液成分及终浓度:1、2mol/L Tris碱2、1mol/L 乙酸3、100 mmol/L EDTA4、水配制1L的50×TAE缓冲液各成分用量:1、 Tris碱(242g)2、冰乙酸(57.1 ml)3、EDTA【200ml的0.5 mol/L EDTA(pH 8.0)】4、水(补足1L)50×TAE缓冲液的配制方法:称下列试剂,1L烧杯Tris 242g Na2EDTA.2H2O 37.2g然后加入800ml的去离子水,充分搅拌溶解。
加入57.1ml的醋酸,充分混匀。
加去离子水定容至1L,室温保存。
AE是使用最广泛的缓冲系统。
其特点是超螺旋在其中电泳时更符合实际相对分子质量(TBE 中电泳时测出的相对分子质量会大于实际分子质量),且双链线状DNA在其中的迁移率较其他两种缓冲液快约10%,电泳大于13kb的片段时用TAE缓冲液将取得更好的分离效果,此外,回收DNA片段时也易用TAE缓冲系统进行电泳。
TAE的缺点是缓冲容量小,长时间电泳(如过夜)不可选用,除非有循环装置使两极的缓冲液得到交换。
loading bufferloading buffer 的中文名字叫上样缓冲液,6*的缓冲液中可以显示两条带,前面的蓝色的条带是溴酚蓝,代表的片段大小是300bp,后面的有点绿色的条带是二甲苯青,代表的片段大小在4000bp左右。
loading buffer的功能主要有两个。
第一,里边的指示剂溴酚蓝和二甲苯酚起到指示的作用,显示电泳的进程,以便我们适时终止电泳;第二,里边的成分甘油可以加大样品密度,使样品密度大于TAE,从而沉降到点样孔中,防止样品飘出点样孔。
另外,有的Buffer是加有SDS的,一般都会写明。
SDS主要是促使聚合酶变性,因为没有除尽的聚合酶会结合在DNA双链上影响它的迁移速率。
细胞裂解后的裂解液,加loading 100℃加热,也是为了中止酶促反应,防止提取的蛋白质降解。
TAE是Tris-乙酸,缓冲容量小,但是溶解度大,易于储存TBE是Tris-硼酸,缓冲容量大,但是溶解度小,不易长期储存,易产生沉淀TAE与TBE的区别首先要知道 TAE 与 TBE 缓冲溶液的成份如下:50x TAE Buffer (Tris-Acetate-EDTA)242 gm Tris base57.1 ml Acetic acid 100ml0.5M EDTAAdd ddH2O to 1 liter and adjust pH to 8.5.10x TBE Buffer (Tris-Borate-EDTA)108 gm Tris base55 gm Boric acid9.3 gm Na4EDTAAdd ddH2O to 1 liter.The pH is 8.3 and requires no adjustment.它们的分别有下列几点:1. TBE 不能太浓 (它只可有 10 times),因为 borate 会很容易沉淀,但一般有少许沉淀是不会有太大问题。
2. TBE 的 buffering capacity 比 TAE 高,用 TBE 来跑出来的 gel,分辨率 (resolution) 会比较高。
3. 因为 TBE 有 borate 离子 (ion),它会影向酵素 (enzyme) 的工作。
因此,若要为分离出的 DNA 进行下一步酵素处理,如 cloning 或 restriction cut 的话,就要切记不要让DNA 碰上 borate ion。
4. TAE的 buffer capacity 比较差,gel 一般比较模糊,但它不会对影向酵素三种缓冲液的配制方法Tris-乙酸(TAE):50×浓贮存液(每升):242g Tris 碱57.1ml 冰乙酸100ml 0.5mmol/L EDTA(pH8.0)使用时再稀释50倍。
Tris-磷酸(TPE):10×浓贮存液(每升):108g Tris 碱15.5ml 85%磷酸(1.679g /ml)40ml 0.5mmol/L EDTA(pH8.0)使用时再稀释10倍。