燃料及燃烧
- 格式:doc
- 大小:718.00 KB
- 文档页数:58


第六章 燃烧与燃料第一节 燃烧与灭火一.燃烧的条件(重点)1.燃烧:是可燃物跟氧气发生的剧烈的发光、发热的氧化反应。
(1)燃烧的现象:发光、发热,反应剧烈。
(2)燃烧的反应类型:氧化反应,不一定是化合反应。
(3)燃烧的反应物:常见的燃烧都是可燃物跟氧气发生反应,但是,不是所有的燃烧都一定有氧气参加。
例如,镁就能在二氧化碳中燃烧:2Mg+CO 2点燃C+2MgO ;钠能在氯气中燃烧:2Na +Cl 2点燃2NaCl(4)燃烧的反应条件:点燃 (5)燃烧的分类及燃烧的产物注意:① “完全燃烧”和“不完全燃烧”又叫“充分燃烧”和“不充分燃烧” ② 要掌握含C 、H 、O 等元素的燃料完全燃烧的化学方程式: 2.燃烧的条件:①物质具有可燃性 ②可燃物要与氧气接触;③可燃物的温度达到其自身的着火点(即可燃物燃烧所需要的最低温度) 燃烧必须要同时满足三个条件,才能发生燃烧的现象。
二.灭火的原理:①.移走可燃物可燃物 ②.隔绝氧气③.使温度降到着火点以下1.灭火原理实质就是破坏物质燃烧的条件,三者破坏其一即可灭火。
2.几种常见的灭火方法:(1) 移走可燃物可燃物:森林火灾开辟隔离带,管道煤气着火先关掉阀门,釜底抽薪等; (2)隔绝氧气:酒精灯用等冒盖灭,油锅着火用用锅盖盖灭,向着火的木柴上覆盖沙子,少量酒精燃烧用湿抹布盖灭等;(3)使温度降到着火点以下:用水等大量的冷却剂灭火,用嘴将灯吹熄,(4)用灭火器灭火:①泡沫灭火器:可用于扑灭木材、棉布等燃烧而引起的一般火灾,不能用于扑灭电器火灾;②干粉灭火器:除了用来扑灭一般火灾外,还用于扑灭电器、油、气等燃烧引起的火灾;③液态二氧化碳灭火器:用于扑灭图书档案、贵重设备、精密仪器的火灾。
3.二氧化碳与灭火(1)原理:二氧化碳不能燃烧也不能支持燃烧,且密度比空气大。
(2)灭火器主要是用二氧化碳灭火,二氧化碳不能扑灭所有的火灾:如镁带燃烧就不能用二氧化碳扑灭。
4火灾处置、自救 (1)火警电话:119(2)电器、管道煤气、天然气着火,首先要关闭电源或气阀。

初中化学燃料及其燃烧知识点总结一、燃烧的条件1、燃烧的定义:燃烧通常指可燃物与氧气发生发光发热的剧烈的氧化反应2、燃烧的条件? 可燃物达到着火点(该物质着火燃烧所需的最低温度)的温度? 可燃物与氧气/空气充分接触(一)二氧化碳与镁带的反应? 反应方程式:2Mg+CO2(点燃→)C+2MgO? 现象? 结论:具有剧烈发光发热现象的化学反应都是燃烧(二)金属钠与氯气的反应? 反应方程式:2Na+Cl2(点燃→)2NaCl? 现象? 置换反应:一种单质与一种化合物反应生成另一种化合物和另一种单质的反应即A+BC→B+AC? 火柴杆竖直之后为何会逐渐熄灭?答:因为火柴杆的温度会达不到着火点3、特殊的燃烧? 自燃白磷:少量白磷保存在冷水中(隔绝氧气)缓慢氧化:积聚热量引发自然(缓慢氧化,不一定引发自燃例如:铁生锈、食物变质、人类衰老、橡胶老化)? 爆炸:可燃性气体、液体的蒸发或粉尘在空气中(必定有氧气)浓度达到爆炸极限时,点火或遇火星会爆炸H2,CO,CH4,C2H5OH,面粉二、灭火与防火1、灭火原理? 降低火场温度? 隔绝可燃物与氧气的接触2、常用灭火器? 水? 酸碱灭火器:化学方程式? 干粉灭火器:化学方程式? STOP30灭火器:价格昂贵附:STOP30有多项优点胜过传统灭火器,它能彻底扑灭不同类型的火灾(例如因纸、油、溶剂和燃料引起的火灾),且可以安全地使用在最高达380伏特的电器用品上。
它是高度耐热的。
STOP30尺寸小巧,重量只725公克,高26公分(厘米),直径73公厘(毫米)。
STOP30于数秒内立即生效,使用者只需要摇晃罐子,取下卡笋,再按下去喷出泡沫。
STOP30 主要由含多价添加剂(阴离子及酸硷性兼备的张力活性剂、甘油及防腐剂)的水组成,以氮气推进, 该成分会形成快速覆盖火焰的泡沫。
泡沫产生一层薄膜,阻绝氧气,防止死灰复燃,令火焰在几秒钟内熄灭。




燃烧和燃料【主要内容】燃烧和燃料【知识要点】一、燃烧的条件1.概念燃烧是可燃物与氧气发生的一种发光、发热的剧烈的氧化反应,是我们经常接触到的一种化学变化。
说明:燃烧的共同特征——发光、发热。
反应的实质——剧烈的氧化反应。
2.燃烧需要的三个条件【实验】如图所示,在烧杯中放入一定量的热水,在烧杯上放一块薄铜片,在铜片的两端分别放一小粒白磷和一小堆红磷,在烧杯中A处也放一小粒白磷,过一会儿后只有薄铜片上的白磷燃烧起来而烧杯中的白磷和铜片上的红磷不燃烧。
白磷在水中燃烧通过以上实验可以说明,燃烧必须同时具备三个条件,缺一不可。
(1)可燃物;(2)与氧气(或空气)接触;(3)温度达到物质燃烧时所需的最低温度(也叫着火点)。
燃烧必须同时具备这三个条件,若缺少一个就不能燃烧。
二、灭火的原理和方法灭火的原理是由燃烧的条件决定的,即破坏燃烧的条件之一,就可以灭火。
可见,燃烧的条件和灭火的原理是从不同的角度来说明同一问题,两者不是相互割裂的。
原理一:清除可燃物或使可燃物与其它物品隔离。
原理二:将可燃物与氧气(或空气)隔绝。
原理三:将可燃物温度降到着火点以下。
例如:实验室熄灭酒精灯时,是用灯帽盖灭,原理是为了使可燃物与氧气隔绝。
又如:柴垛失火,人们一般都是用水去扑灭,原理是降低柴垛周围的温度,使之低于柴垛的着火点;也可以迅速的转移走未烧着的柴禾,原理是清除可燃物或使可燃物与其他物品隔离。
常见的灭火器简介一般指装有灭火剂的消防器材。
常用的灭火剂为二氧化碳或能产生二氧化碳的物质。
因为二氧化碳不支持燃烧,又比空气重,能够覆盖在燃着的物体表面,隔绝空气,使火熄灭。
(1)泡沫灭火器灭火器内分别装有硫酸铝溶液和碳酸氢钠溶液,使用时将灭火器倒置,两种溶液混合发生下列化学反应。
Al2(SO4)3+6NaHCO3=2Al(OH)3↓+3Na2SO4+6CO2↑产生的大量二氧化碳气体带着泡沫喷到燃烧物表面,达到灭火的目的。
泡沫是用甘草或皂角制取的液体产生的。

2 燃料及燃烧2.l 冶金企业常用燃料1、概述燃料的定义:凡燃烧时能放出大量的热,该热量能经济而有效地用于现代工业生产或日常生活的所有物质,统称燃料。
冶金生产大多数需要在高温下进行,其所需热量,除电炉外,大部分仍靠燃烧燃料供给,所以燃料是冶金生产不可缺少的重要原材料之一。
冶金生产所使用的燃料,一般应具备如下条件:(l) 燃烧所放出的热量必须满足生产工艺要求;(2) 便于控制和调节燃烧过程;(3) 蕴藏量丰富,成本低,使用方便;(4) 燃烧产物必须是气体,对人、动植物、厂房、设备等无害。
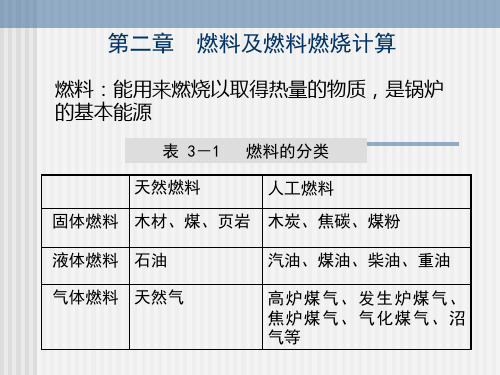
燃料的种类很多,按物态可分为固体燃料、液体燃料和气体燃料三类;按来源可分为天然产品和加工产品两种。
工业用燃料分类见表2—1。
燃料的一般分类表 表2—1来源燃料的固态天然产品加工产品固体燃料木柴、煤、油页岩等木炭、焦炭、粉煤液体燃料石油焦油、重油、煤油、汽油等高炉煤气、焦炉煤气、气体燃料天然煤气发生炉煤气等冶金工业生产是燃料的巨大消耗者,冶金工作者必须熟悉各种燃料的性质,会正确选用,并能合理组织燃烧过程,以降低燃料消耗量。
2、常用燃料的特性常用燃料的特性主要包括以下两方面:第一:燃料的化学组成。
必须分清哪些组成物是发热的,哪些组成物是有害的。
第二:燃料的发热能力。
这是评价燃料质量的重要指标。
⑴燃料的化学组成及其成分换算① 气体燃料的化学组成及干湿成分换算气体燃料是由几种较简单的化合物所组成的机械混合体。
其中:CO、H2、CH4、C2H4、C m H n、H2S等是可燃性气体成分,能燃烧放出热量。
CO2、N2、SO2、H2O、O2等则是不燃成分,不能燃烧放热,故其含量均不宜过多,以免降低燃料的发热能力。
C m H n总称为重碳氢化合物,,包括C3H6、C2H6、C2H2……等。
每单位体积(m2)重碳氢化合物燃烧,约放出71176 kJ热量。
气体燃料中的氧,在高温预热的情况下,能与可燃成分作用,从而降低气体燃料燃烧时的放热量。





燃烧和燃料的概念及其实验方法是什么燃烧是一种物质发生氧化反应时所释放的能量,是化学学科的一个重要领域。
而燃料则是燃烧过程中所需要的物质。
那么,燃烧和燃料的定义是什么?燃烧是指化学反应中有机物和无机物在空气中或氧气中与氧发生反应,释放出大量的热与光能,转化为气体和灰渣的过程。
而燃料则是一种被用来供给燃烧所需化学能的物质,这些物质可以是任何形式的化学物质,例如木材、石油、天然气等。
燃料的主要特点是含有的化学能可以通过反应与氧结合而被释放。
那么,在现实生活中,我们如何进行燃烧和燃料的实验呢?一、燃烧的实验方法1、燃烧中几个参数的测量:在燃烧中,可以测量不同方面的性能参数,如燃烧速度、热量、气体生成量等等。
2、燃烧温度和火焰形态的测量:燃烧时,可以通过悬挂一个热电偶并从中测出温度来确定燃烧过程中的燃烧温度。
通过对燃烧流体的速度,激波和火焰扩散等性质的研究还可以了解燃烧过程的特征。
同时,使用高速摄影仪可以观察燃烧火焰的特点。
3、热过程的研究:燃烧的热过程是燃烧过程中重要的部分。
精密的热量计可以被用来测量燃烧过程中的热能,并用于计算其他参数,如燃料的热能密度。
4、燃料的颗粒:燃料中的颗粒可以用来研究燃烧的速度和稳定性。
使用高分辨率的显微镜可以观察颗粒的尺寸、形状、排布等特征。
二、燃料的实验方法1、组成分析:燃料的组成可以通过其化学和物理特性测定。
如,测定其沸点范围、密度、折射率、水溶性和酸度,以及离子色谱分析和原子发射光谱分析等。
2、燃料使用特性:燃料使用特性可以是在低压下的燃烧点火和传输性能以及在高温和高压下的燃烧和爆炸的分析。
3、燃料的物理特性:燃料的物理特性包括燃料的物理性质、力学性质和热力学特性(例如比热、热传导系数、热膨胀系数和焓等)。
4、燃料的热量测定:燃料的热量可以用于计算能源转换过程中的能储存和输出。
燃料的热值可以通过测定燃烧体系下辐射热输出、燃烧后生成的烟气的温度或生成的气体的成分来计算。
2 燃料及燃烧2.l 冶金企业常用燃料1、概述燃料的定义:凡燃烧时能放出大量的热,该热量能经济而有效地用于现代工业生产或日常生活的所有物质,统称燃料。
冶金生产大多数需要在高温下进行,其所需热量,除电炉外,大部分仍靠燃烧燃料供给,所以燃料是冶金生产不可缺少的重要原材料之一。
冶金生产所使用的燃料,一般应具备如下条件:(l) 燃烧所放出的热量必须满足生产工艺要求;(2) 便于控制和调节燃烧过程;(3) 蕴藏量丰富,成本低,使用方便;(4) 燃烧产物必须是气体,对人、动植物、厂房、设备等无害。
燃料的种类很多,按物态可分为固体燃料、液体燃料和气体燃料三类;按来源可分为天然产品和加工产品两种。
工业用燃料分类见表2—1。
燃料的一般分类表表2—1燃料的固态来源天然产品加工产品固体燃料木柴、煤、油页岩等木炭、焦炭、粉煤液体燃料石油焦油、重油、煤油、汽油等气体燃料天然煤气高炉煤气、焦炉煤气、发生炉煤气等冶金工业生产是燃料的巨大消耗者,冶金工作者必须熟悉各种燃料的性质,会正确选用,并能合理组织燃烧过程,以降低燃料消耗量。
2、常用燃料的特性常用燃料的特性主要包括以下两方面:第一:燃料的化学组成。
必须分清哪些组成物是发热的,哪些组成物是有害的。
第二:燃料的发热能力。
这是评价燃料质量的重要指标。
⑴燃料的化学组成及其成分换算①气体燃料的化学组成及干湿成分换算气体燃料是由几种较简单的化合物所组成的机械混合体。
其中:CO、H2、CH4、C2H4、C m H n、H2S等是可燃性气体成分,能燃烧放出热量。
CO2、N2、SO2、H2O、O2等则是不燃成分,不能燃烧放热,故其含量均不宜过多,以免降低燃料的发热能力。
C m H n总称为重碳氢化合物,,包括C3H6、C2H6、C2H2……等。
每单位体积(m2)重碳氢化合物燃烧,约放出71176 kJ热量。
气体燃料中的氧,在高温预热的情况下,能与可燃成分作用,从而降低气体燃料燃烧时的放热量。
若氧的含量超过一定数量,则有爆炸危险。
因此,氧的含量应受到限制,一般应小于0.2%。
气体燃料的成分系以各组成物的体积百分数表示。
具体表示方法有湿成分和干成分两种:湿成分包括水分在内,即:CO湿+ H2湿+CH4湿+N2湿+……+H2O 湿=100%干成分不包括水分在内,即:CO 干+ H 2干+CH 4干+N 2干+……=100% 式中:CO 湿、H 2湿……等符号分别代表湿气体燃料中各成分的体积百分含量;CO 干、H 2干……等符号则分别代表干燥气体燃料中各成分的体积百分含量。
气体燃料的湿成分只能代表某一固定温度下的气体燃料的成分。
故不具有代表性,在一般的情况下气体燃料的化学组成用干成分表示,而气体燃料在使用时所具有的实际成分为湿成分,所以湿成分是气体燃料的供用成分,在进行燃烧计算时必须以湿成分为依据。
气体燃料的干、湿成分之间可以进行换算,其换算式以CO 为例为:气体燃料中的其它各项成分均可依照类似的公式进行换算. 式中:H 2O 湿为湿气体燃料中水分的体积百分含量。
用1 m 3干气体所能吸收的水蒸汽的质量(克)来表示,即用符号干O H 2g 代表饱和水蒸汽的含量,则干O H 2g 的单位是g/m 3干气体。
进行干湿成分的换算时,必须首先把干O H 2g 变成H 2O 湿:式中:0.00124——1克水蒸汽的体积。
②液体和固体燃料的化学组成及各成分的换算a、液体和固体燃料的化学组成固体和液体燃料虽然物理状态及化学分子结构不同,但它们的化学元素成分都相同,都是由碳、氢、氧、氮、硫等五种元素所组成。
此外,固体和液体燃料中还含有水分和一些矿物杂质(通常统称灰分)。
上述七种物质就是固体和液体燃料的化学组成。
其中碳与氢燃烧并大量放热是主要组成物,硫虽能燃烧放热,但生成物SO2有害,氮、氧、灰分、水分则都不能放热。
分述如下:碳[C]:是固体和液体燃料的主要成分。
固体燃料中碳的含量变动在50~90%之间,液体燃料中碳含量一般在85%以上。
碳完全燃烧生成CO2,氧气不足时则不完全燃烧生成CO。
根据化学反应式可看出:氧充足时,碳完全燃烧,所放出的热量多。
因此不需要CO气氛(即还原性气氛)的情况下,应避免碳不完全燃烧。
氢[H]:是固体和液体燃料的第二主要成分。
在燃烧中有两种存在形式:一种叫可燃氢,燃烧时能大量放热;另一种叫化合氢,与氧结合为水,不能燃烧放热。
单位重量的氢燃烧所放出的热量,比单位重量的碳多几倍,但氢在固、液体燃料中的含量少,故起作用仍次于碳。
氢燃烧生成水,水呈蒸汽状态时。
氮[N2]:氮不参加燃烧反应,不能放热,是燃料中的惰性物质。
氮存在时相对降低了碳、氢等可燃物的含量,但因含量较少,通常只有l~2%左右,故危害不大。
燃料燃烧后氮仍以本身形态进入废气。
氧[O]:氧是固、液体燃料中的有害组成物,它不能燃烧,也不能助燃。
硫[S]:是有害组成物,在燃料中有三种存在形式:(1)有机硫;(2)黄铁矿硫;(3)硫酸盐硫。
水分[H2O]:是有害组成物。
本身不能放热,还要吸收大量热以加热其蒸汽至燃烧产物的温度。
灰分[A]:是最有害的组成物。
燃料中的灰分就是一些不能燃烧的矿物杂质,如SO2、A12O3、CaO、Fe2O3等。
b、固体和液体燃料的成分:表示方法有四种:第一:供用成分C用+ H用+ O用+ N用+S用+A用+W用=100%C用、H用、O用……为实用燃料中各成分的百分含量,简称供用成分或供用质。
固体和液体燃料中各成分的百分含量是重量百分含量,供用成分则是进行燃烧计算的依据。
第二:干燥成分C干+ H干+ O干+N干+S干+A干=100%第三:可燃成分C燃+H燃+O燃+N燃+S燃=100%第四:有机成分C机+H机+ O机+N机=100%c、换算方法上述四种成分表示方法之间可以相互换算,换算方法如下:设有100kg工作燃料,分析结果知其中含C——50kg,W——20Kg,A——10Kg,……以供用成分表示:C用——50%,W用——20%,H用——10%……今将其换算为干燥成分,根据定义知:把各量代入并将上式稍加变化,则:同理亦可将其换算成为可燃成分,即:以上各式中的用W 100100-及用用A W 100100--等称为成分换算系数。
在进行燃烧计算时,必须将已知成分换算成供用成分。
3、燃料的发热量燃料发热量的高低是衡量燃料价值的重要指标。
A 、发热量的概念发热量的定义:单位质量或单位体积的燃料在完全燃烧情况下所能放出热量的千焦数叫做燃料的发热量。
对固体、液体燃料而言,发热量的单位是kJ/kg ;对气体燃料而言则以kg/m 3表示,发热量的代表符号一般以Q 表示。
燃料中含有水和氢,氢燃烧后也生成水,燃料燃烧后该两部分水均进入废气。
由于废气中水的存在状态不同,放出的热量不一样。
如果废气中的水均冷却成0℃的液态水,则放出的热量多。
反之,如果冷却成20℃的水蒸气,则放出的热量少。
为了把二者区分开,通常把前者叫燃料的高发热量,用Q 高表示。
后者为燃料的低发热量,用Q 低表示。
固、液体燃料高低发热量可用下式进行换算:Q高—Q低=25(W用+9H用) kJ/kgB、发热量计算式计算原理是根据燃料中各可燃成分的燃烧热,乘以相应成分的百分数,加起来就等于整个燃料的发热量。
固体、液体的低发热量计算式如下:Q低=339C用+1030H用—109(O用—S用)—25W用kJ/kg式中: C用、H用……分别代表供用燃料中各组成物质量百分含量的绝对值,例如C用=75%,即以75代入。
气体燃料的低发热量计算式如下:湿湿湿湿湿湿低S1H238CmH.711H7C.5986CH.593108H7CO.127Q2n4242+++ ++=C、标准燃料所谓标准燃料是指发热量等于29308kJ的燃料。
例如,某燃料的发热量为26377kJ,则它的发热量相当于26377÷29308=0.9kg标准燃料。
因此,消耗1吨该种燃料相当于消耗了0.9吨标准燃料。
4、常用燃料的种类、性质和用途(1)冶金生产中常用煤气的种类和性质冶金生产常用煤气有高炉煤气,焦炉煤气,发生炉煤气,天然煤气。
A、高炉煤气高炉煤气是炼铁生产的副产品,冶炼每吨生铁大约得到4000标米3的煤气。
其中主要可燃成分为CO,含量随着炼铁生产波动而波动,一般不超过三分之一。
大量是不可燃的N2,含量超过50%,CO2含量超过10%,高炉煤气发热量很低,仅3560~3980kJ/m3,一般与焦炉煤气混合使用。
B、焦炉煤气焦炉煤气是炼焦生产的副产品,每炼一吨焦炭大约得到300~380标米3煤气。
其中主要成分是H2,含量超过50%,其次是CH4,含量占25%,其余是少量CO、N2、CO2、H2S等。
焦炉煤气发热量比较高,可达16750~l8840kJ/m3,一般做为民用燃料,也可与高炉煤气混合使用。
C、发生炉煤气在没有高炉煤气和焦炉煤气的地区,可以将固体燃料直接加工得到发生炉煤气,其主要成分是CO,含量不到三分之一,其次是H2,含量可达10%,不燃成分主要是N2,含量超过50%,发生炉煤气发热量比较低,仅5020~6280kJ/m3。
D、天然气天然气是一种发热量很高的优质燃料,它的主要可燃成分是甲烷CH4,含量在80%以上,发热量约为3490~37680kJ/m3,理论燃烧温度高达1090℃。
E、使用煤气安全知识使用煤气要注意安全。
输送管道要严密无缝隙。
防毒、防爆,严格遵守煤气安全制度。
煤气能和空气构成爆炸性混合物,所以煤气管道要避免混入空气,一般保持煤气管内是正压,以免在管内发生爆炸事故。
由于输送管道保持正压,煤气管道必须严防漏气,以免煤气逸出,引起中毒或厂房内形成爆炸性混合物。
一般有煤气设备的厂房内必须装抽风机以改善通风条件,严禁烟火,采取措施预防某些机器开动时火花的形成。
煤气设备及管道上应安装发声、发光或其他低压警报器或指示仪器,以提醒工作人员及时处理。
一般指示灯亮或煤气降压铃响后,应立即关闭阀门,防止回火。
为了减弱爆炸的破坏力,煤气设备上应安装安全阀。
在煤气管道的个别地方应设有放散管,直通车间房顶外,以便发现可疑情况时能将煤气放散到大气中。
煤气管道在与煤气系统接通时,应首先用蒸汽将管道内的空气经放散管吹净。
2、液体燃料液体燃料包括汽油、煤油、柴油及重油等。
冶金炉及其他工业炉用的液体燃料主要是重油。
重油较稠浓,为黑褐色或绿褐色,发热量高达39780~41870kJ/kg。
为了能够安全和有效地使用重油,必须掌握下列几点:(1)重油的粘度粘度是表示流体质点之间内摩擦力大小的一个物理指标。
重油的粘度随温度的升高而显著降低。
为了便于输送和燃烧,必须把重油加热,以便降低粘度,提高其流动性和雾化性。
重油粘度表示的方法:我国通常用恩氏粘度(°E)表示,它是用恩格拉粘度计测出的粘度,其定义是:(2) 重油的闪点将重油在规定条件下加热,重油随温度的升高有可燃蒸汽挥发出来,可燃蒸汽与周围空气混合后,当接触外界火源时,能发生闪火现象,也就是爆炸燃烧的现象。