【化学】化学方程式练习题(含答案)
- 格式:docx
- 大小:78.47 KB
- 文档页数:11

【化学】 化学方程式的计算练习题(含答案)经典一、中考化学方程式的计算1.碳酸氢钠用于焙制糕点,在270℃时分解:323222NaHCO Na C ΔO H O CO ++↑。
现取3NaHCO 16.8g ,在敞口容器中加热到质量不再改变为止,减少的质量为( ) A .4.4gB .6.2gC .8.8gD .10.6g【答案】B【解析】【分析】【详解】根据题意可知,在敞口容器中加热到质量不再改变为止,剩余物质为固体碳酸钠。
此题为固体的差量计算,设减少的质量为x 。
323222NaHCO Na CO +H O +CO 1681066216.8g x ↑△固体减少的质量16816.8g =62xx=6.2g2.铝被称为“年轻的金属”,工业上用电解氧化铝的方法制取金属铝。
反应的化学方程式为2Al 2O 3通电 4Al +3O 2↑。
请计算生成1.08t 金属铝,理论上需要氧化铝的质量是多少____?【答案】2.04t【解析】【分析】【详解】解:设生成1.08t 金属铝,理论上需要氧化铝的质量为x 2322Al O 4Al +3O 204108x 1.08t↑通电 204x =108 1.08tx=2.04t答:生成1.08t 金属铝,理论上需要氧化铝的质量为2.04t 。
3.我国科学家实现电催化高效分解硫化氢制氢技术,反应的化学方程式为H 2S 一定条件S ↓ +H 2 .请计算生产 3吨 H 2,理论上需要 H 2S 多少吨?【答案】51吨【解析】【分析】【详解】解:设理论上需要H 2S 的质量为x22S +H 342x3tH S ↓一定条件34x =23tx=51 t答:理论上需要H 2S 51吨。4.某工厂需要16kg 氧气作原料,若用电解水的方法制取这些氧气,消耗水的质量是_________?(要求写出计算过程)【答案】18kg【解析】【分析】【详解】设消耗水的质量为x2222H O2H +O 3632x 16kg↑↑通电 36x =3216kgx=18kg答:消耗水的质量是18kg 。

化学方程式的计算练习题(含答案)一、中考化学方程式的计算1.请根据如图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题:计算稀盐酸中溶质质量。
【答案】7.3g【解析】【分析】【详解】根据质量守恒反应前后物质总质量不变可得二氧化碳的质量等于12g+100g+100g-207.6g=4.4g设稀盐酸中溶质质量为x3222CaCO2HCl=CaCl CO H O7344x 4.4g73x=,x=7.3g44 4.4g++↑+答:稀盐酸中溶质质量7.3g【点睛】根据质量守恒,求出二氧化碳质量,根据二氧化碳质量求稀盐酸中溶质质量2.波尔多液是一种运用广泛的农药,由熟石灰和硫酸铜配制而成。
某工厂用以下反应:2Cu+O2+2H2SO4=2CuSO4+2H2O 来生产硫酸铜,若要制得 40kg 硫酸铜。
试计算:(1)硫酸铜中铜元素质量分数是_____。
(2)若恰好消耗稀硫酸的质量是 200kg,则该稀硫酸溶质的质量分数是多少_____?【答案】40% 12.25%【解析】【分析】【详解】(1)CuSO4中Cu元素质量分数=6464100%=100%=40% 6432416160⨯⨯++⨯。
(2)设消耗的硫酸的质量为x 。
22442H SO 2CuSO 2Cu O 2=2982160x 40kg2H O+++⨯⨯ x 29840kg 2160⨯=⨯ x=24.5kg则稀硫酸溶质的质量分数=24.5kg 100%=12.25%200kg⨯。
3.向 100 克 MgCl 2 和 HCl 的混合溶液中,逐滴加入 10%的氢氧化钠溶液,反应情况,如图所示。
(1)当滴加氢氧化钠溶液的质量至 N 点时所得溶液的 pH 值为_______(填编号); A 大于 7 B 等于 7 C 小于 7(2)通过计算,确定 M 点时所得溶液中溶质的质量分数,写出计算过程____。
【答案】A 9.2%(详见解析)【解析】【分析】向 100 克 MgCl 2 和 HCl 的混合溶液中,逐滴加入 10%的氢氧化钠溶液,氢氧化钠先与盐酸反应,等盐酸完全反应后再与氯化镁反应。



【化学】化学《化学方程式》练习题及答案一、选择题1.下图是甲转化为丙的微观过程。
下列说法不正确...的是A.反应前后原子种类不变B.转化①中甲和O2反应的分子个数比为1:1C.转化②是化合反应D.丙中氢、硫、氧元素的质量比为1:16:32【答案】B【解析】【分析】根据微观示意图可知甲物质是H2S,乙物质是SO2,丙物质是H2SO4。
【详解】A、根据质量守恒定律可知,化学反应前后原子的种类、数目和质量不变,不符合题意;B、转化①发生的化学方程式是2H2S+3O22SO2+2H2O,甲和O2反应的分子个数比为2:3,符合题意;C、转化②是二氧化硫和过氧化氢反应生成硫酸,是多种物质反应生成一种物质,属于化合反应,不符合题意;D、丙中氢、硫、氧元素的质量比⨯⨯⨯=::::,不符合题意。
故选B。
12321164116322.某金属单质 X与非金属单质Y可发生反应:2X+Y=X2Y。
某实验探究小组进行了两次实验,测得数据如下表:实验序号X的用量/g Y的用量/g生成X2Y的质量/g17.4 1.68.029.6 3.212.0参加反应的X与Y的质量比为 ( )A.4:1 B.3:1 C.2:1 D.37:8【答案】A【解析】【分析】【详解】由两次实验数据表,Y的用量增加1倍,而生成X2Y的质量却没有增加1倍,说明第2次反应时,Y有剩余,9.6gX完全反应,生成12.0gX2Y,则同时参加反应的Y的质量为12.0g﹣9.6g=2.4g;故参加反应的X与Y的质量比为9.6g:2.4g=4:1.故选A.3.某仓库工作人员违章操作,在雨天转运“保险粉”引起爆炸。
“保险粉”化学名为连二亚硫酸钠(Na2S2O4),主要用于印染工业。
该化学品在潮湿空气中极不稳定,易分解并引起燃烧,反应的化学方程式为:2Na2S2O4=Na2S2O3+Na2SO3+X。
下列有关说法错误的是A.X 的化学式为 SO2B.连二亚硫酸钠与水能剧烈反应,化学性质很活泼C.Na2SO3 是一种盐,其中硫元素的化合价为+3 价D.Na2S2O4 通常要在干燥阴凉处密闭贮存【答案】C【解析】【详解】A、由反应的化学方程式为2Na2S2O4=Na2S2O3+Na2SO3+X,Na原子个数前后相等,由S、O 原子个数守恒,则X的化学式为SO2,说法正确,不符合题意;B、连二亚硫酸钠在潮湿空气中极不稳定,易分解并引起燃烧,说法正确,不符合题意;C、Na2SO3中Na元素为+1价,O元素为-2价,则由化合物中正负化合价的代数和为0可知,S元素的化合价为+4价,说法错误,符合题意;D、由该化学品在潮湿空气中极不稳定,易分解并引起燃烧可知,该物质应在干燥阴凉处密闭贮存,说法正确,不符合题意。


【化学】化学化学方程式的计算题20套(带答案)一、中考化学方程式的计算1.欲测得某块大理石中所含碳酸钙的含量,现取该大理石加入到足量稀盐酸中(杂质不与稀盐酸反应),产生CO2的质量与稀盐酸的质量关系如图所示,请计算。
(1)该实验中最多制得CO2的质量为_____。
(2)该大理石中所含碳酸钙的质量_____(写出计算过程)。
【答案】8.8g 20g【解析】【分析】碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳。
【详解】(1)由图像可知,该实验中最多制得CO2的质量为8. 8g。
(2)设该大理石中碳酸钙的质量为x3222CaCO+2HCl=CaCl+H O+CO10044x8.8g100x =448.8gx=20g答:大理石中所含碳酸钙的质量为20g。
2.请根据如图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题:计算稀盐酸中溶质质量。
【答案】7.3g【解析】【分析】【详解】根据质量守恒反应前后物质总质量不变可得二氧化碳的质量等于12g+100g+100g-207.6g=4.4g设稀盐酸中溶质质量为x3222CaCO2HCl=CaCl CO H O7344x 4.4g73x=,x=7.3g44 4.4g++↑+答:稀盐酸中溶质质量7.3g【点睛】根据质量守恒,求出二氧化碳质量,根据二氧化碳质量求稀盐酸中溶质质量3.有一种自生氧防毒面具,其使用的生氧剂的主要成分是(KO2)。
取100g生氧剂放入质量为20g的烧杯中,再向其中加入20g水,使生氧剂KO2全部反应,其充分反应后(4KO2+2H2O═4KOH+3O2↑),称得烧杯及烧杯中物质的总质量为116g,计算(假设杂质不含钾元素且不与稀硫酸反应)(1)100g生氧剂生成氧气的质量_____;(2)KO2中钾元素的质量分数为_____;(计算结果精确到 0.1%)(3)要将烧杯中的溶液完全中和,通过计算,需要溶质质量分数为10%的稀硫酸溶液的质量_____。

化学方程式配平1、化学方程式配平常用方法:最小公倍数法、奇数配偶法(先配奇数大):(1) P + O2 P2O5 (2) C + O2CO(3) Al + O2Al2O3 (4)Fe + O2Fe3O4(5) Mg + O2MgO (6) H2O2MnO2 H2O + O2↑(7) H2O H2↑+ O2↑(8) H2+ O2H2O1观察法:先金属后原子团(1)CuSO4 +NaOH —Na2SO4 + Cu(OH)2(2)Mg + HCl —MgCl2+ H2↑(3)Fe2O3 + H2SO4Fe2(SO4)3+ H2O(4)Al + H2SO4 —Al2(SO4)3+ H2↑(5)Fe(OH)3 + H2SO4Fe2(SO4)3+ H2O(6)Al2(SO4)3 +NaOH —Na2SO4 + Al(OH)33配平下列的各个化学反应的方程式:(1)KMnO4—K2MnO4+ MnO2+ O2↑(2)Al + CuSO4 —Al2(SO4)3 + Cu(3)Zn + HCl —ZnCl2 + H2↑(4)Al2O3 + H2SO4Al2(SO4)3 + H2O(5)Fe2(SO4)3+NaOH —Na2SO4+ Fe(OH)3(6)Fe(OH)3+ H2SO4Fe2(SO4)3+ H2O(7)CH4+ O2点燃CO2 + H2O(8) C + CO2高温CO(9)NH3+ O2催化剂NO + H2O(10) CO + Fe2O3高温Fe + CO2二练习1 在X + 2O2===CO2 + 2H2O的反应中,根据质量守恒定律可判断出X的化学式为:()A COB CH4C CH3OHD C2H42某纯净物X在空气中完全燃烧,反应式为:X + 3 O2=== 2CO2 + 3 H2O,根据质量守恒定律可判断出X的化学式为:()A C2H4B C2H4OC C2H6D C2H6O3在4Cu + 10HNO3 = 4Cu(NO3)3 + X + 5H2O反应方程式中,X的化学式为:()A NOB NO2C N2OD N2O34物质X和B2能发生下列反应:2X + B2 = 2 AB3,则X的化学式是:()A AB2B A2B2C AB3D A2B35某化合物R在空气燃烧后生成二氧化碳和水,下列关于R化学式叙述正确的是:()A R一定含有碳,氢,氧三种元素B R一定含有碳和氢元素,不含有氧元素C R一定含有碳和氢元素,可能含有氧元素D R不一定含有碳和氢元素,但一定不含有氧元素6物质W在氧气中燃烧后,生成了4.4克CO2和3.6克的水,消耗的氧气为6.4克,则W中所含有的元素是:()A 一定含有C H元素,不含O元素B 一定含有C H 元素,可能有O元素C 一定含有C H O三种元素D 条件不足,不能判断7氢气与氧气反应生成水的反应过程中,氢气与氧气的质量之比是:()A 1 :1B 2 :1C 2 :32D 4 :328对于质量守恒定律的解释不正确的是:()A 化学反应前后,分子的数目不变B 化学反应前后,原子的种类不变。

【化学】初三化学化学方程式的计算测试卷(有答案)经典一、中考化学方程式的计算1.将部分变质的烧碱配成溶液中后逐滴滴加稀盐酸,产生气体质量与所加稀盐酸质量关系如图所示:(1)当加入稀盐酸至 50g 前,没有气体产生的原因是______________。
(2)完全反应后,产生气体的质量是_____________g。
(3)当滴加稀盐酸至图中 A 点时,溶液中含有的溶质是______________。
(4)计算稀盐酸中溶质的质量分数_______________(写出规范的计算过程)。
【答案】稀盐酸先中和烧碱溶液 2.2 NaCl 7.3%(详见解析)【解析】【分析】烧碱是氢氧化钠的俗称,氢氧化钠容易和空气中的二氧化碳反应生成碳酸钠而变质。
向氢氧化钠和碳酸钠的混合物中滴加盐酸,盐酸先和氢氧化钠发生中和反应,生成氯化钠和水,待氢氧化钠反应完后,盐酸再和碳酸钠反应生成氯化钠、水和二氧化碳。
【详解】(1)将部分变质的烧碱中含有碳酸钠、氢氧化钠,加入稀盐酸先中和烧碱溶液;(2)根据图示可知,完全反应后,产生气体的质量是2.2g;(3)当滴加稀盐酸至图中 A 点时,碳酸钠、氢氧化钠完全反应,溶液中含有的溶质是NaCl;(4)设与碳酸钠反应的 HCl 质量为x则Na CO+2HCl=2NaCl+H O+CO23227344x 2.2g73x=44 2.2gx=3.65g根据图示可知,与碳酸钠反应消耗盐酸的质量=100g-50g=50g,稀盐酸中溶质的质量分数=3.65g100%=7.3% 50g。
答:稀盐酸中溶质的质量分数为7.3%。
2.酸、碱、盐是初中化学学习的重要内容。
(1)盐酸、硫酸等常见的酸都具有相似的化学性质,是因为它们在水溶液中都解离出____________(填离子符号)。
(2)“84消毒液”可有效杀死新冠病毒,某“84消毒液”瓶体部分标签如图所示:①该瓶“84消毒液”中NaClO的质量为_________g。
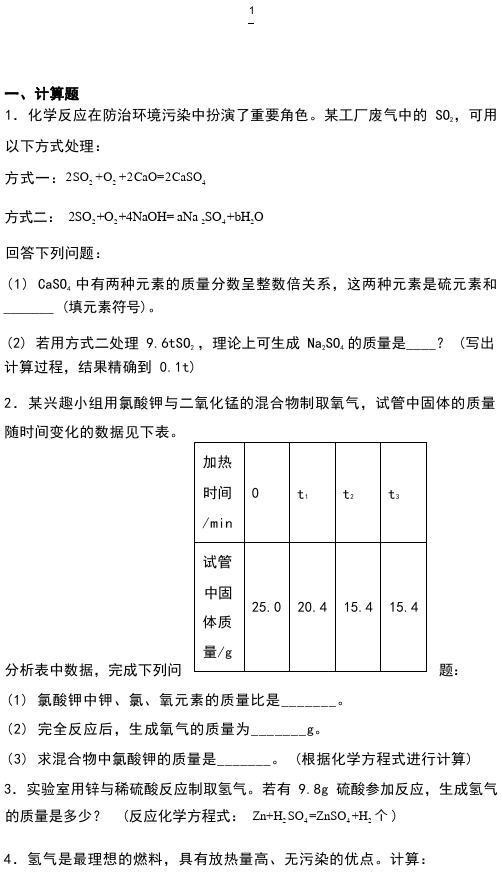
1.化学反应在防治环境污染中扮演了重要角色。
某工厂废气中的 SO2,可用以下方式处理:方式一:2SO2 +O2+2CaO=2CaSO4方式二:2SO2 +O2 +4NaOH= aNa 2SO4 +bH2O回答下列问题:(1) CaSO4中有两种元素的质量分数呈整数倍关系,这两种元素是硫元素和_______ (填元素符号)。
(2) 若用方式二处理 9.6tSO2 ,理论上可生成 Na2SO4的质量是____? (写出计算过程,结果精确到 0.1t)2.某兴趣小组用氯酸钾与二氧化锰的混合物制取氧气,试管中固体的质量随时间变化的数据见下表。
(1) 氯酸钾中钾、氯、氧元素的质量比是_______。
(2) 完全反应后,生成氧气的质量为_______g。
(3) 求混合物中氯酸钾的质量是_______。
(根据化学方程式进行计算) 3.实验室用锌与稀硫酸反应制取氢气。
若有 9.8g 硫酸参加反应,生成氢气的质量是多少? (反应化学方程式:Zn+H2 SO4=ZnSO4+H2个)4.氢气是最理想的燃料,具有放热量高、无污染的优点。
计算:分析表中数据,完成下列问题:(1) 10kg 氢气完全燃烧可生成水的质量是多少?(2) 消耗氧气的质量至少是多少?5.碳酸氢钠固体受热易分解生成一种盐和两种氧化物,反应的化学方程式为______;将 10g 碳酸钠和碳酸氢钠的混合物充分加热至固体的质量不再改变,冷却,称量剩余固体的质量为 6.9g,则原混合物中碳酸钠和碳酸氢钠的质量比为______。
6.实验室常用氯酸钾和二氧化锰的混合物制取氧气。
现有氯酸钾和二氧化锰的混合物 50g,完全反应后称量剩余物质的质量为 40.4g。
请计算:(1) 制得氧气的质量为__________。
(2) 混合物中氯酸钾的质量分数。
7.加热氯酸钾和二氧化锰固体混合物来制取氧气时,反应时间和剩余固体质量的关系如图所示。
计算:的质量是___________g。

化学⽅程式习题化学⽅程式练习题⼀、选择题1、1.6 g某物质在氧⽓中完全燃烧,⽣成4.4 g⼆氧化碳和3.6 g⽔,关于该物质组成的推断正确的是() A.只含碳、氢两种元素 B.⼀定含有碳、氢元素,可能含有氧元素C.⼀定含有碳、氢、氧三种元素D.⽆法确定2、在反应A+B C+2D中,已知2.9 g A跟4.9 g B完全反应,⽣成6.0 g C,⼜知道D的相对分⼦质量为18,则A的相对分⼦质量是( )A.40B.58C.29D.863、下列化学⽅程式中,正确的是 ( )A.C+O2CO2B.2HgO Hg2+O2↑C.4Fe+3O22Fe2O3D.4P+5O22P2O54、“中国航天,给⼒中国”。
载⼈航天飞船可⽤反应2Na2O2+2CO22R+O2来提供氧⽓,物质R的化学式是( ) A.CO B.Na2OC.NaOHD.Na2CO35、在反应2A+B2C中,1.6 g的A完全反应⽣成2 g C,⼜知B的相对分⼦质量为32,则C的相对分⼦质量为( ) A.28 B.64 C.44 D.806、⼩明同学从S+O2SO2中获得以下信息:①该反应反应物是硫和氧⽓;②反应条件是点燃;③反应前后元素种类和原⼦个数不变;④反应前后分⼦总数保持不变;⑤参加反应的硫和氧⽓的质量⽐为2∶1。
其中正确的信息是( )A.①②④⑤B.①②③C.④⑤D.①②③⑤7、化学反应前后,下列各项中,肯定没有变化的是( )①原⼦数⽬②原⼦的种类③分⼦数⽬④分⼦的种类⑤元素的种类⑥物质的总质量⑦物质的种类 A.①②⑤⑥ B.①②③⑤ C.①②⑤⑦ D.③④⑥⑦8、在化学反应2A+B2====2AB中,A与B2反应的质量关系如图所⽰,现将6 g A和8 g B2充分反应,则⽣成AB的质量为( )A.9 gB.11 gC.12 gD.14 g9、下列说法正确的是( )A.蜡烛燃烧后,看不到有其他物质⽣成,因此不存在守恒B.铁⽣锈后,铁锈的质量⼀定等于铁的质量C.在化学反应A+B C+D中,所加⼊的反应物A、B的质量分别为ag和bg,反应的⽣成物C、D 的质量分别为cg和dg,则a+b=c+d的关系⼀定成⽴D.催化剂可以改变其他物质的化学反应速率,有催化剂参加的反应,遵守质量守恒定律10、如图所⽰,⼆分⼦的甲反应⽣成⼆分⼦的⼄与⼀分⼦的丙,已知甲、⼄、丙三者为不同的纯净物。

【化学】化学化学方程式的计算题20套(带答案)及解析一、中考化学方程式的计算1.在盛有24.3g 硫酸钠和氯化钠组成的固体混合物的烧杯中,加入100g 水使硫酸钠和氯化钠全部溶解。
向其中逐渐滴加溶质质量分数为20%的氯化钡溶液。
生成沉淀的总质量与所滴入氯化钡溶液的质量关系曲线如图Z7-6所示,请根据题意回答问题。
(1)过程中观察到的现象_____。
(2)滴加到B 点时,溶液中的溶质是_____(填化学式)。
(3)当滴加氯化钡溶液至图中A 点时,所得溶液中溶质的质量分数。
_____(结果保留一位小数)【答案】生成白色沉淀,溶液变浑浊; NaCl 和BaCl 2 10.6%【解析】【分析】【详解】(1)硫酸钠和氯化钡生成硫酸钡沉淀和氯化钠,所以会看到有白色沉淀生成,故填:生成白色沉淀,溶液变浑浊;(2)硫酸钠和氯化钡生成硫酸钡沉淀和氯化钠,A 点表示恰好完全反应,此时溶质为氯化钠,B 点表示氯化钡过量,此时溶质为氯化钡和氯化钠,故填:NaCl 和BaCl 2; (3)当滴加氯化钡溶液至图中A 点时,所得溶液中溶质为氯化钠设生成氯化钠质量为x 反应硫酸钠质量为y ,生成沉淀质量为z 。
2244BaCl Na SO BaSO 2NaCl 208142233117104g 20%y z x 208104g 20%208104g 20%208104g 20%===117x 142y 233zx=11.7g y=14.2g z=23.3g+=↓+⨯⨯⨯⨯,,,,反应后氯化钠质量为:11.7g+(24.3g-14.2g)=21.8g ,反应后溶液质量为:24.3g+100g+104g-23.3g=205g,反应后溶液质量分数为;21.8g 100%10.6%205g ⨯≈ 答:溶质质量分数为10.6%2.如图是某胃药标签的部分内容,某校同学测定该药品 中 NaHCO 3 含量的过程如下:取 10 粒该药剂研碎后放入烧杯中,加入 50g 水后充分搅拌,再向其中滴加稀盐酸至恰好完全反应(已知药品中的其它成分既不溶于水,也不与稀盐酸反应),共消耗稀盐酸 11.5g 。
【化学】化学《化学方程式》练习题及答案一、选择题1.在一个密闭容器内有四种物质,一定条件下充分反应后,测得反应前后各物质的质量如表,下列推理正确的是物质X Y Z Q反应前质量/g410121反应后质量/g01215待测A.反应物是X和Y,成物是Q和ZB.参加反应的Y和Q的质量比是1∶1C.参加反应的X与Q的质量比是1∶3D.反应后生成15 g Z【答案】C【解析】由表中数据分析可知,反应前后X的质量减少了4 g﹣0 g=4 g,故X是反应物,参加反应的X的质量为4 g;反应前后Y的质量增加了12 g﹣10 g=2 g,故Y是生成物;同理确定Z 是生成物,生成的Z的质量为15 g﹣1 g=14 g;由质量守恒定律,Q应是反应物,且参加反应的Q的质量为14 g+2 g﹣4 g=12 g,故待测的数值为21g﹣12 g=9 g。
A、根据分析,可知反应物是X和Q,生成物是Y和Z,故选项说法错误;B、参加反应的Y的质量为12 g ﹣10 g=2 g,参加反应的Q的质量为14 g+2 g﹣4 g=12 g,故参加反应的Y和Q的质量比是1∶6,故选项说法错误;C、参加反应中X、Q的质量比为4 g∶12 g=1∶3,故选项说法正确;D、根据表格中的数据,反应后生成Z的质量为15 g﹣1 g=14 g,故选项说法错误。
故选C。
2.如图为某反应的微观示意图,下列说法正确的是()A.该反应属于分解反应B.反应前后分子种类没有改变C.反应前后原子数目发生改变D.参加反应的两种分子个数比为1:1【答案】D【解析】A、根据图可知:两种单质生成一种化合物,属于化合反应,不属于分解反应,故错误;B、根据图可知:氢分子和氯分子变化成了氯化氢分子,反应前后分子种类发生了改变,故错误;C 、由微粒的变化可知,反应前后原子数目没有发生改变,故错误;D 、由微粒的变化可知,参加反应的两种分子个数比为1:1,故正确。
点睛:化学反应的实质一般是指在化学变化中,分子分成原子,原子重新组合成新的分子(或直接聚集构成新物质)。


【化学】化学《化学方程式》练习题及答案一、选择题1.CH 4和某种氮的氧化物反应的化学方程式为CH 4+2口催化剂N 2+CO 2+2H 2O ,则框内物质的化学式是 A .NO B .NO 2C .N 2OD .N 2O 5【答案】B 【解析】试题分析:化学变化前后各种原子的个数不变,反应后有2N 、C 、4H 、4O ,而反应前有4H 、一个C 原子,反应前后差2N 、4O ,所以框内物质的化学式为NO 2,故选B 考点:质量守恒定律的应用2.将一定质量的氧化铜和氧化铁混合粉末与足量的CO 充分反应后,测得质量减少了4.0g 。
另取等质量的该粉末用适量的稀硫酸完全溶解后,再加入足量的氢氧化钠溶液,得到了20.5g 的沉淀。
则粉末中的氧化铜的质量分数为 A .20% B .40%C .50%D .80%【答案】C 【解析】 【分析】分别假设氧化铜和氧化铁的质量,进而结合化学方程式、关系式及对应的数据求解,进而求出粉末中氧化铜的质量分数。
【详解】设粉末中氧化铜的质量为x ,氧化铁的质量为y ,21CO +CuO Cu +CO 806416x m 高温固体质量减少116x xm ==80523223CO +Fe O 2Fe +3CO 16011248ym 高温固体质量减少248y 3ym ==16010氧化铜与稀硫酸反应生成硫酸铜和水,硫酸铜与氢氧化钠反应生成氢氧化铜沉淀和硫酸钠;氧化铁和稀硫酸反应生成硫酸铁和水,硫酸铁和氢氧化钠反应生成氢氧化铁沉淀和硫酸钠,根据元素守恒列关系式:423CuO ~CuSO ~Cu(OH)8098xm398x 49xm ==80402324334Fe O ~Fe (SO )~2Fe(OH)160214ym4214y 107ym ==16080结合题干,列出方程:x 3y+=4.051049x 107y+=20.54080解得x=8g ,y=8g则粉末中氧化铜的质量分数为:8g100%50%8g+8g⨯= ,故选C 。

化学方程式练习题(含答案)经典一、化学方程式选择题1.科学家采用“组分转化”技术,将 CO2和H2按一定比例混合,在一定条件下反应的化学方程式为2CO2 + 6H2= X + 4H2O中,X的化学式是A.CH4 B.C2H4 C.H2CO3 D.H2C2O4【答案】B【解析】化学反应前后各种原子个数相等,反应前有2C、4O、12H,反应后(X除外)有4O、8H,所以x中有有2C、4H,X的化学式为C2H4,故选B。
点睛:要顺利解答此题,必须熟练掌握质量守恒定律并会灵活应用,化学反应前后各种原子个数相等,根据反应前后原子个数的差量即可推断出X的化学式。
2.某反应前后分子变化的微观示意图如下(图中“●”和“○”分别代表不同元素的原子),下列说法不正确的是()A.该反应前后涉及到三种物质B.反应后分子种类没有改变C.反应后分子数增多D.该反应属于分解反应【答案】B【解析】【详解】由化学反应的微观示意图可知,各物质反应的微粒个数关系是:A、由图示可知,该反应前后涉及到三种物质,故A正确;B、由微粒的变化可知,反应后分子种类发生了改变,故B不正确;C、由微粒的变化可知,该反应后分子数增多,故C正确;D、该反应由一种物质生成了两种物质,属于分解反应,故D正确。
故选B。
【点睛】化学变化中分子的种类一定改变,数目可变可不变。
3.如图表示某个化学反应,据图分析判断,下列各项中,不正确的是A .该反应属于置换反应B .反应中乙、丙两物质质量比为2: 7C .图示中x 的数值为4D .反应前后氢元素的化合价发生了改变【答案】B 【解析】 【分析】由化学反应的微观模型图可知,该反应是在一定条件下氢气与四氯化硅(SiCl 4)反应生成了硅和氯化氢气体,反应的化学方程式为:42SiCl +2H Si+4HCl 一定条件,由方程式可知: 【详解】A 、该反应是一种单质和一种化合物反应生成了另一种单质和另一种化合物,属于置换反应,故A 正确;B 、反应中乙、丙两物质质量比就是氢气和硅的质量比为:(2×1×2):28=1:7,故B 不正确;C 、由方程式可知,图示中x 的数值为4,故C 正确;D 、由方程式可知,氢元素的化合价由0价变成了+1价,故D 正确。
《化学方程式》练习题(含答案)一、单选题1. 实验室加热一定质量的高锰酸钾制氧气,各物理量随加热时间变化的图像正确的是( )A. B.C. D.2. 下列关于2C+O22CO的说法中,正确的是( )A. 表示碳加氧气等于一氧化碳B. 该反应中,分子、原子的种类均发生了改变C. 参加反应的碳与氧气的质量比为3:8D. 参加反应的氧气与生成的一氧化碳的分子个数比为1:23. 化学反应前后肯定没有发生变化的是( ) ①原子数目; ②分子数目; ③元素种类; ④物质种类; ⑤原子种类; ⑥物质的总质量A. ① ④ ⑥B. ① ③ ⑤ ⑥C. ① ② ⑥D. ② ③ ⑤4. 乙烷(C2H6)是重要的化工原料,与氯气反应前后分子种类变化的微观示意图如图。
下列说法正确的是( )A. 甲中碳、氢元素质量比为1:3B. 乙的相对分子质量为71C. 甲和丙的元素组成相同D. 生成丙与丁的分子个数比为1:15. 下列化学方程式书写正确的是( )A. Mg+O=点燃MgO2B. 4Fe+3O=点燃2Fe2O32C. 2KMnO4=K2MnO4+MnO2+O2↑D. CO2+Ca(OH)2=CaCO3↓+H2O6. 某化学反应的微观示意图如图所示,下列有关说法正确的是( )A. 该反应的两种反应物均为化合物B. 该反应前后没有发生变化的粒子只有氧原子和氢原子C. 该反应的化学方程式为4NH3+5O24NO+6H2OD. 该反应读成:氨气加氧气在一定条件下生成一氧化氮加水7. 一定质量的某化合物完全燃烧,需要3.2g氧气,生成4.4g二氧化碳和1.8g水。
下列判断错误的是( )A. 参加反应的该化合物的质量为3.0gB. 该化合物中一定含有碳、氢、氧三种元素C. 该化合物中碳、氢、氧的原子个数比为2:4:1D. 该化合物中碳元素的质量分数为40%8. 从2H2+O22H2O中获取的信息错误的是( )A. 在反应前后,元素的种类没有变化B. 在常温下氢气与氧气混合就可以发生反应C. 4g氢气与32g氧气完全反应,可以生成36g水D. 在反应前后,氢原子和氧原子的数目都没有改变9. 漂白粉可用于自来水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO)2]。
【化学】化学化学方程式的计算题20套(带答案)含解析一、中考化学方程式的计算1.硝酸铵是农业生产中常用的化学肥料。
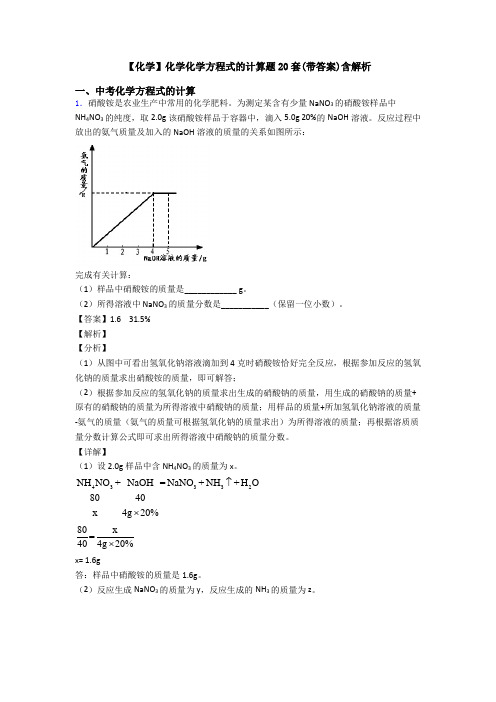
为测定某含有少量NaNO 3的硝酸铵样品中 NH 4NO 3的纯度,取2.0g 该硝酸铵样品于容器中,滴入5.0g 20%的NaOH 溶液。
反应过程中放出的氨气质量及加入的NaOH 溶液的质量的关系如图所示:完成有关计算:(1)样品中硝酸铵的质量是____________ g 。
(2)所得溶液中 NaNO 3的质量分数是___________(保留一位小数)。
【答案】1.6 31.5%【解析】【分析】(1)从图中可看出氢氧化钠溶液滴加到4克时硝酸铵恰好完全反应,根据参加反应的氢氧化钠的质量求出硝酸铵的质量,即可解答;(2)根据参加反应的氢氧化钠的质量求出生成的硝酸钠的质量,用生成的硝酸钠的质量+原有的硝酸钠的质量为所得溶液中硝酸钠的质量;用样品的质量+所加氢氧化钠溶液的质量-氨气的质量(氨气的质量可根据氢氧化钠的质量求出)为所得溶液的质量;再根据溶质质量分数计算公式即可求出所得溶液中硝酸钠的质量分数。
【详解】(1)设2.0g 样品中含NH 4NO 3的质量为x 。
43332NH NO NaOH NaNO NH H O4g 20%+=++8040x ↑⨯48g 0x =4020%⨯ x= 1.6g答:样品中硝酸铵的质量是1.6g 。
(2)反应生成 NaNO 3的质量为 y ,反应生成的NH 3的质量为z 。
43332NH NO NaOH N +=++408517y aNO NH H O40%zg 2↑⨯404g 20%=85y⨯ 404g 20%=17z⨯ y= 1.7gz= 0.34g 反应后所得溶液中NaNO 3的质量分数为= 1.7g+(2g-1.6g)100%=31.5%2g+5g-0.34g⨯ 答:所得溶液中 NaNO 3的质量分数是31.5%。
【点睛】做本道题时要将4克氢氧化钠溶液和5克氢氧化钠溶液区分清,不能乱用,参加反应的氢氧化钠溶液的质量是4克,所加的氢氧化钠溶液的质量是5克。

化学方程式的计算练习题附答案一、初中化学利用化学方程式选择题1.在加热条件下,将一定量的一氧化碳气体通过12g氧化铜粉末,充分反应后,将生成的气体通入足量氢氧化钠溶液中,测得溶液增重4.4g,则加热后得到的固体混合物中,铜、氧元素的质量比为A.14:1 B.12:1 C.8:1 D.4:12.密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:下列说法不正确的是A.X的值为165.6B.该反应可能为复分解反应C.反应过程中,B与D的质量比为36∶142D.若A与C的相对分子质量之比为98∶40,则A与C的化学计量数比为2∶13.25℃时,某气态碳氢化合物与氧气混合后装入密闭容器中,经充分反应后,又恢复25℃,此时容器内气体分子是反应前的一半。
再经足量的氢氧化钠溶液吸收后,容器内几乎成真空。
此碳氢化合物可能是( )A.CH4 B.C2H6 C.C2H2 D.C3H84.科学家最新发现,可以将树木纤维素转变为超级储能装置,该反应的微观示意图如下。
下列说法正确的是A.反应前后分子总数不变B.反应中 X、Z 两种物质的质量比为 3:7C.反应中 Y 和 W 的物质的量之比为 4:5D.参加反应的 Y 中氮元素的质量一定等于生成 Z 的质量5.向一定量的锌粉中滴加稀盐酸至过量,下图表示反应过程中某种物质的质量m随加入盐酸质量的变化关系,则m不可能表示()A.溶液总质量B.消耗锌粉的质量C.生成ZnCl2的质量D.生成H2的质量6.关于化学反应2X+Y=2Z的叙述正确的是()A.Z可能是单质,也可能是化合物B.反应中X、Y、Z三种物质的质量比是2:1:2C.若X和Y的相对分子质量分别为M和N,则Z的相对分子质量为M+ND.若ag的X完全反应生成bg的Z,则同时消耗(b﹣a)g 的Y7.已知2A+3B==C+3D,用足量的A和49 g B恰好完全反应,生成57 g C和1 g D,若B 的相对分子质量为98,则A的相对分子质量为( )A.16 B.27 C.44 D.568.如图所示:在密闭容器中充入CO和2CO的混合物10g,测得其中氧元素含量为64%,再向密闭容器中通入足量的氧气,通电使电火花塞点火让其中的一氧化碳完全燃烧成二氧化碳。

初二化学化学方程式练习题及答案一、填空题1. 氢气燃烧会生成__________。
答案:水2. 铁(Fe)和硫(S)反应会生成__________。
答案:硫化铁(FeS)3. 氧气和铁(Fe)反应会生成__________。
答案:氧化铁(Fe2O3)4. 碳(C)和氧气反应会生成__________。
答案:二氧化碳(CO2)5. 氯气和钠(S)反应会生成__________。
答案:氯化钠(NaCl)6. 氧气和氢气反应会生成__________。
答案:水7. 氢气和氯气反应会生成__________。
答案:氯化氢(HCl)8. 碳酸氢钠(NaHCO3)分解会生成__________。
答案:二氧化碳(CO2)、水(H2O)、碳酸钠(Na2CO3)9. 氯化铜(CuCl2)和氢气反应会生成__________。
答案:铜(Cu)和盐酸(HCl)10. 二氧化硫(SO2)加水会生成__________。
答案:亚硫酸(H2SO3)二、简答题1. 什么是化学方程式?请用一个例子解释。
答案:化学方程式是用化学符号和化学式来表示化学反应的式子。
例如:化学方程式2H2 + O2 → 2H2O可以用来表示氢气和氧气反应生成水的化学反应。
2. 化学方程式中的反应物和生成物分别是什么?答案:反应物是化学反应开始时存在的物质,生成物是化学反应结束时产生的物质。
3. 如何平衡化学方程式?请以氮气和氢气反应生成氨气的方程式为例说明。
答案:平衡化学方程式需要保持反应物和生成物的质量守恒和电荷守恒。
以氮气和氢气反应生成氨气的方程式为例:N2 + H2 → NH3。
这个方程式已经平衡,因为反应物和生成物中的氮原子数目和氢原子数目已经相等。
4. 请列举三种化学反应类型及其示例。
答案:三种化学反应类型包括置换反应、双替反应和氧化还原反应。
- 置换反应的示例:AgNO3 + Cu → Cu(NO3)2 + Ag氯化银和铜反应生成硝酸铜和银。
化学】化学方程式练习题(含答案)一、化学方程式选择题1.髙铁酸钾( K2FeO4)是一种新型、高效的水处理剂,可用于自来水的消毒和净化.髙铁Δ酸钾受热时发生分解反应: 4K2FeO4 2X+4K2O+3O2↑,则 X 的化学式是A. Fe B.FeO C. Fe2O3 D. Fe3O4【答案】 C【解析】【分析】【详解】试题分析:根据质量守恒定律化学反应前后原子的种类和数目不变,反应物中钾、铁、氧原子个数分别为 8、 4、16,反应后的生成物中钾、铁、氧原子个数分别为8、0、10,则2X中含有 4个铁原子和 6个氧原子,则每个 X分子由 2 个铁原子和 3个氧原子构成,则物质 R 的化学式为 Fe2O3 ,故选 C。
考点:质量守恒定律的应用2.某个化学反应的微观示意图如图。
有关说法正确的是()A.该反应为分解反应B.该反应不遵守质量守恒定律C.该反应前后分子种类未发生变化D.该反应的化学方程式为 H2+Cl2 2HCl答案】 D解析】A、该反应由两种物质生成了一种物质,属于化合反应,错误;B、由微粒的变化可知,反应前后原子的种类及数目不变,该反应遵守质量守恒定律,错误;C、由微粒的变化可知,该反应前后分子种类发生了变化,错误;D、该反应是氢气和氯气在点燃的条件下反应生成了氯化氢气体,化学方程式为: H2+Cl2 2HCl,正确。
故选 D。
3.如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆圈代表不同的原子.下列说法正确的是( )A .此反应有单质生成B .原子在化学变化中是可分的C .此反应有三种新物质生成D .参加反应的两种分子的个数比为 2 :1 【答案】 A 【解析】 【分析】 详解】试题分析:根据质量守恒定律可得出各物质微粒的个数关系如图:A 、由反应的微观示意图及微粒的构成可知,此反应有单质生成.故 应的微观示意图及微粒的变化可知,原子在化学变化中是不可分的,故 由反应的微观示意图及微粒的构成可知,此反应有两种新物质生成,故 由各物质微粒的个数关系图可知,参加反应的两种分子的个数比为 误.故选 A考点:微粒观点及模型图的应用;单质和化合物的判别;化学反应的实质4.在一个密闭容器中加入四种物质,在一定条件下充分反应,测得反应前后各物质的质量 如下表:物质甲乙丙丁反应前质量 /g22 21 5 反应后质量 /g102 9待测通过分析,判断下列说法不正确的是 A .甲是生成物 B .测得反应后丁的质量为 4g C .乙可能是催化剂D .该反应是分解反应D 说法正确; B 、由反 B 说法错误; C 、【答案】 B【解析】试题分析:本题可分析甲、乙、丙三种物质反应前后的质量变化情况,确定是反应物还是生成物;然后根据质量守恒定律确定丁是反应物还是生成物,进而可以确定反应类型,由表中数据分析可知,反应前后,甲的质量增加了 8g,故甲是生成物,且生成甲的质量为8g;乙的质量不变,乙可能作该反应的催化剂,也可能没有参加反应;同理可以确定丙是反应物,参加反应的丙的质量为 12g;由质量守恒定律,丁应是生成物,且生成的丁的质量为 12g﹣ 8g=4g,故反应后丁物质的质量为 4g+5g= 9g;A、由以上分析可知甲是生成物,故 A 说法正确; B、反应后丁物质的质量为 4g+5g= 9g,故 B 说法错误; C、乙的质量不变,乙可能作该反应的催化剂,故C 说法正确; D、一种物质反应生成两种物质,所以属于分解反应,故 D 说法正确,大阿阿香 B。
考点:考查质量守恒定律及其应用5.在化学反应 A+B2=2C中,已知 20gA 和足量 B2充分反应后,生成 30gC。
已知 B的相对原子质量为 16,则 C 的相对分子质量是()A. 20 B.32 C.48 D.96【答案】 C【解析】根据质量守恒定律可知 20gA 和 B2充分反应生成 30gC 时参加反应的 B2质量应为:30g- 20g=10g;设 C 的相对分子质量是 x,则A+B2=2C32 2x10g 30g32 10g 2x 30g x=48 答案: C。
点睛:依据质量守恒定律可知反应物B2的质量,进而确定了 B2和 C的质量关系,然后依据化学反应中物质之间的质量比等于其相对分子质量和的比求解即可。
6.下列各组物质充分反应后,溶液质量比反应前的溶液质量减小的是()A.铁片浸入稀硫酸中B.铁片浸入硫酸铜溶液中 C.氧化铁粉末加入稀盐酸中 D.氢氧化钠粉末加入稀盐酸中【答案】 B 【解析】A、Fe+ H2SO4 == FeSO4 + H 2↑,溶液增加的质量56 2 56-2 ,不符合题意;B、Fe+ CuSO4 == Cu + FeSO 4 溶液减小的质量160 152 160-152 ,符合题意;C、 Fe2O3 + 6HCl== 2FeCl 3 + 3H2O ,反应后无固体、气体生成,溶液质量增多,不符合题意; D、NaOH + HCl == NaCl + H 2O,反应后无固体、气体生成,溶液质量增多,不符合题意。
故选 B。
点燃7.下列关于 S+O2 SO2 的理解正确的是()A.表示硫与氧气在点燃条件下反应生成二氧化硫 B.参加反应的硫与氧气的质量比是2: 1C.反应前后硫原子、氧分子的个数均不变 D.参加反应的氧气与生成的二氧化硫的分子个数比为2: 1【答案】 A【解析】【详解】点燃A、 S+O2 SO2,可表示硫与氧气在点燃条件下反应生成二氧化硫,故选项说法正确。
B、参加反应的硫与氧气的质量比是 32: 32= 1: 1,故选项说法错误。
C、反应前后硫原子的个数不变,但氧分子参加了反应,个数发生了改变,故选项说法错误。
点燃D、由 S+O2 SO2,参加反应的氧气与生成的二氧化硫的分子个数比为1: 1,故选项说法错误。
故选 A。
8.关于分子和原子两种微粒的叙述正确的是A.物质只能由分子构成B.分子在不断运动,原子静止不动C.相同原子可能构成不同的分子D.化学变化中分子数目一定发生变化【答案】 C【解析】 A 、物质可以由分子、原子、离子微观三粒子构成,故错误;B、分子和原子都在不断的做无规则的运动,故错误;C、相同原子可能构成不同的分子,比如碳原子和氧原子可以构成一氧化碳和二氧化碳,故正确;D、化学变化的过程中,分子的数目可能改变,可能不变,但分子的种类一定改变,故错误。
故选 C。
9.如图为某反应的微观示意图,下列说法正确的是(答案】 D 解析】A 、根据图可知:两种单质生成一种化合物,属于化合反应,不属于分解反应,故错误B 、根据图可知:氢分子和氯分子变化成了氯化氢分子,反应前后分子种类发生了改变,故 错误;C 、由微粒的变化可知,反应前后原子数目没有发生改变,故错误;D 、由微粒的变化可知,参加反应的两种分子个数比为 1:1,故正确 。
点睛:化学反应的实质一般是指在化学变化中,分子分成原子,原子重新组合成新的分子(或直接聚集构成新物质)10. 在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前 后各物质的质量变化见下表。
下列说法错误的是 ( )物质甲乙 丙 丁 反应前物质的质量 (g) 8 32 5 4 反应后物质的质量 (g)16X524A .该反应为分解反应B .丙可能是该反应的催化剂C .甲、丁两物质反应前后质量变化之比为 2: 5D .X 值为 28 【答案】 D 【解析】【分析】 根据质量守恒定律,在化学反应中,反应前参加反应的各物质的质量总和等于生成物的各 质量总和,反应后增加的是反应物,减少的是生成物。
【详解】A 、反应后甲增加了 16g-8g=8g ,则甲是生成物,丁增加了 24g-4g=20g ,则丁是生成 物,丙反应前后质量没变,丙可能没参加反应或是催化剂,根据质量守恒定律,则A .该反应属于分解反应B .反应前后分子种类没有改变C .反应前后原子数目发生改变D .参加反应的两种分子个数比为 1: 1有 8g+32g+5g+4g=16g+X+5g+24g ,则 X=4g ,则反应表达式是乙甲+丙,属于分解反应,故 A 正确;B、丙反应前后质量没变,可能是该反应的催化剂或者没参加反应,故 B 正确;C. 反应后甲增加了 16g-8g=8g ,丁增加了 24g-4g=20g ,则甲、丁两物质反应前后质量变化之比为8: 20=2:5 ,故 C正确;D、在密闭容器中,则有 8g+32g+5g+4g=16g+X+5g+24g ,则 X=4g ,故 D 不正确。
故选 D。
11.在化学反应 A+2B=C+D中,若 5.6g A和 7.3g B恰好完全反应,生成 12.7g C,现在要得到 0.4g D,需要 A的质量为()A.5.6g B. 11.2g C. 14.6g D.无法计算【答案】 B【解析】【详解】生成 D 的质量: 5.6g+7.3g﹣ 12.7g= 0.2g 设参加反应 A 物质的质量为 xA +2B =C +D5.6g 0.2gx 0.4g5.6g =0.2gx 0.4gx= 11.2g答:参加反应 A 物质的质量为 11.2g。
12.2018 年 10 月 28 日,我国首艘国产航母第三次试海成功。
用到的金属钛主要通过下列反应制得:①2FeTiO3+6C+7Cl2═2X+2TiCl4+6CO,② TiCl4+2Mg═Ti+2MgCl2.则 X 的化学式为() A. FeC3l B.FeCl2 C.Fe2O3 D.FeO【答案】 A【解析】【详解】由 2FeTiO3+6C+7Cl2 ═2X+2TiCl4+6CO可知,反应前铁原子是 2 个,反应后应该是 2个,包含在 2X中,反应前后钛原子都是 2个,碳原子都是 6 个,氧原子都是 6个,反应前氯原子是 14 个,反应后应该是 14 个,其中 6 个包含在 2X 中,因此 X 的化学式是 FeCl3。
故选A。
13.下列是酒精被氧化,最终生成乙酸的过程。
下列说法正确的是(答案】 B解析】 详解】A 、甲乙均为有机物,完全燃烧的产物相同,故 A 错误;B 、由反应的图示结合质量守恒定律可知,参加反应的两种物质分子个数之比为 1:2,故 B 正确;C 、根据反应图示可知,转化①不属于化合反应,故 C 错误;D 、根据甲和丙的化学式,丙物质中碳元素的质量分数小于甲物质,故 D 错误。
故选 B 。
14. 用“ ”和“ ”代表两种不同的单质分子,它们在一定条件下能发生化学反 应,反应前后的微观示意图如图所示,下列说法正确的是(A .该反应是分解反应B .该反应有 2 种生成物C .每个生成物分子由 3 个原子构成D .参加反应的“ ”和“ ”分子的个数比是 3: 1 【答案】 D 解析】 分析】 详解】A 、通过反应的微观示意图可看出,反应物中有一个分子过量,该反应是由两种物质反应 生成一种物质,属于化合反应,故 A 不正确;B 、该反应只有 1 种生成物,故 B 不正确;C 、根据微观示意图可看出,每个生成物分子由 4 个原子构成,故 C 不正确;D 、由于反应物中有一个分子过量,参加反应的 “ ”和“ ”分子的个数比是 3︰ 1,故 D正确。